استجابة الخلية البائية متعددة النسائل (Polyclonal B cell response) هو الوضع الطبيعي للاستجابة المناعية للنظام المناعي التكيفي في الثدييات. هذه الاستجابة تضمن أن يتم التعرف على مستضد واحد ويتم مهاجمته من خلال أجزاءه المتداخلة التي تدعى الحواتم، من خلال استنساخات متعددة من الخلايا البائية.[1][2]
يتعرف الجهاز المناعي -في سياق الاستجابة المناعية الطبيعية- على أجزاء من مسببات الأمراض (مثل الجراثيم) على أنها أجسام غريبة (من خارج الجسم) ويزيلها أو يثبط عملها بشكل فعال من أجل تقليل أضرارها المحتملة. تُسمى هذه المادة التي تعّرف الجهاز المناعي عليها باسم «المستضد». قد يستجيب الجهاز المناعي للمستضدات بطرق متعددة مثل إنتاج الأضداد أو كما تُعرف بـ«الأجسام المضادة» بواسطة الخلايا البائية (اللمفاويات البائية) والتي تندرج تحت ما يُعرف بالمناعة الخلطية. تكون الأضداد قابلة للذوبان ولا تتطلب اتصالًا خلويًا-خلويًا مباشرًا بين العامل الممرض والخلية البائية من حتى تعمل.
يمكن أن تكون المستضدات بأحجام كبيرة ومعقدة. تنتج الاستجابة المناعية العديدَ من الأجسام المضادة المختلفة بواسطة العديد من الخلايا البائية المختلفة ضد المستضد نفسه من أجل أن تصبح فعالة، بسبب أن جسم الضد الواحد لا يمكنه أن يرتبط إلا بمنطقة صغيرة نوعية على المستضد. ومن هنا يأتي المصطلح «متعدد النسائل»،[3][4][5] وهو عبارة عن مجموعة من الخلايا الناشئة عن الخلية «الأم». تُعرف الأجسام المضادة الناتجة عن هذه العملية باسم الأجسام المضادة متعددة النسائل. تختلف الأجسام المضادة متعددة النسائل عن جزيئات الجسم المضاد أحادي النسيلة والتي تتطابق وتتفاعل ضمن حلقة واحدة فقط (أي أنها أكثر تحديدًا).
بالرغم من منح الاستجابة متعددة النسائل مزايا عديدة للجهاز المناعي، والتي أهمها زيادة احتمالية التفاعل ضد المستضدات، فهي تزيد أيضًا من احتمالية الإصابة بأمراض المناعة الذاتية والناتجة عن تفاعل النظام المناعي ضد خلايا الجسم الأصلية المنتجة داخل المضيف.
الاستجابة الخلطية للعدوى
تُعرف الأمراض القادرة على الانتقال من كائن حي لآخر باسم الأمراض المعدية، ويُعرف العامل البيولوجي المسبب للمرض باسم العامل الممرض، وتعرف العملية التي يدخل العامل الممرض للجسم من خلالها باسم عملية التلقيح،[6] أما الكائن الحي الذي يصاب بهذا العامل الممرض؛ فيُعرف باسم المضيف الحيوي. تُعرف الحالة التي تحدث عندما يثبت العامل الممرض نفسه في الجسم باسم «الاستعمار»، والذي يمكن أن يؤدي للإنتان، وبالتالي الضرر المباشر للمضيف إما من خلاله أو من خلال المواد الضارة التي يمكن أن تنتجها والمسماة «السموم» أو «الذيفانات».[7] يؤدي هذا الأمر إلى أعراض مختلفة وعلامات مميزة للأمراض المعدية، كذات الرئة أو الخناق (الديفتيريا) على سبيل المثال.
تعد مكافحة الأمراض المعدية المختلفة مهمة للغاية من أجل نجاة الكائن الحي الذي تعرض لها. يتحقق ذلك من خلال القضاء على مسببات الأمراض والسموم أو تثبيط فعاليتها. تُعرف مجموعة الخلايا والأنسجة والأعضاء المختلفة والمتخصصة في حماية الجسم من الإنتان باسم الجهاز المناعي. يحقق الجهاز المناعي المناعة من خلال الاتصال المباشر لبعض خلايا الدم البيضاء بشكل مباشر مع العامل الممرض، الذي يندرج تحت اسم المناعة الخلوية، أو عن طريق إنتاج مواد قادرة على الانتقال لأماكن بعيدة عن مكان إنتاجها لتستهدف الخلايا والسموم المسببة للأمراض المرتبطة بشكل خاص بها وتحييدها عن طريق العملية المعروفة باسم المناعة الخلطية. تُعرف هذه المواد بالأضداد (الأجسام المضادة) القابلة للذوبان والتي تؤدي وظائف مهمة في مكافحة الإنتان.[8]
استجابة الخلية البائية
تخدم الأضداد وظائف مختلفة من أجل حماية المضيف من خطر العوامل الممرضة. تُنتج أشكالها القابلة للذوبان، التي تنفذ هذه الوظائف، بواسطة الخلايا البائية البلازمية، وهي نوع من خلايا الدم البيضاء. يُنظم هذا الإنتاج بإحكام، ويتطلب تنشيط الخلايا البائية بواسطة الخلايا التائية المفعّلة (نوع آخر من خلايا الدم البيضاء)، ويحدث هذا الإجراء بشكل متسلسل. تتضمن الخطوات الرئيسية:[9]
- التعرف على العامل الممرض بشكل نوعي أو غير نوعي (بسبب مستضداته) وابتلاعه لاحقًا بواسطة الخلايا البائية أو البلاعم. ينشط هذا الأمر الخلية البائية بشكل جزئي فقط.
- معالجة المستضد.
- عرض المستضد (أو تجلية المستضد).
- تفعيل الخلايا التائية المساعدة بواسطة الخلايا المقدمة للمستضد.
- التحفيز الثانوي للخلايا البائية بواسطة الخلية التائية المفعلة ما يؤدي لتفعيلها بالكامل.
- تكاثر الخلايا البائية مع إنتاج الأجسام المضادة القابلة للذوبان.
التعرف على العوامل الممرضة
تُخلّق العوامل الممرضة البروتينات القادرة على لعب دور مستضدات «يمكن التعرف عليها»؛ قد تعبّر عن الجزيئات إما على سطحها أو قد تطلقها ضمن البيئة المحيطة (سوائل الجسم). الأمر الذي يجعل هذه المواد قابلة للتعرف عليها هو أنها ترتبط بشكل نوعي وبقوة ببروتينات مضيفة معينة تسمى الأضداد. يمكن تثبيت نفس الأضداد على سطح خلايا الجهاز المناعي، وفي هذه الحالة تلعب دور مستقبلات، أو يمكن أن تُفرز في الدم، وتُعرف حينها باسم الأضداد القابلة للذوبان. تكون البروتينات كبيرة نسبيًا على المستوى الجزيئي لذلك لا يمكن التعرف عليها بشكل كامل،[1] ولكن يمكن التعرف على مقاطع أو أجزاء منها والتي تسمى الحواتم. تلامس الحاتمة منطقة صغيرة جدًا لجزيء الضد (من 15 إلى 22 حمضًا أمينيًا) تُعرف بالمُستوقِع، وهو مكان ارتباط الضد بالمستضد. تكون الأجسام المضادة المرتبطة بالغشاء في الجهاز المناعي هي مستقبلات الخلايا البائية (بي سي آر). في حين لا تُصنف مستقبلات الخلايا التائية كيميائيًا كجسم مضاد، فهي تخدم وظيفة مماثلة بسبب ارتباطها بشكل خاص بحواتم معقدة مع جزيئات معقد التوافق النسيجي الأعظمي (إم إتش سي).[10] يكون الارتباط بين المستوقع ومستضده المقابل له نوعيًا للغاية بسبب تركيبته، ويسترشد بالعديد من الروابط غير التساهمية، على عكس اقتران الأنواع الأخرى من الروابط (أي ذرة أو أيون أو جزيء يرتبط بأي مستقبل بدرجة من الخصوصية والقوة). لا تنشأ خصوصية الربط من التفاعل «بطريقة القفل والمفتاح»، ولكنها تتطلب كلًا من المستوقع والحاتمة الخاضعة لتغيرات طفيفة بالتوافق مع وجود بعضهما البعض.[11]
التعرف النوعي على الحاتمة عبر الخلايا البائية
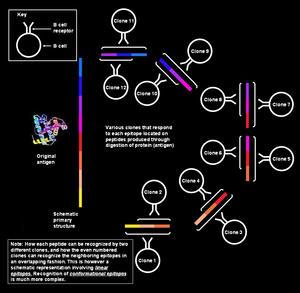
في الشكل الموجود، عُرضت الأقسام المختلفة التي تظهر على خط مستقيم بشكل مستمر، ما يعني أنها تكوّن متسلسلة، وبالرغم من ذلك بالنسبة للموقف الذي نناقشه هنا (تعرف الخلية البائية على المستضدات على سبيل المثال) فإن هذا التفسير يُعتبر بسيطًا للغاية. تُعرف هذه الحواتم باسم الحواتم المتسلسلة أو الخطية، وذلك لأن جميع الأحماض الأمينية الموجودة عليها تقع على نفس التسلسل (الاستقامة). هذا النمط من التعرف ممكن فقط عندما يكون الببتيد صغيرًا (6-8 أحماض أمينية طويلة)،[1] بالإضافة إلى استخدامه بواسطة الخلايا التائية (اللمفاويات التائية).
ومع ذلك، فإن الخلايا الذاكرة/الساذجة البائية تتعرف على البروتينات السليمة الموجودة على سطح العوامل الممرضة. يكون البروتين الموجود في تركيبته الثلاثية مطويًا لدرجة تجعل بعض حواتم الأحماض الأمينية تكمن ضمن الجزء الداخلي من البروتين في هذه الحالة، بالإضافة لوقوع القطاعات المحيطة بها على السطح. لا يتلامس المستوقع الموجود على مستقبلات الخلايا البائية إلا مع الأحماض الأمينية الموجودة على سطح البروتين. قد تكون الأحماض الأمينية السطحية في الواقع متقطعة ضمن البنية الأولية للبروتين، ولكنها تتداخل مع بعضها بسبب أنماط طيّ البروتين المعقدة. تُعرف هذه الحواتم باسم الحواتم المطابقة، وتميل إلى أن تكون أطول من الحواتم الخطية (15-22 حمضًا أمينيًا). وبالمثل، تنتج الخلايا البلازمية المنتمية لنفس النُسيلة أجسامًا مضادة ترتبط بنفس الحواتم المطابقة في بروتينات العامل الممرض.[12][13][14][15]
يؤدي ارتباط مستضد معين مع جزيئات الـ«بي سي آر» المقابلة إلى زيادة إنتاج جزيئات «إم إتش سي-2»: يستمد هذا الأمر أهميته بسبب عدم حدوث نفس الأمر عندما يُستَوعب المستضد من خلال عملية غير محددة نسبيًا تسمى الاحتساء الخلوي، إذ يكون المستضد مع السائل المحيط «متشربًا» باعتباره حويصلًا صغيرًا ضمن الخلية البائية. يُعرف هذا المستضد باسم المستضد غير النوعي، وهو لا يؤدي لتنشيط الخلية البائية أو إنتاج الأضداد ضدها لاحقًا.
معرض صور
انظر أيضاً
مراجع
- Goldsby, Richard (2003). "Antigens (Chapter 3)". Immunology (الطبعة Fifth). New York: W. H. Freeman and Company. صفحات 57–75. .
- "Definition of Polyclonal from MedicineNet.com". Webster's New World Medical Dictionary. مؤرشف من الأصل في 7 أغسطس 20123 مايو 2008.
- Frank, Steven A. (2002). "Specificity and Cross-Reactivity (Chapter 4)". Immunology and Evolution of Infectious Disease. Princeton University. صفحات 33–56. 23 يونيو 2008.
- "Etymology of "clone". Online etymology dictionary. مؤرشف من الأصل في 15 فبراير 201726 يونيو 2008.
- Bansal, R.K. (2005). "Reproductive Cloning-An Act Of Human Rights Violation". Journal of Indian Association of Forensic Medicine. 27 (3): 971–973. مؤرشف من الأصل في 16 ديسمبر 201923 يونيو 2008.
- "Definition of inoculation". TheFreeDictionary.com (citing Dorland's Medical Dictionary for Health Consumers. © 2007 by Saunders, an imprint of Elsevier, Inc.). مؤرشف من الأصل في 14 نوفمبر 201910 يونيو 2008.
- Pier, Gerald B. (2005) [1945]. "Molecular mechanisms of microbial pathogenesis (Chapter 105)". In Kasper, Braunwald, Fauci, Hauser, Longo, Jameson (المحررون). Harrison's Principles of Internal Medicine. 1 (الطبعة Sixteenth). McGraw-Hill. صفحة 700. .
- Goldsby (2007). "Organization and Expression of Immunoglobulin Genes (Chapter 5)". Immunology (الطبعة Fifth). New York. صفحات 105–136. .
- Nairn, Roderick (2004) [1954]. "Immunology (Chapter 8)". In Geo F. Brooks; Janet S. Butel; Stephen A. Morse (المحررون). Jawetz, Melnick, & Adelberg's Medical Microbiology (الطبعة Twenty-Third Edition International). Lange publications/McGraw-Hill. صفحات 133–135, 138–139. .
- Goldsby (2007). "T-Cell Maturation, Activation and Differentiation (Chapter 10)". Immunology (الطبعة Fifth). صفحات 221–246. .
- Nair, Deepak; Singh Kavita; Siddiqui Zaved; Nayak Bishnu; Rao Kanury; Salunke Dinakar (2002-01-09). "Epitope Recognition by Diverse Antibodies Suggests Conformational Convergence in an Antibody Response" ( كتاب إلكتروني PDF ). The Journal of Immunology. 168 (5): 2371–2382. doi:10.4049/jimmunol.168.5.2371. PMID 11859128. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 17 ديسمبر 200803 مايو 2008.
- "Immunochemical Applications". Technical Tips. EMD biosciences. مؤرشف من الأصل في 11 أبريل 200807 مايو 2008.
- Davis, Cheryl. "Antigens". Biology course. Western Kentucky University. مؤرشف من الأصل في 29 مارس 200812 مايو 2008.
- Ceri, Howard. "Antigens". Immunology course. University of Calgary. مؤرشف من الأصل في 5 أكتوبر 200812 مايو 2008.
- Khudyakov, Yury; Howard A. Fields (2002). Artificial DNA: Methods and Applications. Florida: CRC Press. صفحة 227. . مؤرشف من الأصل في 25 يناير 2020.





