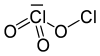
ثلاثي أكسيد ثنائي الكلور هو مركب كيميائي من أكاسيد الكلور صيغته Cl2O3.
| ثلاثي أكسيد ثنائي الكلور[1] | |
|---|---|
| الاسم النظامي (IUPAC) | |
dichlorine trioxide |
|
| أسماء أخرى | |
chlorine trioxide |
|
| المعرفات | |
| رقم CAS | |
| CAS | 17496-59-2 |
| بوب كيم | 167661 |
| الخواص | |
| الصيغة الجزيئية | Cl2O3 |
| الكتلة المولية | 118.90 غ/مول |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
التحضير
يمكن أن يستحصل على المركب من تفكك ثنائي أكسيد الكلور بالأشعة فوق البنفسجية؛[3] وذلك إلى جانب سداسي أكسيد ثنائي الكلور Cl2O6.
الخواص
يوجد المركب على شكل غاز بني غامق، ويتم التبريد إلى درجات حرارة تبلغ -75 °س للحصول على شكل شبه مستقر منه. يبدأ المركب عند الدرجة −45 °س بالتفكك إلى الكلور والأكسجين وذلك بشكل متفجر.[4]
هناك حالتا أكسدة للكلور فيه وهي I وV؛ ويعتقد أن تكون البنية على الشكل OCl−ClO2، مع احتمالية وجود متصاوغات على الشكل Cl−O−ClO2.[5]
طالع أيضاً
مراجع
- Lide, David R. (1998). Handbook of Chemistry and Physics (الطبعة 87). Boca Raton, Florida: CRC Press. صفحات 4–51. .
- وصلة : معرف بوب كيم — الرخصة: محتوى حر
- Egon Wiberg, Arnold Frederick Holleman (2001) Inorganic Chemistry, Elsevier (ردمك )
- N. N. Greenwood and A. Earnshaw (1997). Chemistry of the Elements. Butterworth-Heinemann. .
- Wiberg&Holleman