متلازمة نونان ذات الصبغيات المتعددة (أو كما تعرف بمتلازمة ليوبارد أو متلازمة القلب والجلد أو متلازمة غورلين الثانية أو متلازمة التصبغات المتعددة المنتشرة أو اعتلال عضلة القلب التقدمي[1] أو متلازمة كابوت- ريموين- كونيسمارك- استيرلي- ريتشاردسون أو متلازمة موينان) والتي تعتبر جزء من المتلازمات المرتبطة بمسار طفرات جينات Ras/MAPK،[2] هي مرض وراثي سائد[3] يصيب العديد من أجهزة الجسم وينتج عن طفرة في الجين المسؤول عن إنتاج بروتين التيروسين فوسفاتيز. هذا المرض عبارة عن مجموعة من الأعراض، التي تنطوي في معظمها على الجلد، والهيكل العظمي وجهاز القلب والأوعية الدموية، والتي قد أو قد لا توجد في جميع المرضى. لاتزال طبيعة إحداث الطفرات لكل هذه الأعراض غير واضحة بالمرة. ومع ذلك، لا تزال البحوث جارية. تحدث متلازمة نونان ذات الصبغيات المتعددة نتيجة للعديد من الطفرات المغلطة على نفس الجين. وبالنظر إلى الإحصائيات، تعتبر متلازمة نونان من المتلازمات الشائعة (1: 1000 إلى 1: 2500 ولادة حية) كما يشيع الورم العصبي الليفي من النوع الأول (1: 3500) . ومع ذلك، لا توجد بيانات وبائية كافية لمتلازمة نونان ذات التصبغات المتعددة.[4]
| متلازمة نونان ذات التصبغات المتعددة | |
|---|---|
منظر لثلاثة أرباع الوجه يظهر بروز الفكل السفلي والأذن منخفضة المستوى
| |
| معلومات عامة | |
| الاختصاص | طب الجلد، وطب القلب، وطب الروماتزم |
| من أنواع | مرض وراثي سائد |
الأعراض والعلامات
استخدم مصطلح متلازمة ليوبارد (بالانجليزية: LEOPARD) كاسم بديل لمتلازمة نونان ذات التصبغات المتعددة في عام 1969،[5] حيث يرمز كل حرف من تلك الحروف السبعة (بالانجليزية) إلى عرض معين من الأعراض الآتية بالإضافة إلى نمش الجلد المميز الناتج عن التصبغات التي تشبه جلد النمر.
- التصبغات الجلدية: بقع جلدية يتراوح لونها ما بين البنية الحمراء والبني الداكن، والتي تحدث عادةً في عدد كبير من المصابين (أكثر من10،000) على جزء كبير من الجلد، وتغطي أحيانًا أكثر من 80٪ من الجلد. يمكن أن تظهر تلك البقع أيضًا داخل وجنة الفم، أو على سطح صلبة العين. تتميز تلك البقع بحدود غير منتظمة يتراوح حجمها من 1 ملم في القطر إلى (بقع القهوة بالحليب) والتي تبلغ عدة سنتيمترات في القطر. كما يلاحظ أيضًا بعض مناطق البهاق من نوع نقص التصبغ.
- اضطرابات مقاومية تخطيط كهربائية القلب: تظهر في صورة مقاومة انتقال النبضات الكهربية عبر فروع الزمة العضلية القلبية عند إجراء تخطيط كهربائية القلب.
- فرط تباعد العين: تتباعد عيون المرضى المصاب بتلك المتلازمة، مما يؤدي إلى الشكل المتشابه لوجهه. تعتبر تشوهات الوجه ثاني أكثر التشوهات حدوثًا بعد التصبغات الجلدية. تشمل تلك التشوهات: منبت الأنف العريض، جحوظ الفك السفلي، والآذان المنخفضة المستوى والتي يحتمل أن تكون ملتفة.
- تضيق رئوي: تضيق الجذع الرئوي عند خروجه من القلب. تشمل التشوهات القلبية الأخرى تضيق الصمام الأبهري أو انسدال الصمام التاجي.
- تشوهات الأعضاء الجنسية: عادةً ما يصاحب تلك المتلازمة الخصية الهاجرة في الذكور (عدم نزول الخصية إلى كيس الصغن) أو الخصية الواحدة. بينما تعاني الإناث من عدم تخليق أحد المبيضين أو كلاهما، والذي يصعب تحديده الا بعد التصوير بالأشعة التلفزيونية فوق الصوتية عند بلوغ الأنثى عام واحد.
- فشل النمو: بطء أو توقف النمو، يولد معظم المصابون بهذه المتلازمة بوزن وطول طبيعيين، ثم يحدث تأخر في النمو عادةً خلال السنة الأولى.
- صمم: صمم عصبي ( تشوهات الأعصاب السمعية)
ليس من الضروري وجود كل هذه السمات لتشخيص المتلازمة. يعتمد التشخيص الطبي على وجود التصبغات مع اثنين من الأعراض الأخرى، مثل تشوهات تخطيط القلب وفرط تباعد العين، أو عدم وجود تلك التصبغات مع وجود ثلاثة من السمات المذكورة أعلاه، مع قريب من الدرجة الأولى (أم، طفل، أخ) مخص طبيًا بتلك المتلازمة.[6]
- تشمل بعض التشوهات الجلدية الإضافية (النمش الإبطي، نقص التصبغ الموضعي، تشابك جلد ما بين الأصابع، مرونة الجلد).
- لوحظ التخلف العقلي المتوسط في حوالي 30٪ من المصابين بالمتلازمة.
- تم توثيق عدد من الحالات المصابة مصحوبة بالآتي: الرأرأة (حركات العين اللاإرادية)، والنوبات، أو انخفاض القدرة على شم الروائح).
- في عام 2004، تم توثيق حالة مصابة بتمدد الأوعية الدموية في الطرف العلوي والتي تطلبت تدخلًا جراحيًا.[7]
- في عام 2006، تم ا توثيق حالة مصابة بابيضاض الدم النقوي الحاد.[8]
نظرًا لندرة المتلازمة نفسها، يصعب تحديد ما إذا كانت بعض الأمراض الإضافية هي في الواقع جزء من المتلازمة أم لا.
طفلة تبلغ من العمر 21 شهرًا، الجيل الثالث للمرض، أكدت الاختبارات الجينية حدوث طفرة بالجين Y279C، Y279C تظهر فرط تباعد العينين وتشابه الوجه.
التشخيص
يمكن تأكيد تشخيص المرض بإجراء اختبار وراثي. في دراسة ل 10 رضع مع بعض الأعراض الطبية لتلك المتلازمة قبل عيد ميلادهم الأول، تأكد تشخيص إصابة 8 (80٪) حالات بالطفرة المشتبه بها. تم العثور على مريض إضافي مع الطفرة المشتبه بها فيما بعد مصابًا بالورم العصبي الليفي من النوع الأول، بعد تقييم الأم.
توجد خمس تنوعات جينية مسؤولة عن متلازمة ذات الصبغيات المتعددة: Y279C, T468M, A461T, G464A, and Q510P والتي يبدو أنها تشكل عائلة فريدة من طفرات الجينات المغلطة غير التطفرات المتحولة في باقي الجينات.[9]
آلية المرض
في الطفرات المهيمنة المتسببة في متلازمة نونان ذات التصبغات المتعددة (Y279C و T468M)، تسبب تلك الطفرات فقد قدرة تحفيز بروتين SHP2 (الناتج الجيني لجين PTPN11)، والذي يعتبر سلوك غير مفهوم لهذه العائلة من الجينات،[10] مما يؤثر على عامل النمة والإشارات المرتبطة به. وبينما تأكد البحوث الأخرى تلك الآلية،[11][12] لا تزال هناك حاجة إلى مزيد من البحوث لتحديد كيفية ارتباط تلك التأثيرات بتلك المتلازمة.
التنبؤالطبي
لا تعتبر تلك المتلازمة مرض يهدد الحياة، في حد ذاته، إذ يعيش معظم المصابون المؤكد تشخيصهم حياةً طبيعية. إلا أن اعتلال عضلة القلب الانسدادي وغيرها من الآثار المرضية المؤثرة على جهاز القلب والأوعية الدموية قد تكون سبب الوفاة في أولئك الذين يعانون من التشوهات القلبية العميقة.[13]
العلاج
عند تأكيد التشخيص الإصابة بتلم المتلازمة، يجب أن يتابع المرضى بشكل دوري مع طبيب القلب، وأخصائي الغدد الصماء، وأخصائي الأمراض الجلدية، وغيرها من التخصصات المناسبة للأعراض الموجودة.
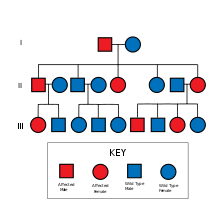
كما يفُفضل أن يسعى المصابون بتلك المتلازمة القادرين على إنجاب الأطفال إلى المشورة الوراثية قبل اتخاذ قرار لإنجاب الأطفال. وبما أن المتلازمة تظهر بنمط غير مكتمل أو غير عادي، لذا يجب إجراء فحص لجميع أفراد الأسرة.[13] وحيث أن تلك المتلازمة تنتقل في صورة وراثية سائدة، فمن المحتمل أن يصاب كل مولود بنسبة 50% بتلك المتلازمة إذا كان أحد الأبوين مصابًا. وعلى الرغم من أن تلك المتلازمة كاملة الاختراق ( إحدى خصائص الطفرات)، وحيث أنها تتمتع بالتعبير المتباين، يمكن أن تظهر الأعراض بصورة طفيفة في أحد الأجيال، بينما تظهر بصورة شديدة الخطورة في الجيل التالي.
عند اتخاذ قرار الإنجاب وحمل الأم، يجب أن يُتابع الجنين طوال فترة الحمل خوفًا من التشوهات القلبية. وفي حالة حدوث أحد التشوهات القلبية الجسيمة، يجب أن يتلقى الأبوين المشورة بشأن استمرارية الحمل من عدمه.
تشمل الرعاية الروتينية علاج الأعراض كالآتي:[13]
- بالنسبة لأولئك الذين يعانون من مشاكل الغدد الصماء (مستويات منخفضة من هرمون منبه الغدة الدرقية [وهو هرمون يُفرز من الغدة النخامية مسؤول عن تنظيم هرمونات الغدة الدرقية]، هرمون منشط للحوصلة)، ينصح باستخدام علاج دوائي بديل لتلك الهرمونات.
- النسبة لأولئك الذين يشعرون بالانزعاج من ظهور البقع الجلدية، قد يكون التدخل الجراحي بالتبريد مفيدًا في حالات البقع الجلدية الكثيرة التي. قد يساعد العلاج البديل أيضًا باستخدام كريمات التريتينوين أو الهيدروكينون.
- تستخدم العلاجات الدوائية لأولئك الذين يعانون من التشوهات القلبية، إذ تبرر خطورة تلك التشوهات القلبية استخدام مثل تلك الأدوية. يجب إجراء تخطيط كهربائية القلب بصورة إلزامية قبل أي تدخل جراحي، ويرجع ذلك إلى احتمال حدوث اضطراب النظم القلبية.
وبائيات
وصفت العديد من المؤلفات الطبية تلك التلازمة أنها نادرة للغاية.[13][14] لذا لا توجد أي بيانات وبائية أو إحصاءات تشير إلى الأعداد المصابة بتلك المتلازمة على مستوى العالم. ومع ذلك، تم ذكر حوالي 200 حالة مصابة بتلك المتلازمة في مختلف المؤلفات الطبية.[15]
التاريخ
وصف زيسلر وبيكر لأول مرة متلازمة ذات تصبغات جلدية متعددة، وفرط تباعد العين، والصدر الجؤجؤي (الصدر الجاحظ) وجحوظ الفك السفلي في عام 1936.[16] ثم أُضيف إلى تلك الأوصاف أوصافًا متقطعة على مر السنين. في عام 1962، ارتبطت التشوهات القلبية والقامة القصيرة لأول مرة بتلك المتلازمة.[17] وفي عام 1966، أضيفت ثلاث حالات عائلية، أم وابنها وابنتها.[18] وأضيفت حالة أخرى من أم مصابة وطفلين لأبوين مختلفين، في عام 1968.[19]
كان يعتقد في وقت متأخر حتى عام 2002 [20] أن متلازمة نونان ذات التصبغات المتعددة كانت مرتبطة بالورم العصبي الليفي من النوع الأول (متلازمة فون ريكلينهاوزن). في الواقع، حيث أن التصنيف الدولي للأمراض والمراجعة العاشرة للتصنيف الدولي للأمراض تفتقر إلى رمز تشخيصي محدد لمتلازمة نونان ذات التصبغات المتعددة، لا يزال الرمز التشخيصي للورم عالصبي الليفي من النوع الأول يستخدم لتشخيص تلك المتلازمة، على الرغم من ثبوت عدم ارتباط الجين بالجين المسؤول عن الورم العصبي الليفي من النوع الأول.[21]
مقالات ذات صلة
مراجع
- James, William; Berger, Timothy; Elston, Dirk (2005). Andrews' Diseases of the Skin: Clinical Dermatology (الطبعة 10th). Saunders. .
- Tidyman WE, Rauen KA (June 2009). "The RASopathies: developmental syndromes of Ras/MAPK pathway dysregulation". Current Opinion in Genetics & Development. 19 (3): 230–6. doi:10.1016/j.gde.2009.04.001. PMC . PMID 19467855.
- Coppin BD, Temple IK (1997). "Multiple lentigines syndrome (LEOPARD syndrome or progressive cardiomyopathic lentiginosis)". Journal of Medical Genetics. 34 (7): 582–6. doi:10.1136/jmg.34.7.582. PMC . PMID 9222968.
- Tullu MS, Muranjan MN, Kantharia VC, et al. (1 April 2000). "Neurofibromatosis-Noonan syndrome or LEOPARD Syndrome? A clinical dilemma". J Postgrad Med. 46 (2): 98–100. PMID 11013475. مؤرشف من الأصل في 14 مارس 2020.
- Gorlin RJ, Anderson RC, Blaw M (1969). "Multiple lentigenes syndrome". Am. J. Dis. Child. 117 (6): 652–62. doi:10.1001/archpedi.1969.02100030654006. PMID 5771505.
- Voron DA, Hatfield HH, Kalkhoff RK (1976). "Multiple lentigines syndrome. Case report and review of the literature". Am. J. Med. 60 (3): 447–56. doi:10.1016/0002-9343(76)90764-6. PMID 1258892.
- Yagubyan M, Panneton JM, Lindor NM, Conti E, Sarkozy A, Pizzuti A (April 2004). "LEOPARD syndrome: a new polyaneurysm association and an update on the molecular genetics of the disease". J. Vasc. Surg. 39 (4): 897–900. doi:10.1016/j.jvs.2003.11.030. PMID 15071461.
- Uçar C, Calýskan U, Martini S, Heinritz W (March 2006). "Acute myelomonocytic leukemia in a boy with LEOPARD syndrome (PTPN11 gene mutation positive)". J. Pediatr. Hematol. Oncol. 28 (3): 123–5. doi:10.1097/01.mph.0000199590.21797.0b. PMID 16679933.
- Digilio MC, Sarkozy A, de Zorzi A, et al. (2006). "LEOPARD syndrome: clinical diagnosis in the first year of life". American Journal of Medical Genetics. 140 (7): 740–6. doi:10.1002/ajmg.a.31156. PMID 16523510.
- Tartaglia M, Martinelli S, Stella L, et al. (2006). "Diversity and functional consequences of germline and somatic PTPN11 mutations in human disease". American Journal of Human Genetics. 78 (2): 279–90. doi:10.1086/499925. PMC . PMID 16358218.
- Hanna N, Montagner A, Lee WH, et al. (2006). "Reduced phosphatase activity of SHP-2 in LEOPARD syndrome: consequences for PI3K binding on Gab1". FEBS Lett. 580 (10): 2477–82. doi:10.1016/j.febslet.2006.03.088. PMID 16638574.
- Kontaridis MI, Swanson KD, David FS, Barford D, Neel BG (2006). "PTPN11 (Shp2) mutations in LEOPARD syndrome have dominant negative, not activating, effects". J. Biol. Chem. 281 (10): 6785–92. doi:10.1074/jbc.M513068200. PMID 16377799. مؤرشف من الأصل في 08 أكتوبر 2008.
- LEOPARD Syndrome في موقع إي ميديسين
- "LEOPARD Syndrome". NORD — National Organization for Rare Disorders. مؤرشف من الأصل في 03 مارس 2015.
- "Noonan syndrome with multiple lentigines". U.S. National Library of Medicine. مؤرشف من الأصل في 19 أبريل 2019.
- Zeisler EP, Becker SW (1936). "Generalized lentigo: its relation to systemic nonelevated nevi". Arch Dermatol Syphilol. 33: 109–125. doi:10.1001/archderm.1936.01470070112010.
- Moynahan EJ (1962). "Multiple symmetrical moles, with psychic and somatic infantilism and genital hypoplasia: first male case of a new syndrome". Proceedings of the Royal Society of Medicine. 55 (11): 959–960. PMC . PMID 19994192.
- Walther RJ, Polansky BJ, Grotis IA (1966). "Electrocardiographic abnormalities in a family with generalized lentigo". N. Engl. J. Med. 275 (22): 1220–5. doi:10.1056/NEJM196612012752203. PMID 5921856.
- Matthews NL (1968). "Lentigo and electrocardiographic changes". N. Engl. J. Med. 278 (14): 780–1. doi:10.1056/NEJM196804042781410. PMID 5638719.
- National Library of Medicine MeSH: C05.660.207.525 - تصفح: نسخة محفوظة 04 مارس 2016 على موقع واي باك مشين.
- Ahlbom BE, Dahl N, Zetterqvist P, Annerén G (1995). "Noonan syndrome with café-au-lait spots and multiple lentigines syndrome are not linked to the neurofibromatosis type 1 locus". Clin. Genet. 48 (2): 85–9. doi:10.1111/j.1399-0004.1995.tb04061.x. PMID 7586657.
مصادر خارجية
- اختبارات الجينات (بمعاهد الصحة الوطنية الأمريكيةجامعة واشنطن)
- من سمى متلازمة غورلين.
- 981603547
- Dermnetnz
- DermIS