موت الخلايا (بالانجليزية:cell death)[1][2] هو توقف الخلية البيولوجية عن أداء وظائفها. قد يكون ذلك نتيجة لعملية طبيعية حيث تموت الخلايا القديمة وتُستبدل بأخرى جديدة، أو قد تنتج عن عوامل أخرى مثل المرض أو إصابة عضو محدد، أو موت الكائن الحي نفسه. وتشمل أنواع موت الخلايا:
موت الخلايا المبرمج
موت الخلية المبرمج (بالانجليزية:programmed cell death) هو موت الخلايا من خلال عملية منظمة طوال دورة حياة الكائن الحي. على سبيل المثال، يحدث تكوّن أصابع اليدين والقدمين في الجنين البشري عن طريق موت الخلايا النامية بين الأصابع، والنتيجة هي أن أصابعنا منفصلة عن بعضها. يقوم موت الخلايا المبرمج بوظيفته في تطوير الأنسجة في كل من النباتات والحيوانات متعددة الخلايا.
يُعد كلا من موت الخلايا المبرمج أو النوع الأول من موت الخلايا، والالتهام الذاتي أو النوع الثاني من موت الخلايا على حد سواء أشكال موت منظم للخلايا،[3] في حين أن النخر هو عملية غير فسيولوجية تحدث نتيجة للعدوى أو الإصابة، ويحدث في عدة أشكال مختلفة. وُجد في الآونة الأخيرة شكل مبرمج من أشكال النخر، necroptosis، مما دعا للاعتراف به باعتباره نموذج بديل لموت الخلايا المبرمج. ويُفترض بأن necroptosis يمكن أن يكون بمثابة نسخة احتياطية عند حجب إشارات موت الخلايا المبرمج بفعل عوامل داخلية المنشأ أو خارجية مثل الفيروسات أو الطفرات.
الالتهام الذاتي
يتميز الالتهام الذاتي بتشكيل فجوات كبيرة تلتهم عضيات الخلية في تسلسل معين قبل تدمير النواة.[4]
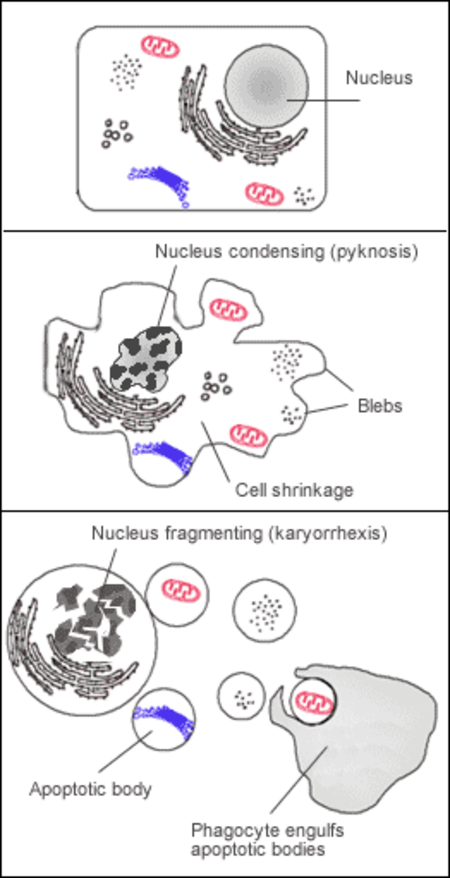
موت الخلايا المبرمج (PCD) يحدث في الكائنات متعددة الخلايا[5]. والأحداث البيوكيميائية تؤدي إلى تغييرات مميزة في شكل الخلية وموتها. وتشمل هذه التغييرات؛ انكماش الخلية، التجزؤ النووي، تكثيف الكروماتين، وتكسير صِبغيات الحمض النووي. ويُعتقد الآن - في سياق تنموي - أن الخلايا تُحفّز لتموت من تلقاء نفسها، بينما في سياق التماثل الساكن؛ غياب بعض عوامل البقاء على قيد الحياة يمكن أن يؤدي إلى موت الخلايا. هناك بعض الأدلة على أن أعراض موت الخلايا المُبرمَج مثل تنشيط إنزيمات النواة الداخلية يمكن أن يحدث دون سبب وراثي، لكن في حقيقة الأمر لابد أن يحدث موت الخلايا المبرمَج نتيجة لعوامل وراثية. كما أصبح من الواضح ارتباط كل من الانقسام وموت الخلايا المبرمج بطريقة ما، ويتحقق التوازن اعتمادًا على العوامل المناسبة للنمو أو للموت.[6]
الالتهام الذاتي، هو عملية الهدم التي تؤدي إلى تكسير محتويات السيتوبلازم عن طريق الليسوسومات، وتكون تجمعات بروتين غير طبيعية، وتلف العضيات. يتم تنشيط الالتهام الذاتي عمومًا بسبب نقص تغذية الخلية، ولكن يمكن أن يحدث فسيولوجيًا أو نتيجة لمرض مثل أمراض الأعصاب، القلق، العدوى والسرطان.
أنواع أخرى
وقد تم اكتشاف مسارات أخرى لموت الخلايا المبرمج. مثل الطريق الغير معتمد على موت الخلايا المبرمج الخلايا أو "necroptosis"، هذه المسارات البديلة لموت الخلايا فعالة مثل موت الخلايا المبرمج ويمكن أن تعمل إما كآليات احتياطية أو باعتبارها النوع الرئيسي من PCD.
هناك أشكال أخرى من موت الخلايا المُنظّم[7] وهي مطابقة تقريبًا لموت الخلايا المبرمج إلا في طريقة التحفيز؛ مثل:
- التقرن، وهو شكل من موت الخلايا يحدث فقط في العيون
- ferroptosis؛ وهو شكل من موت الخلايا اعتمادًا على الحديد[8]
- Anoikis
- تكسير فاليريان.
- أيضًا Eryptosis وهو موت خلايا الدم الحمراء المُبرمَج، وغيرهم الكثير.
- موت الخلايا المُفعّل (AICD) هو موت الخلية المبرمج الناتج عن التفاعل بين مستقبلات (Fas، CD95) و (FASL، CD95).[9] ويحدث ذلك نتيجة التحفيز المتكرر من مستقبلات الخلايا الليمفاوية التائية(TCR)، كما أنه يساعد في الحفاظ على المناعة.[10] لذلك، أي تغيير في العملية قد يؤدي إلى أمراض المناعة الذاتية. مما يعني أن موت الخلايا المُفعّل AICD هو مُنظّم سلبي للخلايا اللمفاوية التائية المُنشّطَة.
- موت الخلايا نتيجة نقص التروية، أو ورام، هو شكل عَرَضي أو سلبي لموت الخلايا. وتتميز هذه العملية بتورم الميتوكوندريا، تشكل الفجوات في السيتوبلازم، وزيادة حجم النواة والسيتوبلازم.[11]
- موت الخلية المناعي هو شكل من موت الخلايا التي تسببها بعض عوامل تثبيط المناعة مثل anthracyclines، أو العلاج الإشعاعي والعلاج الضوئي(PDT).[12]
موت الخلايا في النباتات
تخضع النباتات لعمليات خاصة من موت الخلايا المُبرمج، تشبه طريقة الالتهام الذاتي. إلا أنه هناك سمات مختلفة تفرق بين موت الخلايا في النباتات والحيوانات متعددة الخلايا.
مقالات ذات صلة
المصادر
- Engelberg-Kulka H, Amitai S, Kolodkin-Gal I, Hazan R (2006). "Bacterial Programmed Cell Death and Multicellular Behavior in Bacteria". PLoS Genetics. 2 (10): e135. doi:10.1371/journal.pgen.0020135. PMC . PMID 17069462. مؤرشف من الأصل في 4 يناير 2015.
- Green, Douglas (2011). Means To An End. New York: Cold Spring Harbor Laboratory Press. . مؤرشف من الأصل في 02 أبريل 2019.
- Kierszenbaum, Abraham (2012). Histology and Cell Biology - An Introduction to Pathology. Philadelphia: ELSEVIER SAUNDERS.
- Schwartz LM, Smith SW, Jones ME, Osborne BA (1993). "Do all programmed cell deaths occur via apoptosis?". PNAS. 90 (3): 980–4. doi:10.1073/pnas.90.3.980. PMC . PMID 8430112. ;and, for a more recent view, see Bursch W, Ellinger A, Gerner C, Fröhwein U, Schulte-Hermann R (2000). "Programmed cell death (PCD). Apoptosis, autophagic PCD, or others?". Annals of the New York Academy of Sciences. 926: 1–12. doi:10.1111/j.1749-6632.2000.tb05594.x. PMID 11193023.
- Green, Douglas (2011). Means To An End. New York: Cold Spring Harbor Laboratory Press. . مؤرشف من الأصل في 02 أبريل 2019.
- D. Bowen, Ivor (1993). Cell Biology International 17. Great Britain: Portland Press. صفحات 365–380. doi:10.1006/cbir.1993.1075. ISSN 1095-8355. مؤرشف من الأصل في 04 سبتمبر 2017.
- Kroemer G, Martin SJ (2005). "Caspase-independent cell death". Nature Medicine. 11 (7): 725–30. doi:10.1038/nm1263. PMID 16015365.
- Dixon Scott J.; Lemberg Kathryn M.; Lamprecht Michael R.; Skouta Rachid; Zaitsev Eleina M.; Gleason Caroline E.; Patel Darpan N.; Bauer Andras J.; Cantley Alexandra M.; et al. "Ferroptosis: An Iron-Dependent Form of Nonapoptotic Cell Death". Cell. 149 (5): 1060–1072. doi:10.1016/j.cell.2012.03.042. مؤرشف من الأصل في 04 يوليو 2013.
- Zhang J, Xu X, Liu Y. (2004), Activation-Induced Cell Death in T Cells and Autoimmunity. Cell Mol Immunol. 1(3):186-92
- Kabelitz D, Janssen O. (1997), Antigen-induced death of T-lymphocytes. Front Biosci. 2:d61-77
- "Oncosis"10 أغسطس 2010.
- Garg AD, Nowis D, Golab J, Vandenabeele P, Krysko DV, Agostinis P (2010). "Immunogenic cell death, DAMPs and anticancer therapeutics: an emerging amalgamation". Biochim Biophys Acta. 1805 (1): 53–71. doi:10.1016/j.bbcan.2009.08.003. PMID 19720113. مؤرشف من الأصل في 20 ديسمبر 2017.