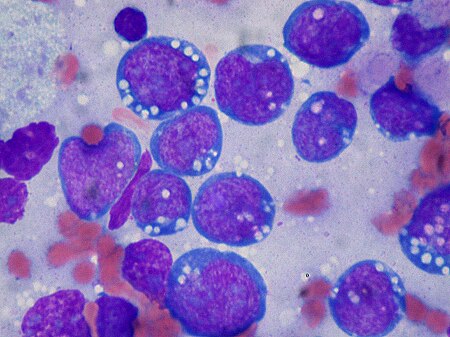
لمفومة بيركت ( Burkitt's lymphoma) (أو ورم بيركت أو لمفومة خبيثة من نمط بيركت) هو سرطان في الجهاز اللمفي (بالتحديد، اللمفاويات البائية). سميت هذه اللمفومة تبعًا لدنيس بارسونس بيركت، الجراح الإيرلندي الذي وصف هذا المرض للمرة الأولى عام 1956 خلال عمله في أفريقيا الاستوائية.[1]
| لمفومة بيركت | |
|---|---|
| معلومات عامة | |
| الاختصاص | علم الدم |
| الأسباب | |
| الأسباب | عدوى فيروس إبشتاين بار |
| الإدارة | |
| أدوية | |
| التاريخ | |
| سُمي باسم | دينيس بارسونز بوركيت |
التصنيف
في الوقت الراهن يمكن تقسيم سرطان بيركيت سريرياً إلى ثلاثة أنواع رئيسية: النوع المستوطن، والنوع المتفرق والنوع المرتبط بنقص المناعة.
- يحدث النوع المستوطن منه (النوع الإفريقي أو الكلاسيكي) في أفريقيا الاستوائية. حيث يعتبر أكثر أنواع السرطانات الخبيثة شيوعًا بين الأطفال في تلك المنطقة، ويعتقد أن الأطفال المصابين بهذا المرض غالبًا ما يكون لديهم ملاريا مزمنة حيث تعمل الأخيرة على خفض المقاومة لفيروس إبشتاين-بار، والسماح له بالبقاء في الجسم. ويصيب هذا النوع بشكل خاص الفك أو عظام الوجه الأخرى، اللفائفي القاصي، الأعور، المبايض، الثدي أو الكلى.
- النوع المتفرق منه (المعروف أيضا باسم "النوع غير الأفريقي") وهو شكل آخر من أشكال سرطان الغدد الليمفاوية اللاهودجكيني الذي وجد خارج أفريقيا.
و الخلايا السرطانية فيه لها مظهرٌ مماثل ٌ للخلايا السرطانية الموجودة في النوع المستوطن. و يعتقد أيضاً أن ضعف المناعة يوفر فرصةً لتطور فيروس ابشتاين بار. سرطانات الغدد الليمفاوية اللاهودجكينية ومن ضمنها سرطان بيركيت، تشكل ما نسبته 30-50٪ من إجمالي سرطانات الغدد الليمفاوية في مرحلة الطفولة. إصابة الفك في هذا النوع أقل شيوعاً مقارنة بالنوع المستوطن، أما منطقة اللفائفي الأعوري فهي المنطقة الأكثر عرضة للإصابة في هذا النوع .
- النوع المرتبط بنقص المناعة وهو غالبًا ما يرتبط بالإصابة بفيروس العوز المناعي البشرية (الإيدز) [2] أو يصيب المرضى بعد عمليات الزرع نتيجةً لتناولهم العقاقير المثبطة للمناعة. ويمكن أن يكون سرطان بيركت من الأمراض المصاحبة للمظاهر الأولية لمرض الايدز.
علماً أنه يكاد يكون من المستحيل تمييز هذه الأنواع الثلاثة من سرطان بيركت بالاعتماد على المظهر المجهري أو الكيمياء المناعية. قد يكون سرطان بيركت المرتبط بنقص المناعة الأكثر تعدداً للأشكال أو قد يحتوي على أعداد أكثر من الخلايا البلازمية ولكن هذه الصفات ليست مميزة له.
علم الأوبئة
يشكل سرطان بيركت 2٪ من الحالات المصابة بمختلف أنواع سرطانات الخلايا الليمفاوية.[3]
خصائص الخلية البائية الخبيثة
تمتلك الخلايا الليمفاوية البائية الطبيعية جينات معاد ترتيبها لسلاسل البروتينات المناعية ( السلاسل الخفيفة والثقيلة) و كل خلية بائية تمتلك تريباً جينيا فريداً للسلسلة الثقيلة(IgH) . و بما أن سرطان بيركت وسرطانات الخلايا الليمفاوية البائية الأخرى تتكاثر بالاستنساخ، فمن المفترض أن تمتلك جميع خلايا الورم السرطانية في المريض الواحد جينات متطابقة للسلسلة الثقيلة (IgH). وعند تحليل الحمض النووي لخلايا الورم باستخدام الرحلان الكهربي(electrophoresis)، يظهر شريط نسيلي (clonal band) لأن جينات (IgH) المتطابقة تتحرك لنفس الموقع . أما عند تحليل العقدة الليمفاوية الطبيعية أو الفاعلة (reactive lymph node) باستخدام التقنية نفسها تظهر لطخة(smear) بدلاً من الشريط النسيلي. هذه التقنية مفيدة لأنه في بعض الأحيان تكون هناك عمليات فاعلة حميدة (مثل كثرة الوحيدات العدوانية infectious mononucleosis ) أو سرطانات الغدد الليمفاوية الخبيثة التي يصعب تمييزها.
الوصف المجهري
يتكون الورم من صفائح من الخلايا الليمفاوية المتماثلة بالشكل والحجم و التي تمتاز بدرجة عالية من النشاط التكاثري والموت الخلوي المبرمج.(Apoptosis) و عند استخدام قوة منخفضة بالمجهر، يظهر الورم كالسماء المليئة بالنجوم (starry sky)[4] و ذلك نتيجة لاحتواء البلاعم (macrophages) على أجسام قابلة للانصباغ وهي عبارة عن بقايا الخلايا السرطانية الميتة. معظم خلايا الورم متوسطة الحجم (أي أن حجم نواة الخلية مماثل لأنوية الخلايا البلعمية النسيجية ( histiocytes)و الخلايا المبطنة لجدران الأوعية الدموية( . و تمتلك الخلية السرطانية كمية قليلة من السيتوبلازم القاعدي. و الإطار المحيط بالخلية غالبا ًما يبدو مربع الشكل.
الكيمياء المناعية
تمتلك الخلايا السرطانية في سرطان بيركيت بشكل عام الواسمات المناعية (markers) المميزة للخلايا البائية الطبيعية وهي (CD20، (CD22,CD19، إضافة إلى امتلاكها واسمات مناعية أخرىCD10 و BCL6. لكنها سالبة بالنسبة ل BCL2 و. TdT ويتم التأكد بنسبة قريبة من 100٪ من النشاط الانقسامي العالي لسرطان بيركت من خلال انصباغ الخلايا عند استخدام Ki67.[5]
علم الوراثة
تتميز جميع أنواع سرطان بيركيت باختلال تنظيم الجين c-myc الموجود على 8q24 ( و تعني الموقع 24 من الذراع القصيرة للكروموسوم الثامن) و يتمثل هذا الاختلال بوجود إحدى الطفرات الجينية الثلاثة.[6]
- أكثر هذه الطفرات شيوعاً (8;14) (q24;q32)[6] و تعني أن الجزء الموجود في الموقع 24 على الذارع القصيرة من الكروموسوم الثامن انتقل إلى الموقع 32 على الذارع القصيرة من الكروموسوم الرابع عشر . و تصيب هذه الطفرة الجينين c-myc و IGH@ [7] و توجد في حوالي 85٪ من الحالات [6] . كما تم العثور على شكل آخر لهذه الطفرة وهو (8;14;18) [7].
- وهناك نوع نادر من الطفرات وهو (2;8) (p12;q24)[8] و تعني أن الجزء الموجود في الموقع 12 على الذارع الطويلة من الكروموسوم الثاني انتقل إلى الموقع 24 على الذارع القصيرة من الكروموسوم الثامن.
و تصيب هذه الطفرة الجينين c-myc و IGK@.
- وهناك نوع آخر نادر من الطفرات وهو (8;22) (q24;q11)[8] و تعني أن الجزء الموجود في الموقع 24 على الذارع القصيرة من الكروموسوم الثامن انتقل إلى الموقع 11 على الذارع القصيرة من الكروموسوم الثاني والعشرين. و تصيب هذه الطفرة الجينين c-myc و IGL@.
و توجد هاتين الطفرتين (8;22) (q24;q11) و (2;8) (p12;q24)في 15٪ من الحالات [6].
العلاج
يشتمل على جرعات مضبوطة من ) EPOCH نظام العلاج الكيميائي لبعض السرطانات الليمفاوية ويضم إيتوبوسيد، بريدنيزون، أونكوفين، سيكلوفوسفاميد، وهيدروكسي دونوروبسين ) بالإضافة إلى الريتوكسن (ريتوكسيماب ) [9]
كما هو الحال في جميع أنواع السرطانات، يعتمد تأثير العلاج الكيميائي على وقت التشخيص. والسرطانات ذات النمو السريع ومنها البيركيت تستجيب للعلاج أسرع من السرطانات ذات النمو البطيء. لكن يمكن أن تكون الاستجابة السريعة للعلاج الكيميائي خطرة على المريض فقد تسبب بظاهرة تسمى "متلازمة انحلال الورم". و من الضروري خلال العلاج الكيميائي مراقبة المريض مراقبةً حثيثة وشرب كميات كافية من الماء.
- سيكلوفوسفاميد
- دوكسوروبيسين
- فينكريستين
- ميثوتريكسيت
- سيتارابين
- إيفوسفاميد
- إيتوبوسيد
- ريتوكسيماب [10]
وطرق العلاج الأخرى هي العلاج المناعي، زراعة نخاع العظم، زراعة الخلايا الجذعية، الجراحة لاستئصال الورم، والعلاج الإشعاعي.
مآل المرض
أظهر العلاج باستخدام جرعات مضبوطة من EPOCHوالريتوكسن ( ريتوكسيماب ) معدل بقاء يصل إلى 8 سنوات في 91٪ من الحالات قليلة الخطورة، و 90٪ من الحالات ذات الخطورة القليلة المتوسطة، و 67٪ من الحالات ذات الخطورة العالية المتوسطة، و 31٪ من الحالات عالية الخطورة، إلى جانب الآثار الجانبية المرتبطة بالعلاج الكيميائي.[9]
مراجع
- Burkitt D (1958). "A sarcoma involving the jaws in African children". The British journal of surgery. 46 (197): 218–23. doi:10.1002/bjs.18004619704. PMID 13628987.
- Bellan C, Lazzi S, De Falco G, Nyongo A, Giordano A, Leoncini L (2003). "Burkitt's lymphoma: new insights into molecular pathogenesis". J. Clin. Pathol. 56 (3): 188–92. doi:10.1136/jcp.56.3.188. PMC . PMID 12610094. مؤرشف من الأصل في 14 ديسمبر 2019.
- Turgeon, Mary Louise (2005). Clinical hematology: theory and procedures. Hagerstown, MD: Lippincott Williams & Wilkins. صفحة 283. .
Frequency of lymphoid neoplasms. (Source: Modified from WHO Blue Book on Tumour of Hematopoietic and Lymphoid Tissues. 2001, p. 2001.)
- Fujita S, Buziba N, Kumatori A, Senba M, Yamaguchi A, Toriyama K (2004). "Early stage of Epstein-Barr virus lytic infection leading to the "starry sky" pattern formation in endemic Burkitt lymphoma". Arch. Pathol. Lab. Med. 128 (5): 549–52. doi:10.1043/1543-2165(2004)128<549:ESOEVL>2.0.CO;2. PMID 15086279.
- . .
- Hoffman, Ronald (2009). Hematology : basic principles and practice ( كتاب إلكتروني PDF ) (الطبعة 5th ed.). Philadelphia, PA: Churchill Livingstone/Elsevier. صفحات 1304–1305. . مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 3 مارس 2016.
- Liu D, Shimonov J, Primanneni S, Lai Y, Ahmed T, Seiter K (2007). "t(8;14;18): a 3-way chromosome translocation in two patients with Burkitt's lymphoma/leukemia". Mol. Cancer. 6: 35. doi:10.1186/1476-4598-6-35. PMC . PMID 17547754.
- Smardova J, Grochova D, Fabian P; et al. (2008). "An unusual p53 mutation detected in Burkitt's lymphoma: 30 bp duplication". Oncol. Rep. 20 (4): 773–8. PMID 18813817. مؤرشف من الأصل في 13 فبراير 2012.
- Wyndham H. Wilson, Kieron Dunleavy, Stefania Pittaluga, Upendra Hegde, Nicole Grant, Seth M. Steinberg, Mark Raffeld, Martin Gutierrez, Bruce A. Chabner, Louis Staudt, Elaine S. Jaffe, and John E. Janik (2008). "Phase II Study of Dose-Adjusted EPOCH-Rituximab in Untreated Diffuse Large B-cell Lymphoma with Analysis of Germinal Center and Post-Germinal Center Biomarkers". Journal of Clinical Oncology. 26 (16): 2717–2714. doi:10.1200/JCO.2007.13.1391. PMC . PMID 18378569.
- Yustein JT, Dang CV (2007). "Biology and treatment of Burkitt's lymphoma". Curr. Opin. Hematol. 14 (4): 375–81. doi:10.1097/MOH.0b013e3281bccdee. PMID 17534164.