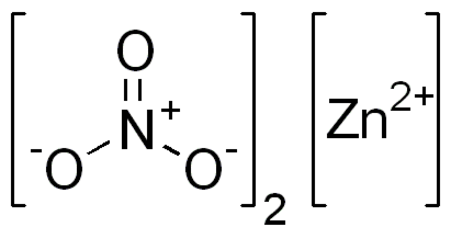
نترات الزنك (أو نترات الخارصين) مركب كيميائي له الصيغة Zn(NO3)2، ويكون على شكل بلورات عديمة اللون.
| نترات الزنك | |
|---|---|
| الاسم النظامي (IUPAC) | |
نترات زنك |
|
| المعرفات | |
| رقم CAS | 7779-88-6 19154-63-3 (رباعي هيدرات) 10196-18-6 (سداسي هيدرات) |
| بوب كيم | 24518 |
| الخواص | |
| الصيغة الجزيئية | Zn(NO3)2 |
| الكتلة المولية | 189.39 غ/مول |
| المظهر | بلورات عديمة اللون |
| الكثافة | 2.065 غ/سم3 (سداسي هيدرات عند 14°س) |
| نقطة الانصهار | 110 °س (لا مائي) |
| الذوبانية في الماء | 184.3 غ/100 مل ماء (سداسي هيدرات) |
| المخاطر | |
| ترميز المخاطر | |
| توصيف المخاطر | |
| تحذيرات وقائية | |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
الخواص
- ينحل نترات الزنك بشكل جيد جداً في الماء، كما توجد منه عدة أشكال مائية بالإضافة إلى الشكل اللامائي، مثل رباعي وسداسي الهيدرات، كما يمكن أن يكون ثنائي أو تساعي الهيدرات.
- يتميز نترات الزنك بخواصه المؤكسدة فهو يتفاعل مع المواد المختزلة بشكل عنيف.
التحضير
تحضر الأشكال المائية من نترات الزنك من تفاعل فلز الزنك مع حمض النتريك الممدد كما في المعادلة:
Zn + 2HNO3 + 6H2O → Zn(NO3)2.6H2O + H2
أما الشكل اللامائي من نترات الزنك فيحصل عليه من تفاعل الزنك مع رباعي أكسيد ثنائي النيتروجين حسب المعادلة:
2Zn + 3N2O4 → 2Zn(NO3)2 + N2
الاستخدامات
- يستخدم لتحضير مركبات الزنك الأخرى، مثل فوسفات الزنك. كما يستخدم كمادة بادئة من أجل الترسيب الكهرضوئي لمركب كبريتيد الزنك. في تطبيق آخر يستعمل محلول نترات الزنك كمادة بادئة لتحضير شرائح رقيقة من طبقات أكسيد الزنك وذلك عن طريق التحلل الحراري.[2]
- يستعمل كمرسخ لوني في صباغة.
المراجع
- معرف بوب كيم: https://pubchem.ncbi.nlm.nih.gov/compound/24518 — تاريخ الاطلاع: 14 أكتوبر 2016 — العنوان : Celloxan — الرخصة: محتوى حر
- S. A. Studenikin, Nickolay Golego, Michael Cocivera (1998). "Optical and electrical properties of undoped ZnO films grown by spray pyrolysis of zinc nitrate solution". J. Appl. Phys. 83 (4). doi:10.1063/1.366944.