| Acide α-linolénique | |
Nomenclature de la chaîne hydrocarbonée 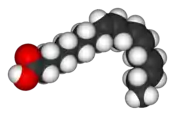 Structure 3D de la molécule d'acide α-linolénique |
|
| Identification | |
|---|---|
| Nom UICPA | acide (9Z,12Z,15Z)-octadéca-9,12,15-triénoïque |
| Synonymes |
ALA |
| No CAS | |
| No ECHA | 100.006.669 |
| No CE | 207-334-8 |
| PubChem | 5280934 |
| ChEBI | 27432 |
| SMILES | |
| InChI | |
| Apparence | liquide incolore |
| Propriétés chimiques | |
| Formule | C18H30O2 [Isomères] |
| Masse molaire[1] | 278,429 6 ± 0,017 1 g/mol C 77,65 %, H 10,86 %, O 11,49 %, |
| Propriétés physiques | |
| T° fusion | −11 °C |
| T° ébullition | 232 °C (23 hPa) |
| Solubilité | Insoluble dans l'eau ; soluble dans les solvants organiques. |
| Masse volumique | 0,914 g·cm-3 à 25 °C |
| Point d’éclair | 113 °C |
| Précautions | |
| SIMDUT[2] | |
Produit non contrôlé |
|
| Directive 67/548/EEC | |
| Composés apparentés | |
| Isomère(s) | Acide γ-linolénique |
| Unités du SI et CNTP, sauf indication contraire. | |
L'acide α-linolénique (ALA) est un acide gras polyinsaturé oméga-3 correspondant à l'acide tout-cis-Δ9,12,15 octadécatriénoïque (18:3). Sa formule brute est C18H30O2 et sa masse molaire 278,43 g·mol-1. C'est un acide carboxylique avec une chaîne de 18 atomes de carbone et trois doubles liaisons cis ; la première des doubles liaisons est positionnée sur le troisième atome de carbone compté depuis la fin de la chaîne, notée ω. C'est le principal acide gras Oméga-3.
L'acide α-linolénique est un acide gras essentiel car il fait partie des aliments, indispensables, non synthétisés par les mammifères. C'est aussi l'acide gras principal qui compose les membranes thylacoïdes des feuilles vertes des plantes. Les plantes vertes et aussi les animaux qui en mangent sont sources de cet acide gras. Certaines graines et donc les huiles tirées de ces graines sont riches en ALA, en particulier les graines de chia, de lin, de cameline, de colza, de chanvre, de soja et les noix. Mais ces huiles et graines contiennent aussi des oméga-6 qui sont en concurrence avec les oméga-3 au niveau cellulaire, alors que leurs effets physiologiques sont opposés.
Effets sur la santé
Des études ont montré qu'une plus grande consommation d'ALA réduisait les risques de maladies cardiovasculaires[3],[4],[5],[6], mais le mécanisme mis en jeu reste obscur. Le corps est capable de convertir l'acide α-linolénique en acide eicosapentaénoïque (EPA) et en acide docosahexaénoïque (DHA), mais on ne sait pas lequel des trois a un effet bénéfique contre l'arythmie cardiaque.
D'une manière générale les études ne permettent pas de mettre en évidence un effet de la consommation d'ALA (ou plus généralement d'oméga-3) sur la prévalence de certains cancers[7],[5],[8], sauf peut-être pour le cancer du sein[9].
Plusieurs études réalisées au tournant du XXIe siècle ont montré une corrélation entre la consommation d'acide α-linolénique, et un risque accru de cancer de la prostate[10],[11]. Ce risque a été évalué indépendamment de la source du composé (viande ou huile végétale par exemple)[12]. Cependant, une méta-analyse plus récente (2009) a mis en évidence des biais dans les publications antérieures et a conclu que dans l'éventualité où l'acide α-linolénique contribue effectivement à un risque accru de cancer de la prostate, l'augmentation de ce risque serait assez faible[13], tandis qu'une étude de 2006 n'avait trouvé aucune association entre l'apport total d'acide α-linolénique et le risque global de cancer de la prostate[14]. Par ailleurs, une étude in vitro de 2013 indique que l'ALA pourrait limiter le développement de cellules cancéreuses sans altérer celui des cellules saines[15].
L'acide α-linolénique pourrait également intervenir dans l'apparition de la dégénérescence maculaire lié à l'âge[16].
D'autres recherches donnent des résultats intéressants in vivo contre l'ischémie[17].
Du point de vue des allégations de santé (réglementées par une autorisation centralisée pour l'Union européenne[18]), l'allégation de santé suivante a été autorisée en 2012: "L'acide alpha-linolénique contribue à l'entretien de taux de cholestérol sanguins normaux" sous conditions que l'aliment possède les propriétés pour être une source d'oméga-3 (Règlement 1924/2006)[19] et que la quantité ingérée d'ALA soit d'au moins 2g/jour.
Références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ « Acide linolénique » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ Alpha-linolenic acid and risk of cardiovascular disease: a systematic review and meta-analysis
- ↑ The cardiovascular effects of flaxseed and its omega-3 fatty acid, alpha-linolenic acid
- 1 2 Dietary alpha-linolenic acid is associated with reduced risk of fatal coronary heart disease, but increased prostate cancer risk: a meta-analysis
- ↑ Rapport de l'AFSSA sur l'intérêt nutritionnel des oméga-3
- ↑ Effects of Omega-3 Fatty Acids on Cancer Risk: A Systematic Review
- ↑ Meta-Analysis of Long-Chain Omega-3 Polyunsaturated Fatty Acids (LCω-3PUFA) and Prostate Cancer
- ↑ Omega-3 fatty acids for breast cancer prevention and survivorship
- ↑ (en) Josep M. Ramon, Ricard Bou, Soledad Romea, M. Eugenia Alkiza, Merce Jacas, Josefa Ribes et Joaquim Oromi, « Dietary fat intake and prostate cancer risk: a case–control study in Spain », Cancer Causes & Control, vol. 11, no 8, , p. 679-685 (lire en ligne) DOI 10.1023/A:1008924116552
- ↑ (en) Ingeborg A. Brouwer, Martijn B. Katan et Peter L. Zock, « Dietary α-Linolenic Acid Is Associated with Reduced Risk of Fatal Coronary Heart Disease, but Increased Prostate Cancer Risk: A Meta-Analysis1,2 », Journal of Nutrition, vol. 134, no 4, , p. 919-922 (lire en ligne)
- ↑ (en) E. De Stéfani, H. Deneo-Pellegrini, P. Boffetta, A. Ronco et M. Mendilaharsu, « Alpha-linolenic acid and risk of prostate cancer: a case-control study in Uruguay », Cancer epidemiology, biomarkers & prevention, vol. 9, no 3, , p. 335-338 (lire en ligne)
- ↑ (en) Joel A Simon, Yea-Hung Chen et Stephen Bent, « The relation of α-linolenic acid to the risk of prostate cancer: a systematic review and meta-analysis », American Journal of Clinical Nutrition, vol. 89, no 5, , p. 1558S-1564S (lire en ligne) DOI 10.3945/ajcn.2009.26736E
- ↑ (en) Daniel O. Koralek, Ulrike Peters, Gerald Andriole, Douglas Reding, Victoria Kirsh, Amy Subar, Arthur Schatzkin, Richard Hayes et Michael F. Leitzmann, « A Prospective Study of Dietary Alpha-linolenic Acid and the Risk of Prostate Cancer (United States) », Cancer Causes & Control, vol. 17, no 6, , p. 783-791 (lire en ligne) DOI 10.1007/s10552-006-0014-x
- ↑ (en) Rashmi Deshpande, Prakash Mansara, Snehal Suryavanshi et Ruchika Kaul-Ghanekar, « Alpha-linolenic acid regulates the growth of breast and cervical cancer cell lines through regulation of NO release and induction of lipid peroxidation », Journal of Molecular Biochemistry, vol. 2, no 1, , p. 6-17 (lire en ligne)
- ↑ Hong Jiang, Xin Shi, Yahui Fan et Duolao Wang, « Dietary omega-3 polyunsaturated fatty acids and fish intake and risk of age-related macular degeneration », Clinical Nutrition (Edinburgh, Scotland), vol. 40, no 12, , p. 5662–5673 (ISSN 1532-1983, PMID 34749130, DOI 10.1016/j.clnu.2021.10.005, lire en ligne, consulté le )
- ↑ Nicole R. Bonetti, Luca Liberale, Alexander Akhmedov et Lisa Pasterk, « Long-term dietary supplementation with plant-derived omega-3 fatty acid improves outcome in experimental ischemic stroke », Atherosclerosis, vol. 325, , p. 89–98 (ISSN 1879-1484, PMID 33915355, DOI 10.1016/j.atherosclerosis.2021.04.005, lire en ligne, consulté le )
- ↑ EU Register of Health Claims
- ↑ Règlement 1924/2006