| Catalase | ||
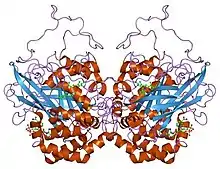
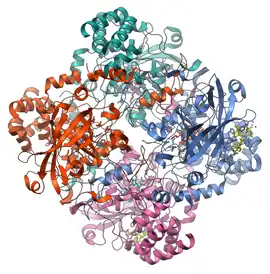 Structure d'une catalase d'érythrocyte humain (PDB 1DGB) | ||
| Caractéristiques générales | ||
|---|---|---|
| Symbole | CAT | |
| N° EC | 1.11.1.6 | |
| Homo sapiens | ||
| Locus | 11p13 | |
| Masse moléculaire | 59 756 Da[1] | |
| Nombre de résidus | 527 acides aminés[1] | |
| HUGO | 1516 | |
| OMIM | 115500 | |
| UniProt | P04040 | |
| RefSeq (ARNm) | NM_001752.3 | |
| RefSeq (protéine) | NP_001743.1 | |
| Ensembl | ENSG00000121691 | |
| PDB | 1DGB, 1DGF, 1DGG, 1DGH, 1F4J, 1QQW | |
|
GENATLAS • GeneTests • GoPubmed • HCOP • H-InvDB • Treefam • Vega | ||
| Liens accessibles depuis GeneCards et HUGO. | ||
Une catalase (du grec kataluein, « dissoudre ») est une oxydoréductase héminique qui catalyse la dismutation du peroxyde d'hydrogène en eau et dioxygène :
Ces enzymes sont formées de quatre chaînes polypeptidiques d’environ 500 résidus d'acides aminés[2], comportant chacune une molécule d'hème. Ces hèmes et leur environnement protéique sont les sites actifs de l'enzyme. Pour catalyser la réaction, l’atome de fer de l'hème réalise une coupure hétérolytique de la liaison O-O du peroxyde d'hydrogène, créant de ce fait une molécule d’eau et un groupe Fe(IV)=O hautement oxydant ; ce dernier peut ensuite oxyder une autre molécule de peroxyde d'hydrogène pour donner du dioxygène. Ce processus est illustré plus spécifiquement par les équations suivantes[3] :
Avec une vitesse maximale de 200 000 réactions catalytiques par seconde, elle est une des enzymes les plus efficaces connues[4]. Sa vitesse de réaction ne semble en effet limitée que par la diffusion, c’est-à-dire par la vitesse limite avec laquelle les molécules parviennent au site actif de l'enzyme. Chez les eucaryotes on la trouve dans le peroxysome des cellules pour la catalase A et dans le cytosol pour la catalase T.
On trouve la catalase chez tous les organismes aérobies et plus particulièrement dans les navets ou dans la plupart des racines des plantes, dans la levure et dans le foie des animaux.

| IUBMB | Entrée IUBMB |
|---|---|
| IntEnz | Vue IntEnz |
| BRENDA | Entrée BRENDA |
| KEGG | Entrée KEGG |
| MetaCyc | Voie métabolique |
| PRIAM | Profil |
| PDB | RCSB PDB PDBe PDBj PDBsum |
| GO | AmiGO / EGO |
Usage en microbiologie

Cette enzyme est utilisée en bactériologie systématique pour l'identification des bactéries. Il s'agit de mettre en contact une colonie de la bactérie à étudier en présence d'eau oxygénée (à 10 volumes). Une effervescence (dû à un dégagement de dioxygène) signe la présence d'une catalase.
Les bactéries anaérobies strictes ne possèdent pas d'enzymes détruisant le peroxyde d'hydrogène provenant des mécanismes aérobies et ne peuvent donc cultiver en aérobiose.
La plupart des bactéries à Gram négatif cultivant en aérobiose possèdent une catalase (catalase +). La recherche de la catalase sur ce type de bactéries ne présente donc aucun intérêt, sauf un sérovar de Shigella dysenteriae.
Pour les bactéries à Gram positif, la recherche de cette enzyme permet de différencier :
- les bactéries des genres Staphylococcus, Listeria, Corynebacterium et Micrococcus (catalase +) ;
- des bactéries des genres Enterococcus, Streptococcus, Pediococcus, Lactococcus et Leuconostoc (catalase -).
Technique
- Sur une lame de verre propre, déposer une goutte de H2O2 une pipette pasteur boutonnée, puis la mettre en contact avec une colonie isolée, prélevée directement avec une anse plastique à usage unique. Il ne faut pas utiliser une anse en "platine" pouvant catalyser la réaction (il est possible de vérifier son inactivité dans une goutte d'eau oxygénée sans bactéries)[5] :
- si des bulles de dioxygène se forment, la bactérie possède la catalase ;
- si rien n'est observable, la bactérie ne possède pas l'enzyme.
Il est déconseillé de faire ce test à partir d'un bouillon de culture ensemencé, car l'enzyme n'est peu produite dans un milieu anaérobie.
En cas de doute sur le résultat, recommencer avec une plus grosse colonie. Il est ensuite possible, en combinant les résultats avec ceux d'autres tests (Gram+, Gram-), de faire des hypothèses sur le type de bactérie.
Attention au prélèvement réalisé sur une gélose au sang frais : le sang a une activité catalasique.
Rôle du test « catalase » dans l'identification d'une espèce
Ce test est important pour la première orientation dans l'identification d'une souche pure bactérienne Gram positive, comme indiqué ci-dessus. L'identification sera poursuivie, en fonction de la coloration de Gram, par une galerie appropriée.
Marqueur biochimique
La catalase « CAT » est un marqueur biochimique de la défense contre des antioxydants. Elle joue un rôle dans la détoxication d'organismes contaminés par des métaux lourds, notamment étudié chez la moule pour le cuivre, le cadmium et le plomb par exemple, pour lesquels on a montré une corrélation positive entre l'activité CAT et le degré de pollution du milieu par ces métaux[6]. Ces derniers s'accumulent chez la moule proportionnellement à la concentration environnementale, induisant une augmentation des excrétions azotées et phosphorées et du relargage, remarquable, de métaux bioaccumulés[6]. Ce processus améliore la protection antioxydante de moules déjà exposées aux métaux. Plus la moule est contaminée par des métaux toxiques, plus son activité CAT est élevée, et inversement, une décontamination des moules se traduit par une diminution de l'activité CAT. La catalase peut donc être utilisée comme biomarqueur de défense antioxydant et bioindicateur « sensible, rapide et efficace » de la qualité et de la santé d'un environnement aquatique[6].
Notes et références
- 1 2 Les valeurs de la masse et du nombre de résidus indiquées ici sont celles du précurseur protéique issu de la traduction du gène, avant modifications post-traductionnelles, et peuvent différer significativement des valeurs correspondantes pour la protéine fonctionnelle.
- ↑ « UniProt », sur www.uniprot.org (consulté le )
- ↑ (en) Mercedes Alfonso-Prieto, Xevi Biarnés, Pietro Vidossich et Carme Rovira, « The Molecular Mechanism of the Catalase Reaction », Journal of the American Chemical Society, vol. 131, no 33, , p. 11751–11761 (ISSN 0002-7863 et 1520-5126, DOI 10.1021/ja9018572, lire en ligne, consulté le )
- ↑ « PDB101: Molecule of the Month: Catalase », sur RCSB: PDB-101 (consulté le )
- ↑ (en) Karen Reiner, « Catalase Test Protocol »
 [PDF], sur asm.org,
[PDF], sur asm.org, - 1 2 3 Kamel Boudjema, Étude des biomarqueurs de la bioaccumulation des métaux traces (cuivre, cadmium et plomb) chez la moule Perna perna Born (1780) exposée à une toxification aigüe (mémoire de magister), (lire en ligne).
Annexes
Articles connexes
- Acatalasia
Liens externes
- Joffin Jean-Noël, Leyral Guy, Dictionnaire des Techniques, CRDP d'Aquitaine réseau Canopé, 2014, 5e édition, 418 p., (ISBN 978-2-8661-7515-3)Notices dans des dictionnaires ou encyclopédies généralistes :
- Ressource relative à la santé :