| Coenzyme A | |
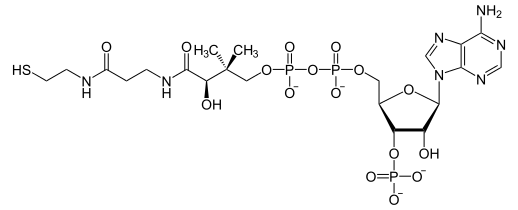  Structure de la coenzyme A |
|
| Identification | |
|---|---|
| Nom UICPA | [(2R,3S,4R,5R)-5-(6-aminopurin-9-yl)-4-hydroxy-3-phosphonooxyoxolan-2-yl]méthyl-diphosphate-[(3R)-3-hydroxy-2,2-diméthyl-4-oxo-4-[[3-oxo-3-(2-sulfanyléthylamino)propyl]amino]butoxy] |
| Synonymes |
CoA ou CoA-SH |
| No CAS | |
| No ECHA | 100.001.472 |
| No CE | 201-619-0 |
| DrugBank | DB01992 |
| PubChem | 68163312 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C21H36N7O16P3S |
| Masse molaire[1] | 767,534 ± 0,031 g/mol C 32,86 %, H 4,73 %, N 12,77 %, O 33,35 %, P 12,11 %, S 4,18 %, |
| Écotoxicologie | |
| LogP | -5,340[2] |
| Unités du SI et CNTP, sauf indication contraire. | |
La coenzyme A (CoA) est une coenzyme de transfert de groupements acyle intervenant dans de très nombreuses voies du métabolisme (cycle de Krebs, bêta-oxydation).
Elle a été isolée la première fois en 1951 par le biochimiste allemand Feodor Lynen (qui reçut en 1964 le prix Nobel) sous la forme d'acétyl-coenzyme A (« acide acétique activé ») à partir de cellules de levure.
Structure
La coenzyme A est composée de différents éléments : un nucléotide, l'adénosine diphosphate (ADP), une vitamine, la vitamine B5 (acide pantothénique) et un acide aminé, la cystéine, légèrement modifiés et liés entre eux.
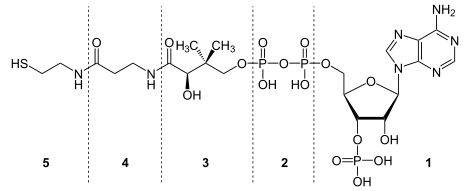
Dans le détail, la coenzyme A est composée :
- de l'adénosine 3'phosphate
- du pyrophosphate
- de l'acide pantoïque (3 + 4 = acide panthoténique)
- de la β-alanine
- de la cystéamine (2-aminoéthanethiol)
Sa partie réactive est la fonction thiol (-SH) de la thioéthanolamine et elle est très souvent symbolisée par HS-CoA (ou CoA-SH).
Biosynthèse
La coenzyme A est synthétisée en 5 étapes, à partir du pantothénate, base conjuguée de l'acide pantothénique (vitamine B5).
- Le pantothénate est phosphorylé en 4'-phosphopantothénate par la pantothénate kinase (PanK; CoaA; CoaX).
- Une molécule de cystéine est ajoutée au 4'-phosphopantothénate par la phosphopantothénoylcystéine synthétase (CoaB) pour former la 4'-phospho-N-pantothénoylcystéine (PPC)
- La PPC est décarboxylée en 4'-phosphopantéthéine par action de la phosphopantothénoylcystéine décarboxylase (PPC-DC, CoaC)
- La 4'-phosphopantéthéine est adénylylatée (ajout d'adénosine monophosphate) pour former le déphospho-CoA par action de l'enzyme phosphopantéthéine adénylyl transférase (CoaD)
- Le déphospho-CoA est finalement phosphorylé en coenzyme A par réaction avec l'ATP par action de la déphosphocoenzyme A kinase (CoaE).
Réactivité avec les acides carboxyliques
Grâce à la fonction thiol de la cystéamine, la coenzyme A est capable de former avec les fonctions carboxyle de certains composés (comme les acides gras par exemple) des thioesters, appelés carboxyl-CoA. Cette liaison thioester est particulièrement riche en énergie.
CoA-SH + R-COOH → CoA-S-CO-R ( + H2O )
La coenzyme A participe ainsi directement (en tant qu'acyl-CoA) au métabolisme des graisses, et indirectement (en tant qu'acétyl-CoA) au métabolisme des glucides et des protéines.
On dit que la coenzyme A, à travers les liaisons thioesters fortement énergétiques qu'elle forme avec ses partenaires, « active » ces derniers, et leur permet ainsi de participer à des réactions auxquelles ils ne participeraient pas s'ils n'étaient pas activés par la coenzyme.
Principaux thioesters carboxyl-CoA
- acétyl-CoA
- Propionyl-CoA
- Acétoacétyl-CoA
- Coumaroyl-CoA (intervenant dans la biosynthèse des flavonoïdes et des coumarines)
- Acyles d'acides dicarboxyliques
- Malonyl-CoA
- Succinyl-CoA
- HMG-CoA (intervenant dans la biosynthèse des terpénoïdes)
- 3-méthylglutaconyl-CoA
- Méthylmalonyl-CoA
- Pimelyl-CoA (intervenant dans la biosynthèse de la biotine/Vitamine B8)
- Butyryl-CoA
Sources en CoA
Notes et références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ (en) « Coenzyme A », sur ChemIDplus