Une liaison covalente est une liaison chimique dans laquelle deux atomes se partagent deux électrons (un électron chacun ou deux électrons venant du même atome) d'une de leurs couches externes afin de former un doublet d'électrons liant les deux atomes. C'est une des forces qui produisent l'attraction mutuelle entre atomes.
La liaison covalente implique généralement le partage équitable d'une seule paire d'électrons, appelé doublet liant. Chaque atome fournissant un électron, la paire d'électrons est délocalisée entre les deux atomes. Le partage de deux ou trois paires d'électrons s'appelle respectivement « liaison double » et « liaison triple ».
Au contraire des liaisons ioniques où les atomes sont liés par attraction coulombienne non-directionnelle, les liaisons covalentes sont fortement directionnelles. En conséquence, les molécules liées par covalence tendent à adopter des formes caractéristiques possédant des angles de liaison spécifiques.
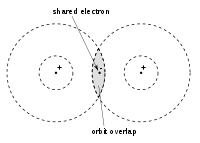
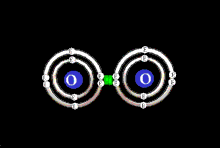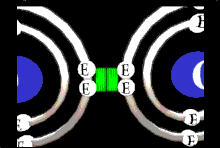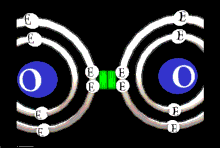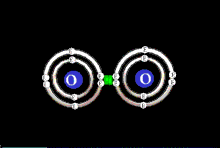
Une liaison covalente est une liaison dans laquelle deux électrons de valence sont partagés entre deux non-métaux. Dans ce type de liaison, il doit y avoir une différence d’électronégativité inférieure à 1,7 sur l’échelle de Pauling. Il y a formation d’une liaison covalente (sauf pour les liaisons de coordinence) lorsqu’il y a un recouvrement de deux orbitales atomiques ayant chacune un électron de valence. Grâce à ce recouvrement, il y aura la formation d’une seule et unique orbitale commune comme le montre la figure plus bas. Ce recouvrement d’orbitales atomiques conduit à la formation d’une orbitale moléculaire (non illustrée). Il y a un partage d’électrons entre deux atomes d’hydrogène afin de former une seule molécule de dihydrogène. Cette liaison covalente est présentée comme étant : H–H.
Histoire
L'idée de la liaison covalente remonte à Lewis, qui en 1916 décrit le partage de paires d'électrons entre atomes[1]. Il présenta la « notation de Lewis » dans laquelle les électrons de valence (de la couche électronique externe) sont représentés comme des points autour des symboles atomiques. Les paires d'électrons situés entre les atomes représentent les liaisons covalentes et les paires multiples représentent des liaisons doubles ou triples.
Tandis que l'idée des paires partagées d'électrons fournit une image qualitative efficace de la liaison covalente, la mécanique quantique est nécessaire pour comprendre la nature de ces liaisons et pour pouvoir prévoir les structures et les propriétés des molécules simples. En 1927, Walter Heitler et Fritz London furent crédités de la première explication quantique correcte de la liaison chimique, spécifiquement celle de la molécule de dihydrogène[2].
Leur travail était basé sur le modèle de liaison de valence, qui suppose qu'une liaison chimique est formée lorsqu'il y a un bon recouvrement entre orbitales atomiques. Ces orbitales sont connues pour avoir des angles spécifiques les unes avec les autres. Le modèle de la liaison de valence peut donc prévoir avec succès les angles de liaison observés dans des molécules simples.
Aujourd'hui le modèle des liaisons de valence a été en grande partie supplanté par le modèle des orbitales moléculaires. Dans ce modèle, lorsque les atomes se rapprochent, leurs orbitales atomiques interagissent et forment alors un ensemble d'orbites moléculaires qui s'étend sur toute la molécule.
La moitié de ces orbites tend à être des orbitales liantes et l'autre moitié anti-liantes.
Les électrons des orbitales liantes provoquent la formation d'une liaison chimique, alors que ceux des orbitales anti-liantes tendent à les empêcher. La formation d'une liaison chimique n'est possible que lorsque les électrons occupant des orbitales liantes sont plus nombreux que ceux occupant des orbitales anti-liantes.
Ordre de liaison
La différence entre le nombre de paires d'électrons contenues dans des orbitales liantes et anti-liantes détermine l'ordre de liaison.
Par exemple, dans une molécule diatomique, il y a une liaison simple qui se forme s'il y a un excès de deux électrons dans les orbitales liantes (H2), une liaison double si quatre électrons sont en excès (O2) et une liaison triple si cet excès est de six électrons (N2). Les liaisons triples sont relativement rares dans la nature ; on en trouve par exemple dans le monoxyde de carbone (CO).
L'ordre de liaison n'a pas besoin d'être un nombre entier et les liaisons peuvent être délocalisées sur plus de deux atomes. Par exemple, dans le benzène, l'ordre de liaison entre deux atomes de carbone adjacent est de 3/2. Les électrons des orbitales liantes sont répartis uniformément sur chacun des 6 atomes de carbone : c'est la résonance (chimie). D'autres exemples sont les anions dérivés du dioxygène O2 : l'ajout d'électrons dans des orbitales π* antiliantes fait passer l'ordre de liaison de 2 à 3/2 pour le superoxyde O2− et à 1 pour le peroxyde O22−.
Les longueurs et les énergies de dissociation des liaisons sont inversement proportionnelles à l'ordre de liaison : plus l'ordre de liaison est élevé, plus cette liaison est courte et forte.
Lorsque les électrons sont délocalisés sur de nombreux atomes, on a une liaison métallique.
Liaison covalente et électronégativité
La liaison covalente se produit le plus fréquemment entre des atomes d'électronégativités semblables. La différence de niveau d'énergie entre les deux atomes n'est pas suffisante pour produire le transfert d'électrons d'un atome vers l'autre. Cependant, la répartition des électrons dans une liaison covalente entre atomes différents ne sera pas exactement symétrique. En effet, la densité électronique sera déplacée vers l'atome le plus électronégatif : la liaison covalente est polarisée. La direction de la polarisation est donnée par des charges partielles (Δ+ pour l'atome le moins électronégatif et Δ- pour le plus électronégatif). Plus la différence d'électronégativité est grande entre les atomes, plus les charges partielles sont élevées : la liaison est polarisée et a un caractère « ionique ». Les liaisons covalentes sont plus communes entre non-métaux, tandis que la liaison ionique est plus fréquente lorsqu'un ou chacun des deux atomes est un métal.
Dans une liaison comme H–Cl, les électrons ne sont pas rigoureusement au centre de la liaison. En effet, le noyau du chlore (Z = 17) contient 17 protons tandis que l'hydrogène (Z = 1) n'en contient qu'un seul. Par conséquent, des électrons de valence placés entre les deux noyaux seront plus attirés par le noyau du chlore que par le noyau de l'hydrogène.
L'électronégativité est ainsi une grandeur servant à décrire par quel atome les électrons seront le plus attirés.
Enthalpie de liaison
Dans une liaison covalente, plus le nombre de liaisons augmente, plus cela requiert de l'énergie pour les briser. Le bris d'une liaison covalente est un processus endothermique (qui requiert de l'énergie) tandis que la formation d'une liaison covalente est un processus exothermique. Pour calculer la variation d'enthalpie dans une réaction chimique, il est nécessaire de calculer la différence entre l'énergie requise pour rompre les liaisons dans les réactifs et l'énergie requise pour former les liaisons dans les produits :
- ΔrH = ∑D (liaisons rompues des réactifs) – ∑D (liaisons formées des produits)
- où D représente l'énergie de liaison par mole de liaison et est toujours affecté d'un signe positif.
Par exemple, pour déterminer si la réaction
- H2(g) + Cl2(g) → 2 HCl(g)
est exothermique ou endothermique à l'aide de la formule précédente :
- sachant que D(H–H) = 432 kJ/mol, D(Cl–Cl) = 239 kJ/mol et D(H–Cl) = 427 kJ/mol[3],
- ΔrH = D(H–H) + D(Cl–Cl) − 2 D(H–Cl)
- ΔrH = 432 + 239 − (2 × 427) = −183 kJ/mol.
Cette réaction est exothermique : il est donc plus favorable de former HCl.
Cas de la molécule de dihydrogène

Il y a une variation de l'énergie potentielle du système lors du rapprochement de deux atomes d'hydrogène. L'énergie potentielle relative du système est égale à zéro, lorsque les deux atomes d'hydrogène sont isolés et extrêmement éloignés l'un de l'autre. Cette énergie potentielle nette est l'énergie qui se définit comme étant l'attraction et la répulsion entre des particules chargées qui sont, dans ce cas, les électrons (charge négative) et les protons (charge positive). Il y a une répulsion lorsque deux protons ou encore deux électrons essaient de s'approcher et il y a une attraction lorsqu'un électron et un proton essaient de s'approcher. Puisque naturellement, un système tend à atteindre un état d'énergie minimale, la formation d'une molécule de dihydrogène H2 avec deux atomes d'hydrogène isolés est favorable, puisque cela demande moins d'énergie. Lorsque les noyaux des atomes d'hydrogène se rapprochent l'un de l'autre, l'énergie potentielle diminue jusqu'au moment où la distance entre les noyaux est de 74 pm, ce qui correspond au niveau énergétique minimum du système. Si la distance entre les noyaux des atomes d'hydrogène devient inférieure à 74 pm, l'énergie potentielle augmente à cause des répulsions. Donc, une liaison covalente a des effets au niveau de l'énergie.
Propriétés électroniques de la liaison covalente
En utilisant les résultats de la mécanique quantique, il est en théorie possible de calculer la structure électronique, les niveaux d'énergie, les distances et les angles de liaisons, les moments dipolaires et le spectre électromagnétique de molécules simples. Malheureusement, en pratique, les distances et les angles de liaisons ne peuvent pas être raisonnablement prévues par la mécanique quantique car les calculs sont trop lourds et trop complexes. À la place, on utilise des approximations sans réel fondement théorique (méthodes de Slater), mais qui donnent des résultats plutôt précis.
En ce qui concerne les molécules plutôt simples, les calculs des niveaux d'énergie aboutissent généralement à des résultats assez précis pour déterminer l'Enthalpie standard de formation et l'énergie de la barrière d'activation cinétique de celles-ci.
Notes et références
- ↑ (en) Gilbert N. Lewis, « The Atom and the Molecule », J. Am. Chem. Soc., vol. 38, no 4, , p. 762–785 (DOI 10.1021/ja02261a002)
- ↑ (de) W. Heitler et F. London, « Wechselwirkung neutraler Atome und homöopolare Bindung nach der Quantenmechanik », Z. Phys., vol. 11, no 3, , p. 455-472 (DOI 10.1007/BF01397394)
- ↑ S. Zumdahl, S., Chimie générale, 2e éd., Les Éditions CEC Inc., 1998, p. 247, tableau 6.4
Voir aussi
Bibliographie
- Chang, R. et Papillon, L. Chimie fondamentale, principes et problèmes, Les Éditions de la Chandelière Inc., 1998, p. 275
- S. Zumdahl, S., Chimie générale, 2e éd., Les Éditions CEC Inc., 1998, p. 243-249
- L. Dekock, R.B. et Gray, H., Chemical structure and bonding, Copyright, 1980, p. 82-86