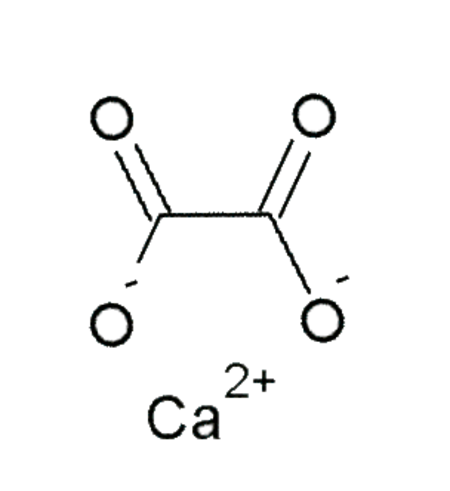
أكسالات كالسيوم مركب كيميائي له الصيغة CaC2O4 ، ويكون على شكل مسحوق بلوري أبيض إبري، وهو ملح الكالسيوم لحمض الأكساليك. يوجد منه شكل مائي أحادي الهيدرات، حيث تدخل جزيئة ماء في البنية البلورية.
| أكسالات الكالسيوم | |
|---|---|
| الاسم النظامي (IUPAC) | |
إيثان ديوات الكالسيوم |
|
| المعرفات | |
| رقم CAS | 563-72-4 5794-28-5 (أحادي هيدرات) |
| بوب كيم | 33005 |
| الخواص | |
| الصيغة الجزيئية | CaC2O4 |
| الكتلة المولية | 128.10 غ/مول |
| المظهر | بلورات بيضاء أبرية |
| نقطة الانصهار | 200 °س (فقدان الماء البلوري) |
| الذوبانية في الماء | غير منحل عملياً في الماء |
| المخاطر | |
| ترميز المخاطر | |
| توصيف المخاطر | |
| تحذيرات وقائية | |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
الخواص
- أكسالات الكالسيوم غير منحل عملياً في الماء، لكنه ينحل في الحموض المعدنية الممددة.
- بتسخين المركب إلى درجة حرارة بين 180 و200°س يبدأ المركب أحادي الهيدرات بفقدان الماء البلوري ويتحول إلى الشكل الخالي من الماء. بمتابعة التسخين يتفكك المركب إلى كربونات الكالسيوم وأحادي أكسيد الكربون.
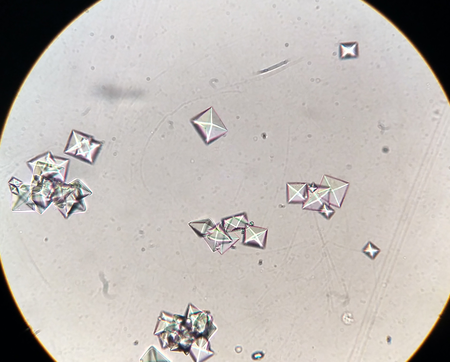
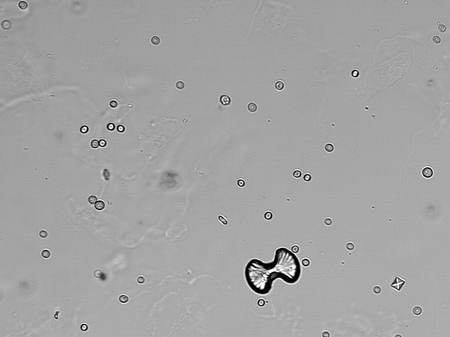
- تتبع بلورات أكسالات الكالسيوم تتبع النظام البلوري المعيني القائم.
الوفرة الطبيعية والتحضير
يدخل مركب أكسالات الكالسيوم في تركيب الحصى الكلوية. كما يوجد في بعض النباتات مثل ديفنباخيا والقلقاس، كما يوجد في بعض أوراق الراوند. يمكن أن يعثر على مركب أكسالات الكالسيوم في الطبيعة أيضاً على شكل معدن ويْـويليت Whewellite.
يحضر أكسالات الكالسيوم مخبرياً كناتج ثانوي من عملية تحضير حمض الأكساليك، حيث يتفاعل أكسالات الصوديوم مع هيدروكسيد الكالسيوم حيث يترسب أكسالات الكالسيوم من المحلول. للحصول على حمض الأكساليك يضاف حمض الكبريتيك لاحقاً.
Na2C2O4 + Ca(OH)2 → CaC2O4 + 2NaOH
الاستخدامات
نظراً لعدم انحلالية مركب أكسالات الكالسيوم فإنه يستخدم في الكيمياء التحليلية للتحليل الكمي لأيونات الكالسيوم.
معرض صور
المصادر
- معرف بوب كيم: https://pubchem.ncbi.nlm.nih.gov/compound/33005 — تاريخ الاطلاع: 18 نوفمبر 2016 — العنوان : CALCIUM OXALATE — الرخصة: محتوى حر
- موسوعة رومب الكيميائية Römpp Lexikon Chemie, Georg Thieme Verlag