اضطراب تعاطي المواد الأفيونية هي حالة طبية تتميز بنمط إشكالي من أشباه الأفيون التي تسبب مشاكل أو اضطرابات خطيرة طبيًا.[1] وغالبًا ما يتضمن هذا رغبة قوية في استخدام المواد الأفيونية، وزيادة تحمل الدواء لأشباه الأفيونيات ولظهور ما يُعرف بمتلازمة الانسحاب عند توقف تعاطي الأفيون فجأة.[2][3] الإدمان والاعتماد هي مكونات اضطراب تعاطي المخدرات ويمثل الإدمان أشد أشكال تلك الاضطرابات.[2][4] يمكن أن يظهر الاعتماد على الأفيون في صورة اعتماد جسدي، أو اعتماد نفسي، أو كليهما.[2][5]
| إدمان الأفيون | |
|---|---|
| معلومات عامة | |
| الاختصاص | طب نفسي |
| من أنواع | إدمان، وتعاطي المخدرات |
| الإدارة | |
| أدوية | |
تشمل المواد الأفيونية مواد مثل المورفين، والهيروين، والكودين وأوكسيكودون، والتي يمكن شراؤها بطريقة غير قانونية أو موصوفة. غالبًا ما يعتمد تشخيص اضطراب تعاطي مواد الأفيون على معايير الجمعية الأمريكية للأطباء النفسيين في الدليل التشخيصي والإحصائي للاضطرابات النفسية.[6] وتشمل هذه المعايير الانشغال بالرغبة في الحصول على المواد الأفيونية واستخدامها، فضلًا عن استخدامها أكثر من مجرد الرغبة في تعاطيها على الرغم من العواقب الاجتماعية والمهنية الناجمة عن هذه السلوكيات.[3]
يمكن علاج اضطراب تعاطي المواد الأفيونية باستخدام العلاج بالبدائل الأفيونية باستخدام الميثادون أو البيوبرينورفين).[7] يقلل وجود مثل هذا العلاج من خطر الوفاة.[7] بالإضافة إلى ذلك، قد يستفيد الأفراد الذين يعانون من اضطراب تعاطي شبائه الأفيون من اثني عشر خطوة في برامج الدعم التي يقدمها مهنيوا الصحة النفسية مثل العلاج الفردي أو الجماعي.[8] كما يعتبر النالوكسون مفيدًا في علاج الجرعة الزائدة من المواد الأفيونية.[9]
في عام 2013 أثرت اضطرابات استخدام المواد الأفيونية على حوالي 0.4٪ من الناس،[6] إذ تأثر حوالي 16 مليون شخص في وقت واحد.[10] وأدى ذلك إلى وفاة 122,000 شخص في جميع أنحاء العالم في عام 2015،[11] مقارنةً ب 18,000 حالة وفاة في عام 1990.[12] في الولايات المتحدة في عام 2015 كان هناك 33,000 حالة وفاة بسبب تعاطي جرعات زائدة من المخدرات التي تنطوي على المواد الأفيونية.[13] ومن بين 000 33 حالة وفاة، كان هناك حوالي 15000حالة وفاة ناجمة عن تعاطي الأفيون الموصوف من قبل الأطباء و000 13 من الهيروين.[14][15]
الأفيون عبارة عن العصارة اللبنية التي تفرزها ثمار نبات الخشخاش غير الناضجة. ويحتوي الأفيون على عدد كبير من المركبات الكيميائية إلا أن أهمها مركب المورفين الذي يستخدم طبياً كمهدئ للآلام ويعتبر من أقوى المركبات الطبيعية في إيقاف الألم. ويعتبر المورفين المادة الأساسية لتحضير الهيروين وعليه فإن الهيروين هو أحد مشتقات الأفيون. ويعتبر الأفيون والمورفين والهيروين من المخدرات التي تثبط الجهاز العصبي المركزي وتسبب الفتور وجميعهم يسبب الاعتماد النفسي والاعتماد العضوي لدى الشخص الذي يتعاطاها بدون إشراف طبي دقيق. والهيروين لا يستخدم في الأغراض الطبية ويساء استخدامه في غير الأغراض الطبية.
الأفيون عبارة عن العصارة اللبنية التي تفرزها ثمار نبات الخشخاش غير الناضجة. ويحتوي الأفيون على عدد كبير من المركبات الكيميائية إلا أن أهمها مركب المورفين الذي يستخدم طبياً كمهدئ للآلام ويعتبر من أقوى المركبات الطبيعية في إيقاف الألم. ويعتبر المورفين المادة الأساسية لتحضير الهيروين وعليه فإن الهيروين هو أحد مشتقات الأفيون. ويعتبر الأفيون والمورفين والهيروين من المخدرات التي تثبط الجهاز العصبي المركزي وتسبب الفتور وجميعهم يسبب الاعتماد النفسي والاعتماد العضوي لدى الشخص الذي يتعاطاها بدون إشراف طبي دقيق. والهيروين لا يستخدم في الأغراض الطبية ويساء استخدامه في غير الأغراض الطبية.
الأعراض والعلامات
تشمل الأعراض والعلامات الآتي:[3][6]
- سلوك البحث عن المخدرات
- حيازة وصفات طبية متعددة من مختلف مقدمي الخدمات
- زيادة الجرعات مع مرور الوقت
- الشهوة الأفيونية
- مضاعفات طبية متعددة من تعاطي المخدرات مثل الإيدز، ودخول المستشفيات عدة مرات، والخراجات (خراج (طب)))
- العواقب القانونية أو الاجتماعية الثانوية لاستخدام المخدرات
- أعراض الانسحاب
- الإمساك
أعراض الانسحاب
تشمل أعراض الانسحاب من المواد الأفيونية، ولكنها لا تقتصر عليها:[16]
الأعراض المبكرة
- تغيرات درجة الحرارة
- الانفعال
- القلق
- تغيير في الرغبة الجنسية (ابصورة غير طبيعية أو منخفضة)
- الجفاف
- التعب
- آلام العضلات
- الضباب العقلي / الارتباك / عدم وجود الحافز
- الأرق
- تململ الساقين
- سيلان في الانف
- التعرق
- التثاؤب
- الشعور بتنميل البشرة
الأعراض المتأخرة
- التشنج في البطن
- الإسهال
- اتساع حدقة العين
- قشعريرة
- الغثيان
- القيء
متلازمة السمية
تشمل أعراض وعلامات متلازمة السمية الآتي:[3]
الجرعة الزائدة
تشمل الأعراض التالية علامات وأعراض تناول جرعات زائدة من الأفيون، لكنها لا تقتصر عليها:[17]
- تقبض الحدقة
- انخفاض معدل ضربات القلب
- انخفاض درجة حرارة الجسم
- انخفاض معدل التنفس
- تغير مستوى الوعي. قد يكون المدمنين غير قادرين على الاستجابة أو في حالة اللاوعي.
- الوذمة الرئوية (تراكم السوائل في الرئتين)
- الصدمة
- الموت
الاسباب
وقد ثبت أن معظم الذين يتعاطون الأفيون يعانون من واحد على الأقل من الأمراض النفسية المرافقة[18] المواد الأفيونية هي مسكنات ممتازة للألم الحاد، بالإضافة إلى قدرتها على إنتاج النشوة التي تجذب المدمنين.[19] يمكن أن يتطور اضطراب تعاطي المواد الأفيونية نتيجةً للعلاج الذاتي، على الرغم من أن هذا الأمر مازال محل جدل.[18] وقد أخذت نظم التقييم في الاعتبار احتمال إدمان الأفيون في مرضى الألم المزمن.[20]
وطبقًا لأوراق المنشورة المتعلقة بمعالجة الاعتماد على المواد الأفيونية والتي نشرها مكتب الأمم المتحدة المعني بالمخدرات والجريمة ومنظمة الصحة العالمية (منظمة الصحة العالمية)، ينبغي على مقدمي الرعاية ألا يعالجوا اضطراب تعاطي المواد الأفيونية الناتج عن ضعف الإرادة.[21][22] بالإضافة إلى ذلك، لا يشكل إزالة السموم وحده العلاج المناسب.
الآلية
بالإضافة لتخفيف الاوجاع، يؤثر الافيون على جهاز الاعصاب المركزي اذ يؤدي لانخفاض التناغم العاطفي والحسي فيها ولشعور بالنشوة. يعتبر المورفين نموذجًا للافيون وله مشتقات كثيرة. يتم تعريف الإدمان على الافيون على انه التعاطي المستمر للافيون رغم الضرر الكبير الذي يلحقة بالإدراك المعرفي، السلوك والحالة النفسية. يؤدي الاستعمال المتكرر إلى التعود على الافيون، وإلى ظواهر الفطام أو استخدام الافيون غير المحدود.
الإدمــــــان
الإدمان هو اضطراب في الدماغ يتميز باستمرار تعاطي المخدرات القهري بصورة قهرية على الرغم من العواقب السلبية.[4][23][24][25] الإدمان هو أحد مكونات اضطراب تعاطي المخدرات ويمثل أشد شكل من أشكال هذا الاضطراب.[4]
يلعب زيادة التعبير الجيني لعامل النسخ الجيني "ΔFosB" في النواة المتكئة دورا حيويا في تطوير إدمان المواد الأفيونية عن طريق تحوير السلوكيات التي تسعى للمخدرات القهرية بشكل مباشر.[23] ومثل أي حالة من حالات الإدمان، يرفع إدمان الأفيون من زيادة التعبير الجيني لعامل النسخ الجيني "ΔFosB" في النواة المتكئة.[23][26][27][28][29][30]
الإدمان هو عبارة عن اضطراب سلوكي يُظهر تكرار لفعل من قبل الفرد لكي ينهمك بنشاط معين بغض النظر عن العواقب الضارة بصحة الفرد أو حالاته العقلية أو حياته الاجتماعية. العوامل التي تم اقتراحها كأسباب للإدمان تشمل عوامل وراثية، بيولوجية، دوائية واجتماعية. الافيون فعال جدا في تخفيف الاوجاع المزمنة والاوجاع الحادة، ولكن هذه المواد تحمل في ثناياها خطر الإدمان. كمية المدمنين على الهيروين (نوع من الافيون) في الولايات المتحدة مرتفعة منذ التسعينيات وتزداد بشكل ملحوظ حسب التقديرات، أما بالنسبة للأفيون، يمكنك إضافة قرابة 100 الف شخص إضافي.
أظهر التصوير العصبي تغييرات وظيفية وهيكلية في دماغ المدمنين.[31] وأظهرت دراسة أجريت في عام 2017 أن التناول المزمن للأفيون، مثل الهيروين، قد يسبب تأثيرًا طويل الأجل في منطقة المدار الجبهي، وهي منطقة ضرورية لتنظيم السلوكيات المرتبطة بالمكافأة، والاستجابات العاطفية، والقلق.[32] بالإضافة إلى ذلك، أظهرت الدراسات العصبية والدراسات العصبية النفسية عدم انتظام الدوائر المرتبطة بالعاطفة والإجهاد والانبساطية العالية.[33]
مستقبلات الأفيونات
وقد ثبت وجود أساس جيني لفعالية المواد الأفيونية في علاج الألم لعدد من الاختلافات المحددة؛ ومع ذلك، لا تزال الأدلة على الاختلافات الطبية في آثار المواد الأفيونية غامضة. وقد لعب علم الصيدلة الجيني لمستقبلات الأفيونيات والتنشؤ الداخلي للربيطات دورًا حيويًا في الدراسات المتعلقة. اختبرت هذه الدراسات على نطاق واسع عدد من الأنماط الظاهرية)، بما في ذلك الاعتماد على المواد الأفيونية، والاعتماد على الكوكايين، والاعتماد على الكحول، والاعتماد على الميثامفيتامين والذهان، والاستجابة لعلاج النالتريكسون، وسمات الشخصية، وغيرها من الأنماط الظاهرية الأخرى. تم الإبلاغ عن المتغيرات الرئيسية والثانوية نتيجةً (لإدمان المخدرات) لكل جين مسؤول عن الترميز لتلك المستقبلات والربيطات، فضلًا عن المناطق التنظيمية. اتخذت النهج الأحدث طريقًا بعيدًا بتحليل جينات في مناطق محددة بعيناه في الجينوم بأكمله، وتستند إلى شاشة غير متحيزة من الجينات في جميع أنحاء الجينوم بأكمله، والتي ليس لها علاقة واضحة بالنمط الظاهري. أسفرت الدراسات المتعلقة بالجينوم البشري عن عدد من الجينات المتورطة في هذا الأمر، على الرغم من أن العديد منها يرمز إلى بروتينات غير مترابطة على ما يبدو في بعض العمليات مثل التصاق الخلايا، والتنظيم النسخي، وتحديد بنية الخلية، والحمض النووي الريبوزي، والحمض النووي الريبوزي منقوص الأكسجين، ومعالجة البروتين.[34]
حاليا، لا توجد توصيات بالجرعات المحددة للمواد الأفيونية بسبب عدم وجود دليل واضح يربط الجينات بتأثير المخدرات، أو سميتها، أو احتمال الإصابة بالاعتماد.
جين 118A> G
في حين تم تحديد أكثر من 100 متغير لمستقبلات ميو الأفيونية، فإن معظم مستقبلات ميو- تعتبر متغير غير مترادف لجين 118A> G، والذي يؤدي إلى تغييرات وظيفية للمستقبل، بما في ذلك انخفاض توافر الموقع الملزم، وانخفاض الحمض النووي الريبوزي الرسول، وتغيير إشارة التنبيه، وزيادة تقارب البيتا إندورفين. من الناحية النظرية، كل هذه التغييرات الوظيفية من شأنها أن تقلل من تأثير المواد الأفيونية الخارجية، مما يتطلب جرعة أعلى لتحقيق نفس التأثير العلاجي. وهذا يشير إلى إمكانية لزيادة قدرة الإدمان في هؤلاء الأفراد الذين يحتاجون إلى جرعات أعلى لتحقيق السيطرة على الألم. ومع ذلك، فإن الأدلة التي تربط بين البديل 118A> G والاعتماد على المواد الأفيونية مختلطة، مع إظهار بعض الأمور المعقدة في عدد من مجموعات الدراسة، ولكن كانت النتائج السلبية في مجموعات أخرى. أحد التفسيرات للنتائج المختلطة هو إمكانية وجود متغيرات أخرى تكون في اختلال التوازن الارتباطي مع المتغير 118A> G وبالتالي تساهم في الأنماط الفردية المختلفة التي ترتبط بشكل أكثر تحديدًا مع الاعتماد على المواد الأفيونية.[35]
جينات المستقبلات غير الأفيونية
يرمز جين البريبرينكيفالين، إلى الأفيونات الذاتية التي تعدل الإحساس بالألم، وتدخل في مساعر الثواب والإدمان. ارتبط تكرار (كا) في تسلسل 3 'المرافق لجين البريبرينكيفالين مع احتمال أكبر من تطوير الاعتماد على الأفيون في الدراسات المتكررة. وقد ارتبط التغير في جين MCR2، وترميز مستقبلات الميلانوكورتين 2 بالآثار الواقية وزيادة احتمالية تطوير الإدمان على الهيروين. كما يلعب جين CYP2B6 من عائلة (سيتوكروم بي 450) دورًا أيضًا في تكسير المواد الأفيونية وبالتالي قد يلعب هذا دورًا في تطوير الاعتماد وتعاطي الجرعات الزائدة.[36]
التشخيص
تتطلب القواعد الإرشادية للدليل التشخيصي والإحصائي للاضطرابات النفسية وجود اضطرابات أو إعاقات تتعلق بتعاطي الأفيون لتشخيص إدمان الأفيون. يجب وجود معيار أو اثنين من المعايير الآتية خلال سنة محددة لتشخيص إدمان الأفيون:[6]
- تناول المزيد من المواد الأفيونية أكثر من المقصود.
- عدم قدرة على تقليل كمية المواد الأفيونية المستخدمة
- استهلاك كميات كبيرة من الوقت في محاولة الحصول على المواد الأفيونية، واستخدام المواد الأفيونية، أو التعافي من أخذها
- رغبة الفرد الشديدة للمواد الأفيونية
- صعوبة أداء الواجبات المهنية في العمل أو المدرسة
- استمرار استخدام المواد الأفيونية مما يؤدي إلى عواقب اجتماعية وعائقات شخصية
- انخفاض الأنشطة الاجتماعية أو الترفيهية
- استخدام المواد الأفيونية على الرغم من خطورتها جسديًا
- استمرار استخدام المواد الأفيونية على الرغم من تفاقم الحالة البدنية أو النفسية (مثل الاكتئاب، والإمساك)
- تحمل الدواء)
- الأعراض انسحابية)
الوقاية
توجد جهود عدة لخفض عدد المواد الأفيونية الموصوفة في محاولة للحد من اضطراب تعاطي شبائه الأفيون والوفيات المتصلة باستعمال شبائه الأفيون.
الوفيات المرتبطة بالمواد الأفيونية
يستخدم النالوكسون، ومضادات المستقبلات الأفيونية، لتقليل خطر الوفاة بسبب الجرعات الزائدة للمواد الأفيونية.[9] ويوصى باستخدام مجموعات النالوكسون للأشخاص العاديين الذين يتعاطون جرعة زائدة من المواد الأفيونية، وللأشخاص الموصوف لهم وصفات طبية كبيرة لشبائه الأفيون، أو أولئك الذين يستخدمون برامج علاج استخدام المواد، أو الذين تم إطلاق سراحهم مؤخرا من السجن.[9]
علاج إدمان الافيون
ينطوي العلاج ببدائل الأفيون، والذي يسمى أيضًا العلاج بالإبداع الأفيوني أو العلاج بالصيانة الأفيونية، على استبدال أشباه الأفيونيات، مثل الهيروين، مع باستخدام عقاقير طويلة المفعول لكنها قليلة التأثير على المزاج.[37] تشمل العقاقير التي تستخدم في العلاج ببدائل الأفيون على الميثادون أو بيوبرينورفين والتي تؤخذ تحت إشراف طبي.[37]
يعتمد مبدأ العلاج ببدائل الأفيون على قدرة البرنامج على تسهيل استقرار حياة المدمن، في حين أن المريض يعاني من انخفاض أعراض انسحاب المخدرات ورغبة أقل في تعاطي المخدرات، إلا أنه لم يكن هناك تأثير قوي ُمبهج نتيجة لعقاقير العلاج.[37] في بعض البلدان (وليس الولايات المتحدة، أو أستراليا)،[37] تفرض اللوائح فترة زمنية محدودة للأشخاص على برامج العلاج بالإماهة الفموية التي تنتهي عند استقرار الوضع الاقتصادي والنفسي والاجتماعي للمريض. وعادةً ما يتم استبعاد المرضى الذين يعانون من فيروس نقص المناعة البشرية / الإيدز أو التهاب الكبد C من هذا الشرط. في الممارسة العملية، استطاع 40-65٪ من المرضى الامتناع بشكل كامل عن المواد الأفيونية واستطاع 70 -95٪ الحد من استخدامها بشكل كبير.[37] وإلى جانب ذلك، يتم التخلص من الدواء أو تقليلها بشكل متزامن في المجال الطبي (كالمواد المخففة غير المعقمة، ومعدات التعقيم غير المعقمة)، ومجال الصحة النفسية، والعلاقات)، والمجال القانوني (كالاعتقال والسجن) بالنظر إلى القضايا التي يمكن أن تنشأ عن استخدام المواد الأفيونية غير المشروعة.[37] كما يمكن أن يساعد كلونيدين أو لوفيكسيدين في علاج أعراض الانسحاب.[38]
وقد أظهر العلاج ببدائل الأفيون أنه هو العلاج الأكثر فعالية لتحسين الحالة الصحية والمعيشية للأشخاص الذين يعانون من مشكلة استخدام الأفيون غير المشروع أو الاعتماد عليه، بما في ذلك خفض الوفيات[37][39] والتكاليف الاجتماعية الشاملة، مثل الخسائر الاقتصادية من الجرائم المتصلة بالمخدرات ونفقات الرعاية الصحية.[37] وتؤيد منظمة الصحة العالمية، ومكتب الأمم المتحدة المعني بالمخدرات والجريمة (برنامج الأمم المتحدة المعني بالمخدرات والجريمة)، وبرنامج الأمم المتحدة المشترك المعني بفيروس نقص المناعة البشرية / الإيدز، والحقن، وخفض خطر الإصابة بفيروس نقص المناعة البشرية / الإيدز، أن العلاج ببدائل الأفيون خفض بشكل كبير من خطر الإصابة من الحقن والعدوى المتعلقة بها كفيروس نقص الكناعة البشرية.[40] يستخدم العلاج بالميثادون كعلاج بديل للأفيون في 55 دولة على مستوى العالم، في حين أن لا تستخم بعض البلدان مثل روسيا ذلك.[41]
الميثادون
العلاج باستخدام الميثادون، هو شكل من أشكال العلاج ببدائل المواد الأفيونية، يقلل و / أو يلغي استخدام المواد الأفيونية غير المشروعة، والجريمة المرتبطة باستخدام الأفيون، ويحسن من صحة المرضى الإنتاجية والاجتماعية.[42][43] وبالإضافة إلى ذلك، فإن التسجيل في برنامج العلاج بالميثادون ينطوي على إمكانية الحد من انتقال الأمراض المعدية المرتبطة بحقن الأفيون، مثل التهاب الكبد وفيروس نقص المناعة البشرية.[42] تشمل الآثار الرئيسية للعلاج باستخدام الميثادون تخفيف شغف المخدرات، وقمع متلازمة الامتناع عن التعاطي، ومنع الآثار البهيجة المرتبطة بالمواد الأفيونية. كما وُجد ان العلاج باستخدام الميثادون آمن طبيا وغير مهدئ حتى على النساء الحوامل المدمنين على المواد الأفيونية.[42] وتعطى المعالجة بالميثادون للمدمنين الذين يشعرون بعدم القدرة على المُضي في رحلة العلاج وتخليص أجسامهم من تلك السموم. وبالنسبة للأفراد الذين يرغبون في الابتعاد تمامًا عن المخدرات، يمكنهم البدء في برنامج خفض الميثادون. برنامج الحد من الميثادون هو برنامج يوصف فيه للفرد كمية من الميثادون التي تزداد تدريجيًا حتى تهدأ أعراض الانسحاب، بعد فترة من الاستقرار، يتم تخفيض الجرعة تدريجيًا حتى يصل الفرد إلى درجة من عدم الاعتماد على الميثادون أو درجة تسمح بالتبديل إلى استخدام مادة أفيونية مختلفة مع أعراض انسحاب أسهل، مثل سوبوكسون.[44] وقد تبين أن سمية الميثادون ترتبط مع مظاهر محددة من جين CYP2B6.[45]
ويظهر بعض الانتعاش في الإدراك بعد الامتناع لفترات طويلة، ولكن ليس في تلك التي تستخدم الميثادون.[33][46]
بيوبيرنورفين
غالبًا ما تستخدم مستحضرات تحت اللسان من البوبرينورفين لعلاج الاعتماد على المواد الأفيونية (أي الاعتماد على الهيروين، وأوكسيكودون، والهيدروكودون، والمورفين، والأوكسي مورفون ، والفنتانيل أو المواد الأفيونية الأخرى). وقد وافقت إدارة الغذاء والدواء الأمريكية في أكتوبر / تشرين الأول 2002 على استخدام مستحضرات سوبوكسون وسوبوتكس لهذا الغرض.[47] تحتوي بعض تركيبات البوبرينورفين على نالوكسونكمضاد أفيوني لمنع الناس من سحق الأقراص وحقنها، بدلا من استخدامها في صورة أقراص تحت اللسان.[47]
ديامورفين
في سويسرا وألمانيا وهولندا والمملكة المتحدة، يُعالج متعاطوا المخدرات عن طريق الحقن على المدى الطويل الذين لا يستفيدون من الميثادون والأدوية الأخرى باستخدام مادة الديامورفين القابلة للحقن والتي تعطى تحت إشراف الطاقم الطبي. أثبت العلاج باستخدام الديامورفين لهذه المجموعة من المرضى، تحسن حالتهم الاجتماعية والصحية.[48]
ديهيدروكودين
يستخدم ثنائي هيدروكودايين أحيانًا كبديل للميثادون أو البوبرينورفين في بعض البلدان الأوروبية.[49]
العلاج بمساعدة الهيروين
تم توفير العلاج بمساعدة الهيروين (الهيروين الموصوف طبيًا) في سويسرا منذ عام 1994.[50] ووجدت دراسة أجريت عام 2001 ارتفاع معدل الاحتفاظ بالعلاج وتحسن كبير في الحالة الصحية والاجتماعية واحتمال تجسن المشهد غير القانوني للمخدرات في المشاركين المسجلين.[50] ووجدت الدراسة أن السبب الأكثر شيوعًا لهذا الانخفاض كان بداية العاج باستخدام الميثادون أو العلاج بالامتناع.[50] ووجدت الدراسة أيضًا أن العلاج بمساعدة الهيروين مفيد من حيث التكلفة على مستوى المجتمع بسبب انخفاض التجريم وتحسين الصحة العامة للمشاركين.[50]
وأدخل برنامج العلاج بمساعدة الهيروين في سويسرا لمكافحة الزيادة في استخدام الهيروين في الثمانينات والتسعينيات، وكتب في القانون لعام 2010 كدعامة واحدة لاستراتيجية مكونة من أربع ركائز تستخدم القمع والوقاية والعلاج والحد من المخاطر.[51] وعادة ما تستوفي نسبة صغيرة من المرضى الذين يتلقون الهيروين المعايير.[52][53] ومنذ ذلك الحين، اعتمدت برامج العلاج بمساعدة الهيروين في هولندا والمملكة المتحدة وألمانيا وإسبانيا والدنمارك وبلجيكا وكندا ولوكسمبورغ.[54]
المورفين الممتد المفعول
ويتيح المورفين الموسع للإفراج إمكانية الحد من تعاطي شبائه الأفيون ومع أعراض اكتئاب أقل ولكن الآثار الجانبية أكثر عموما بالمقارنة مع الأشكال الأخرى من المواد الأفيونية المفعول. لم يتم العثور على الاحتفاظ في العلاج لتكون مختلفة إلى حد كبير.[55] يتم استخدامه في سويسرا.[52]
نالتريكسون
تمت الموافقة على استحدام النالتريكسون من قبل إدارة الاغذية والعقاقير في عام 1984 لعلاج إدمان المواد الأفيونية من خلال منع الانتكاس بعد إزالة السموم. يتاح النالتريكسون على حد سواء كدواء عن طريق الفم أو حقن شهرية (المعتمدة في عام 2010). ويتساءل بعض المؤلفين عما إذا كان النالتريكسون الفموي فعالًا في علاج إدمان المواد الأفيونية كالميثادون والبوبرينورفين بسبب عدم امتثال المرضى أم لا.[56]
العلاج السلوكي
العلاج السلوكي المعرفي
برامج الاثنتي عشرة خطوة
في حين أن العلاج الطبي قد يساعد مع الأعراض الأولية لانسحاب الأفيونيات، فبمجرد أ، يتغلب مدمن الأفيون على المراحل الأولى من الانسحاب، تستخدم طريقة للرعاية الوقائية على المدى الطويل كالحضور في مجموعات تتكون في 12 خطوة مثل زمالةالكحوليون المجهولون أو زمالة المدمنين المجهولين. يمكن أن يكون الحضور والمشاركة في برنامج من 12 خطوة وسيلة فعالة للحصول على نتيجة مرضية من العلاج ألأولي والحفاظ عليه.[57] ومن بين الأقليات الرئيسية في المدن الداخلية التي لديها "تاريخ طويل من استخدام الهيروين (في المقام الأول)، امتنع 51.7٪ من الأفراد الذين لديهم حضور مستمر لبرامج الاثنتي عشرة خطوة لأكثر من 3 سنوات بشكل مستمر، على النقيض من 13.5٪ من الأفراد الذين لديهم حضور مستمر لبرامج الاثنتي عشرة خطوة بصورة متقطعة.[58][59]
لابد أن يخضع المريض لبرنامج علاجي طبي، ونفسي، واجتماعي، وديني، وإرشادي متكامل لعدة أسابيع وذلك لصياغة وإعداد المريض لمواجهة الحياة من جديد بصورة طبيعية دون اللجوء للمخدر مرة أخرى مع الإستمرار في المتابعة مع المراكز التأهيلية لمدة كافية قد تزيد عن سنة حسب حالة كل مريض وهذا هو صمام الأمان الرئيس للحد من الانتكاسة. هناك ثلاث امكانيات مركزية من اجل علاج إدمان الافيون: الامتناع عن الافيون، استعمال مضادات لتاثير الافيون واستعمال الافيون الامن.
القرار بشان استعمال وسائل العلاج الدوائي خلال فترة الفطام أو الامتناع الكلي عن المخدر، يتعلق، في المقام الأول، برغبة المدمن، بالإضافة إلى مدة تعاطيه للمخدر، مدى تعلقه بالمخدر، عوامل بيئية، عوامل اجتماعية وعوامل نفسية تخص المدمن.
وبائيات
أدت اضطرابات استخدام المواد الأفيونية إلى وفاة 122,000 في جميع أنحاء العالم في عام 2015،[11] مقارنةً ب18،000 حالة وفاة في عام 1990.[12] وارتفعت الوفيات من جميع الأسباب من 47.5 مليون في عام 1990 إلى 55.8 مليون في عام 2013.[11][12]
الولايات المتحدة
في عام 2012 كان يقدر حوالي 9.2 في المئة من السكان الذين تزيد أعمارهم عن 12 سنة قد استخدموا المخدرات غير المشروعة في الشهر السابق.[60] في عام 2015، كان يقدر حوالي 20.5 مليون أمريكي لديهم اضطراب تعاطي المخدرات.[61] ومن بين هؤلاء البالغ عددهم 20.5 مليون شخص، استخدم مليونان اثنا منهم الأدوية المستخدمة لعلاج الألم (معظمها من الأفيونيات) واستخدم نصف مليون شخص منهم الهيروين.[61]
في عام 2015، كان هناك 33,000 حالة وفاة بسبب جرعة زائدة من المخدرات التي تحتوي على المواد الأفيونية في الولايات المتحدة.[13] من بين هؤلاء، كان هناك حوالي 15000 منهم يستخدمون الأفيونيات الموصوفة طبيًا مع 13,000 شخص يستخدمون الهيروين.[14][15]
وبلغت نسبة استهلاك المواد الأفيونية غير الطبية ذروتها في عام 2010 تقريبًا، ثم بدأت في الانخفاض بين عامي 2011 و 2013 ([70]).
وفيما بين البالغين، ارتفع معدل الإقامة في المستشفيات الداخلية في الولايات المتحدة فيما يتعلق بزيادة استخدام الأفيونيات بنسبة 5 في المائة سنويًا في المتوسط خلال الفترة ما بين 1993 و 2012. وارتفعت النسبة المئوية للإقامة الداخلية بسبب الإفراط في استعمال الأفيونيات المقبولة من قسم الطوارئ من 43 في المائة في عام 1993 إلى 64 في المائة في عام 2005، ولكنها ظلت ثابتة نسبيًا منذ عام 2005.[62]
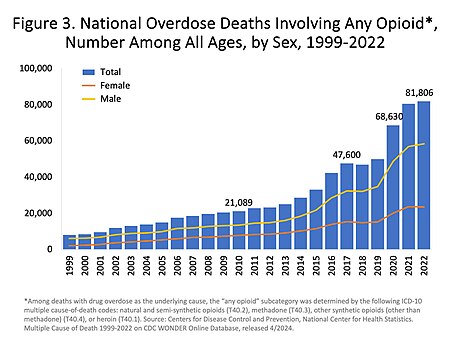
ويتفاوت انتشار تعاطي شبائه الأفيون أو الاعتماد على الأفيون أو شبائه الأفيون حسب العمر والجنس، من بين عدد لا يحصى من العوامل الأخرى. كان الرجال أكثر عرضة لاستعمال الأفيونيات والاعتماد عليها أكثر من النساء،[63][64] كما يمثل الرجال أيضًا النسبة الأكبر من الحالات التي تتعاطى جرعات زائدة من المواد الأفيونية عن النساء، على الرغم من أن هذه الفجوة أخذت في الانكماش.[63] ومن المرجح أن توصف مسكنات الألم للمرأة بصورة أكبر، وأن تُعطى جرعات أعلى، وتستخدمها لفترات أطول، مما يجعل من اعتمادها عليها يأخذ شكلًا أسرع.[65]
كما أن الوفيات الناجمة عن تعاطي شبائه الأفيون تميل إلى الانحراف في الأعمار الأكبر من الوفيات الناجمة عن استخدام العقاقير غير المشروعة الأخرى.[64][66][67] وهذا لا يعكس استخدام الأفيونيات ككل، ولكنه يشمل الأفراد في الفئات السكانية العمرية الأصغر سنًا. تزداد الجرعات الزائدة من المواد الأفيونية بصورة أكبر بين الأفراد الذين تتراوح أعمارهم بين 40 و 50 عام،[67] على عكس الجرعات الزائدة من الهيروين، إذ ترتفع النسبة بين الأفراد الذين تتراوح أعمارهم بين 20 و 30 عام.[66] يمثل الأطفال الذين تتراوح أعمارهم بين 21 و 35 عاما 77٪ من الأفراد الذين يدخلون العلاج لعلاج اضطرابات تعاطي المواد الأفيونية،[68] ومع ذلك، كان متوسط عمر استخدام المسكنات لأول مرة في عمر 21.2 سنة في عام 2013.[69]
التاريخ
ليفاستيلميثادول
كان يستخدم ليفاستيلميثادول سابقًا لعلاج الاعتماد على المواد الأفيونية. في عام 2003 توقفت الشركة المصنعة لهذا العقار عن إنتاجه. تسبب الليفاستيلميثادول في آثار طويلة الأمد، مما سمح للشخص الذي يتلقى العلاج بزيارة العيادة ثلاث مرات فقط في الأسبوع، بدلًا من العلاج اليومي كما هو الحال مع الميثادون.[70] في عام 2001، تمت إزالة ليفاستيلميثادول من السوق الأوروبية بسبب تقارير عن اضطراب النظم القلبية التي تهدد الحياة.[71] في عام 2003، توقفت شركة روكسان لابوراتوريز عن إنتاج ليفاستيلميثادول في الولايات المتحدة.[72]
البحوث
تستخدم العقاقير التالية في علاج إدمان الأفيون بصورة تجريبية ، إلا أنها لا تزال بعيدةُ عن الاعتراف بها واستخدامها بشكل أساسي.
معرض صور
مقالات ذات صلة
المصادر
- "Injury Prevention & Control: Opioid Overdose – Opioid Basics". www.cdc.gov (باللغة الإنجليزية). United States Centers for Disease Control and Prevention. مؤرشف من الأصل في 7 يوليو 201909 مارس 2017.
- "Opioid Use Disorder: Diagnostic Criteria" ( كتاب إلكتروني PDF ). Diagnostic and Statistical Manual of Mental Disorders, Fifth Edition. American Psychiatric Association. صفحات 1–927 مارس 2017.
- Substance Use and Mental Health Services Administration. "Substance Use Disorders". مؤرشف من الأصل في 11 يناير 2019.
- Volkow ND, Koob GF, McLellan AT (January 2016). "Neurobiologic Advances from the Brain Disease Model of Addiction". N. Engl. J. Med. 374 (4): 363–371. doi:10.1056/NEJMra1511480. PMID 26816013.
Addiction: A term used to indicate the most severe, chronic stage of substance-use disorder, in which there is a substantial loss of self-control, as indicated by compulsive drug taking despite the desire to stop taking the drug. In the DSM-5, the term addiction is synonymous with the classification of severe substance-use disorder.
- Nestler EJ (2015). "Reflections on: "A general role for adaptations in G-Proteins and the cyclic AMP system in mediating the chronic actions of morphine and cocaine on neuronal function". Brain Res. doi:10.1016/j.brainres.2015.12.039. PMID 26740398.
Specifically, opiates in several CNS regions including NAc, and cocaine more selectively in NAc induce expression of certain adenylyl cyclase isoforms and PKA subunits via the transcription factor, CREB, and these transcriptional adaptations serve a homeostatic function to oppose drug action. In certain brain regions, such as locus coeruleus, these adaptations mediate aspects of physical opiate dependence and withdrawal, whereas in NAc they mediate reward tolerance and dependence that drives increased drug self-administration.
- American Psychiatric Association (2013), Diagnostic and Statistical Manual of Mental Disorders (5th ed.), Arlington: American Psychiatric Publishing, صفحات 540–546,
- Sordo, Luis; Barrio, Gregorio; Bravo, Maria J; Indave, B Iciar; Degenhardt, Louisa; Wiessing, Lucas; Ferri, Marica; Pastor-Barriuso, Roberto (26 April 2017). "Mortality risk during and after opioid substitution treatment: systematic review and meta-analysis of cohort studies". BMJ: j1550. doi:10.1136/bmj.j1550.
- Substance Abuse and Mental Health Services Administration. "Treatment for Substance Use Disorders". مؤرشف من الأصل في 8 يناير 2019.
- "Opioid Overdose Prevention Programs Providing Naloxone to Laypersons — United States, 2014". www.cdc.gov (باللغة الإنجليزية). مؤرشف من الأصل في 24 أغسطس 201909 مارس 2017.
- Longo, Dan L.; Schuckit, Marc A. (28 July 2016). "Treatment of Opioid-Use Disorders". New England Journal of Medicine. 375 (4): 357–368. doi:10.1056/NEJMra1604339.
- GBD 2015 Mortality and Causes of Death, Collaborators. (8 October 2016). "Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980-2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet (London, England). 388 (10053): 1459–1544. doi:10.1016/S0140-6736(16)31012-1. PMID 27733281.
- GBD 2013 Mortality and Causes of Death, Collaborators (17 December 2014). "Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013". Lancet. 385: 117–171. doi:10.1016/S0140-6736(14)61682-2. PMC . PMID 25530442.
- "Drug Overdose Death Data| Drug Overdose | CDC Injury Center". www.cdc.gov (باللغة الإنجليزية). مؤرشف من الأصل في 20 سبتمبر 201909 مارس 2017.
- "Heroin Overdose Data| Drug Overdose | CDC Injury Center". www.cdc.gov (باللغة الإنجليزية). مؤرشف من الأصل في 7 سبتمبر 201909 مارس 2017.
- "Prescription Opioid Overdose Data | Drug Overdose | CDC Injury Center". www.cdc.gov (باللغة الإنجليزية). مؤرشف من الأصل في 24 أغسطس 201909 مارس 2017.
- "Opiate withdrawal". Medline Plus. مؤرشف من الأصل في 5 يوليو 201601 نوفمبر 2014.
- Kosten TR, Haile CN. Opioid-Related Disorders. In: Kasper D, Fauci A, Hauser S, Longo D, Jameson J, Loscalzo J. eds. Harrison's Principles of Internal Medicine, 19e New York, NY: McGraw-Hill; 2014. Accessed March 09, 2017. - تصفح: نسخة محفوظة 14 أبريل 2020 على موقع واي باك مشين.
- Chen, Kevin W.; Banducci, Annie N.; Guller, Leila; MacAtee, Richard J.; Lavelle, Anna; Daughters, Stacey B.; Lejuez, C.W. (2011). "An examination of psychiatric comorbidities as a function of gender and substance type within an inpatient substance use treatment program". Drug and Alcohol Dependence. 118 (2–3): 92–9. doi:10.1016/j.drugalcdep.2011.03.003. PMC . PMID 21514751.
- Praveen, KT; Law, F; O'Shea, J; Melichar, J (2012). "Opioid dependence". American family physician. 86 (6): 565–6. PMID 23062049.
- Webster, L. R.; Webster, R. M. (2005). "Predicting aberrant behaviors in opioid-treated patients: Preliminary validation of the Opioid Risk Tool". Pain Medicine. 6 (6): 432–42. doi:10.1111/j.1526-4637.2005.00072.x. PMID 16336480.
- Substitution maintenance therapy in the management of opioid dependence and HIV/AIDS prevention ( كتاب إلكتروني PDF ). World Health Organization. 2004. . مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 1 يوليو 2015.
- "Treatment of opioid dependence". WHO. مؤرشف من الأصل في 30 أكتوبر 201328 أغسطس 2016.
- Nestler EJ (December 2013). "Cellular basis of memory for addiction". Dialogues Clin Neurosci. 15 (4): 431–443. PMC . PMID 24459410.
DESPITE THE IMPORTANCE OF NUMEROUS PSYCHOSOCIAL FACTORS, AT ITS CORE, DRUG ADDICTION INVOLVES A BIOLOGICAL PROCESS
- Malenka RC, Nestler EJ, Hyman SE (2009). "Chapter 15: Reinforcement and Addictive Disorders". In Sydor A, Brown RY (المحررون). Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (الطبعة 2nd). New York: McGraw-Hill Medical. صفحات 364–375. .
- "Glossary of Terms". Mount Sinai School of Medicine. Department of Neuroscience. مؤرشف من الأصل في 10 مايو 201909 فبراير 2015.
- Robison AJ, Nestler EJ (November 2011). "Transcriptional and epigenetic mechanisms of addiction". Nat. Rev. Neurosci. 12 (11): 623–637. doi:10.1038/nrn3111. PMC . PMID 21989194.
- Olsen CM (December 2011). "Natural rewards, neuroplasticity, and non-drug addictions". Neuropharmacology. 61 (7): 1109–22. doi:10.1016/j.neuropharm.2011.03.010. PMC . PMID 21459101.
- Ruffle JK (Nov 2014). "Molecular neurobiology of addiction: what's all the (Δ)FosB about?". The American Journal of Drug and Alcohol Abuse. 40 (6): 428–37. doi:10.3109/00952990.2014.933840. PMID 25083822.
- Bourdy R, Barrot M (November 2012). "A new control center for dopaminergic systems: pulling the VTA by the tail". Trends Neurosci. 35 (11): 681–690. doi:10.1016/j.tins.2012.06.007. PMID 22824232.
- "Morphine addiction – Homo sapiens (human)". KEGG. Kanehisa Laboratories. 18 June 2013. مؤرشف من الأصل في 20 يونيو 201811 سبتمبر 2014.
- Goldstein, Rita Z.; Volkow, Nora D. (2011-11-01). "Dysfunction of the prefrontal cortex in addiction: neuroimaging findings and clinical implications". Nature Reviews Neuroscience (باللغة الإنجليزية). 12 (11): 652–669. doi:10.1038/nrn3119. ISSN 1471-003X. PMC . PMID 22011681. مؤرشف من الأصل في 24 مايو 2017.
- Ieong, Hada Fong-ha; Yuan, Zhen (2017-04-19). "Abnormal resting-state functional connectivity in the orbitofrontal cortex of heroin users and its relationship with anxiety: a pilot fNIRS study". Scientific Reports (باللغة الإنجليزية). 7. doi:10.1038/srep46522. ISSN 2045-2322. مؤرشف من الأصل في 29 ديسمبر 2019.
- Ieong, Hada Fong-ha; Yuan, Zhen (2017-01-01). "Resting-State Neuroimaging and Neuropsychological Findings in Opioid Use Disorder during Abstinence: A Review". Frontiers in Human Neuroscience (باللغة الإنجليزية). 11. doi:10.3389/fnhum.2017.00169. ISSN 1662-5161. مؤرشف من الأصل في 22 يوليو 2017.
- Hall, F. Scott; Drgonova, Jana; Jain, Siddharth; Uhl, George R. (December 2013). "Implications of genome wide association studies for addiction: Are our a priori assumptions all wrong?". Pharmacology & Therapeutics. 140 (3): 267–279. doi:10.1016/j.pharmthera.2013.07.006. PMC . PMID 23872493.
- Bruehl, Stephen; Apkarian, A. Vania; Ballantyne, Jane C.; Berger, Ann; Borsook, David; Chen, Wen G.; Farrar, John T.; Haythornthwaite, Jennifer A.; Horn, Susan D.; Iadarola, Michael J.; Inturrisi, Charles E.; Lao, Lixing; Mackey, Sean; Mao, Jianren; Sawczuk, Andrea; Uhl, George R.; Witter, James; Woolf, Clifford J.; Zubieta, Jon-Kar; Lin, Yu (February 2013). "Personalized Medicine and Opioid Analgesic Prescribing for Chronic Pain: Opportunities and Challenges". The Journal of Pain. 14 (2): 103–113. doi:10.1016/j.jpain.2012.10.016. PMC . PMID 23374939.
- Khokhar, Jibran Y.; Ferguson, Charmaine S.; Zhu, Andy Z.X.; Tyndale, Rachel F. (February 2010). "Pharmacogenetics of Drug Dependence: Role of Gene Variations in Susceptibility and Treatment". Annual Review of Pharmacology and Toxicology. 50 (1): 39–61. doi:10.1146/annurev.pharmtox.010909.105826.
- Richard P. Mattick et al.: National Evaluation of Pharmacotherapies for Opioid Dependence (NEPOD): Report of Results and Recommendation
- Gowing, L; Farrell, M; Ali, R; White, JM (3 May 2016). "Alpha₂-adrenergic agonists for the management of opioid withdrawal". The Cochrane database of systematic reviews (5): CD002024. doi:10.1002/14651858.CD002024.pub5. PMID 27140827.
- Michel et al.: Substitution treatment for opioid addicts in Germany, Harm Reduct J. 2007; 4: 5. نسخة محفوظة 17 مارس 2020 على موقع واي باك مشين.
- WHO; UNODC; UNAIDS (January 2013). WHO, UNODC, UNAIDS technical guide for countries to set targets for universal access to HIV prevention, treatment and care for injecting drug users – 2012 revision. صفحة 13. .
- Michael Schwartz (22 July 2008). "Russia Scorns Methadone for Heroin Addiction". The New York Times. مؤرشف من الأصل في 05 مارس 201805 أبريل 2014.
- Joseph, H; Stancliff, S; Langrod, J (2000). "Methadone maintenance treatment (MMT): A review of historical and clinical issues". The Mount Sinai journal of medicine, New York. 67 (5–6): 347–64. PMID 11064485.
- Connock, M; Juarez-Garcia, A; Jowett, S; Frew, E; Liu, Z; Taylor, RJ; Fry-Smith, A; Day, E; Lintzeris, N (2007). "Methadone and buprenorphine for the management of opioid dependence: A systematic review and economic evaluation". Health technology assessment. 11 (9): 1–171, iii–iv. doi:10.3310/hta11090. PMID 17313907. مؤرشف من الأصل في 13 مارس 2012.
- http://www.rcgp.org.uk-PDF-drug_meth%20guidance.
- Bunten, H; Liang, W J; Pounder, D J; Seneviratne, C; Osselton, D (28 July 2010). "OPRM1 and CYP2B6 Gene Variants as Risk Factors in Methadone-Related Deaths". Clinical Pharmacology & Therapeutics. 88 (3): 383–389. doi:10.1038/clpt.2010.127. PMID 20668445.
- Darke, Shane; Sims, Jamie; McDonald, Skye; Wickes, Wendy (2000-05-01). "Cognitive impairment among methadone maintenance patients". Addiction (باللغة الإنجليزية). 95 (5): 687–695. doi:10.1046/j.1360-0443.2000.9556874.x. ISSN 1360-0443. مؤرشف من الأصل في 6 ديسمبر 2017.
- "Subutex and Suboxone Approved to Treat Opiate Dependence". FDA. 8 October 2002. مؤرشف من الأصل في 22 يوليو 201701 نوفمبر 2014.
- Haasen, C.; Verthein, U.; Degkwitz, P.; Berger, J.; Krausz, M.; Naber, D. (2007). "Heroin-assisted treatment for opioid dependence: Randomised controlled trial". The British Journal of Psychiatry. 191: 55–62. doi:10.1192/bjp.bp.106.026112. PMID 17602126.
- Robertson, J. Roy; Raab, Gillian M.; Bruce, Malcolm; McKenzie, James S.; Storkey, Helen R.; Salter, Amy (2006). "Addressing the efficacy of dihydrocodeine versus methadone as an alternative maintenance treatment for opiate dependence: A randomized controlled trial". Addiction. 101 (12): 1752–9. doi:10.1111/j.1360-0443.2006.01603.x. PMID 17156174.
- Rehm J, Gschwend P, Steffen T, Gutzwiller F, Dobler-Mikola A, Uchtenhagen A (2001). "Feasibility, safety, and efficacy of injectable heroin prescription for refractory opioid addicts: a follow-up study". Lancet. 358 (9291): 1417–23. doi:10.1016/S0140-6736(01)06529-1. PMID 11705488. مؤرشف من الأصل في 20 يونيو 201804 مارس 2016.
- "Drogenpolitik: Heroinabgabe gemäss Experten ein Erfolg - NZZ Schweiz". مؤرشف من الأصل في 2 يوليو 201904 مارس 2016.
- "Bundesamt für Gesundheit - Substitutionsgestützte Behandlung mit Diacetylmorphin (Heroin)". مؤرشف من الأصل في 7 أغسطس 2016.
- "Dank der ärztlichen Heroinabgabe können rund 1400 Süchtige legal konsumieren – Einige schaffen den Anschluss an die Gesellschaft: Heroinsüchtige mitten im Leben - NZZ". مؤرشف من الأصل في 24 يونيو 2016.
- "Heroin Assisted Treatment | Drug Policy Alliance". مؤرشف من الأصل في 14 مايو 201804 مارس 2016.
- Ferri, Marica; Minozzi, Silvia; Bo, Alessandra; Amato, Laura; Ferri, Marica (2013). "Slow-release oral morphine as maintenance therapy for opioid dependence". Reviews. doi:10.1002/14651858.CD009879.pub2.
- Minozzi S, Amato L, Vecchi S, Davoli M, Kirchmayer U, Verster A (2011). "Oral naltrexone maintenance treatment for opioid dependence". Cochrane Database of Systematic Reviews (4): CD001333. doi:10.1002/14651858.CD001333.pub4. PMID 21491383.
- Brigham, Gregory (2003). "12-Step Participation as a Pathway to Recovery: The Maryhaven Experience and Implications for Treatment and Research". Science & Practice Perspectives. 2 (1): 43–51. doi:10.1151/spp032143. PMC . PMID 18552722.
- "PPT – Alexandre B. Laudet, Ph.D PowerPoint presentation - free to view - id: 1460c1-YWY2O". PowerShow. مؤرشف من الأصل في 21 أغسطس 2017.
- Manning, V; Best D., Faulkner N., Titherington E., Morinan A., Keaney F., Gossop M., Strang J. (November 2012). "Does active referral by a doctor or 12-Step peer improve 12-Step meeting attendance? Results from a pilot randomised control trial". Drug Alcohol Depend; Research study. 126 (1–2): 131–7. doi:10.1016/j.drugalcdep.2012.05.004. PMID 22677458.
- Substance Abuse and Mental Health Services Administration, Results from the 2012 National Survey on Drug Use and Health: Summary of National Findings, NSDUH Series H-46, HHS Publication No. (SMA) 13-4795. Rockville, MD: Substance Abuse and Mental Health Services Administration, 2013.
- American Society of Addiction Medicine. "Opioid Addiction 2016 Facts and Figures" ( كتاب إلكتروني PDF ). مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 11 أبريل 2017.
- Owens PL, Barrett ML, Weiss AJ, Washington RE, Kronick R (August 2014). "Hospital Inpatient Utilization Related to Opioid Overuse Among Adults, 1993–2012". HCUP Statistical Brief #177. Rockville, MD: Agency for Healthcare Research and Quality. مؤرشف من الأصل في 3 سبتمبر 2019.
- "Prescription Opioid Overdose Data". Center for Disease Control and Prevention. مؤرشف من الأصل في 7 سبتمبر 201912 سبتمبر 2016.
- Paulozzi, Len (12 April 2012). "Populations at risk for opioid overdose" ( كتاب إلكتروني PDF ). FDA. Division of Unintentional Injury Prevention, National Center for Injury Prevention and Control Centers for Disease Control and Prevention. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 15 فبراير 201712 سبتمبر 2016.
- "Opioid Addiction: 2016 Facts and Figures" ( كتاب إلكتروني PDF ). American Society of Addiction Medicine. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 11 أبريل 201712 سبتمبر 2016.
- "How Bad is the Opioid Epidemic?". مؤرشف من الأصل في 10 أغسطس 201912 سبتمبر 2016.
- Han, Benjamin; Polydorou, Soteri; Ferris, Rosie; Blaum, Caroline S.; Ross, Stephen; McNeely, Jennifer (2015-11-10). "Demographic Trends of Adults in New York City Opioid Treatment Programs—An Aging Population". Substance Use & Misuse. 50 (13): 1660–1667. doi:10.3109/10826084.2015.1027929. ISSN 1082-6084. PMID 26584180. مؤرشف من الأصل في 14 أبريل 2020.
- "Facts & Faces of Opioid Addiction: New Insights". MAP Health Management. 2015. مؤرشف من الأصل في 29 فبراير 202012 سبتمبر 2016.
- "Opioids". Substance Abuse and Mental Health Services Administration. 23 February 2016. مؤرشف من الأصل في 3 ديسمبر 201812 سبتمبر 2016.
- James W. Kalat, Biological Psychology. Cengage Learning. Page 81.
- EMEA April 19, 2001 EMEA Public Statement on the Recommendation to Suspend the Marketing Authorisation for Orlaam (Levacetylmethadol) in the European Union - تصفح: نسخة محفوظة 04 فبراير 2017 على موقع واي باك مشين.
- US FDA Safety Alerts: Orlaam (levomethadyl acetate hydrochloride) Page Last Updated: Aug 20, 2013 نسخة محفوظة 18 يناير 2017 على موقع واي باك مشين.
- Brewer, C; H Rezae, C Bailey (1988). "Opioid withdrawal and naltrexone induction in 48–72 hours with minimal drop-out, using a modification of the naltrexone-clonidine technique". The British Journal of Psychiatry. 153 (3): 340–343. doi:10.1192/bjp.153.3.340. PMID 3250670. مؤرشف من الأصل في 13 فبراير 2018.
- Ling, W; L Amass, S Shoptaw, JJ Annon, M Hillhouse, D Babcock, G Brigham, J Harrer, M Reid, J Muir, B Buchan, D Orr, G Woody, J Krejci, D Ziedonis (2005). "A multi-center randomized trial of buprenorphine–naloxone versus clonidine for opioid, detoxification: findings from the National Institute on Drug Abuse Clinical Trials Network". Addiction. 100 (8): 1090–1100. doi:10.1111/j.1360-0443.2005.01154.x. PMC . PMID 16042639.
- Herman, BH; F Vocci, P Bridge (1995). "The effects of NMDA receptor antagonists and nitric oxide synthase inhibitors on opioid tolerance and withdrawal: Medication development issues for opiate addiction" ( كتاب إلكتروني PDF ). Neuropsychopharmacology. 13 (4): 269–293. doi:10.1016/0893-133X(95)00140-9. PMID 8747752. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 2 فبراير 2017.
- Alper, Kenneth R.; Lotsof, Howard S.; Kaplan, Charles D. (January 2008). "The ibogaine medical subculture". Journal of Ethnopharmacology. 115 (1): 9–24. doi:10.1016/j.jep.2007.08.034. PMID 18029124.
- Boyer, Edward W.; Kavita M. Babu, Jessica E. Adkins, Christopher R. McCurdy, John H. Halpern (28 June 2008). "Self-treatment of opioid withdrawal using kratom (Mitragynia speciosa korth)". Addiction. 103 (6): 1048–1050. doi:10.1111/j.1360-0443.2008.02209.x. PMC . PMID 18482427.
وصلات خارجية
- Heroin information from the National Institute on Drug Abuse
- Opioid information at Opioids.Net
- Opioid Dependence Treatment and Guidelines
- Opioid Risk Tool (ORT) for Narcotic Abuse