| Isoleucine | |
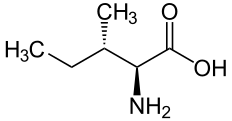 L ou (2S,3S)-(+)-isoleucine 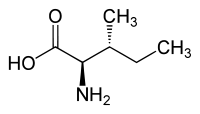 D ou (2R,3R)-(–)-isoleucine |
|
| Identification | |
|---|---|
| Nom UICPA | Acide 2-amino-3-méthylpentanoïque |
| Synonymes |
I, Ile |
| No CAS | (racémique) (D) (L) D-allo-Isoleucine L-allo-Isoleucine |
| No ECHA | 100.000.726 |
| No CE | 200-798-2 (L) 206-269-2 (D) 216-142-3 L-allo 216-143-9 D-allo |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C6H13NO2 [Isomères] |
| Masse molaire[1] | 131,172 9 ± 0,006 5 g/mol C 54,94 %, H 9,99 %, N 10,68 %, O 24,39 %, |
| Propriétés biochimiques | |
| Codons | AUU, AUC, AUA |
| pH isoélectrique | 6,02[2] |
| Acide aminé essentiel | oui |
| Occurrence chez les vertébrés | 3,8 %[3] |
| Cristallographie | |
| Classe cristalline ou groupe d’espace | L-isoleucine : P21 [4] |
| Paramètres de maille | L-isoleucine : a = 9,681 Å |
| Précautions | |
| SIMDUT[5] | |
Produit non contrôlé |
|
| Unités du SI et CNTP, sauf indication contraire. | |
L’isoleucine (abréviations IUPAC-IUBMB : Ile et I) est un acide α-aminé faisant partie des 20 acides aminés majeurs codés par le génome (exception faite de la Sélénocystéine) servant à la synthèse des protéines. Cet acide aminé est l'un des 9 acides aminés essentiels pour l'homme, c'est-à-dire non synthétisable de novo par les cellules mais indispensable à son bon fonctionnement, son apport est donc alimentaire.
Elle est codée sur les ARN messagers par les codons AUU, AUC et AUA. Elle forme un résidu apolaire aliphatique dans les protéines.
Du point de vue de son catabolisme chez l'homme, l'isoleucine est un acide aminé mixte : il est à la fois cétoformateur et glucoformateur. C'est-à-dire que sa dégradation peut former des précurseurs du glucose, en passant par le cycle de Krebs puis la néoglucogenèse ; ou former des corps cétoniques à partir de l'acétyl-CoA transformé en Acetoacétyl-CoA pour rejoindre la voie de cétogenèse.
On le retrouve donc dans les voies des corps cétoniques (cétogenèse) et dans la néoglucogenèse pour produire de l'énergie nécessaire au bon fonctionnement du métabolisme.
Découverte
L’isoleucine a été découverte en 1904 par Félix Ehrlich[6], dans des mélasses.
Synthèse biologique
L'isoleucine est synthétisé dans le corps humain à partir de l'hydroxyéthyl thiamine pyrophosphate[7].
Structure
  |
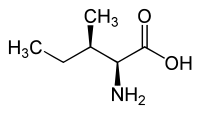
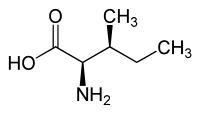
| L(+)-isoleucine (2S,3S) et D(–)-isoleucine (2R,3R) |
  |
| L-allo-isoleucine (2S,3R) et D-allo-isoleucine (2R,3S) |
Biochimie
En plus du carbone α, elle possède un deuxième carbone asymétrique en position 3 (carbone β), et seule la forme 2S-3S est incorporée dans les protéines.
Notes et références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ (en) Francis A. Carey, « Table of pKa and pI values », sur Département de chimie de l'université de Calgary, (consulté le )
- ↑ (en) M. Beals, L. Gross, S. Harrell, « Amino Acid Frequency », sur The Institute for Environmental Modeling (TIEM) à l'université du Tennessee (consulté le )
- 1 2 « L-Isoleucine », sur www.reciprocalnet.org (consulté le )
- ↑ « Isoleucine (l-) » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ (de) Felix Ehrlich, « Ueber das natürliche Isomere des Leucins », Berichte der deutschen chemischen Gesellschaft, vol. 37, no 2, , p. 1809–1840 (ISSN 0365-9496, DOI 10.1002/cber.19040370295, lire en ligne, consulté le )
- ↑ Jeremy Mark Berg, John L. Tymoczko, Lubert Stryer et Gregory Joseph Gatto, Biochimie, Médecine-sciences publications-[Lavoisier], (ISBN 978-2-257-20427-1), p. 723