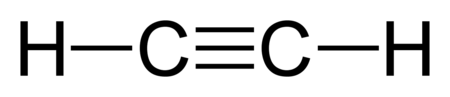الألكاينات هي هيدروكربونات بها رابطة ثلاثية على الأقل بين ذرتي كربون.[1][2][3] صيغتها العامة CnH2n-2 وتعرف الألكاينات أيضا باسم الأسيتيلينات, نسبة إلى أبسط أنواع الألكاينات الاسيتيلين C2H2 وذلك على الرغم من أن الأسيتيلين هو أيضا اسم أول مركبات هذه السلسة، وإن كان اسمه الرسمي إيثاين.
بناء الألكاينات
ذرات الكربون في رابطة الألكاينات تكون مهجنة تهجين sp وبها 2 أوربيتال p مدار sp مهجن واحد. تتداخل الأوربيتالات p لينتج من هذا رابطتان باي. بالإضافة إلى ذلك، يتداخل المداران sp لتكوين رابطة سيجما sp-sp, وبذلك يكون العدد النهائي للروابط يساوي 3. وهذا يجعل الزاوية بين H-C-C 180 في الأسيتيلين. ونظرا لأن عدد الإلكترونات التي تساهم في تكوين هذه الرابطة الثلاثية، فإنها تكون رابطة قوية وتبلغ 837 KJ/mole. وتساهم الرابطة سيجما بمقدار 39 KJ/mole, وتساهم الرابطة باي الأولى بمقدار 268 KJ/mole, والرابطة باي الثانية تكون ضعيفة وتبلغ طاقتها 202 KJ/mole. وطول الرابطة C-C يكون 1021 أنجستروم وهذا أقل بكثير من طول الرابطة في الألكينات والتي تبلغ 1034 أنجستروم، والألكانات وتبلغ 1053 أنجستروم.
تسمية الألكاينات
1- نختار أطول سلسلة متصلة تحوى الرابطة الثلاثية، ويكتب اسم الألكين على حسب عدد ذرات الكربون في هذه السلسلة منتهياً بالمقطع (اين ) على أن يسبق الاسم رقم ذرة الكربون الموجودة في الرابطة الثلاثية الأقل رقماً
2- يتم ترقيم السلسلة من الطرف القريب للرابطة الثلاثية بغض النظر عن موقع المجموعات المتفرعة. ثم يتبع باقي النظام السابق في تسمية الألكانات.
الخواص الفيزيائية
بعكس الألكانات والألكينات فإن الألكاينات تكون غير ثابتة ونشيطة للغاية. وهذا سبب زيادة الحرارة الخارجة من الأسيتيلين أثناء عمليات اللحام.
درجة الغليان ودرجة الذوبان تزداد بزيادة عدد ذرات الكربون .
أمثلة للألكاينات
أصغر الألكاينات هو الإيثاين أسيتلين|أسيتيلين
C2H2
أطراف الألكاينات
أطراف الألكاينات بها ذرة هيدروجين واحدة كمستبدل ألفا. وهو أول عضو في جدولها homologe columm
الأسيتيليدات الفلزية
تتفاعل الألكاينات الطرفية مع القواعد القوية مثل الصوديوم, أميد الصوديوم, إن-بيوتيل ليثيوم, كاشف جرينيارد وينتج أنيون من الألكاين الطرفي واسيتيليد فلزي. الأسيتيلين حمضي إلى حد ما، وله ثابت تفكك الحمض بقيمة (25(وهذه قيمة متوسطة بين الأمونيا (35) والإيثانول (16). وسبب هذه الحامضية هو أن الشحنة السالبة في الأسيتيليد تثبت كنتيجة لصفات المدار s المميزة في المدار sp والتي يشغلها زوج من الإلكترونات. الإلكترونات في المدار s تستفيد من الاقتراب النسبي للنواة الموجبة الشحنة وبالتالى يؤدى هذا إلى طاقة أقل.
تصنيع الألكاينات
تصنع الألكاينات بصفة عامة عن طريق نزع الماء المهلجن من الألكيل دايهاليد المتجاور, أو عن طريق تفاعل الأسيتيليدات الفلزية مع هاليد الألكيل الأساسي. وفي إعادة ترتيب فريتش-بوتينبرج-فايتشيل يتم تحضير الألكاين من بروميد الفينيل.
تفاعلات الألكاينات
الألكاينات تدخل في كثير من التفاعلات العضوية
- تفاعلات الإضافة المحبة للإلكترونات
- إضافة الهيدروجين للألكينات أو الألكانات.
- إضافة الهالوجين إلى هاليد الفينيل أو هاليد الألكيل.
- إضافة هاليد الهيدروجين لهاليد الفينيل أو هاليد الألكيل المشابه.
- إضافة الماء لمركب الكاربونيل (عن طريق وسيط الإينول).
- تفاعلات الإضافة الحلقية
- تفاعل ديلز-ألدير مع 2-بيرون لإنتاج مركب أروماتي بعد تصاعد ثاني أكسيد الكربون.
- إضافة هويزن 3,1-ثنائية القطبية الحلقية لإنتاج مركبات الترايازول.
- تحلق بيرجمان للإيني دايأينات لإنتاج المركبات الأروماتية.
- تجمع ألكاين ثلاثي لإنتاج لمركبات الأروماتية.
- مزج الألكاينات في تحولات الألكاينات لإنتاج مركبات ألكاينية جديدة.
- تفاعلات الاستبدال المحبة للنواة لفلزات الأسيتيليدات.
- تكون رابطة كربون-كربون جديدة مع هاليدات الألكيل.
- تفاعلات الإضافة المحبة للنواة ]] لفلزات الأسيتيليدات.
- التفاعل مع مركبات الكربونيل لإنتاج مركبات وسيطة من الألكوكسيد ثم ينتج الهيدروكسي ألكاين بعد الإزالة الحامضية.
- تفاعل الهيدرة بورونية للألكاينات مع بورون عضوي لإنتاج بورونات فينيلية
- ثم اختزال عن طريق بيروكسيد الهيدروجين لإنتاج الألدهيد أو الكيتون المقابل.
- الانقسام التأكسدي بواسطة برمنجنات البوتاسيوم لإنتاج الأحماض الكربوكسيلية.
استخدام الألكاينات
اقرأ أيضا
مراجع
- Lam, Jørgen (1988). Chemistry and biology of naturally-occurring acetylenes and related compounds (NOARC): proceedings of a Conference on the Chemistry and Biology of Naturally-Occurring Acetylenes and Related Compounds (NOARC). Amsterdam: Elsevier. .
- Kenneth N. Campbell(1963)."Phenylacetylene". Org. Synth.; Coll. Vol. 4: 763.
- Alkyne. Encyclopædia Britannica نسخة محفوظة 27 أبريل 2015 على موقع واي باك مشين.