منذ ما يزيد على 2000 سنة مضت، تمكن العالم الإغریفی " تالیز " من إنتاج ومضات كهربائية بسيطة عن طريق حك قطعة من القماش بالكهرمان، وهو عبارة عن راتينج أصفر يتكون من عصارة الأشجار الميتة منذ فترات زمنية طويلة، لكن الأمر استغرق فترة طويلة من الوقت قبل أن يتمكن الإنسان من تسخير هذه القوة لإنتاج البطاريات الكهربائية، وبالتالى إنتاج تيار ثابت من الكهرباء.
 مجموعة مختلفة من بطاريات الخلايا الكهربائية | |
| النوع | منبع استطاعة |
|---|---|
| مبدأ العمل | القوة المحركة الكهربائية |
| الرمز الإلكتروني | |
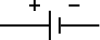 | |
| إعداد الدبوس | قطبان، سالب وموجب. القطب الموجب هو القطب الأطول دائماً. |
أول بطارية كهربائية في التاريخ
في عام 1800 ميلادية، نشر ألساندرو فولتا (1745-1827م) التفاصيل الخاصة بأول بطارية كهربائية في التاريخ. وقد كانت البطارية الكهربائية التي اخترعها فولتا تنتج الكهرباء عن طريق التفاعل الكيميائي بين بعض المحاليل المعينة والأقطاب الكهربائية المعدنية ( الإلكترودات). جدير بالذكر أن بعض العلماء الآخرين، مثل جون فردريك دانييل ( 1790 - 1845م ) ، قد طور تصمیم فولتا عن طريق استخدام مواد و مختلفة في الأقطاب الكهربائية. كما أن البطاريات الكهربائية المستخدمة اليوم تتبع التصميم الأساسی نفسه ولكن مع استخدام مواد حديثة .
كانت البطارية الكهربائية التي اخترعها فولتا تتكون من أقراص من الزنك والفضة أو النحاس يتم الفصل بينهما عن طريق فواصله مبتلة بحمض مخفف أو محلول ملحي كانت الكهرباء تتدفق خلال سلك يربط بين القرصين العلوي والسفلى. الجدير بالذكر هنا أن الفولت، وهو وحدة كهربائية. تمت تسميته على اسم ألساندرو فولتا .
بداية التطوير في بطارية فولتا
تلى ذلك طريقة كان يتم فيها توصيل الكثير من الخلايا معاً حيث كانت كل خلية منها تتكون من زوجين من الأقطاب الكهربائية المصنوعة من معادن مختلفة وذلك لإنتاج قدر أكبر من الجهد الكهربى (الفولت) ، وبالتالى تیار كهربي بكمية أكبر،. وتتكون الخلية " الفولتية " الشهيرة من أقطاب كهربائية مصنوعة من النحاس والزنك مغموسة في حمض مخفف. وقد تمكن المخترع الإنجليزی " کروکشانك " من اختراع بطارية «الحوض» الكهربائية هذه في عام 1800م .
وقد كان يتم لحم الألواح المعدنية وظهر كل منها للآخر ثم يتم تثبيتها بالأسمنت في فتحات صغيرة ضيقة في صندوق خشبي، ثم يملأ الصندوق بعد ذلك بحمض مخفف أو محلول من كلوريد الأمونيوم .
كهرباء يعتمد عليها .. وبطاريات قابلة للشحن
كانت خلية دانييل أول مصدر يعتمد عليه للحصول على الكهرباء. فكانت هذه الخلية تنتج جهداً كهربائياً مستمراً لفترة لا بأس بها من الوقت، وتشتمل الخلية على قطب كهربائي من النحاس مغموس في محلول كبريتات النحاس و قطب كهربائي آخر من الزنك مغمور في حمض الكبريتيك. وكانت السوائل تحفظ منفصلة في وعاء مسامى .
كان العالم الفرنسي " جاستون بلانتی " رائدا في مجال تصميم بطارية الحمض والرصاص، والذي يمكن إعادة شحنها عندما تنفد منها الكهرباء. تشتمل هذه البطاريات على أقطاب كهربائية من الرصاص وأكسيد الرصاص توضع في حمض الكبريتيك.
وظلت البطاريات في حالة تطوير حتى وصلت في عصرنا إلى ما هي عليه من اشكال واحجام وسعات مختلفة لكل الأجهزة الكهربائية في حياتنا واصبحت صناعه تجنى المليارات حول العالم لاستخدامها الواسع في مختلف الصناعات والمجالات .[1][1]
تصنيف البطاريات الكهربائية
يمكن تصنيف المدخرات الكهربائية في مجموعتين أساسيتين هما:
- مدخرات كهربائية رئيسية غير قابلة للشحن مرة أخرى. هذا النوع يستنفذ طاقة التفاعل الكيميائية بإنتاج طاقة كهربائية مكافئة حتى تنتهي عملية التفاعل ولا يمكن استرجاعها. تتميز هذه المدخرات بسعتها العالية ومن أمثلتها مدخرات الزنك والكربون، المدخرات القلوية.
- مدخرات ثانوية قابلة للشحن مرة أخرى. هذا النوع يشترط شحنها بالكهرباء قبل استعمالها ومن أمثلتها مدخرة الرصاص ومدخرة النيكل كانديوم
أنواع خلايا المدخرة
يمكن لأي من الصنفين السابقين أن يكون مؤلفاً من أحد أنواع الخلايا التالية:
- خلايا سائلة
- خلايا جافة
أداء المدخرة
يختلف أداء وخواص المدخرات بحسب أنواعها ومع دورة التحميل، دورة الشحن بسبب عوامل عدة منها كيميائية، التيار المأخوذ والحرارة.
ظاهرة الذاكرة
تعاني بعض المدخرات القابلة للشحن مثل مدخرات النيكل كادميوم من مشكلة تدعى تأثير الذاكرة أو تأثير المدخرة الكسلة. تنجم هذه المشكلة بسبب تشغيل المدخرة تحت ظروف التشغيل الخاصة بها لفترة من الزمن. يتلخص هذا التشغيل الخاطئ في أمرين:
- شحن المدخرة (خاصة الشحن لأول مرة) حتى تصل إلى جهد أدنى من الجهد الاسمي لها.
- تشغيل أو تحميل أو تفريغ المدخرة ثم إعادة شحنها قبل تفريغها تماماً.
عند حدوث أمور كهذه فإن خلايا المدخرة تتعامل (وكأنها تبرمجت) مع الوضع الجديد متناسية الخصائص الأصلية لها وبالتالي بكفاءة أدنى من المتوقع.
هناك مقترحات لتجنب مثل هذه المشكلة منها ما يلي:
- عند شحن المدخرة لأول مرة ينبغي شحنها لأطول فترة ممكنة (تحدد عادة من قبل المنتج) وكذلك التأكد من وصولها للجهد الاسمي لها أو أعلى قليلاً.
- عند إعادة شحن المدخرة ينبغي التأكد من وصولها للجهد الاسمي لها.
- بعد مرور فترة على شحن وتفريغ المدخرة العشوائي (لا يؤثر كثيراً على الأداء) ينصح بإعادة تفريغها تماما ثم إعادة شحنها للجهد الاسمي مرة كل أسبوعين تقريباُ من أجل إنعاش ذاكرة الخلايا.
مميزات البطارية
- خفيفة.
- متعددة الأحجام والأشكال.
- توفر طاقة عالية.
- سعتها كبيرة.
- الطاقة الكهربية فيها متواصلة بنفس القوة إلى أن تنفد البطارية.
- عمرها طويل مقارنة مع الأنواع السابقة.
انظر أيضاً
- مركم
- خلية جلفانية
- بطارية السيارة
- خلية ثانوية
- بطارية نظائر مشعة
- بطارية الليمون
- تفاعل أكسدة-اختزال
- بطارية ليثيوم أيون
- تآكل جلفاني
- شاحن البطارية
المراجع
- "قصص 26: اختراعات | قصة اختراع البطاريات الكهربائية". قصص 26. مؤرشف من الأصل في 28 فبراير 201827 فبراير 2018.


