قصور الدرقية (Hypothyroidism) هو اضطراب غدد صم شائع، حيث لا تنتج الغدة الدرقية هرمونات الغدة الدرقية بشكل كاف. وقد يؤدي ذلك إلى عدد من الأعراض، مثل التعب، وضعف القدرة على تحمّل البرد، وزيادة الوزن. أما لدى الأطفال، يؤدي قصور الدرقية إلى التأخر في النمو والتطوّر الفكري، وهو ما يسمى الفدامة في الحالات الشديدة. المسبب الرئيسي عالميًا لقصور الدرقية هو نقص اليود في النظام الغذائي.[1][2] أما الدول والتي يحوي نظام سكانها الغذائي على كمية كافية من اليود، فالسببين الأكثر شيوعًا لقصورر الدرقية هما مرض مناعي ذاتي يدعى التهاب الغدة الدرقية لهاشيموتو وأسباب علاجية المنشأ مثل علاج فرط الدرقية.[3] وأما الأسباب الأقل شيوعًا فتشمل: إصابة الوطاء أو الغدة النخامية الأمامية، أدوية معينة، عدم وجود غدّة درقيّة فعّالة عند الولادة، أو عملية سابقة للغدة الدرقية. يُمكن تشخيص قصور الدّرقية، عند الاشتباه به، بواسطة اختبارات الدم التي تقيس مستويات هرمون منبّه الدرقيّة (TSH) والثيروكسين.
يمكن علاج قصور الدرقية بالليفوثيروكسين المصنّع؛ ويتم تعديل الجرعة حسب الأعراض واعتدال مستويات هرمون منبّه الدرقية (TSH). في الدول الغربية، يحدث قصور الدرقية في %0.4-0.3 من السكان، بينما يُعتقد أن قصور الدرقية دون السريري، شكل أخف من قصور الدرقية يتمتيز بمستويات ثيروكسين طبيعية ومستوى مرتفع لهرمون منبّه الدرقية، يحدث في %8.5-4.3 من السكان. ومن المعروف أن الكلاب أيضًا يحدث لديها قصور الدرقية، وفي ظروف نادرة قد يحدث ذلك في القطط والخيول.
علامات وأعراض
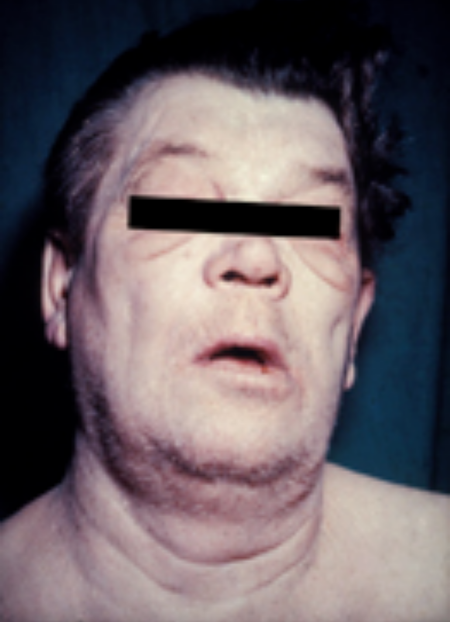
عادة ما لا تكون أبة أعراض أو تكون أعراض خفيفة فقط لدى الأشخاص الذين يعانون من قصور الدرقية. ترتبط علامات وأعراض عديدة بقصور الدرقية، وقد يكون ذلك ذو صلة بالسبب الكامن من وراء قصور الدرقية، أو تأثير مباشر لعدم وجود كمية كافية من هرمونات الدرقية.[4][5] قد يظهر التهاب الغدة الدرقية لهاشيموتو مع تأثير الحجم الناتج عن الدراق (تضخم الغدة الدرقية).[4]
| أعراض [6] | علامات[6] |
|---|---|
| الإرهاق والتعب | بشرة جافة وخشنة |
| الإحساس بالبرد وعدم تحمّل البرد | أطراف باردة |
| ضعف الذاكرة والقدرة على التركيز | وذمة مخاطية (ترسبات موكوبوليساكاريد في الجلد) |
| الإمساك وعسر الهضم | فقدان الشعر |
| زيادة الوزن بالرغم من فقدان الشهية | بطء القلب |
| ضيق النفس | استسقاء الأطراف |
| بحة الصوت | تأخر الاسترخاء في المنعكسات الوترية |
| ضعف الرغبة الجنسية[7] في الجنسين | متلازمة النفق الرسغي |
| في الإناث، غزارة الطمث (وبعدها ندرة الطموث وحتى انقطاع الحيض) | انصباب جنبي، واستسقاء بطني، وانصباب تاموري |
| مذل | تساقط الثلث الخارجي من الحواجب (في البالغين) |
| ضعف السمع |
غيبوبة الوذمة المخاطية
غيبوبة الوذمة المخاطية هي حالة نادرة ولكنها مهددة للحياة من قصور الدرقية المتطرّف. قد تحدث في أولئك الذين لديهم قصور الدرقية عندما يمرضون مرض آخر، ولكن قد تكون العرض الأول من قصور الغدة الدرقية. يتميّز المرض بدرجة حرارة جسم منخفضة للغاية (دون رعشة)، والارتباك، وبطء القلب وانخفاض جهد التنفس. قد تكون هناك علامات جسديّة تدلّ على قصور الدرقية، مثل التغييرات الجلدية أو ضخامة اللسان.[8]
الحمل
يرتبط قصور الدرقية حتى الخفيف أو دون السريرية مع ضعف الخصوبة وزيادة خطر الإجهاض التلقائي.[9] قصور الدرقية في مرحلة مبكرة من الحمل، حتى مع أعراض محدودة أو معدومة، قد يزيد من خطر الإصابة بمقدّمات الارتعاج، وأولاد مع انخفاض الذكاء، وخطر وفاة الرضع في الفترة المحيطة بالولادة.[9][10] تُصاب النساء بقصور الدرقية في 0.3-0.5% من حالات الحمل.[10] كما يرتبط قصور الدرقية دون السريري أثناء الحمل بسكري الحمل وولادة الطفل قبل أسبوع 37 من الحمل.[11]
الأطفال
قد يكون الأطفال حديثي الولادة مع قصور الدرقية ذوي وزن وطول طبيعي عند الولادة (على الرغم من أن الرأس قد يكون أكبر من المتوقّغ وقد يكون اليافوخ الخلفي مفتوح). قد يعاني بعضهم من النعاس، وانخفاض قوة العضلات، وبكاء مبحوح الصوت، ومشاكل في الإطعام، والإمساك، وضخامة اللسان، وفتق السرّة، وجفاف الجلد، وانخفاض درجة حرارة الجسم، واليرقان.[12] أما الدُّراق فهو أمر نادر في هذه الحالة، على الرغم من أنه قد يتطوّر في وقت لاحق في الأطفال ذوي غدة درقية التي لا تنتّج هرمون غدة درقية ذو أداء سليم.[12] قد يتطوّر الدّراق كذلك عند الأطفال الذين ينشأون في المناطق التي تعاني من نقص اليود.[13]
أسباب المرض
ينتج قصور الدرقية من خلل في وظيفة الغدى الدرقية نفسها (قصور الدرقية الأولي) أو عن طريق تحفيز غير كافي بواسطة هرمون منبّه الدرقية (قصور الدرقية المركزي).[1][14] قصور الدرقية الأولي هو نحو ألف مرة أكثر شيوعًا من قصور الدرقية المركزي.[15]
يُعتبر نقص اليود السبب الأكثر شيوعًا لقصور الدرقية الأولي والدُّراق المتوطّن في جميع أنحاء العالم.[1][2] أما في المناطق مع الكميات الكافية من اليود، عادة ما ينتج قصور الدرقية من مرض مناعي ذاتي يدعى التهاب الغدة الدرقية لهاشيموتو (التهاب الغدة الدرقية المناعية المزمنة).[1][2] قد يرافق الدُّراق التهاب الغدة الدرقية لهاشيموتو. يتميّز التهاب الغدة الدرقية لهاشيموتو بارتشاح الغدة الدرقية عن طريق خلايا لمفاوية تائية وأجسام مضادة ذاتية ضد مستقدرات خاصة للغدة الدرقية مثل بيروكسيدراز الغدة الدرقية، ثايروغلوبولين ومستقبلة هرمون منبّه الدرقية.[1]
بعد الولادة، تُصاب حوالي 5% من النساء بالتهاب الدرقية التالي للوضع والذي يحدث حتى تسعة أشهر بعد الولادة.[16] ويتميّز بفترة قصيرة من فرط الدرقية تليها فترة من قصور الدرقية؛ تبقى 20-40% من هذه الحالات مع قصور درقية دائم.[16]
يرتبط التهاب الغدة الدرقية المناعي الذاتي مع غيرها من أمراض مناعية مثل سكري النمط الأول، وفقر الدم الخبيث، والوهن العضلي الوبيل، والداء البطني (السيلياك)، والتهاب المفاصل الروماتويدي، والذئبة الحمامية المجموعية.[1] وقد تحدث كجزء من متلازمة الغدد الصماء بالمناعة الذاتية (النمط الأول والنمط الثاني).[1]
السببيات والأشكال الرئيسية
يعاني من قصور الدرقية نحو 3% من السكان.[17] السبب الرئيسي عالمياً هو عوز اليود. عند الأفراد الذين مستويات اليود لديهم سوية الأسباب هي التهاب الغدة الدرقية لهاشيموتو أو قلة النسيج الدرقي (بعد استئصال جراحي مثلاً) أو عوز هرمونات الوطاء أو النخامية.
يُصنّف قصور الدرقية حسب العضو المصدر[18][19] للمرض إلى:
- أولي، وأشيع أشكاله التهاب الغدة الدرقية لهاشيموتو وقصور الدرقية التالي لمعالجة فرط الدرقية باليود المشع.
- ثانوي، نتيجة قصور إفراز الهرمون المنبه للدرقية من النخامية. ينجم هذا في أغلب الحالات عن تضرر النخامية نتيجة لورم أو إشعاع أو جراحة[20].
- ثالثي، نتيجة نقص إفراز العامل المطلق للموجهة الدرقية من الوطاء.
الأمراض الناتجة عن قصور الدرقية
- يتسبب في حالة الفَدامَة (Cretinism) ،أو ما يطلق عليه القماءة، في مرحلة الطفولة حيث يبدو الجسم قصيراً والرأس متسعاً والرقبة قصيرة. كما يؤثر نقص الهرمون علي النضوج العقلي للطفل وقد يحدث تخلفاً عقلياً دائماً وتأخراً في النضوج الجنسي.
تشخيص المرض
تعتبر الفحوصات المختبرية لمستويات هرمون منبّه الدرقية أفضل اختبار أول لفحص قصور الدرقية؛ في كثير من الأحيان يتم فحص مستويات هرمون منبّه الدرقية ثانيةً بعد عدة أسابيع للتأكيد.[21] قد تكون المستويات غير طبيعية في سياق أمراض أخرى، من هنا اختبارات فحص هرمون منبّه الدرقية في المرضى في المستشفى هو أمر غير مفضّل إلا في حال اشتباه قوي بخلل وظيفة الغدة الدرقية.[1] تشير مستويات مرتفعة لهرمون منبّه الدرقية أن الغدة الدرقية قد لا تنتج ما يكفي من هرمون الدرقية، ولذلك في الكثير من الأحيان تُفحص بعد ذلك مستويات هرمون T4 الحر.[1][22] من غير المفضل قياس مستويات الهرمون T3 لتقييم قصور الغدة الدرقية.[1] هناك عدد من مقاييس تقييم الأعراض لقصور الغدة الدرقية؛ توفّر هذه المقاييس درجة من الموضوعية ولكن استخدامها للتشخيص محدود الانتشار.[1]
ترتبط العديد من حالات قصور الغدة الدرقية مع ارتفاعات معتدلة في مستويات كيناز الكرياتين وإنزيمات الكبد في الدم. وعادة ما تعود مستوياتها إلة وضعا الطبيع عند معالجة قصور الدرقية بشكل تام.[1] قد ترتفع كذلك مستويات الكولسترول، والبروتين الدهني منخفض الكثافة، والبروتين الشحمي أ؛[1] تأثير قصور الدرقية دون السريري على بارامترات الدهون أقل واضحة المعالم.[13]
منع
يمكن منع قصور الدرقية عند السكان بإضافة اليود إلى الأغذية الشائعة. وقد ألغى هذا الإجراء قصور الدرقية المتوطّن في مرحلة الطفولة حيث كانت شائعة في السابق. بالإضافة إلى تعزيز استهلاك الأغذية الغنية باليود مثل منتجات الحليب والأسماك، أضافت بعض الدول ذات النقص المعتدل لليود الملح بشكل شامل لليود (الملح المعالج باليود).[23] وبتشجيع من منظمة الصحة العالمية،[24] تستخدم اليوم 130 دولة الملح المعالج باليود، حيث يتناول اليوم الملح المعالج باليود %70 من سكان العالم. في بعض الدول، يُضاف الملح المعالج باليود إلى الخبز.[23] بالرغم من ذلك، ظهر نقص اليود من جديد في بعض الدول الغربية نتيجة للمساعي في الحد من تناول الملح.[23]
النساء الحوامل والمرضعات، اللواتي يحتجن إلى %66 أكثر يود مقارنة بغير الحوامل، قد لا تزال غير حاصلة على كمية كافية من اليود.[23][25] توصي منظمة الصحة العالمية باستهلاك يومي من 250 ميكروغرام للنساء الحوامل والمرضعات.[26] لأن العديد من النساء لن تحقق ذلك من المصادر الغذائية وحدها، توصي الجمعية الأمريكية للغدة الدرقية تناول 150 ميكروغرام بأقراص استكمالية عن طريق الفم.[27][28]
العلاج
التعويض الهرموني
معظم الأشخاص المصابين بأعراض قصور الدرقية وتم علاج نقص الثيروكسين الرباعي عن طريق ثيروكسين طويل الأمد يدعى ليفوثايروكسين (ل-ثيروكسين).[1][5] في المرضى الأقل عمرا أو الأصحاء المصابون بقصور الدرقية البين: فإن التعويض الهرموني الكامل(محددة بالوزن) يمكن البدء بها مباشرة بعد التشخيص، أما المرضى الأكبر عمرا أو المصابين بأمراض القلب فيتم البدء بجرعة مخفضة لتجنب الجرعة الزائدة أو حدوث المضاعفات.[1][14] الجرعات الأقل قد تكون مجدية عند مرضى قصور الدرقية دون السريري، أما مرضى قصور الدرقية المركزي قد يحتاجون جرعة أكثر من المعدل العام.[1]
نسبة الثيروكسين وهرمون المحفز للدرقية الحر في الدم يستخدم لتحديد فاعلية الجرعة. يتم ذلك بين( 4-8 ) أسبوع بعد بدء العلاج أو تغيير جرعة الليفوثيروكسين. بعدما يتم الوصول للجرعة المناسبة، يتم تكرار الفحص كل( 6-12 ) شهر، إلا إذا كان هنالك تغيير في الأعراض على المريض.[1] في الأشخاص المصابين بقصور ادرقية المركزي أو الثانوي، مستويات هرمون المحفز للدرقية ليست محددا مهما للقيام بالتعويض الهرموني ويتم اعتماد مستويات الثيروكسين الرباعي لذلك.[1][15] الليفوثيروكسين يفضل أخذه( 30-60 ) دقيقة قبل الفطور، أو أربع ساعات بعد الأكل،[1] لأن بعد المواد مثل الغذاء والكالسيوم من الممكن أن توقف عملية امتصاص الليفوثيروكسين.[29] لا يوجد طريقة يمكن من خلاها زيادة افراز الغدة الدرقية بشكل مباشر.[5]
ليوثيرونين
إضافة الليوثيرونين (الثيروكسين الثلاثي) للليفوثيروكسين تم التوصية به كإجراء لزيادة التحكم بأعراض قصور الدرقية، لكن ذلك لم يتم التأكد منه عن طريق الدراسات.[2][5][30] في عام(2007) جمعية الغدة الدرقية البريطانية أعلنت ان الثيروكسين الرباعي والثلاثي معا لديهم نسبة أعلى من الأعراض الجانبية، ولا فائدة تذكر من إضافة الثيروكسن الثلاثي عن استخدام الرباعي وحده.[5][31] بشكل مشابه فإن أخر مستجدات العلاج الأمريكية لا تشجع العلاج المدمج من الثلاثي والرباعي معا بسبب نقص الأدلة العلمية اللازمة، على الرغم من وجود بعض المرضى الذين أظهروا تحسنا على العلاج المدموج.[1] العلاج بالليوثيرونين وحدهلم يحظى بدراسة كافية ليحدد ما إن يصلح للعلاج، لكن بسبب قصر عمر نصف الحياة فإنه يجب أخذه بأوقات أكثر يوميا.[1]
مرضى قصور الدرقية الذين استمرا بالمعاناة حتى بعد علاجهم بالليفوثيروكسين قد يتطلب الأمر أن يوصف لهم بالليوثيرونين كعلاج مساعد. في( 2012 ) كانت مستجدات العلاج من جمعية الغدة الدرقية الأوروبية توصي بإعطاء العلاج للمرضى على الرغم من الطبيعة المزمنة للمرض أن الأسباب التي أدت للأعراض الأخرى لدى المريض يجب إهمالها. إضافة الليوثيرونين يجب أن يكون تجريبيا، لمدة 3 أشهر، مع وجود جرعة الليفوفلوكساسين الاعتيادية.[32] المستجدات العلاجية تهدف إلى تسريع بالوصول إلى الاستخدام الأمن والتخلص من الاستخدام غير المدروس له.[32]
الغدة الدرقية الحيوانية المجففة
الغدة الدرقية المجففة هي غدة حيوانية المنشأ مستخلصة غالبا من الخنازير،[5] هي تعطي علاجا مدموجا من الثيروكسين الرباعي والثلاثي.[5] تحتوي كذلك على الكاسيتونين (هرمون منتج من الغدة الدرقية يدخل في تنظيم مستى الكالسيوم في الدم)،و الثيروكسين الأحادي والثنائي، وهما غير موجودين في العلاجات الدوائية الهرمونية المصنعة.[33] كانت هذه المستخلصة يوما أحد أهم العلاجات المستخدمة، لكن استخدامها اليوم غير مدعوم بالأدلة العلمية.[2][5] جمعية الغدة الدرقية البريطانية والمستجدات العلاجية الأمريكية لا تنصح استخدامها.[1][31]
قصور الدرقية دون السريري.
هنالك أدلة قليلة على وجود فائدة من علاج قصور الدرقية دون السريري، وهل يحول دون الوصول إلى فرط الدرقية. قصور الدرقية دون السريري غير المعالج يزيد من احتمالية الإصابة بأمراض الشريان التاجي.[34] في عرض للمرض في عام( 2007 ) وجد أن هنالك لا فائدة من الاستعاضة الهرمونية إلا لبعض المرضى الذين لديهم (بعض المؤشرات الدهنية وشكوك في وظائف البطين الأيسر).[35] كما لا يوجد علاقة للقصور دون السريري بكسور العظام.[36]
منذ 2008 الإجماع الأمريكي والبريطاني أن الناس عامة من لديهم مستويات الهرمون المحفز للدرقية اقل من( 10 مل)(وحدة عالمية)/ لتر فإنهم لا يحتاجون للعلاج [4][24][45] المستجدات العلاجية الأمريكية أوصت بالعلاج إذا أن من لديهم مستويات الهرمون مرتفعة لكن أقل من( 10 )وتظهر عليهم أعراض قصور الدرقية، أولديهم مضادات حيوية للبيروكسيديز الدرقي، تاريخ مرضي للقلب، أو أنهم معرضين لأمراض القلب.[1]
الفيسيولوجيا المرضية
هرمون الدرقية ضروري لعمل العديد من أنسجة الجسم، في الإنسان السليم، الغدة تفرز بشكل دائم الثايروكسين الرباعي(T4)، الذي يتحول إلى الثايروكسين ثلاثي اليود في أعضاء الجسم الأخري عن طريق الانزيم المعتمد على السيلينيوم (الايدوثيرونين ديأيوداينيز ).[37] الثايروكسين الثلاثي يرتبط في مستقبل الهرمون الدرقي في نواة الخلية، وهناك يعمل على تحفيز تشغيل بعض الجينات إإنتاج مجموعة من البروتينات.[38] بالإضافة يرتبط الهرمون ب αvβبروتين غلاف الخلية الانتجرن αvβ فيعمل على تحفيز الناقل العكسي للصوديوم والهيدروجين ويقوم بمجموعة أخرى من الوظائف مثل تكوين الأوعية الدموية ونمو الخلية.[38] في الدم أغلب هرمونات الدرقية (99.97%) مربوطة ببروتينات الناقلة مثل الغلوبولين الرابط للثايروكسين، فقط الهرمون الغير مرتبط بالبوتينات الناقلة هو النشيط حيويا.[1]
الغدة الدرقية هي المصدر الوحيد لهرمون الدرقية عملية تصنيع الهرمون تتطلب اليود والحمض الأميني التاروسين، يتم أخد اليود من الدم ويتداخل مع جزيئات الغلوبولين الدرقي. العملية يتحكم به الهرمون المنشط للدرقية الذي تنتجه الغدة النخامية، عدم وجود كمية كافية من اليود من الممكن أن تسبب نقص في هرمون الدرقية.[14]
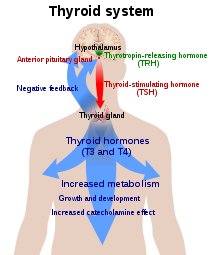
يلعب كل من المهاد والغدتين النخامية والدرقية دورا مهما في المحافظة على هرمون الدرقية بنسبته الطبيعية، إنتاج الهرمون المحفز للدرقية من الغدة النخامية الأمامية يتحفز من الهرمون المطلق الثيروتروبين المنتج من المهاد، إنتاج كل من الهرمون المحفز للدرقي والهرمون المطلق الثثيروتروبين يقل بالارتجاع السلبي للثايروكسين، عدم وجود كمية كافية من الهرمون المطلق الثثيروتروبين والذي بحدث نادرا يؤدي إلى عدم وجود كمية كافي من الهرمون المحفز للدرقية ومن ثم نقص في هرمون الدرقية .[15]
الحمل يؤدي إلى تغيرات واضحة في وظائغ الهرمون الدرقي، الغدة يزداد حجمها بنسبة 50% وتزيد الحاجة لليود. كثير من النساء تعمل لديهن الغدة الدرقية بشكل طبيعي لكن هنالك أدلة مناعية على وجود مضادات ذاتية للغدة أو وجود نقص في اليود أو يتطور لديهن عرض يدل على حدوث قصور الدرقية قبل أو بعد الولادة.[27]
التشخيص
الفحوصات المخبرية لمستويات الهرمون المحفز للدرقية في الدم يعتبر من أفضل الفحوص الأولية لقصور الدرقية، يعقد فحص آخر للهرمون بعد عدة أسابيع للتأكد.مستويات الهرمون قد تكون غير طبيعية بسبب امراض أخرى.[21] وفحص الهرمون المحفز للدرقية لمرضى المقيمين في المستشفى ليس مرغوبا إلا مع وجود شك كبير في اختلال وظائف الدرقية.[1] ارتفاع هرمون المحفز للدرقية دليل على عدم إنتاج الدرقية لهرمونها بكمية كافية وعادة ما يرافقه وجود كمية جيدة من الثايروكسين الرباعي في للدم، حساب مستويات الثيروكسين الثلاثي غير مرغوب للقيام به عند فحص قصور الدرقية.[1][22] هنالك مجموعة من الأعراض المجدولة لقصور الدرقية قد لا تفيد في تشخيص المرض لكنها تعطي مؤشرات جيدة له.[1]
| هرمون المحفز للدرقية | الثيروكسين الرباعي | النتيجة |
|---|---|---|
| طبيعي | طبيعي | عمل الغدة طبيعي |
| مرتفع | منخفض | قصور الدرقية البين |
| طبيعي/ ناقص | منخفض | قصور الدرقية المركزي |
| مرتفع | طبيعي | قصور الدرقية الغير سريري |
كثير من حالات قصور الدرقية مرتبطة بارتفاعات طفيفة بالكيراتين كايناز وانزيمات الكبد في الدم. عادة مايعودون للنسب الطبيعية بعد العلاج التام لقصور الدرقية، .[1] مستويات الكولوسترول، البروتين الشحمي قليل الكثافة، والبروتين الشحمي أ، قد ترتفع.[1] تأثير قصور الدرقية دون السؤريري على مستويات الدهون في الجسم ليست محددة بعد.[13]
قصور الدرقية الشديد وغيبوبة الوذمة المخاطية تتصفان بأنهما تترافقان مع مستويات منخفضة من الصوديوم في الدم وارتفاع في هرمون المدر للبول معا، كذلك تدهور مؤقت حاد في وظائف الكلى لعدة أسباب.[8]
تشخيص قصور الدرقية دون تحسس وجود أي كتل في الغدة الدرقية لا يتطلب تصوير للغدة، مع ذلك في حال الحساس بوجود خلل في شكل الدرقية فإنه يجب تصوير الغدة.[21] إن وجود أجسام مضادة ضد البيروكسيديز الدرقي يجعل وجود عقد درقية هو بسبب المرض المناعي الدرقي وليس قصور الدرقية، ولكن إذا وجدت شكوك حول ذلك يجب أخذ خزعة من الغدة.[1]
إذا كانت مستويات هرمون المحفز للدرقية طبيعية أو أقل ومستويات الثايروكسين الرباعي الحر منخفضة، فإن هذه الفحوصات تدل بشكل جيد علوى وجود قصور الدرقية ( عدو وجود إفراز كافي لهرمون المحففز للدرقية أو الهرمون المطلق للثيروكسين من النخامية أو المهاد). قج يكون هناك أعراض علامات أخرى لقصور النخامية مثل حدوث اختلالات في الدورة الشهرية لدى الإناث أو عدم كفاءة الغدة الكظرية. قد يكون هنالك أيضا دليل على وجود كتلة في الغدة النخامية مثل حدوث صداع وتغييرات في الرؤية.في حال حدوث قصور الدرقية المركزي يجب التحقق من مسبباته.[15][21]
قصور الدرقية البين
في قصور الدرقية البين الأولي، مستويات هرمون المحفز للدرقية مرتفعة بينما هناك انخفاض في الثيروكسين الثلاثي والرباعي، قصور الدرقية البين قد يتم تشخيصه عند الأشخاص الذين عانو من ارتفاع هرمون المحفز للدرقية أكثر من مرى حيث تصل مستوياته إلى أكثر من( 5 مل)(وحدة عالمية)/ للتر، أعراض مناسبة، ووجود مستويات الثيروكسين الرباعي على الحافة الدنيا للمستوى الطبيعي.[39] قد يتم تشخيصه كذلك عند الذين يصل لديهم هرمون المحفز للدرقية أكثر من. 10 مل(وحدة عالمية)/ مللتر.[39]
قصور الدرقية الدون السريري
قصور الدرقية دون السريري هو نوع خفيف من قصور الدرقية يتصف بارتفاع هرمون المحفز للدرقية ووجود مستويات طبيعية للثيروكسنين في الدم،[40][41] هذا النوع من قصور الدرقية غالبا ما يكون سببه التهاب الغدة الدرقية المناعي الهاشيموتو .[42] في البالغين يتم تشخيصه عندما تكون مستويات هرمون المحفز للدرقية أكبر من (5 مل)(وحدة عالمية)/ مللتر وأقل من ( 10 مل)(وحدة عالمية)/ مللتر.[39] حدوث المرض متنوع وقد لا تحدث الأعراض والعلامات المعروفة لقصور الدرقية.[40] هنالك نسبة من مرضى قصور الدرقية دون السريري يصابون بمرض قصور الدرقية البين كل عام. في المرضى الذين لديهم أجسام مناعية تم ملاحظتها ضد البيركسيديز الدرقي يصاب بقصور الدرقية البين( 4.3%)،أما الذين لم تلاحظ عندهم الأجسام المضادة فتنخفض النسبة إلى( 2.6%).[1] مرضى قصور الدرقية دون السريري ولديهم أجسام مضادة واضحة ولا يتطلبون علاجا يجب عليهم إعادة فحوصات وظائف الغدة الدرقية بشكل دوري (سنوي) و بفترات أقصر من المرضى الذين لم تلاحظ عندهم الأجسام المضادة.[21]
الحمل
خلال الحمل الغدة الدرقية يجب أن تنتج( 50% ) أكثر من هرمونها لإنتاج كمية تكفي لتطور الجنين والأم.[11] في الحمل الثيروكسين الحر قد يكون أقل من المتوقع بسبب زيادة ارتباطه بالجلوبيلين الدرقي وانخفاض ارتباطه بالألبيومن. يجب أن يتم تصحيح جداول الفحوصات لتتناسب مع مراحل الحمل،[27] أو يجب اعتماد فحص الكلي للثيروكسين لتشخيص اعتلالات الدرقية.[1] هرمون المحفز للدرقية قد يكون كذلك أقل من الطبيعي خاصة في الثلث الأول للحمل، وكذلك تعديل جداول الفحص للتناسب مع الحمل.[1][27]
خلال الحمل، قصور الدرقية دون السريري يعرف بأنه وجود هرمون المحفز للدرقية بين(2.5- 10 مل)(وحدة عالمية)/ مللتر. مع وجود الثيروكسين بمعدلاته الطبيعية، أما من لديها هرمون المحفز أكثر من( 10 مل)(وحدة عالمية)/ مللتر فيعتبرون مصابين بقصور الدرقية البين حتى وإن كانت معدلات الثيروكسبن طبيعية.[27] الأجسام المضادة للبيروكسيديز الدرقي قد تكون مهمة في تحديد العلاج اللازم، لذلك يجب إجراء هذه الفحوصات في المرأة التي لديها فحوصات الدرقية غير طبيعية.[1]
فحص وتحديد الأجسام المضادة للبيروكسيديز الدرقي يعتبر جزء من التقببم المرضي للإجهاض المتكرر، لأن أي توقف دقيق في عمل الدرقية قد يكون مصاحبا لفقدان الحمل،[1] لكن هذا التقييم ليس عالميا،[43] ووجود الأجسام المضادة قد لا يتنبأ بما سيحدث مستقبلا.[44]
الوقاية
قصور الدرقية قد يتم تجنبه في المجتمعات عن طريق إضافة اليود للأطعمة شائعة التناول.هذا الإجراء الصحي العام ساعد في التخلص من مرض قصور الدرقية المزمن عن الأطفال في البلدان التي كان شائعا فيها. بالإضافة إلى زيادة استهلاك الأطعمة الغنية باليود مثل السمك والألبان. تم أيضا إضافة اليود للملح.[23] بتشييع من منظمة الصحة العالمية,[24] (130 ) لدا لديهم الان ملح باليود و70% من المجتمعات حول العالم بستخدمون الملح باليود. في بعض البلاد، الملح باليود يضاف للخبز.[23] على الرغم من ذلك نقص اليود عاد للظهور في بض البلاد الغربية في خضم المحاولة لتقليل كمية الملح المستخدمة.[23]
المرأة الحامل والمرضع والتي تتطلب اليود بسبة( 66% ) أكثر من المرأة غير الحامل.قد لا يزالون لا يحصلون على الكمية الكافية .[23][25] حيث أن منظمة الصحة العالمية تنصح ب( 250ملغ ) يوميا من اليود للحامل والمرضع.[26] وحيث أن كثير من النساء قد لات تحصل على هذه الكمية من الغذاء وحده، جمعية الغدة الدرقية الأمريكية تنصح بأخذ( 150ملغ )من اليود يوميا على شكل حبوب.[27][28]
الفحص
فحص الغدة الدرقية يجرى في الأطفال حديثي الولادة في العديد من الدول عادة باستخدام هرمون المحفز للدرقية، هذا يؤدي إلى الاكتشاف المبكر للعديد من الحالات وبالتالي تجنب حدوث المضاعفات.[45] يعد فحص الدرقية أكثر فحص شائع للدرقية.[46] بينما يقوم الفحص المعتمد على الهرمون المحفز للدرقية باكتشاف معظم الأسباب، إضافة فحص الثيروكسين الرباعي مطلوب لاكتشاف الاسباب النادرة لقصور الدرقية عند حديثي الولادة.[12] إذا كان فحص الثيروكسين الرباعي من ضمن الفحوصات للأطفال حديثي الولادة، فإن هذا سيساعد في كشف قصور الدرقية الخلقي ذات المنشأ الوسطي في (1:16000 ) إلى( 1:160000 ) طفل. على اعتبار أن هؤلاء الأطفال لديهم قصور في هرمونات الكظرية الأخرى، لاكتشاف المبكر لهذه الحالات قد يجنبنا المضاعفات.[15]
في اليالغين، فحص الدرقية على مستوى المجتمع بأكمله لا يزال موضوعا للمجادلة والنقاش. بعض المنظمات مثل فريق عمل الولايات المتحة للخدمات الوقائية أصدر أن دليل الجدوى غير كافي لدعم توير الفحص للجميع بشكل دوري.[47] بينما قامت منظمات خرى مثل منظمة الدرقية الأمريكية نصحت بفحص متقطع بعد عمر معين في كلا الجنسين أو فقط عند السيدات.[1] فحص الدرقية قد يكون مناسب في بعض الحالات الشائع فيها قصور الدرقية مثل: وجود أمراض مناعية، وجود تاريخ مرضي قوي في العائلة لأمراض الدرقية، أولئك الذين تعرضوا لليود المشع أو أي علاج إشعاعي للرقبة، والذين خاضوا مسبقا جراحة للدرقية، أو كان فحص الدرقية غير طبيعي، أو من لديه أمراض نفسية، أو منت يأخذون الأميودارون أو الليثيوم ، بالإضافة إلى مجموعة من الأعراض الخاصة بالقلب والجلد.[1] يوصى بقيام فحص الدرقية بشكل سنوي لمن لديهم متلازمة داون ،لأن لديهم احتمالية عالية للأمراض الدرقية.[48]
الأوبئة
في العالم حوالي بليون إنسان لديهم نقص في اليود، على العلم أنهم لا يعرف كم احتمالية اصابتهم بقصور الدرقية، في المجتمعات الكبيرة اعتمادا على دراسات في مدن غربية لديها نسبة يود كافية.[49] .3-.4% من المجتمع لديهم قصور الدرقية البين، نسبة كبيرة (4.3-8.5% ) لديهم قصور الدرقية دون السريري.[1] من من لديهم قصور درقية دون سريري( 80% ) لديهم هرمون المحفز للدرقية أقلمن 10 مل(وحدة عالمية)/لتر حيث تعتبر إشارة لبدء العلاج..[41] الأطفال المصابين بقصور الدرقية البين عادة ما يختفي المرض وقلة ما يتطور لديهم لقصور الدرقية البين (حسب ما هو متوقع نتيجة لتطور الأجسام المضادة ومستوى الهرمون المحفز للدرقية، وجود مرض ، وتضخم الغدة الدرقية.[50]
النساء أكثر عرضة للإصابة بقصور الدرقية أكثر من الرجال. في الدراسات المجتمعية النساء أكثر عرضة لارتفاع مستوى هرمون المحفز للدرقية أعلى من (10مل/لتر) بسبع مرات.[1] (2-4%)من الناس المصابين بقصور الدرقية الدائم يتطورلديهم لقصور الدرقية البين كل عام الاحتمالية أكبر لمن لديهم أجسام مضادة لبيروكسيديز الدرقي [1][41] قصور الدرقية دون السريري يتوقع أن يصيب( 2% ) من الأطفال ، في البالغين قصور الدرقية البين أكثر شيوعا في الكبار سنا والقوقازيين.[40] هناك معدلات عالية باعتلالات الغدة الدرقية، وأكثر ظاهرة معروفة هي قصور الغدة الدرقية، في الأشخاص المصابين بمتلازمة داون [12][48] ومتلازمة تيرنر.[12]
قصور الدرقية الشديد وغيبوبة الوذمة المخاطية نادر، مع احتمالية حدوثه(0.22 )كل مليون شخص بالسنة. معظم الحالات تحدث في النساء أكبر من( 60 ) عاما على الرغم من حدوثها في كافة لأعمار.[8] معظم قصور الدرقية هو أولي، قصور الدرقية الثانوي يصيب( 1:20000 -1:80000 ) من المجتمع أو واحد كل ألف مصاب بقصور الدرقية.[15]
التاريخ
الارتباط بين الغدة الدرقية والوذمة المخاطية تأسس في أواخر القرن 19. عندما تم إزالة الغدة الدرقية من الناس والحيوانات حيث ظهر تحسيننا في الأعراض مع زرع أنسجة غدة درقية الحيوان.[2] اليود تم اكتشافه في الأعشاب البحرية في عام 1811 من قبل برنارد كورتوا، وارتبط تناول اليود مع حجم تضخم الغدة الدرقية في عام 1820 من قبل جان فرانسوا.[51] اقترح غاسبار أدولف في عام 1852 أن الإصابة بتضخم الغدة الدرقية المستوطن كان نتيجة لعدم تناول ما يكفي من اليود، وأظهرت يوجين باومان ان اليود موجود في أنسجة الغدة الدرقية في عام 1896.[51]
في عام 1891، قام الطبيب الإنجليزي جورج موراي بحقن مستخلص الغدة الدرقية تحت جلد الأغنام،[52] وجاء بعده علماء آخرون وبقت قصير من خلال صيغة عن طريق الفم.[2][53] وقدم آخرون هرمون الغدة الدرقية بشكل نقي في عام 1914 وأيضاً تم استخدام هرمون الغدة الدرقية الاصطناعية 1930 وبعدها أصبح مستخلص الغدة الدرقية الحيواني متاحا، ويستخدم على نطاق واسع. وقد تم تحديد يوثيرونين في عام 1952.[2]
حيوانات أخرى
ظهرت تغييرات مميزة في جلد الوجه ل لابرادور المصاب في قصور الغدة الدرقية. في الممارسة البيطرية، الكلاب هي الأنواع الأكثر تأثرا عادة بقصور الغدة الدرقية. معظم الحالات تحدث نتيجة لقصور الغدة الدرقية الابتدائي والتي يتم التعرض لها فعليا بنوعين: التهاب الغدة الدرقية والغدد اللمفاوية، والتي ربما تكون مدفوعة المناعة ويؤدي إلى تدمير وتليف الغدة الدرقية، وضمور مجهول السبب، الأمر الذي يؤدي إلى الاستبدال التدريجي للغدة بواسطة الأنسجة الدهنية.[54][55] غالبا ما يكون هناك الخمول، والتعصب الباردة، وممارسة التعصب، وزيادة الوزن. وعلاوة على ذلك، تعتبر التغيرات الجلدية ومشاكل الخصوبة موجودة في الكلاب المصابة بالغدة الدرقية، وكذلك عدد من الأعراض الأخرى.[55] مثل علامات الوذمة المخاطية يمكن أن ينظر إليه في الكلاب، مع بروز طيات الجلد على الجبين، وحالات الوذمة المخاطية غيبوبة.[54] ويمكن تأكيد التشخيص من خلال فحص الدم، والفحص السريري وحده قد يؤدي إلى تشخيص عالي أو واضح.[54][55] ويرتبط التهاب الغدة الدرقية والغدد اللمفاوية مع الأجسام المضادة للكشف ضد ثايروجلوبولين، على الرغم من أنها أصبحت عادة لا يمكن الكشف عنها في مرحلة متقدمة من المرض.[55] العلاج هو مع استبدال هرمون الغدة الدرقية.[54]
الأنواع الأخرى من الحيوانات التي تتأثر، أقل شيوعا وتشمل القطط والخيول، وكذلك الحيوانات المنزلية الكبيرة الأخرى. ففي القطط، الغدة الدرقية عادة ما تكون ناتجة عن المعاملة الطبية مثل الجراحة أو الإشعاع في الخيول الصغيرة ، وقد تم الإبلاغ عن قصور الغدة الدرقية الخلقي في الغالب في غرب كندا وكان له علاقة مرتبطة في النمط الغذائي للأم.[54]
مقالات ذات صلة
- علامة هيرتوجي (علامة الملكة آن)
المراجع
- Garber, JR; Cobin, RH; Gharib, H; Hennessey, JV; Klein, I; Mechanick, JI; Pessah-Pollack, R; Singer, PA; et al. (December 2012). "Clinical Practice Guidelines for Hypothyroidism in Adults" ( كتاب إلكتروني PDF ). Thyroid. 22 (12): 1200–1235. doi:10.1089/thy.2012.0205. PMID 22954017. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 9 مارس 2017.
- Chakera, AJ; Pearce, SH; Vaidya, B (2012). "Treatment for primary hypothyroidism: current approaches and future possibilities". Drug Design, Development and Therapy (Review). 6: 1–11. doi:10.2147/DDDT.S12894. PMC . PMID 22291465.
- Dennis L. Kasper; Anthony S. Fauci; Stephen L. Hauser; Dan L. Longo; J. Larry Jameson; Joseph Loscalzo (2015). Harrison's principles of internal medicine. New York: McGraw-Hill Medical Publishing Division. صفحة 2289. .
- Longo, DL; Fauci, AS; Kasper, DL; Hauser, SL; Jameson, JL; Loscalzo, J (2011). "341: disorders of the thyroid gland". Harrison's principles of internal medicine (الطبعة 18th). New York: McGraw-Hill. .
- Khandelwal D, Tandon N; Tandon (January 2012). "Overt and subclinical hypothyroidism: who to treat and how". Drugs (Review). 72 (1): 17–33. doi:10.2165/11598070-000000000-00000. PMID 22191793.
- Dennis L. Kasper; Anthony S. Fauci; Stephen L. Hauser; Dan L. Longo; J. Larry Jameson; Joseph Loscalzo (2015). Harrison's principles of internal medicine. New York: McGraw-Hill Medical Publishing Division. صفحة 2290. .
- Thyroid week (2010-5-24). "الأسبوع العالمي للتوعية بالغدة الدرقية". مؤرشف من الأصل في 06 مايو 2011.
- Klubo-Gwiezdzinska, J; Wartofsky, L (March 2012). "Thyroid emergencies". Medical Clinics of North America. 96 (2): 385–403. doi:10.1016/j.mcna.2012.01.015. PMID 22443982.
- van den Boogaard, E; Vissenberg, R; Land, JA; et al. (2011). "Significance of (sub)clinical thyroid dysfunction and thyroid autoimmunity before conception and in early pregnancy: a systematic review". Human Reproduction Update (Review). 17 (5): 605–19. doi:10.1093/humupd/dmr024. PMID 21622978.
- Vissenberg, R; van den Boogaard, E; van Wely, M; et al. (July 2012). "Treatment of thyroid disorders before conception and in early pregnancy: a systematic review". Human Reproduction Update (Review). 18 (4): 360–73. doi:10.1093/humupd/dms007. PMID 22431565. مؤرشف من الأصل في 6 يناير 2016.
- Negro R, Stagnaro-Green A; Stagnaro-Green (October 2014). "Diagnosis and management of subclinical hypothyroidism in pregnancy". BMJ. 349 (10): g4929. doi:10.1136/bmj.g4929. PMID 25288580.
- Counts, D; Varma, SK (Jul 2009). "Hypothyroidism in children". Pediatrics in Review. 30 (7): 251–8. doi:10.1542/pir.30-7-251. PMID 19570923.
- Pearce, EN (Feb 2012). "Update in lipid alterations in subclinical hypothyroidism". The Journal of Clinical endocrinology and Metabolism. 97 (2): 326–33. doi:10.1210/jc.2011-2532. PMID 22205712. مؤرشف من الأصل في 17 ديسمبر 2019.
- Gaitonde, DY; Rowley, KD; Sweeney, LB (August 2012). "Hypothyroidism: an update". American Family Physician (Review). 86 (3): 244–51. PMID 22962987. مؤرشف من الأصل في 14 يونيو 2019.
- Persani, L (September 2012). "Clinical review: Central hypothyroidism: pathogenic, diagnostic, and therapeutic challenges". The Journal of Clinical endocrinology and Metabolism (Review). 97 (9): 3068–78. doi:10.1210/jc.2012-1616. PMID 22851492. مؤرشف من الأصل في 17 ديسمبر 2019.
- Stagnaro-Green, A (February 2012). "Approach to the patient with postpartum thyroiditis". The Journal of Clinical endocrinology and Metabolism (Review). 97 (2): 334–42. doi:10.1210/jc.2011-2576. PMID 22312089. مؤرشف من الأصل في 8 أبريل 2020.
- Jack DeRuiter (2002). Thyroid Pathology ( كتاب إلكتروني PDF ). صفحة 30. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 29 أغسطس 2017.
- Simon H (2006-04-19). "Hypothyroidism". University of Maryland Medical Center. مؤرشف من الأصل في 24 مايو 201328 فبراير 2008.
- Department of Pathology (13 يونيو, 2005). "Pituitary Gland -- Diseases/Syndromes". Virginia Commonwealth University (VCU). مؤرشف من الأصل في 02 فبراير 200928 فبراير 2008.
- American Thyroid Association (ATA) (2003). Hypothyroidism Booklet ( كتاب إلكتروني PDF ). صفحة 6. مؤرشف من "hypothyroidism" الأصل ( كتاب إلكتروني PDF ) في 20 مايو 2012.
- So, M; MacIsaac, RJ; Grossmann M (August 2012). "Hypothyroidism". Australian Family Physician. 41 (8): 556–62. PMID 23145394. مؤرشف من الأصل في 29 نوفمبر 2019.
- Brown, RS (2013). "Autoimmune thyroiditis in childhood". Journal of Clinical Research in Pediatric Endocrinology (Review). 5 Suppl 1 (4): 45–9. doi:10.4274/jcrpe.855. PMC . PMID 23154164.
- Charlton, K; Skeaff, S (November 2011). "Iodine fortification". Current Opinion in Clinical Nutrition and Metabolic Care. 14 (6): 618–624. doi:10.1097/MCO.0b013e32834b2b30. PMID 21892078.
- منظمة الصحة العالمية, يونيسف, ICCIDD (2008). Assessment of iodine deficiency disorders and monitoring their elimination ( كتاب إلكتروني PDF ) (الطبعة 3rd). Geneva: World Health Organization. . مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 12 يوليو 2015.
- e-Library of Evidence for Nutrition Actions (eLENA) (2014). "Iodine supplementation during pregnancy". World Health Organization. مؤرشف من الأصل في 23 يوليو 201805 مارس 2014.
- "Reaching Optimal Iodine Nutrition in Pregnant and Lactating Women and Young Children" ( كتاب إلكتروني PDF ). Joint Statement by the World Health Organization and United Nations Children's Fund. World Health Organization. 2007. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 04 مارس 201605 مارس 2014.
- Stagnaro-Green, A; Abalovich, M; Alexander, E; Azizi, F; Mestman, J; Negro, R; Nixon, A; Pearce, EN; Soldin, OP; Sullivan, S; Wiersinga, W; American Thyroid Association Taskforce on Thyroid Disease During Pregnancy and Postpartum (Oct 2011). "Guidelines of the American Thyroid Association for the diagnosis and management of thyroid disease during pregnancy and postpartum". Thyroid. 21 (10): 1081–125. doi:10.1089/thy.2011.0087. PMC . PMID 21787128. مؤرشف من الأصل في 22 مارس 2020.
- Public Health Committee of the American Thyroid Association; Becker, DV; Braverman, LE; Delange, F; Dunn, JT; Franklyn, JA; Hollowell, JG; Lamm, SH; Mitchell, ML; Pearce, E; Robbins, J; Rovet, JF (Oct 2006). "Iodine supplementation for pregnancy and lactation-United States and Canada: recommendations of the American Thyroid Association". Thyroid. 16 (10): 949–51. doi:10.1089/thy.2006.16.949. PMID 17042677.
- Cascorbi, I (August 2012). "Drug interactions--principles, examples and clinical consequences". Deutsches Ärzteblatt International (Review). 109 (33–34): 546–55. doi:10.3238/arztebl.2012.0546. PMC . PMID 23152742.
- Escobar-Morreale, HF; Botella-Carretero, JI; Escobar del Rey, F; Morreale de Escobar, G (August 2005). "Treatment of hypothyroidism with combinations of levothyroxine plus liothyronine". The Journal for Clinical Endocrinology and Metabolism (Review). 90 (8): 4946–54. doi:10.1210/jc.2005-0184. PMID 15928247. مؤرشف من الأصل في 13 فبراير 2013.
- British Thyroid Association Executive Committee (November 2007). "Armour Thyroid(USP) and combinedthyroxine/tri-iodothyronine as thyroid hormone replacement" ( كتاب إلكتروني PDF ). British Thyroid Association. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 23 نوفمبر 201525 ديسمبر 2013.
- Wiersinga, Wilmar M.; Duntas, Leonidas; Fadeyev, Valentin; Nygaard, Birte; Vanderpump, Mark P.J. (2012). "2012 ETA guidelines: the use of L-T4 + L-T3 in the treatment of hypothyroidism". European Thyroid Journal. 1 (2): 55–71. doi:10.1159/000339444. PMID 24782999. مؤرشف من الأصل في 19 سبتمبر 2018.
- Ebling PR (2011). Thyroid-Extract.pdf "ESA Position Statement on Desiccated Thyroid or Thyroid Extract" ( كتاب إلكتروني PDF ). Endocrine Society of Australia. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 20 مارس 201813 ديسمبر 2013.
- Ochs, N; Auer, R; Bauer, DC (June 2008). "Meta-analysis: subclinical thyroid dysfunction and the risk for coronary heart disease and mortality". Annals of Internal Medicine (Meta-analysis). 148 (11): 832–45. doi:10.7326/0003-4819-148-11-200806030-00225. PMID 18490668.
- Villar HC, Saconato H, Valente O, Atallah AN; Saconato; Valente; Atallah (2007). Villar, Heloisa Cerqueira Cesar Esteves (المحرر). "Thyroid hormone replacement for subclinical hypothyroidism". Cochrane Database of Systematic Reviews (Review, meta-analysis) (3): CD003419. doi:10.1002/14651858.CD003419.pub2. PMID 17636722.
- Blum, Manuel R.; Bauer, Douglas C.; Collet, Tinh-Hai; Fink, Howard A.; Cappola, Anne R.; da Costa, Bruno R.; Wirth, Christina D.; Peeters, Robin P.; Åsvold, Bjørn O.; den Elzen, Wendy P. J.; Luben, Robert N.; Imaizumi, Misa; Bremner, Alexandra P.; Gogakos, Apostolos; Eastell, Richard; Kearney, Patricia M.; Strotmeyer, Elsa S.; Wallace, Erin R.; Hoff, Mari; Ceresini, Graziano; Rivadeneira, Fernando; Uitterlinden, André G.; Stott, David J.; Westendorp, Rudi G. J.; Khaw, Kay-Tee; Langhammer, Arnuf; Ferrucci, Luigi; Gussekloo, Jacobijn; Williams, Graham R.; Walsh, John P.; Jüni, Peter; Aujesky, Drahomir; Rodondi, Nicolas (26 May 2015). "Subclinical Thyroid Dysfunction and Fracture Risk". JAMA. 313 (20): 2055. doi:10.1001/jama.2015.5161. PMID 26010634. مؤرشف من الأصل في 18 مايو 2016.
- Maia, AL; Goemann, IM; Meyer, EL; Wajner, SM (17 March 2011). "Type 1 iodothyronine deiodinase in human physiology and disease: Deiodinases: the balance of thyroid hormone". Journal of Endocrinology. 209 (3): 283–297. doi:10.1530/JOE-10-0481. PMID 21415143. مؤرشف من الأصل في 2 يونيو 2018.
- Cheng, SY; Leonard, JL; Davis, PJ (Apr 2010). "Molecular aspects of thyroid hormone actions". Endocrine Reviews. 31 (2): 139–70. doi:10.1210/er.2009-0007. PMC . PMID 20051527.
- Dons, Robert F.; Jr, Frank H. Wians (2009). Endocrine and metabolic disorders clinical lab testing manual (الطبعة 4th). Boca Raton: CRC Press. صفحة 10. . مؤرشف من الأصل في 17 فبراير 2020.
- Bona, G; Prodam, F; Monzani, A (2013). "Subclinical hypothyroidism in children: natural history and when to treat". Journal of Clinical Research in Pediatric Endocrinology (Review). 5 Suppl 1 (4): 23–8. doi:10.4274/jcrpe.851. PMC . PMID 23154159.
- Fatourechi, V. (2009). "Subclinical Hypothyroidism: An Update for Primary Care Physicians". Mayo Clinic Proceedings (Review). 84 (1): 65–71. doi:10.4065/84.1.65. PMC . PMID 19121255.
- Baumgartner C, Blum MR, Rodondi N (December 2014). "SSubclinical hypothyroidism: summary of evidence in 2014". Swiss medical weekly (Review). 144: w14058. doi:10.4414/smw.2014.14058. PMID 25536449. مؤرشف من الأصل في 8 سبتمبر 2016.
- The Practice Committee of the American Society for Reproductive Medicine (November 2012). "Evaluation and treatment of recurrent pregnancy loss: a committee opinion". Fertility and Sterility. 98 (5): 1103–1111. doi:10.1016/j.fertnstert.2012.06.048. PMID 22835448.
- Regan, L; Backos M; Rai, R (2011-05-19). "The investigation and treatment of couples with recurrent first-trimester and second-trimester miscarriage" ( كتاب إلكتروني PDF ). Green-top Guideline No. 17. London: Royal College of Obstetricians and Gynaecologists. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 05 يوليو 201326 ديسمبر 2013.
- American Academy of Pediatrics; Rose, SR; Section on Endocrinology and Committee on Genetics, American Thyroid Association; Brown, RS; Public Health Committee, Lawson Wilkins Pediatric Endocrine Society; Foley, T; Kaplowitz, PB; Kaye, CI; Sundararajan, S; Varma, SK (Jun 2006). "Update of newborn screening and therapy for congenital hypothyroidism". Pediatrics. 117 (6): 2290–303. doi:10.1542/peds.2006-0915. PMID 16740880. مؤرشف من الأصل في 29 يونيو 2019.
- Pollitt, RJ (Jun 2009). "Newborn blood spot screening: new opportunities, old problems". Journal of Inherited Metabolic Disease. 32 (3): 395–9. doi:10.1007/s10545-009-9962-0. PMID 19412659.
- LeFevre, ML (24 March 2015). "Screening for Thyroid Dysfunction: U.S. Preventive Services Task Force Recommendation Statement". Annals of internal medicine. doi:10.7326/M15-0483. PMID 25798805.
- Malt, EA; Dahl, RC; Haugsand, TM; (February 2013). "Health and disease in adults with Down syndrome". Tidsskrift for Den Norske Legeforening (Review). 133 (3): 290–4. doi:10.4045/tidsskr.12.0390. PMID 23381164. مؤرشف من الأصل في 12 مارس 2016.
- Cooper, DS; Braverman LE, المحرر (2012-07-12). Werner & Ingbar's the thyroid : a fundamental and clinical text (الطبعة 10th). Philadelphia: Wolters Kluwer/Lippincott Williams & Wilkins Health. صفحة 552. . مؤرشف من الأصل في 21 مارس 2020.
- Monzani, A; Prodam, F; Rapa, A; Moia, S; Agarla, V; Bellone, S; Bona, G (Jan 2013). "Endocrine disorders in childhood and adolescence. Natural history of subclinical hypothyroidism in children and adolescents and potential effects of replacement therapy: a review". European Journal of Endocrinology. 168 (1): R1–R11. doi:10.1530/EJE-12-0656. PMID 22989466. مؤرشف من الأصل في 9 يونيو 2019.
- Leung, AM; Braverman, LE; Pearce, EN (Nov 13, 2012). "History of U.S. iodine fortification and supplementation". Nutrients. 4 (11): 1740–6. doi:10.3390/nu4111740. PMC . PMID 23201844. مؤرشف من الأصل في 4 مارس 2016.
- Murray, GR (Oct 10, 1891). "Note on the Treatment of Myxoedema by Hypodermic Injections of an Extract of the Thyroid Gland of a Sheep". British Medical Journal. 2 (1606): 796–7. doi:10.1136/bmj.2.1606.796. PMC . PMID 20753415.
- Fox, EL (Oct 29, 1892). "A Case of Myxoedema Treated by Taking Extract of Thyroid by the Mouth". British Medical Journal. 2 (1661): 941. doi:10.1136/bmj.2.1661.941. PMC . PMID 20753901.
- "Hypothyroidism". Merck Veterinary Manual, 10th edition (online version). 2012. مؤرشف من الأصل في 24 مارس 201525 ديسمبر 2013.
- Mooney, CT (May 2011). "Canine hypothyroidism: A review of aetiology and diagnosis". New Zealand Veterinary Journal. 59 (3): 105–114. doi:10.1080/00480169.2011.563729. PMID 21541883.