| Aspartame | ||
| ||
 | ||
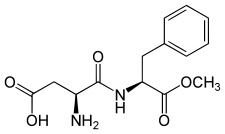
| Ester méthylique de l'aspartyl-phénylalanine. | ||
| Identification | ||
|---|---|---|
| Nom UICPA | (3S)-3-amino-4-[[(1S)-1-benzyl-2-(méthoxy-2-oxoéthyl]amino]-4-oxobutanoïque | |
| Synonymes |
|
|
| No CAS | ||
| No ECHA | 100.041.132 | |
| No CE | 245-261-3 | |
| DrugBank | DB00168 | |
| PubChem | ||
| No E | E951 | |
| SMILES | ||
| InChI | ||
| Apparence | Poudre cristalline blanche, légèrement hygroscopique[1] | |
| Propriétés chimiques | ||
| Formule | C14H18N2O5 [Isomères] |
|
| Masse molaire[2] | 294,303 1 ± 0,014 4 g/mol C 57,14 %, H 6,16 %, N 9,52 %, O 27,18 %, |
|
| pKa | 3,1 et 7,9 (25 °C)[3] | |
| Propriétés physiques | ||
| T° fusion | Décomposition avant fusion. Le produit de la décomposition fond à 246 °C[3] | |
| T° ébullition | >300 °C à 1 013,25 hPa[3] | |
| Solubilité | Peu soluble dans l'eau (10 g l−1 à 20 °C[3]) et l'éthanol[4]. | |
| Masse volumique | 150–600 kg m−3, solide[3] ; 1,347 g cm−3[5] |
|
| Cristallographie | ||
| Classe cristalline ou groupe d’espace | P41[6] | |
| Paramètres de maille | a = 17,685 Å b = 17,685 Å |
|
| Volume | 1 538,46 Å3[6] | |
| Propriétés optiques | ||
| Pouvoir rotatoire | = −2,3° dans HCl 1N[5] | |
| Précautions | ||
| NFPA 704 | ||
| Directive 67/548/EEC[7] | ||
| Classification du CIRC | ||
| Groupe 2B : Peut-être cancérogène pour l’homme[8] | ||
| Écotoxicologie | ||
| DL50 | >4 g kg−1 (rats, oral)[9] >10 g kg−1 (souris, oral)[9] |
|
| Composés apparentés | ||
| Isomère(s) | Musc cétone | |
| Autres composés |
Alitame, Néotame, Suosan |
|
| Unités du SI et CNTP, sauf indication contraire. | ||
L'aspartame est un édulcorant artificiel découvert en 1965. C'est un dipeptide composé de deux acides aminés naturels, l'acide L-aspartique et la L-phénylalanine, ce dernier sous forme d'ester méthylique. Sa consommation est donc déconseillée chez les personnes atteintes de phénylcétonurie.
L'aspartame a un pouvoir sucrant environ 200 fois supérieur à celui du saccharose et est utilisé pour édulcorer les boissons et aliments à faible apport calorique ainsi que les médicaments. Cet additif alimentaire est utilisé dans un grand nombre de produits et autorisé dans de nombreux pays, il est référencé dans l'Union européenne par le numéro E951.
Depuis sa première autorisation de mise sur le marché aux États-Unis par la Food and Drug Administration (FDA) en 1974, l'aspartame a fait l'objet de polémiques sur ses possibles effets nocifs sur la santé bien que des organismes de santé publique (notamment la FDA et l'Autorité européenne de sécurité des aliments — AESA) aient affirmé son innocuité dans les doses d'utilisation autorisées chez l'humain.
Des études sur le modèle animal remettraient en cause l'intérêt des édulcorants dans la lutte contre l'obésité et le diabète de type II. Chez les souris, la saccharine, le sucralose et dans une moindre mesure l'aspartame perturbent le métabolisme du sucre via une action encore mal décrite sur les bactéries intestinales[10]. Comme les aliments riches en sucres, ces produits provoquent une rapide montée de la glycémie qui génère à son tour l'acquisition d'une résistance à l'insuline, symptôme clef du syndrome métabolique. Ce phénomène n'est toutefois pas observé chez l'humain si la consommation d'aspartame a lieu dans le cadre d'exercices physiques intenses[11] ou chez des sujets non diabétiques/pré-diabétiques, qu'ils soient minces ou obèses[12].
Une méta-analyse de 2015 conclut que les édulcorants, bien que ne favorisant pas le diabète de type II, la surconsommation de sucre ou le cancer, ne semblent ni favoriser la perte de poids, ni faciliter la gestion de la glycémie chez les diabétiques et ni réduire le risque de diabète de type II[13].
Histoire
La première apparition de l'aspartame date de la publication de sa synthèse en 1966[14]. Mais il aurait été découvert en 1965 par James Schlatter, chimiste de la société G. D. Searle & Company, lors de la synthèse d'un tétrapeptide devant être testé comme médicament anti-ulcères[15],[16],[17].
Découverte accidentelle
L'aspartame était alors un intermédiaire de synthèse et Schlatter a goûté le produit par accident en humectant son doigt pour attraper une feuille de papier[18],[19],[20]. Le goût sucré fut une découverte inattendue, l'acide aspartique et la phénylalanine n'étant pas sucrés. Le dipeptide non méthylé se révéla avoir une saveur amère. Schlatter synthétisa des composés de structure voisine, mais le produit original fut conservé et commercialisé sous le nom d'aspartame.
Exploitation
Une première autorisation de mise sur le marché limitée aux aliments solides[21] est accordée à l'aspartame aux États-Unis par la Food and Drug Administration (FDA) en [22]. À la suite de l'enquête menée par la FDA et de doutes sur le sérieux des études présentées par le laboratoire Searle (notamment les tests sur les animaux), l'autorisation est suspendue par la FDA en [22].
Son usage sera rétabli aux États-Unis dans les aliments solides en puis dans les liquides en 1983.
Toujours en 1981, l'aspartame est autorisé par un comité commun d'experts de l'OMS et de l'Organisation pour l'agriculture et la nourriture[23]. La même année, le comité scientifique pour les aliments humains (CSAH / SCF en anglais) de la Commission européenne approuve l'aspartame.
L'aspartame est autorisé en France en 1988 et porte le numéro E951 dans la classification européenne des additifs alimentaires[24].
Le brevet de l'aspartame est tombé dans le domaine public en 1992.
En 1994, son emploi en tant qu'édulcorant est harmonisé par l'Union européenne (directive 94/35/CE[25]). L'aspartame est alors approuvé dans plus de 90 pays.
En 1995, l'Union européenne établit les critères de pureté pour l'aspartame (directive 95/31/CE[26]).
En 2002, le comité scientifique de la Commission européenne confirme son avis sur l'innocuité de l'aspartame. La même année, l'Agence française de sécurité sanitaire (AFSSA) conclut dans un rapport : « La consommation d'aspartame chez l'homme, même dans des populations particulièrement exposées comme les enfants diabétiques, ne dépasse pas la dose journalière admissible (DJA), notamment en France ».
En 2003, la directive 2003/115/CE autorise un nouvel édulcorant intense dérivé de l'aspartame : le sel d'aspartame-acésulfame dont l'innocuité a été établie par le comité scientifique de l'alimentation humaine dès [27] et les critères de pureté définis en 2001.
Synthèse
Il existe trois synthèses permettant d’obtenir l’aspartame.
La plus ancienne est la synthèse chimique. Elle utilise comme réactifs de départ l’acide aspartique et la phénylalanine. Cette voie de synthèse offre un rendement faible, de l’ordre de 50 %, et est à l’origine d’un isomère au goût amer (qui doit par la suite être extrait). C’est pourquoi elle fut vite remplacée par la synthèse enzymatique. Cette dernière met en jeu comme catalyseur une enzyme, la thermolysine, dans des conditions expérimentales précises à une température de 37 °C et un pH de 7,5, et offre un rendement de 95 %. Ce rendement est bien meilleur, mais toujours pas suffisant pour les industriels. Une autre voie de synthèse a alors été mise en place : la synthèse biotechnologique. C’est celle qui est utilisée aujourd’hui, elle offre un rendement supérieur à 99,99 %. Elle utilise toujours la thermolysine comme enzyme, mais réutilise un des produits[28].
Structure et propriétés
Structure
L'aspartame est un dipeptide, dérivant de deux acides aminés, l'acide L-aspartique et l'ester méthylique de la L-phénylalanine. Son nom chimique est donc * L-Aspartyl-L-phénylalanate de méthyle.
Propriétés chimiques
L'aspartame possède une base aminée et un groupe acide lui conférant deux constantes d'acidité : 3,1 et 7,9 à 25 °C[3].
Hydrolyse
Après ingestion, l'aspartame s'hydrolyse en acide aspartique, phénylalanine et méthanol. Une dégradation plus poussée produit du formaldéhyde[29], de l'acide formique et une dioxopipérazine.
Il peut également se décomposer pendant son stockage. À température ambiante, il est le plus stable à pH 4,3, avec une demi-vie de 300 jours. On constate une décomposition plus rapide aux pH s'éloignant de 4,3. À pH 7, par exemple, sa demi-vie n'est que de quelques jours.
L'instabilité de l'aspartame augmente avec la température : en phase solide, la recombinaison en dicétopipérazine peut avoir lieu à partir de 105 °C. C'est la raison pour laquelle il est déconseillé de cuire l'aspartame.
Par hydrolyse de l'ester, l'aspartame produit du méthanol (10 % en masse) et de l'aspartyl-phénylalanine. Ce dernier peut se recombiner en dicétopipérazine (acide 2-(5-benzyl-3,6-dioxopipérazin-2-yl)acétique) (à partir de 30 °C[1]) ou bien s'hydrolyser en ces deux acides aminés de base: l'acide aspartique (40 % en masse) et la phénylalanine (50 % en masse).
Réaction de Maillard
La fonction amine de l'aspartame peut participer aux réactions de Maillard avec les groupes aldéhyde.
Propriétés physiques
L'aspartame est un solide cristallin blanc, inodore et légèrement hygroscopique. Il est faiblement soluble dans l'eau (10 g/L à 20 °C[3]) et l'éthanol[4]. Il se dissout plus dans les solutions acides.
Biochimie
L'aspartame, contrairement au sucre, ne peut servir à la formation de graisses dans les tissus adipeux ni aux autres rôles métaboliques utiles de ce dernier[30].
Propriétés sucrantes
L'aspartame a un pouvoir sucrant environ 200 fois supérieur à celui du saccharose à masse égale[4].
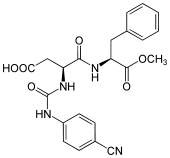
À la différence de la saccharine et de l'acésulfame-K, l'aspartame n'a pas de composante ou d'arrière-goût amer.
L'aspartame est souvent utilisé en mélange avec d'autres édulcorants intenses (acésulfame-K) pour pallier la diminution de la saveur sucrée. La diminution est due à sa décomposition en milieu aqueux ou à sa disparition lors des réactions de Maillard entre celui-ci et les arômes possédant une fonction aldéhyde.
Un dérivé de l'aspartame, le superaspartame, a un pouvoir sucrant de 8 000[31] à 14 000[32] fois supérieur à celui du saccharose.
Utilisation
L'aspartame est l'édulcorant intense le plus fréquemment employé au monde[33], il est utilisé dans près de 5 000 produits (chewing-gum sans sucre, boissons ou gâteaux allégés) et de plus de 600 spécialités pharmaceutiques, dont plus de 2 000 vendues en Europe. Sa consommation est surtout motivée par le fait qu'il n'apporte que très peu d'énergie. L'aspartame a l'avantage, en plus d'être bon marché, de ne pas avoir de pouvoir cariogène.
L'aspartame est utilisé sous forme de sucrettes ou de poudre blanche (en sachet ou boîte) pouvant se substituer au sucre, dans le café ou le thé, les pâtisseries ou autres. Ces produits contiennent, en moyenne 3 % d’aspartame, les autres ingrédients étant de la maltodextrine et de l'acésulfame K.
Réglementation
Le codex Alimentarius reconnaît l'utilisation de l'aspartame comme édulcorant et exhausteur de goût dans une large gamme de produits alimentaires, à des concentrations maximales variant de 0,6 à 3 g suivant l'application[34].
En Europe, l'aspartame est autorisé dans[25] :
- les boissons non alcoolisées (0,6 g/L) ;
- les desserts et produits similaires (0,6 à 1 g/kg) ;
- les confiseries (0,5 à 1 g/kg) ;
- les boissons alcoolisées (bières) (0,6 g/l) ;
- les compléments alimentaires et autres.
La DJA est de 40 mg/kg de masse corporelle par jour. Pour atteindre cette DJA, une personne de 60 kg devrait consommer 280 sucrettes ou vingt canettes de boissons « light » par jour[35]. La quantité réelle d'aspartame n'est pas toujours précisée sur les produits.
Santé
L'aspartame fait partie des additifs alimentaires les plus étudiés[36],[37], il est considéré comme sûr pour la consommation humaine dans plus de 90 pays[38], notamment par les agences de sécurité sanitaire comme l'Autorité européenne de sécurité des aliments[39], le JECFA de l'OMS/FAO et la Food and Drug Administration.
Le 14 juillet 2023, l'aspartame est classé « cancérogène possible » par le Centre international de la recherche sur le cancer, qui dépend de l'Organisation mondiale de la Santé[40],[41],[42].
Obésité
Alors que certaines études suggèrent que la prise d'aliments contenant de l'aspartame a un effet orexigène et favorise l'obésité[43], d'autres suggèrent qu'il n'y a aucune preuve épidémiologique de ces effets[44], et des revues de la littérature suggèrent que l'aspartame a un effet bénéfique[45],[46].
Une étude sur les souris a montré qu'une alimentation riche en aspartame, combinée avec une nourriture riche en graisses, conduisait à une prise de masse importante par rapport aux souris n'ayant pas d'apports en aspartame dans leur nourriture. Il a été montré aussi que la concentration sanguine de glucose entre les repas chez les souris prenant de l'aspartame était plus important. La prise d'aspartame favoriserait par conséquent le diabète. Des études sur l'humain sont toutefois nécessaires[47].
Effets
On a formulé l'hypothèse que la saveur sucrée puisse provoquer une sécrétion d'insuline commandée par le cerveau (cephalic-phase insulin release, ou CPIR). Selon cette hypothèse, cette sécrétion d'insuline sans apport de glucose pourrait provoquer une chute de la glycémie ce qui provoquerait une sensation de faim. Les édulcorants utilisés par les personnes obèses pour perdre du poids auraient alors un effet inverse à celui recherché. Néanmoins, aucune étude n'a mis en évidence ce phénomène[48],[49].
En 2000, une étude financée par le fabricant de l'aspartame, G.D. Searle, de la modification éventuelle de la thermogenèse apportée par une alimentation édulcorée à l'aspartame en comparaison avec une alimentation sucrée au saccharose n'a mis en évidence aucune différence significative[50].
Pour le ministère de la Santé du Canada, l'utilisation de l'aspartame est sans danger pour les diabétiques[38].
Une étude israélienne publiée en dans la revue Nature montre des effets diabétogènes des édulcorants[51]. Cette étude montre l’interaction entre certaines bactéries intestinales et les composés chimiques des édulcorants, non absorbés par l’intestin, qui crée une réaction inflammatoire induisant des troubles métaboliques comme l’intolérance au glucose et le diabète.
Métabolisme
Lors de la digestion, l'aspartame perd son groupe hydroxyméthyle (méthanol), puis se décompose en ses deux acides aminés de base, l'acide aspartique et la phénylalanine. Sous l'effet de la chaleur, il peut aussi se recombiner pour former de la dicétopipérazine. En comparaison avec les aliments courants, l'aspartame est une source mineure de phénylalanine, d'acide aspartique et de méthanol.
Phénylalanine
La phénylalanine est un des huit acides aminés essentiels, elle est notamment naturellement présente dans le lait des mammifères. Seules les personnes souffrant de phénylcétonurie (PKU), une maladie génétique (1/16 000 naissances), doivent contrôler de façon très stricte l'apport en phénylalanine, c'est pourquoi les produits contenant de l'aspartame doivent indiquer qu’ils contiennent une source de phénylalanine[52].
Méthanol
Le méthanol est un alcool toxique, naturellement présent en très faible quantité dans des aliments courants : fruits mûrs, jus de fruits et aliments fermentés (vin, bière, etc.). Des allégations parues sur internet et dans certains médias affirment que le méthanol contenu dans l'aspartame serait toxique. Ces allégations sont sans fondement selon le ministère de la Santé du Canada[38] : « Le méthanol alimentaire, qu'il provienne de l'aspartame ou d'aliments courants, est présent à des concentrations trop faibles pour causer des problèmes de santé. Il ne s'accumule pas dans le corps, mais il est plutôt métabolisé, par les voies du métabolisme normal, en formaldéhyde d'abord, ensuite en acide formique et finalement en eau et en gaz carbonique. »
Acide aspartique
L'acide aspartique est un acide aminé, non toxique pour l'organisme qui ne pose pas de problème lors de la métabolisation de l’aspartame. C'est un constituant courant des protéines de l’organisme.
Dicétopipérazine
La dicétopipérazine n’est pas considérée comme génotoxique (provoquant l'apparition de lésions dans l'ADN, qui peuvent éventuellement conduire à des mutations) ni cancérogène chez le rat et la souris. La dose journalière acceptable de la dicétopipérazine pour l'humain a été fixée à 7,5 mg/kg.
Controverse
Depuis son autorisation, l'innocuité de l'aspartame est controversée.
En 1977, la Food and Drug Administration qui réglemente aux États-Unis le marché des aliments et des médicaments, refuse de délivrer au groupe industriel Searle l'agrément nécessaire à la poursuite de la commercialisation de l'aspartame.
La FDA lance même une procédure pénale contre le groupe, après avoir découvert de nombreuses erreurs dans les essais de toxicité présentés par Searle.
Après la nomination de Donald Rumsfeld à la présidence du groupe Searle en juin 1977, la situation se retourne en faveur de l'entreprise. Ronald Reagan nomme à la tête de la FDA Arthur Hull Hayes (en) (ancien chercheur du Pentagone) qui, en , autorise finalement la mise sur le marché de l'aspartame, contre l'avis du comité scientifique de l'EPA[53]. Notamment, le psychiatre Ralph Walton, appelé en tant qu'expert au cours de l'audition, fait état d'une revue scientifique montrant que les études financées par les industriels producteurs d'aspartame établissaient systématiquement à l'absence d'effets de cette substance alors que des études menées par des laboratoires indépendants concluaient à des doutes sur son innocuité[53].
La commercialisation de l'aspartame sous le nom de marque « NutraSweet » permit à la société Searle d'engranger, sous la direction de D. Rumsfeld, de considérables bénéfices. La vente de Searle à la compagnie Monsanto (en 1985) aurait rapporté à celui-ci la somme de douze millions de dollars[54].
En 1996, Olney et al. publient une étude dont le sous-titre est Augmentation des tumeurs cérébrales, y a-t-il un lien avec l'aspartame ?[55].
En , des chercheurs de la Fondation européenne Ramazzini, à Bologne (Italie), présentent à la presse une nouvelle étude menée sur des rats de laboratoire, semblant montrer un effet cancérogène sur le cerveau[56]. Cette étude est critiquée par deux agences de sécurité sanitaire, notamment pour sa méthodologie insuffisante. L'Autorité européenne de sécurité des aliments (EFSA), après analyse de la méthodologie de l'étude, conclut qu'il n'y a aucune raison de changer les conditions d'utilisation de l'aspartame en Europe[57]. La France a aussi émis des réserves sur la méthode de cette étude et des doutes quant à la validité des résultats[58].
En 2006, une étude[59],[60] avait déjà suggéré que de faibles doses délivrées dans la nourriture de rates Sprague-Dawley à partir de l'âge de huit semaines et durant leur durée de vie augmentait le risque de cancer chez ces rats[61]. Une seconde étude est réalisée par la même équipe[62], mais cette fois avec exposition à des doses de 2 000, 400 ou 0 ppm commençant au stade de l'embryon (à partir du 12e jour de vie), chez des rats mâles et femelles (également Sprague-Dawley). L'étude conclut à un risque dose-dépendant de tumeur maligne (cancers de type lymphomes et leucémies) chez les rats mâles ainsi que chez les femelles, avec aussi des cancers mammaires chez les rates. Les auteurs estiment que ces résultats confirment et renforcent la première démonstration expérimentale de la cancérogénicité multipotentielle à une dose proche de la dose journalière admissible pour l'homme, cette étude démontrant en outre un risque renforcé en cas d'exposition durant la vie fœtale.
Fin 2010, la polémique est relancée par deux autres études.
- La première a porté sur près de 60 000 femmes enceintes. Elle étudie la corrélation entre les cas de naissances avant terme et la consommation de boissons gazeuses aux édulcorants[63]. Pour l’EFSA, « aucune preuve disponible dans l’étude ne permet d’affirmer qu’il existe un lien entre la consommation de boissons non alcoolisées contenant des édulcorants artificiels et l’accouchement prématuré »[64].
- La seconde a été menée sur des souris, par l’Institut Ramazzini (centre privé de recherche en cancérologie environnementale). Elle a conclu que l’exposition à de hautes doses d'aspartame induisait des cancers du foie (carcinomes hépatocellulaires) et du poumon (dans les alvéoles et bronchioles), mais chez les souris mâles uniquement, les femelles étant totalement épargnées par ce phénomène[65] (ce qui suggère un « cancer hormonal »).
Le Pr Narbonne, toxicologue français, incite les Français à la prudence[66], pourtant l’EFSA, en collaboration avec l’ANSES, après avoir examiné les deux études affirme ne pas y trouver d'éléments probants de nature à modifier le profil de sécurité de l’aspartame[67]. Ont notamment été mises en cause par les deux agences : les souris utilisées, connues pour spontanément présenter des tumeurs fréquentes au foie et au poumon et, pour la première étude, le fait que les mises-bas prématurées n'aient pas été spontanées mais déclenchées, sans précisions sur les raisons de ce choix médical. En réponse, l'Institut Ramazzini souligne que le groupe test et le groupe de référence ont été affectés des mêmes déficiences respiratoires à un stade avancé de leur vie, ce qui est plutôt normal quand un sujet devient vieux .
Mi-2011, la polémique est ravivée à la suite de la réponse de Hugues Kenigswald, à la tête de l'unité Additifs alimentaires de l'EFSA, au réseau Environnement santé qui lui demandait de prouver le caractère scientifique des études initiales ayant autorisé la mise sur le marché de l'aspartame : « L'EFSA ne dispose pas du dossier de demande d'autorisation de l'aspartame qui devait contenir ces études. Par ailleurs, les contacts que nous avons eus avec nos collègues de la Commission européenne semblent indiquer que la Commission ne dispose plus de ce dossier »[68]. Ainsi, la question de l'existence des dossiers scientifiques ayant autorisé l'aspartame est désormais posée, de même que celle de l'indépendance des experts[69]. En 2011, en France, des élus et ONG demandent à l'Europe d'invalider la dose journalière pour ce produit[70]. L'EFSA rend ses conclusions à la fin de 2013, qui maintiennent les avis précédents, considérant la dose journalière admissible comme une protection adéquate et l'aspartame sûr pour la population générale[71].
En 2013, Françoise Clavel-Chapelon, directrice de recherche Inserm-université Paris-Sud 11, à l’Institut Gustave-Roussy, et Guy Fagherazzi ont comparé la consommation de boissons sucrées et boissons sucrées « light » au regard du risque de diabète de type 2 [72]:
« L’analyse, menée auprès de 66 188 femmes de la cohorte E3N, confirme une relation entre boissons sucrées et diabète de type 2 et révèle pour la première fois en France, que contrairement aux idées reçues, le risque de diabète est plus élevé lorsqu’il s’agit de boissons light que de boissons sucrées « normales ». »
Un article dans la revue Nature confirme, en , ce constat, ajoutant que les édulcorants altèrent le microbiote intestinal[73].
Notes et références
- 1 2 Aspartam, 01/2005:0973, Pharmacopée européenne 5.5, EDQM, 16 décembre 2005, https://www.edqm.eu
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- 1 2 3 4 5 6 7 (en) « IUCLID Chemical Data Sheet »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?) [PDF] (consulté le ).
- 1 2 3 Parlement européen et Conseil de l'Europe, « Directive 2008/60/CE établissant des critères de pureté spécifiques pour les édulcorants pouvant être utilisés dans les denrées alimentaires », Journal officiel de l’Union européenne, no L 158, , p. 17-40 (résumé, lire en ligne).
- 1 2 (en) Raymond C. Rowe, Paul J. Sheskey et Marian E. Quinn, Handbook of Pharmaceutical Excipients, Londres, Pharmaceutical Press and American Pharmacists Association, , 6e éd., 888 p. (ISBN 978-0-85369-792-3, BNF 42148066), p. 49.
- 1 2 3 « Aspartame », sur reciprocalnet.org (consulté le ).
- ↑ SIGMA-ALDRICH
- ↑ « Publication des résultats de l’évaluation des dangers et des risques liés à l’aspartame », sur who.int, (consulté le )
- 1 2 (en) ChemIDplus, « Aspartame - RN: 3734-33-6 », sur chem.sis.nlm.nih.gov, U.S. National Library of Medicine (consulté le ).
- ↑ Artificial sweeteners induce glucose intolerance by altering the gut microbiota, Nature, 9/10/2014, lire en ligne.
- ↑ Jason Siegler, Keith Howell, Rebecca Vince et James Bray, « Aspartame in conjunction with carbohydrate reduces insulin levels during endurance exercise », Journal of the International Society of Sports Nutrition, vol. 9, , p. 36 (ISSN 1550-2783, PMID 22853297, PMCID 3441850, DOI 10.1186/1550-2783-9-36, lire en ligne, consulté le )
- ↑ Stephen D. Anton, Corby K. Martin, Hongmei Han et Sandra Coulon, « Effects of stevia, aspartame, and sucrose on food intake, satiety, and postprandial glucose and insulin levels », Appetite, vol. 55, , p. 37–43 (ISSN 0195-6663, PMID 20303371, PMCID 2900484, DOI 10.1016/j.appet.2010.03.009, lire en ligne, consulté le ).
- ↑ Bruyère Olivier, Ahmed H. Serge, Atlan Catherine et Belegaud Jacques, « Review of the nutritional benefits and risks related to intense sweeteners », Archives of Public Health : Archives belges de Santé Publique, vol. 73, , p. 41 (ISSN 0778-7367, PMID 26430511, PMCID 4590273, DOI 10.1186/s13690-015-0092-x, lire en ligne, consulté le ).
- ↑ (en) J.M. Davey, A.H. Laird et J.S. Morley, « Polypeptides. Part III. The synthesis of the C-terminal tetrapeptide sequence of gastrin, its optical isomers, and acylated derivatives », Journal of the Chemical Society C: Organic, , p. 555-566 (DOI 10.1039/J39660000555, résumé).
- ↑ (en) M. Goodman et Y.S. Oh, « United States Patent 5298272 - Bridged carboxylic ortho ester sweetener », sur freepatentsonline.com, (consulté le ).
- ↑ JM Schlatter (Searle) Brevet ZA 67 02190, 1968.
- ↑ (en) J.M. Schlatter (Searle), « United States Patent 3492131 - Peptide sweetening agents », sur freepatentsonline.com, (consulté le ).
- ↑ Bernard Fontaine, « Sérendipité : découvrir par hasard - Du faux sucre sur les mains », sur CNRS, (consulté le )
- ↑ « Rapport de l’Agence Française de Sécurité Sanitaire des Aliments », sur le site du ministère des Affaires sociales et de la Santé, (consulté le ).
- ↑ (en) Mazur, R.H. (1984), Discovery of aspartame, dans Aspartame: Physiology and Biochemistry (L. D. Stegink et L. J. Filer Jr., Éds.), Marcel Dekker, New York, p. 3–9.
- ↑ (en) The History of Aspartame, LEDA at Harvard Law School.
- 1 2 (en) History of aspartame, sur wnho.net.
- ↑ (en) « Aspartame (WHO Food Additives Series 15) », International Programme on Chemical Safety (consulté le ).
- ↑ Parlement européen et Conseil de l'Europe, « Directive 89/107/CEE du 21 décembre 1988 relative au rapprochement des législations des États membres concernant les additifs pouvant être employés dans les denrées destinées à l’alimentation humaine », Journal officiel de l’Union européenne, no L 040, , p. 27-33 (résumé, lire en ligne [PDF]).
- 1 2 Parlement européen et Conseil de l'Europe, « La directive 94/35/CE concernant les édulcorants modifiée par la Directive 96/83/CE », Journal officiel de l'Union européenne, no L 237, (résumé, lire en ligne [PDF]).
- ↑ Parlement européen et Conseil de l'Europe, « Directive 95/31/CE établissant des critères de pureté spécifiques pour les édulcorants pouvant être utilisés dans les denrées alimentaires modifiées par les directives 98/66/CE et 2000/51/CE », Journal officiel de l'Union européenne, (résumé, lire en ligne).
- ↑ Parlement européen et Conseil de l'Europe, « Directive 2003/115/CE modifiant la directive 94/35/CE concernant les édulcorants destinés à être employés dans les denrées alimentaires », Journal officiel de l’Union européenne, no L 24, , p. 65-71 (résumé, lire en ligne).
- ↑ « L'aspartame, un édulcorant controversé », sur culturesciences.chimie.ens.fr (consulté le ).
- ↑ (en) C. Trocho, R. Pardo, I. Rafecas, J. Virgili, X. Remesar, J. A. Fernandez-Lopez et M. Alemany, « Formaldehyde derived from dietary aspartame binds to tissue components in vivo », Life Sciences, vol. 63, no 5, , p. 337–349 (DOI 10.1016/S0024-3205(98)00282-3)
- ↑ (en) C. Malo et J.X. Wilson, « Glucose Modulates Vitamin C Transport in Adult Human Small Intestinal Brush Border Membrane Vesicles », J. Nutr., no 130, , p. 63-69 (résumé).
- ↑ (en) Robert Shallenberger, Taste Chemistry, Londres, Springer, , 1re éd., 613 pages (ISBN 978-0-7514-0150-9, LCCN 92011271, lire en ligne), « Chapter 7: Amino acids, peptides and proteins », p. 243
- ↑ (en) A.D. Kinghorn et C.M. Compadre, Alernative Sweeteners : Third Edition, Revised and Expanded, New York, Marcel Dekker, , 572 p. (ISBN 978-0-8247-0437-7, présentation en ligne), « Less common high-potency sweeteners », p. 208-234.
- ↑ « L'aspartame dédouané par l'EFSA », sur Le Monde,
- ↑ (en) Codex Alimentarius Commission, « Updated up to the 31st Session of the Codex Alimentarius Commission for Aspartame (951) », GSFA Online, sur codexalimentarius.net, codex Alimentarius, (consulté le ).
- ↑ (en) « Low Calorie Sweeteners: Role and Benefits »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?) (consulté le ), p. 13.
- ↑ « Aspartame »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?) (consulté le ), Food Standards Australia New Zealand
- ↑ Falsifications and Facts about Aspartame, Food Safety and Technology
- 1 2 3 Aspartame, ministère de la Santé du Canada.
- ↑ Aspartame, Autorité européenne de sécurité des aliments
- ↑ « L’aspartame classé cancérogène possible par le Centre international de recherche sur le cancer », Le Monde.fr, (lire en ligne, consulté le )
- ↑ « L'aspartame est un "cancérogène possible" selon l'Organisation Mondiale de la Santé », sur ici, par France Bleu et France 3, (consulté le )
- ↑ Par Nicolas Berrod et avec Elsa Mari Le 14 juillet 2023 à 00h30, « L’aspartame classé « possiblement cancérogène » : quatre questions sur une décision choc », sur leparisien.fr, (consulté le )
- ↑ (en) B. A. Magnuson et coll, « Aspartame : A Safety Evaluation Based on Current Use Levels, Regulations, and Toxicological and Epidemiological Studies », Critical Reviews in Toxicology, vol. 37, no 8, , p. 629-727 (DOI 10.1080/10408440701516184)
- ↑ (en) EFSA, « Report of the meeting on Aspartame with National Experts », .
- ↑ (en) A. de la Hunty, S. Gibson et M. Ashwell, « A review of the effectiveness of aspartame in helping with weight control », Nutrition Bulletin, vol. 31, no 2, , p. 115–128 (ISSN 1471-9827 et 1467-3010, DOI 10.1111/j.1467-3010.2006.00564.x, lire en ligne, consulté le )
- ↑ A. Pan et F. B. Hu, « Effets satiétogènes des sucres : différences entre boissons et aliments solides », Obésité, vol. 6, no 4, , p. 206–211 (ISSN 1951-6002, DOI 10.1007/s11690-012-0302-4, lire en ligne, consulté le )
- ↑ (en-US) Andy Coghlan, « Why diet drinks with aspartame may actually help make you fatter », New Scientist, (lire en ligne, consulté le ).
- ↑ Am. J. Clin. Nutr., mars 1997, 6 (3): 737-43.
- ↑ (en) K.L. Teff, J. Devine et K. Engelman, « Sweet taste: effect on cephalic phase insulin release in men », Physiol. Behav., vol. 57, no 6, , p. 1089-1095 (DOI 10.1016/0031-9384(94)00373-D, résumé).
- ↑ (en) L. Prat-Larquemin, J.M. Oppert, F. Bellisle et B. Guy-Grand, « Sweet taste of aspartame and sucrose: effects on diet-induced thermogenesis », Appetite, vol. 34, no 3, , p. 245-251 (DOI 10.1006/appe.1999.0310, résumé).
- ↑ (en) Eran Elinav, « Artificial sweeteners induce glucose intolerance by altering the gut microbiota », Nature, Nature Publishing Group, vol. 514, no 7521, , p. 181–186 (ISSN 1476-4687, DOI 10.1038/nature13793, lire en ligne, consulté le ).
- ↑ Julien Tap et Gaetane Collard, les dangers de l'aspartame : rumeurs ou réalité ? [PDF], Rapport bibliographique, IUP SIAL sécurité des aliments, université de Paris XII, Val de Marne, février 2004.
- 1 2 Marie-Monique Robin, « Notre poison quotidien », Arte TV, (résumé).
- ↑ « Winter comes for a Beltway lion ; Rumsfeld rose and fell with his conviction intact », Chicago Tribune, 12-11-2006, p. 17.
- ↑ (en) John Olney et al., « Increasing brain tumor rates: is there a link to aspartame? », Journal Neuropathology and Experimental Neurology, vol. 55, , p. 1115-1123.
- ↑ (en) M. Soffritti, F. Belpoggi, D. Degli Esposti et L. Lambertini, « Aspartame induces lymphomas and leukaemias in rats », Eur. J. Oncol., vol. 10, no 2, , p. 107-116 (résumé, lire en ligne [PDF]).
- ↑ (en) EFSA, « Opinion of the Scientific Panel on food additives, flavourings, processing aids and materials in contact with food (AFC) related to a new long-term carcinogenicity study on aspartame : EFSA-Q-2005-122 », The EFSA Journal, no 356, , p. 1-44 (résumé, lire en ligne [PDF]).
- ↑ V. Gazin, « Veille toxicologique - l'aspartame », Bulletin Vigilances, no 29, , p. 4 (ISSN 1629-3533, lire en ligne [PDF]).
- ↑ Étude conduite par le Cesare Maltoni Cancer Research Center of the European Ramazzini Foundation (CMCRC/ERF) ; Soffritti M., Belpoggi F., Degli Esposti D., Lambertini L., Tibaldi E. et Rigano A., First experimental demonstration of the multipotential carcinogenic effects of aspartame administered in the feed to Sprague-Dawley rats, Environ. Health Perspect., mars 2006, 114(3):379-85.
- ↑ Belpoggi F., Soffritti M., Padovani M., Degli Esposti D., Lauriola M. et Minardi F., Results of long-term carcinogenicity bioassay on Sprague-Dawley rats exposed to aspartame administered in feed, Ann. N. Y. Acad. Sci., septembre 2006, 1076:559-77 (résumé).
- ↑ Soffritti M., Belpoggi F., Tibaldi E., Esposti D.D. et Lauriola M., Life-span exposure to low doses of aspartame beginning during prenatal life increases cancer effects in rats ; Environ. Health Perspect., septembre 2007, 115(9):1293-7 ([résumé]).
- ↑ Soffritti M., Belpoggi F., Tibaldi E., Esposti D.D. et Lauriola M., Life-span exposure to low doses of aspartame beginning during prenatal life increases cancer effects in rats, Environ. Health Perspect., septembre 2007, 115(9):1293-7 (résumé).
- ↑ (en) Halldorsson, Thorhallur I., Strøm, Marin et Petersen, Sesilje B., « Intake of artificially sweetened soft drinks and risk of preterm delivery: a prospective cohort study in 59,334 Danish pregnant women », sur ajcn.org, (consulté le ).
- ↑ « Aspartame - Sucrette story », sur Afis Science - Association française pour l’information scientifique (consulté le ).
- ↑ Soffritti M., Belpoggi F., Manservigi M., Tibaldi E., Lauriola M., Falcioni L. et Bua L. (2010), Aspartame administered in feed, beginning prenatally through life span, induces cancers of the liver and lung in male Swiss mice, Am. J. Ind. Med., décembre 2010, 53(12):1197-206. (résumé.
- ↑ Lire en ligne.
- ↑ EFSA, L’EFSA examine deux publications relatives à la sécurité des édulcorants artificiels, Nouvelle, 28 février 2011.
- ↑ « Rue 89 », sur Rue89 (consulté le ).
- ↑ NOVETHIC Aspartame: l'indépendance des experts remise en question 30/06/11
- ↑ RELAXNEWS, Aspartame : plusieurs associations et parlementaires réclament l'invalidation de la dose journalière, 29 juin 2011.
- ↑ « Une agence européenne blanchit l'aspartame », sur lemonde.fr, (consulté le ).
- ↑ « Les boissons « light » associées à une augmentation du risque de diabète de type 2 », Inserm, 07/02/2013.
- ↑ Lire en ligne.
Bibliographie
![]() : document utilisé comme source pour la rédaction de cet article.
: document utilisé comme source pour la rédaction de cet article.
- (en) De Lewis D. Stegink et Lloyd J. Filer, Aspartame: Physiology and Biochemistry, CRC Press, 1984 (ISBN 9780824772062), 670 p.
- Marie-Monique Robin, Notre poison quotidien, Arte Éditions, Éditions la découverte, 2011, 2013.
Voir aussi
Articles connexes
- Pouvoir sucrant
- Édulcorant
- Liste alphabétique d'édulcorants
Liens externes
- (en) Safety data sheet - Aspartame sur la base de données de la Direction européenne de la Qualité du Médicament et Soins de Santé DEQM
- (en) Summary of Evaluations Performed by the Joint FAO/WHO Expert Committee on Food Additives (résumé des évaluations faites par le comité d'experts communs sur les additifs alimentaires de l'OMS et de la FAO).

