| Nitrate d'ammonium | |
| |
| Identification | |
|---|---|
| Nom UICPA | Nitrate d'ammonium |
| No CAS | |
| No ECHA | 100.026.680 |
| No CE | 229-347-8 |
| No RTECS | BR9050000 |
| PubChem | 22985 |
| ChEBI | 63038 |
| SMILES | |
| InChI | |
| Apparence | solide de formes variables, poudre hygroscopique incolore à blanche[1], en pratique légèrement colorée |
| Propriétés chimiques | |
| Formule | NH4NO3 |
| Masse molaire[2] | 80,043 4 ± 0,001 6 g/mol H 5,04 %, N 35 %, O 59,97 %, |
| Propriétés physiques | |
| T° fusion | 170 °C[1] |
| T° ébullition | Se décompose au-dessous du point d'ébullition à environ 210 °C[1] |
| Solubilité | 1 180 g L−1 (0 °C, eau) 1 920 g L−1 (20 °C) |
| pH | 5,43 (sol. aq. 0,1 M)[4] |
| Masse volumique | 1,7 g cm−3[1] |
| Vitesse de détonation | ~1 500 m s−1 (nitrate d'ammonium industriel)[5] |
| Pression de vapeur saturante | 1,5 kPa (sol. aq. sat.)[4] |
| Thermochimie | |
| ΔfH0solide | −365 kJ/mol |
| ΔfusH° | 5,86 kJ/mol à 169,7 °C[4] |
| Cp | 139,3 J mol−1 °C−1 à 25 °C[4] |
| Cristallographie | |
| Système cristallin | orthorhombique |
| Précautions | |
| SGH[4] | |
  |
|
| SIMDUT[6] | |
 C, |
|
| NFPA 704[7] | |
| Transport | |
| Unités du SI et CNTP, sauf indication contraire. | |
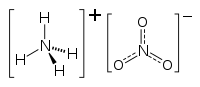
Le nitrate d'ammonium est un composé ionique du cation ammonium et de l'anion nitrate, de formule NH4NO3. Il correspond au corps minéral anhydre naturel, de maille orthorhombique, nommé par les minéralogistes « nitrammite »[8].
Il s'agit aussi de l'ancien nitrate d'ammoniaque, obtenu industriellement depuis le XXe siècle par un mélange d'ammoniaque et d'acide nitrique, deux dérivés potentiels de la chimie de synthèse du gaz ammoniac. Il se présente sous la forme d'une poudre très soluble dans l'eau.
Il est surtout utilisé comme ingrédient d'engrais azotés simples (principalement les « ammonitrates ») ou composés (connus sous la dénomination d'engrais NP, NK ou NPK). C'est aussi un agent explosif puissant.
Propriétés physico-chimiques

C'est une substance cristalline, assez hygroscopique et inodore qui tend à s'agglomérer en grumeaux. Il peut être vendu en solution à 50 % et 95 % en masse.
Sa dissolution dans l'eau, dont la solubilité augmente avec la température, est un processus endothermique :
- NH4NO3 (s) → NH4+ (aq) + NO3− (aq).
Comme la chaleur de dissolution avoisine 6,2 kcal/mol (26 kJ/mol), il est communément utilisé dans les mélanges réfrigérants permettant au dispositif frigorifiant une température de fonctionnement basse de −17 °C.
Cinq formes allotropiques ont été observées[9] :
- une forme orthorhombique à huit motifs par maille existe en dessous de −18 °C à pression atmosphérique ;
- la forme α, de système cristallin tétragonal ou orthorhombique à quatre motifs, de densité 1,61 (déterminée à 25 °C) est attestée entre −18 °C et 32,1 °C. Pour 100 g d'eau pure, sa solubilité est mesurée à 118,3 g à 0 °C, environ 180 g à 18 °C et à 241,8 g à 30 °C. La transition structurale à 32,1 °C est corrélée à une variation de volume faible d'environ 3 %, mais dont l'effet est de déstructurer l'ancien maillage cristallin : la réorganisation, même si elle privilégie la formation de multiples macles, ne peut que fragmenter les grains fragiles, d'où la formation de poussières qui favorisent encore le transport naturel du minéral par voie aérienne ou fluviale. La maille orthorhombique à plusieurs motifs, attestée dans le corps naturel qu'est la mascagnite, paraît ainsi la plus stable ;
- la morphologie cristalline β est attestée entre 32,1 °C et 84,2 °C. La maille est monoclinique ou orthorhombique à quatre motifs. Le corps est plus dense, la masse volumique est 1,725 g/cm3. Pour 100 g d'eau pure, sa solubilité plus élevée est mesurée à 365,8 g à 35 °C, à 580 g à 35 °C, à 871 g à 100 °C ;
- une morphologie quadratique à deux motifs par maille est observée entre 84,2 °C et 125,2 °C ;
- une forme cubique est observée à partir de 125,2 °C et reste stable jusqu'à la fusion du réseau cristallin qui s'opère à 169,6 °C. Le corps chimique correspondant se décompose à partir de 210 °C, température considérée comme sa température d'ébullition.
Cette poudre solide compacte et relativement instable se décompose à haute température en libérant de la chaleur et en formant des produits gazeux, d'où le caractère explosif de cette décomposition. En dessous de 300 °C, la décomposition produit principalement de l'oxyde nitreux et de l'eau :
- NH4NO3 → N2O + 2H2O.
À plus haute température, la réaction ci-dessous prédomine[10] :
- NH4NO3 → N2 + 1⁄2O2 + 2H2O.
Dans certaines conditions, le fait que les deux réactions sont exothermiques et ont des produits gazeux conduit à un emballement de la réaction et le processus de décomposition devient explosif. Cela a entraîné dans le passé de nombreuses catastrophes (voir l'article Liste d'explosions accidentelles impliquant du nitrate d'ammonium pour plus de détails). Pour éviter l'explosion, le nitrate d'ammonium industriel est stocké sous la forme d'un mélange avec des charges inertes, comme la craie ou calcite pulvérisée, parfois de la dolomie, des argiles, des marnes dans le cas des engrais.
Le nitrate d'ammonium est un oxydant puissant, il oxyde facilement des métaux comme le plomb et le zinc. La réaction avec le cuivre peut s'écrire :
- NH4NO3aqueux + Cumétal → Cu(NO3)2aqueux + 2NH3aqueux + N2gaz dégagé ou dissous dans l'eau du milieu + 3H2O.
Il peut réagir à chaud avec le formol en donnant du nitrate de méthylammonium (en) explosif, selon un mécanisme radicalaire :
- NH4NO3 + CH2O → CH3NH3+NO3− + O2.
En réalité, le formol est diversement oxydé.
Il peut réagir également à chaud avec la cellulose ou l'amidon.
C'est pourquoi des impuretés métalliques comme le cuivre, le chlorure d'ammonium ou salmiac, des dérivés chlorés ou certains autres corps chimiques réducteurs ou potentiellement réducteurs comme les hydrocarbures ou les mercaptans qui peuvent le souiller, voire le mazout ou les simples emballages de bois et de papier pour éviter sa prise en motte du fait de son caractère hygroscopique, accélèrent sa décomposition déjà possible dès 185 °C. Par exemple, suivant la dégradation vaporisante :
- NH4NO3solide → N2Ogaz + 2H2Ovapeur d'eau.
Il est très soluble dans l'ammoniaque, soluble dans l'acétone. Il l'est moins dans les alcools. Par exemple, il ne s'en dissout à 20 °C que 17,1 g dans 100 g de méthanol pur et 3,8 g dans un mélange eau/éthanol à 95 % en volume.
Fabrication
On le fabrique par barbotage du gaz ammoniac (le produit de réduction du diazote par le procédé Haber-Bosch[11]) dans l'acide nitrique. Il existe différents procédés tels que Fauser, Krupp Uhde, UCB, Stamicarbon, Norsk hydro, Stengel, AZF Atofina selon diverses modalités dont l'obtention de la neutralisation des solutions, ensuite concentrées pour favoriser la précipitation du sel composé, le séchage et la granulation finale.
Applications
- Le nitrate d'ammonium sert surtout à la fabrication d'engrais chimiques dans l'agriculture conventionnelle, principalement les ammonitrates et les engrais NP, NK ou NPK. Il n'est pas autorisé dans l'agriculture biologique en Suisse[12] ou en Europe[13].
- En tant qu'oxydant, il est utilisé en chimie, par exemple pour oxyder des matériaux avant de les dissoudre dans un verre (technique de la perle fondue en spectrométrie de fluorescence des rayons X).
- Il peut être utilisé dans la fabrication d'engins explosifs, fournissant alors un explosif brisant peu stable. Dans cette dernière utilisation, il est souvent mélangé avec des hydrocarbures comme le gazole et amorcé à l'aide d'un autre explosif comme le TNT ; un mélange de ce type, utilisé dans l'exploitation minière, est nommé la donarite. À cause de sa grande disponibilité, le mélange a été utilisé pour la fabrication de bombes artisanales dans certaines attaques terroristes comme l'attentat d'Oklahoma City, celui de Bali ou encore l'attentat de Marrakech en avril 2011.
- Au contact de l'eau, il se produit une très forte réaction endothermique. Il est ainsi utilisé dans les poches de froid instantané.
- Sous le nom de « propergol », il est utilisé dans l'industrie civile et militaire, en particulier dans l'industrie pétrolière pour la stimulation de puits[14].
- Il est également utilisé en adjonction à faible dose dans le combustible de l'enfumoir des apiculteurs pour endormir les abeilles dans certains cas de déplacement de la reine ou de la colonie car s'il est chauffé, il produit du protoxyde d'azote qui est un gaz anesthésiant. Ainsi, les abeilles perdent tout sens de l'orientation et ne reviendront pas à leur précédent emplacement. Cela n'est que temporaire puisqu'elles vont refaire leur vol d'orientation, ce qui leur permettra de « redéfinir » leur domicile.
Il doit être stocké et manipulé avec les précautions de rigueur[15].
Sécurité, manipulation et stockage
Le Bureau réglementation et sécurité au travail du ministère de l'Agriculture et de la Pêche et l'Union des industries pour la fertilisation (UNIFA) ont élaboré une fiche technique intitulée « La prévention des risques professionnels dans le stockage et l'emploi des engrais solides à base de nitrate d'ammonium »[16].
Le nitrate d'ammonium pur ne brûle pas, mais en tant qu'oxydant puissant, il favorise et accélère la combustion des matières organiques (et de certaines matières inorganiques). Il ne doit pas être stocké à proximité de substances combustibles[17].
Bien que le nitrate d'ammonium soit stable à température et pression ambiantes dans de nombreuses conditions, il peut détoner à partir d'une forte charge d'amorçage. Il ne doit pas être stocké à proximité d'explosifs puissants.
Le nitrate d'ammonium fondu est très sensible au choc et à la détonation, en particulier s'il est contaminé par des matières incompatibles telles que des combustibles, des liquides inflammables, des acides, des chlorates, des chlorures, du soufre, des métaux, du charbon et de la sciure.
Le contact avec certaines substances telles que les chlorates, les acides minéraux et les sulfures métalliques, peut entraîner une décomposition rapide, voire violente, capable d'enflammer les matériaux combustibles voisins ou de les faire exploser.
Le nitrate d'ammonium commence à se décomposer après avoir fondu, libérant ainsi du NOx, HNO3, NH3 et H2O. Il ne doit pas être chauffé dans un espace confiné. La chaleur et la pression résultant de la décomposition augmentent la sensibilité à la détonation et accélèrent la décomposition. La détonation peut se produire à 80 atm. La contamination peut réduire cette valeur à 20 atm.
Le nitrate d'ammonium a une humidité relative critique de 59,4 %, au-delà de laquelle il absorbe l'humidité de l'atmosphère. Il est donc important de stocker le nitrate d'ammonium dans un récipient hermétiquement fermé. Sinon, il risque de s'agglomérer en une grande masse solide. Le nitrate d'ammonium peut absorber suffisamment d'humidité pour se liquéfier. Le mélange du nitrate d'ammonium avec certains autres engrais peut abaisser l'humidité relative critique[18].
Conditions de stockage et enjeux de sécurité en France
Selon une enquête menée par Le Canard enchaîné en août 2020, le ministère de la Transition écologique estime qu'un accident similaire à celui qui s'est produit à Beyrouth début est très peu probable en France car la France a adopté une réglementation parmi les plus strictes d'Europe[19].
Cent-huit sites classés Seveso sont répertoriés, dont 16 avec plus de 2 500 t.
Cependant toujours selon Le Canard, le site georisques.gouv.fr[20] indique par ailleurs qu'il y a 225 sites contenant plus de 550 t de nitrate d'ammonium, dont 180 sites détenant plus de 1 250 t, donc soumis à autorisation.
Par ailleurs de très nombreux sites assurent le stockage de quantités inférieures, sans obligation de déclaration. Il s'agit en particulier de coopératives agricoles[21].
Le média en ligne Reporterre avait enquêté en 2018 sur la coopérative d'Ottmarsheim qui avait été signalée par un lanceur d'alerte. Ce dernier avait signalé les problèmes de stockage sur le site, par ailleurs à proximité immédiate du canal du Rhin[22].
En septembre 2020, une élue de l'opposition municipale de Melun appelle à la mobilisation des habitants pour demander plus d'informations sur les engrais stockés par la coopérative agricole Valfrance à Vaux-le-Pénil, qui stocke plus de quatre mille tonnes d'engrais azotés[23]. Par ailleurs la députée Mathilde Panot demande au nom de son groupe politique, une commission d'enquête parlementaire sur le stockage de nitrate d'ammonium[24].
Explosions accidentelles et pollution de l'air
Le nitrate d'ammonium est notamment directement impliqué dans les explosions :
- de l'usine BASF d'Oppau (Allemagne) le ;
- de l'usine PCT à Tessenderlo (Belgique) en 1942[25] ;
- du cargo français Grandcamp transportant 2 300 tonnes de nitrate d'ammonium à Texas City en ;
- du cargo norvégien Ocean Liberty dans le port de Brest en ;
- de deux remorques routières chargées chacune de 23 tonnes sur un chantier de Kansas City, en ;
- de l'usine de fabrication Terra Industries à Port Neal au sud de Sioux City dans l'Iowa en ;
- de l'usine AZF à Toulouse, le ;
- de l'usine d'ammoniac West Fertilizer près de Waco (Texas), en ;
- d'un entrepôt dans le port de Tianjin (Chine) en 2015 ;
- d'un hangar au port de Beyrouth (Liban) le .
Les engrais azotés sont de puissantes sources de dissémination de molécules azotées qui, souvent alliées aux pollutions primaires des combustions de l'industrie ou du trafic routier, reforment via l'étape gazeuse des particules secondaires polluantes correspondant aux principaux engrais, sulfate d'ammonium et nitrate d'ammonium. Ces dernières particules secondaires sont majoritaires lors des pics de pollution printaniers, d'autant plus importants en période sèche[26].
Toxicologie et écotoxicologie
La toxicité de l'ammonitrate est encore mal comprise. Elle pourrait être tantôt atténuée, tantôt renforcée par le fait que, comme la plupart des sels de nitrate (de potassium, de sodium), l'ammonitrate est fortement soluble dans l'eau (ce qui permet une dilution rapide, mais aussi une contamination rapide des organismes aquatiques ou de l'eau).
Dans certaines conditions (en milieu acide et donc dans l'estomac ou dans certaines zones humides naturellement acides), des nitrites (NO2−) se forment à partir des nitrates.
Toxicité
Le nitrate d'ammonium est irritant et toxique pour l'être humain, la toxicité est jugée faible d'une manière aiguë selon les modèles en vigueur, mais elle reste bien plus efficace de manière chronique et ciblée. L'inhalation de ses poussières cause une irritation vive des voies respiratoires ; le contact avec la peau et les muqueuses peut entraîner des irritations sévères. Par exposition chronique et prolongée, il provoque faiblesses, fatigues et céphalées fréquentes.
Il n'est pas évident que l'être humain ait toujours absorbé une quantité non négligeable de nitrates, via certains légumes ou salades gorgés d'engrais nitratés notamment. Il en consomme aujourd'hui environ 50 à 100 mg (de 200 à 400 mg pour les végétariens) via les légumes, l'eau (ou d'autres boissons en contenant) et enfin via les viandes et les poissons[27].
Selon les bilans biochimique et hématologique faits chez des employés d'usines ou de complexes de stockage de nitrates, chez l'adulte en bonne santé, la toxicité des faibles doses semble faible, même en cas d'expositions répétées ou longues, hormis l'apparition fréquente (ex. : 50 % de 45 employés suivis) d'une inflammation urinaire[27]. Néanmoins, chez ces employés, une exposition permanente (via inhalation de dérivés nitratés) conduit à long terme à une toxicité rénale, avec apparition de leucocytes et de sang dans l'urine, problème non détectable par les analyses de sang qui ne montrent pas d'anomalie des paramètres biochimiques sériques[27].
Le rat de laboratoire exposé (par ingestion) durant trois semaines à des doses plus importantes de nitrate d'ammonium (200, 400 et 600 mg/kg de poids corporel) présentent cependant une réponse biochimique et hématologique rapide avec :
- augmentation du rapport hépato-corporel (phénomène dose-dépendant)[27] ;
- modification sanguine avec croissance du taux de glucose, de cholestérol, de créatinine, de lactate déshydrogénase et transaminase (TGO, TGP)[27] ;
Une détoxification existe, dont un indice est la diminution du taux de glutathion dans les organes de détoxification que sont le foie, les reins, la rate, les intestins (phénomène également constaté dans les testicules de rats mâles de laboratoire exposés)[27].
Les marqueurs indirects d'une intoxication pourraient être le glutathion sérique et la méthémoglobine.
En soi, la toxicité aiguë de l'ion nitrate est considérée comme faible, mais le nitrite qu'il forme dans l'organisme est toxique (transformant l'hémoglobine en méthémoglobine qui empêche la fonction de transport de l'oxygène par le sang[28],[29].
Écotoxicité
Pour les végétaux
Au-delà d'une certaine dose, l'ammonitrate est toxique pour les plantes dites « supérieures »[30] et la toxicité a été étudiée chez d'autres organismes modèles ou bioindicateurs potentiels (paramécies, mousses, lichens)[31] ; cette toxicité se traduit chez la plupart des espèces par une réduction de la croissance, des feuilles plus petites et un retard de développement du système racinaire. À dose plus importante, les symptômes d'une chlorose apparaissent et peuvent conduire à la mort de la plante[30].
La toxicité de l'ion ammonium pour les plantes est encore imparfaitement connue ; elle est généralement attribuée à un effet synergique associant :
- une carence nutritive induite par l'excès d'ammonium (qui altère l'absorption des ions métalliques)[30] ;
- une acidification du milieu d'enracinement (qui inhibe la croissance racinaire secondaire)[30] ;
- une perturbation de l'équilibre osmotique de la plante (par modifications du pH intracellulaire)[30] ;
- un désaccouplement du phénomène de photophosphorylation liée au transport d'électrons, à la suite de l'accumulation d'ions ammonium dans les feuilles[30] ;
- l'altération du métabolisme des phytohormones et de la polyamine[30].
Une bonne mycorhization semble améliorer la régulation de l'absorption des différentes formes de l'azote par les arbres, et donc diminuer leur stress en condition de pollution azotée ou de stress par excès d'ions ammonium[32].
Dans le milieu aquatique
Quand un cours d'eau traverse un bassin agricole ou y naît, il peut se charger en nitrates (dès la source parfois) et s'eutrophiser. Peut-être aussi en raison des pesticides souvent associés aux nitrates, ceci conduit souvent à un colmatage du substrat de sable ou de gravier qui est recherché par certains poissons pour y pondre[33]. Ces conditions biogéochimiques sont propices à l'anoxie du substrat, et à une nouvelle production de nitrites et d'ammonium dans le substrat même[33]. Selon les concentrations souvent trouvées en France (15 à 60 mg/L), un phénomène en chaîne pourrait se créer et s'autoalimenter dans un tel substrat après la ponte des salmonidés : les œufs (nombreux à mourir) puis les larves qui meurent, font augmenter le taux de nitrate dans le substrat qui à son tour aggrave le taux de mortalité des embryons de salmonidés enfouis sous les graviers[33]. Même si dans la nature les saumons adultes mouraient souvent par millions chaque année après la ponte, leurs corps étaient en partie rapidement consommés par des animaux piscivores ou nécrophages, ou ils étaient baignés par une eau non chargée en nitrates, en polluant peut-être moins le substrat que ne le font les larves mortes qui s'y décomposent. « Les teneurs en nitrite expliquent une partie des mortalités, notamment lorsque la concentration en oxygène est faible, ce qui est constaté sur schiste[33]. Les teneurs en ammoniaque sont en revanche trop faibles pour influencer la survie ». Les taux de nitrite et d'ammonium diffèrent selon les compartiments interstitiels et varient beaucoup selon la nature du sédiment (« granulométrie et teneur en matière organique »)[33].
Pour les animaux
Certaines espèces y semblent plus vulnérables, en particulier pour des espèces dont le stade larvaire est aquatique tels que les amphibiens qui se montrent également vulnérables à de faibles doses de chlorure d'ammonium, de sulfate d'ammonium et de nitrate de sodium (avec des variations de sensibilité selon l'espèce considérée)[34]. La dose mortelle pour les stades les plus sensibles (œuf, têtard) peut être atteinte dans de l'eau ayant ruisselé (ou circulé dans des drains agricoles) « suffisamment » longtemps dans un bassin agricole moyen[34].
Cycle de l'azote et climat
Le nitrate d'ammonium n'étant pas complètement absorbé par les plantes mais soluble dans l'eau, il ruisselle, ce qui cause l'eutrophisation de milieux naturels sensibles. L'apparente facilité et l'avantage économique de l'apport massif d'engrais chimique contribuent à négliger la fertilisation organique (fumier, lisier, compost, résidus de récolte), ce qui entraîne un déficit de la vie du sol et une diminution de l'humus. L'azote contenu dans les fourrages importés ne retourne pas sur les territoires où ils ont été produits. Le cycle de l'azote est perturbé au niveau mondial. La fonction d'absorption des gaz à effet de serre par le sol est compromise[35],[36].
Le nitrate d'ammonium est fortement émetteur de gaz à effet de serre (GES), principalement de protoxyde d'azote N2O qui a un pouvoir réchauffant 298 fois supérieur au dioxyde de carbone, mais également de CO2 de manière indirecte par la minéralisation du sol. Sur une exploitation agricole céréalière moyenne, la part des émissions de GES, directes et indirectes, dues aux engrais azotés, est de 55 %[37].
Équilibre thermodynamique
À des températures inférieures à 170 °C, les particules atmosphériques de nitrate d'ammonium existent en équilibre avec l'ammoniac et l'acide nitrique gazeux. Le processus est décrit par la réaction réversible suivante[38] :
- NH3(g) + HNO3(g) ↔ NH4NO3(s, aq)
Le sens de la réaction et l'état de nitrate d'ammonium dépendent de la température et de l'humidité relative (humidité de déliquescence en fonction de la température)[39]. La constante de dissociation (Kp) du nitrate d'ammonium est égale au produit des pressions partielles des gaz ammoniac et acide nitrique à l'équilibre[40]. La constante de dissociation (Kp) du nitrate d'ammonium est exprimée en ppb2, elle dépend seulement de la température.
Il existe plusieurs expressions de la constante de dissociation du nitrate d'ammonium pur, notamment :
avec T : température en kelvins (K).
Notes et références
- 1 2 3 4 NITRATE D'AMMONIUM, Fiches internationales de sécurité chimique .
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ Liste de solubilités et de pKs de sels dans l'eau.
- 1 2 3 4 5 PubChem 22985.
- ↑ (en) Henri-Noël Presles, Pierre Vidal et Boris Khasainov, « Experimental study of the detonation of technical grade ammonium nitrate », Comptes Rendus Mécanique, vol. 337, nos 11-12, , p. 755–760 (DOI 10.1016/j.crme.2009.10.007, lire en ligne, consulté le ).
- ↑ « Nitrate d'ammonium » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 24 avril 2009.
- ↑ (en) « Ammonium nitrate – Hazardous Substance Fact Sheet » [PDF], sur nj.gov/health, février 2016.
- ↑ Le chimiste Hans Rudolf Glauber le catalogue en 1659 comme un « nitrum flammans », c'est-à-dire un nitre inflammable.
- ↑ ENSIACET 2002, p. 3-6.
- ↑ (en) Norman N. Greenwood et Alan Earnshaw, Chemistry of the Elements, Butterworth-Heinemann (en), , 2e éd. (ISBN 0080379419), p. 469.
- ↑ Barbara Demeneix, « Nitrate d’ammonium, iode : retour sur l’histoire explosive de deux substances essentielles », sur The Conversation, (consulté le ).
- ↑ « Liste des intrants 2023 », sur shop.fibl.org (consulté le ).
- ↑ « Agriculture biologique », sur INAO (consulté le ).
- ↑ (en) John E. Schatz, « Improved modeling of the dynamic fracturing of rock with propellants », sur OnePetro (consulté le ).
- ↑ Alfred Mathis, Le stockage des produits chimiques, vol. 92, lycée Jean-Rostand, Strasbourg, Parlons sécurité, (lire en ligne [PDF]), p. 943–956.
- ↑ Bureau réglementation et sécurité au travail du ministère de l'Agriculture et de la Pêche, Union des industries pour la fertilisation (UNIFA) et INERIS (relecture), « Fiche technique : La prévention des risques professionnels dans le stockage et l'emploi des engrais solides à base de nitrate d'ammonium » [PDF], sur agriculture.gouv.fr, (consulté le ), 8 p.
- ↑ (en) « Chemical Advisory - Solid Ammonium Nitrate (AN) Storage, Handling and Management », sur US EPA, (consulté le ).
- ↑ (en) « Guidance for the Compatibility of Fertilizer Blending Materials (2006) », sur Fertilizers Europe (consulté le ).
- ↑ Christophe Labbé, « La France assise sur 2 millions de tonnes d'ammonitrate », Le Canard enchaîné, , p. 3.
- ↑ georisques.gouv.fr.
- ↑ « Enquête France 3. Le délicat stockage, en France, du nitrate d'ammonium, cette substance responsable des explosions de Beyrouth », sur Franceinfo, (consulté le ).
- ↑ « Stockage dangereux d’ammonitrate : la centrale de Fessenheim exposée à un risque majeur ? », sur Reporterre (consulté le ).
- ↑ Sophie Bordier, « Seine-et-Marne : faut-il s’inquiéter du nitrate d’ammonium des engrais stockés chez Valfrance ? », sur leparisien.fr, (consulté le ).
- ↑ « Suites d'AZF : LFI demande une commission d'enquête parlementaire sur les sites de stockage de nitrate d'ammonium », sur France 3 Occitanie (consulté le ).
- ↑ Olivier Perrin, « Avant le drame de Beyrouth, du nitrate d’ammonium avait déjà fait des ravages en 1942 », Le Temps, (lire en ligne, consulté le ).
- ↑ Journées du 17 mars 2015 en mesure de qualité de l'air, sur airparif.asso.fr.
- 1 2 3 4 5 6 Boukerche S, Aouacheri W et Saka S (2007), Les effets toxiques des nitrates : étude biologique chez l'homme et chez l'animal. Dans Annales de Biologie Clinique, vol. 65, , no 4, p. 385-391.
- ↑ Savino F, Maccario S, Guidi C et al. (2006), Methemoglobinemia caused by the ingestion of courgette soup given in order to resolve constipation in two formula-fed infants, Ann. Nutr. Metab., 50, 368-71.
- ↑ Jaffé ER (1981), Methemoglobinemia, Clin. Haematol., 10, 99-122.
- 1 2 3 4 5 6 7 Gerendás, J., Zhu, Z., Bendixen, R., Ratcliffe, R. G. et Sattelmacher, B. (1997), Physiological and biochemical processes related to ammonium toxicity in higher plants, Zeitschrift für Pflanzenernährung und Bodenkunde, 160(2), 239-251.
- ↑ Khaldi F (2003), Toxicité du nitrate d’ammonium NH4NO3 sur trois modèles biologiques : les paramécies, les mousses et les lichens. Effet sur leur métabolisme respiratoire, mémoire de magister en biochimie appliquée, université Badji Mokhtar, Annaba, 86 p.
- ↑ Boxman, A. W. et Roelofs, J. G. (1988), Some effects of nitrate versus ammonium nutrition on the nutrient fluxes in Pinus sylvestris seedlings. Effects of mycorrhizal infection, Canadian Journal of Botany, 66(6), 1091-1097 (résumé).
- 1 2 3 4 5 Massa, F. (2000), Sédiments, physico-chimie du compartiment interstitiel et développement embryo-larvaire de la truite commune (Salmo trutta) : Étude en milieu naturel anthropisé et en conditions contrôlées (thèse de doctorat) (résumé).
- 1 2 Schuytema G S et Nebeker AV (1999), Comparative toxicity of ammonium and nitrate compounds to Pacific treefrog and African clawed frog tadpoles, Environmental Toxicology and Chemistry, 18(10), 2251-2257 (résumé).
- ↑ Frédéric Deshusses, « Dans le labyrinthe de l’azote », sur lecourrier.ch, (consulté le ).
- ↑ (en) « European Nitrogen Assessment - Technical Summary », EU Science Hub, Cambridge University Press, (ISBN 9781107006126, lire en ligne, consulté le ).
- ↑ https://grandest.chambre-agriculture.fr/fileadmin/user_upload/National/FAL_commun/publications/Grand-Est/44_livret_levier_energie_ACSE_2020_01.pdf
- 1 2 (en) A. W. Stelson, « A note on the equilibrium relationship between ammonia and nitric acid and particulate ammonium nitrate », Atmospheric Environment (1967), vol. 13, no 3, , p. 369-371.
- ↑ (en) K. G. Dassios, « The mass accommodation coefficient of ammonium nitrate aerosol », Atmospheric Environment, vol. 33, no 18, , p. 2993-3003.
- 1 2 (en) A. W. Stelson, « Relative humidity and temperature dependence of the ammonium nitrate dissociation constant », Atmospheric Environment (1967), vol. 16, no 5, , p. 983-992.
- ↑ (en) M. Mozurkewich, « The dissociation constant of ammonium nitrate and its dependence on temperature, relative humidity and particle size », Atmospheric Environment. Part A. General Topics, vol. 27, no 2, , p. 261-270.
Bibliographie
- Boukerche S, Aouacheri W et Saka S (2007), Les effets toxiques des nitrates : étude biologique chez l'homme et chez l'animal. Dans Annales de Biologie Clinique, vol. 65, , no 4, p. 385-391.
- Bates SS, Worms J et Smith JC (1993), Effects of ammonium and nitrate on growth and domoic acid production by Nitzschia pungens in batch culture, Canadian Journal of Fisheries and Aquatic Sciences, 50 (6), 1248-1254.
- Morlaix, M et Lassus P (1992), Influence de l'azote et du phosphore sur la croissance et la toxicité de Prorocentrum lima (Ehrenberg) Dodge, Cryptogamie Algologie, 13 (3), 187-195.
- Codomier L, Segot M, Combaut G et Teste J (1981), Sur le développement d’Asparagopsis armata (Rhodophycée, Bonnemaisoniale) en culture. Effets de certaines substances azotées ou phosphorées inorganiques ou organiques, Botanica marina, 24 (1), 43-50.
- Chakroun A, Jemmali A, Hamed KB, Abdelli C et Druart P (2007), Effet du nitrate d’ammonium sur le développement et l’activité des enzymes anti-oxydantes du fraisier (Fragaria x ananassa L.) micropropagé, Revue de Biotechnologie, Agronomie, Société et Environnement, 11 (2).
- Paul Pascal, Nouveau Traité de Chimie Minérale, 1956, t. X azote-phosphore, édition Masson, 1956, 963 p.
Voir aussi
Articles connexes
- Engrais
- Nitrate
- Ammonitrate
- ANFO
- Eutrophisation
- Dystrophisation
Liens externes
- Vidéo expliquant quelques propriétés du nitrate d'ammonium, Canal-U
- « Le nitrate d'ammonium – Description, production, utilisations et précautions d'usage » [PDF], dossier collectif d'ingénieurs en chimie des procédés, ENSIACET, , Toulouse
- « Nitrate d'ammonium », Société chimique de France