| Valine | |
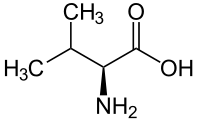 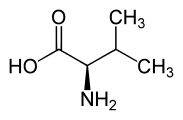 L ou S(+)-valine et D ouR(–)-valine |
|
| Identification | |
|---|---|
| Nom UICPA | acide 2-amino-3-méthylbutanoïque |
| Synonymes |
V, Val |
| No CAS | (racémique) (L) ou S(+) (D) ou R(–) |
| No ECHA | 100.000.703 |
| No CE | 200-773-6 (L) 211-368-9 (D) |
| FEMA | 3444 |
| Propriétés chimiques | |
| Formule | C5H11NO2 [Isomères] |
| Masse molaire[1] | 117,146 3 ± 0,005 6 g/mol C 51,26 %, H 9,46 %, N 11,96 %, O 27,32 %, |
| pKa | 2,3 (COOH) et 9,6 (NH2) |
| Propriétés biochimiques | |
| Codons | GUU, GUC, GUA, GUG |
| pH isoélectrique | 5,96[2] |
| Acide aminé essentiel | oui |
| Occurrence chez les vertébrés | 6,8 %[3] |
| Précautions | |
| SIMDUT[4] | |
Produit non contrôlé |
|
| Unités du SI et CNTP, sauf indication contraire. | |
La valine (abréviations IUPAC-IUBMB : Val et V) est un acide α-aminé dont l'énantiomère L est l'un des 22 acides aminés protéinogènes, et l'un des 9 acides aminés essentiels pour l'homme. Elle est caractérisée par un groupe apolaire isopropyle. Son nom provient de la valériane[5]. Elle est encodée sur les ARN messagers par les codons GUU, GUC, GUA et GUG.
Sa chaîne latérale est de nature aliphatique ramifiée et symétrique.
Biosynthèse
La valine est biosynthétisée dans les plantes en plusieurs étapes à partir de l'acide pyruvique. Est ensuite formé un intermédiaire, l'α-cétoisovalérate qui subit une amination réductive avec le glutamate.Cette biosynthèse implique les enzymes[6] :
- Acétolactate synthase ;
- Acide acétohydroxy isoméroreductase ;
- Dihydroxyacide déshydratase ;
- Valine aminotransférase.
La première partie de cette voie métabolique permet d'obtenir aussi la leucine.
Maladies du métabolisme
La dégradation de la valine est perturbée dans les maladies métaboliques suivantes
- Acidémie méthylmalonique
- Acidémie propionique
- Acidurie combinée malonique et méthylmalonique (CMAMMA)
- Maladie du sirop d'érable
Production
La société Metabolic Explorer a annoncé avoir développé un procédé de production de la L-valine par voie fermentaire en décembre 2021[7].
Notes et références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ (en) Francis A. Carey, « Table of pKa and pI values », sur Département de chimie de l'université de Calgary, (consulté le )
- ↑ (en) M. Beals, L. Gross, S. Harrell, « Amino Acid Frequency », sur The Institute for Environmental Modeling (TIEM) à l'université du Tennessee (consulté le )
- ↑ « Valine (l-) » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ « Valine - Nutrition-expertise.fr », sur nutrition-expertise.fr via Wikiwix (consulté le ).
- ↑ Lehninger, Albert L.; Nelson, David L.; Cox, Michael M. (2000), Principles of Biochemistry (3rd ed.), New York: W. H. Freeman, (ISBN 1-57259-153-6) .
- ↑ Françoise de Vaugelas, « Metex met au point un second procédé de fermentation »
 , sur Formule Verte, (consulté le )
, sur Formule Verte, (consulté le )