الأنفلونزا، والمعروفة باسم "النزلة الوافدة" أو الخُنان، هو مرض معد تسببه فيروسات مخاطية قويمة.[2] أعراض الأنفلونزا يمكن أن تكون خفيفة أو قوية جدا.[3] تشمل الأعراض : حمى، ثر أنفي، التهاب الحلق، ألم عضلي، صداع، سعال و إعياء. تبدأ هذه الأعراض عادة بعد يومين من التعرض للفيروس، وتستمر لمدة أقل من أسبوع. ولكن السعال قد يستمر لأكثر من أسبوعين.[2] في الأطفال، قد يكون هناك غثيان و تقيؤ، ولكن هذه الأعراض ليست شائعة لدى البالغين. يحدث الغثيان والقيء أكثر شيوعا نتيجة التهاب المعدة والأمعاء بسبب العدوى، والتي يشار إليها أحيانا باسم "انفلونزا المعدة" أو "انفلونزا على مدار 24 ساعة".[4] تشمل مضاعفات الأنفلونزا ما يلي : الالتهاب الرئوي الفيروسي والالتهاب الرئوي الجرثومي الثانوي، والتهابات الجيوب الأنفية، وتفاقم المشاكل الصحية السابقة مثل الربو أو قصور القلب.[3][5]
| إنفلونزا | |
|---|---|
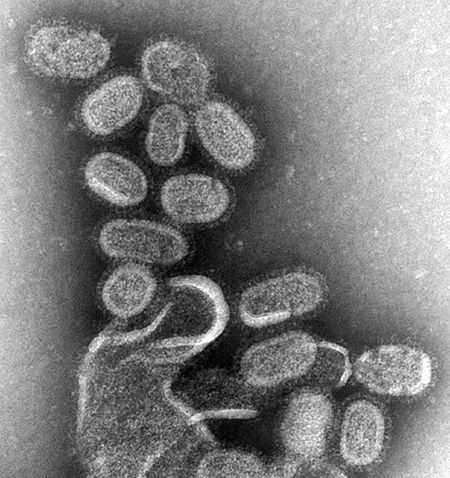
صورة بواسطة مجهر إلكتروني نافذ لجزيئات فيروس إنفلونزا مصبوغة سالبا ومكبرة نحو 100000 مرة.
| |
| معلومات عامة | |
| الاختصاص | طب الأسرة، وطب الرئة، وأمراض معدية |
| من أنواع | مرض تنفسي، ومرض فيروسي |
| الموقع التشريحي | جهاز تنفسي[1] |
| الأسباب | |
| الأسباب | فيروس إنفلونزا |
| المظهر السريري | |
| الأعراض | حمى، وسيلان الأنف، وألم عضلي، وصداع، وإعياء |
| الإدارة | |
| أدوية | |
| حالات مشابهة | مستدمية نزلية |
| التاريخ | |
| وصفها المصدر | الموسوعة السوفيتية الأرمينية |
أسبابها
هناك ثلاثة أنواع من فيروسات الأنفلونزا تُصيب البشر، تسمى النوع A، النوع B، والنوع C.[5] عادة ما ينتشر الفيروس عن طريق الهواء من السعال أو العطس.[2] يحدث هذا غالبا على مسافات قصيرة نسبيا.[6] ويمكن أيضا أن تنتشر عن طريق لمس الأسطح الملوثة بالفيروس ومن ثم لمس الفم أو العينين.[3][6] قد يكون الشخص معديا للآخرين قبل وأثناء الوقت الذي تظهر فيه الأعراض الخاصة بالمرض.[3] ويمكن تأكيد العدوى عن طريق اختبار الحلق، والبلغم، أو الأنف للفيروس. وهناك عدد من الاختبارات السريعة المتاحة. ومع ذلك، قد لا يزال الناس لديهم العدوى إذا كانت النتائج سلبية. وهناك نوع من تفاعل البوليميراز المتسلسل الذي يكشف عن الحمض النووي الريبوزي الخاص بالفيروس ويعد هذا الاختبار الأكثر دقة.[5]
وقاية وعلاج
غسل اليدين يقلل من خطر العدوى لأن الفيروس يموت عندما يستخدم الشخص الصابون.[2] ارتداء قناع جراحي مفيد أيضا.[7] وتوصي منظمة الصحة العالمية بالتطعيمات السنوية ضد الأنفلونزا لمن يتعرضون لمخاطر عالية. اللقاح عادة ما يكون فعالا ضد ثلاثة أو أربعة أنواع من الأنفلونزا.[8] وعادة ما يكون جيد التحمل، وقد لا يكون اللقاح الذي يتم تصنيعه لمدة سنة واحدة مفيدا في السنة التالية، لأن الفيروس يتطور بسرعة. الأدوية المضادة للفيروسات مثل مثبطات نورامينيداز أوسيلتاميفير تستخدم لعلاج الإنفلونزا.[7][9]
تاريخ الفيروس
تنتشر الأنفلونزا في جميع أنحاء العالم في تفشي سنوي، مما يؤدي إلى حوالي ثلاثة إلى خمسة ملايين حالة من الأمراض الشديدة وحوالي 250.000 إلى 500.000 حالة وفاة.[2] في المناطق الشمالية والجنوبية من العالم، تحدث الفاشيات بشكل رئيسي في فصل الشتاء بينما في المناطق المحيطة بفاشيات خط الاستواء قد تحدث في أي وقت من السنة.[2] يحدث الموت في الغالب في الشباب، وكبار السن والذين يعانون من مشاكل صحية أخرى.[2][5] في القرن العشرين، وقعت ثلاثة جائحات إنفلونزا : الأنفلونزا الإسبانية في عام 1918 (50 مليون حالة وفاة تقريبا)، والأنفلونزا الآسيوية في عام 1957 (مليوني حالة وفاة)، وانفلونزا هونغ كونغ في عام 1968 (مليون حالة وفاة).[10] أعلنت منظمة الصحة العالمية تفشي نوع جديد من الأنفلونزا A / H1N1 فيروس الإنفلونزا أ ليكون جائحة إنفلونزا الخنازير 2009.[11] قد تؤثر الأنفلونزا أيضا على حيوانات أخرى، بما في ذلك الخنازير والخيول والطيور..[12]
العلامات والأعراض
ما يقرب من 33% من الأشخاص المصابين بالأنفلونزا ليس لديهم أعراض.[15]
أعراض الإنفلونزا يمكن أن تبدأ فجأة بعد يوم أو يومين بعد العدوى. وعادة ما تكون الأعراض الأولى هي قشعريرة أو إحساس بارد، ولكن الحمى شائعة أيضا في وقت مبكر من العدوى، مع درجات حرارة الجسم التي تتراوح بين 38 و 39 درجة مئوية (حوالي 100 إلى 103 درجة فهرنهايت). معظم المرضى يقضون أيام مرضهم على السرير مع آلام في جميع أنحاء أجسادهم، والتي هي أسوأ في ظهورهم والساقين.[16][17] قد تشمل أعراض الأنفلونزا ما يلي :
- حمى و إرتعاد
- سعال
- احتقان الأنف
- تقيؤ
- ثر أنفي
- عطاس
- ألم عضلي
- إعياء
- صداع
- دموع
- تورد
- حبرة [18]
- في الأطفال، أعراض المرض أغلبها في الجهاز الهضمي مثل الإسهال و الألم البطني، (قد تكون شديدة في الأطفال المصابين بالأنفلونزا ب).[19][20][21]
يمكن أن يكون من الصعب التمييز بين البرد والإنفلونزا الشائعة في المراحل الأولى من هذه الالتهابات. الأنفلونزا هي خليط من أعراض البرد والالتهاب الرئوي البارد، وآلام في الجسم، والصداع، والتعب. الإسهال ليس عادة أحد أعراض الأنفلونزا لدى البالغين، على الرغم من أنه قد شوهد في بعض الحالات البشرية من فيروس انفلونزا الطيور H5N1 ويمكن أن يكون عرضا لدى الأطفال.[14][14][20][22][23]
وبما أن الأدوية المضادة للفيروسات فعالة في علاج الأنفلونزا إذا أعطيت في وقت مبكر (انظر قسم العلاج أدناه)، فمن المهم تحديد الحالات في وقت مبكر. يمكن لمجموعات من الحمى مع السعال والتهاب الحلق و / أو احتقان الأنف تحسين دقة التشخيص. وتشير دراستان أنه خلال الفاشيات المحلية من الأنفلونزا، يكون معدل انتشار المرض أكثر من 70%، وبالتالي المرضى الذين يعانون من أي من هذه المجموعات من الأعراض يمكن أن تتعامل مع مثبطات النيورامينيداز دون اختبار. حتى في حالة عدم وجود تفشي محلي، قد يكون هناك ما يبرر العلاج لدى كبار السن خلال موسم الإنفلونزا طالما أن نسبة الانتشار أكثر من 15%.[24][25][26]
لا تزال الاختبارات المتاحة للأنفلونزا تتحسن بشكل ملحوظ. مراكز الولايات المتحدة لمكافحة الأمراض والوقاية منها (CDC) تحافظ على ملخص محدث للاختبارات المخبرية المتاحة.وفقا ل (CDC)، اختبارات التشخيص السريع لديها حساسية 50-75% وخصوصية 90-95% عند مقارنتها بالثقافة الفيروسية. قد تكون هذه الاختبارات مفيدة بشكل خاص خلال موسم الإنفلونزا (انتشار = 25%) ولكن في غياب تفشي محلي، أو موسم الإنفلونزا يكون معدل (الانتشار = 10%)[24][27][28]
أحيانا، يمكن أن تسبب الأنفلونزا مرضا شديدا بما في ذلك الالتهاب الرئوي الفيروسي الأولي أو الالتهاب الرئوي الجرثومي الثانوي. وهناك أعراض واضحة مثل صعوبة في التنفس. بالإضافة إلى ذلك، إذا كان الطفل يبدو عليه التحسن في البداية، ثم ينتكس مع ارتفاع في درجة الحرارة، يكون ذلك علامة الخطر لأن هذا الانتكاس يمكن أن يكون الالتهاب الرئوي الجرثومي.[29][30][31]
فيروس الأنفلونزا
أنواع فيروس الأنفلونزا
فيروس الأنفلونزا حسب تصنيف الفيروسات عبارة عن فيروس حمض نووي ريبوزي يتشكل من خمسة أجناس من عائلة الفيروسات المخاطية القويمة.[32]
هذه الفيروسات ترتبط فقط بذاتها بفيروسات انفلونزا الخنازير البشرية، وهي فيروسات الحمض النووي الريبي التي تنتمي إلى عائلة المارامكسيروس التي تعتبر هي السبب الشائع لالتهابات الجهاز التنفسي لدى الأطفال مثل الخناق، ويمكن أن تسبب أيضا مرضا مشابها للإنفلونزا لدى البالغين.[33][34]
تم اقتراح عائلة رابعة من فيروسات الأنفلونزا - الأنفلونزا د .[35][36][37][38][39][40][41] هذا النوع الجديد هو فيروس إنفلونزا البقر D الذي عُزل لأول مرة في عام 2012.
فيروس إنفلونزا أ
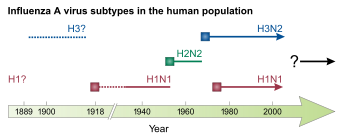
الطيور المائية البرية هي المضيف الطبيعي لمجموعة كبيرة ومتنوعة من الأنفلونزا A. أحيانا، تنتقل الفيروسات إلى أنواع أخرى، ومن ثم قد تسبب تفشي مدمر في الدواجن المحلية أو تؤدي إلى جائحة الأنفلونزا البشرية. الفيروسات من النوع A تكون هي الأكثر شراسة بين أنواع الأنفلونزا الثلاثة وتسبب أشد الأمراض. يمكن تقسيم فيروس الأنفلونزا A إلى أنماط مصلية مختلفة استنادا إلى استجابة الأجسام المضادة لهذه الفيروسات. والأنماط المصلية التي تأكدت لدى البشرهي :[42][43]
- فيروس الإنفلونزا أ - H1N1 تسبب في جائحة إنفلونزا 1918 و جائحة إنفلونزا الخنازير 2009
- فيروس الإنفلونزا أ H2N2 تسبب في خلق فيروس الإنفلونزا أ H2N2 عام 1957
- فيروس الإنفلونزا أ H3N2 تسبب في إنفلونزا هونغ كونغ عام 1968
- إتش 5 إن 1، تسبب في إنفلونزا الطيور عام 2004
- فيروس الإنفلونزا أ H7N7 - هذا الفيروس حيواني المنشأ [44]
- فيروس الإنفلونزا أ H1N2 - مستوطنة في البشر والخنازير والطيور
- H9N2
- فيروس الإنفلونزا أ H7N2
- فيروس الإنفلونزا أ H7N3
- فيروس الإنفلونزا أ H10N7
- فيروس الإنفلونزا أ H7N9
فيروس إنفلونزا ب

تصيب أنفلونزا ب البشر بشكل حصري تقريبا، وهي أقل شيوعا من الأنفلونزا أ. والحيوانات الأخرى الوحيدة المعروفة بأنها عرضة للإصابة بالأنفلونزا B هي الختم وفيريت. هذا النوع من الأنفلونزا يتغير بمعدل 2-3 مرات أبطأ من النوع A، وبالتالي أقل تنوعا وراثيا. ونتيجة لهذا النقص في التنوع المستضدي، يتم عادة الحصول على درجة من الحصانة ضد الإنفلونزا B في سن مبكرة. ومع ذلك، فإن الإنفلونزا ب تتحور بما فيه الكفاية بحيث لا يمكن الحصانة الدائمة منها. هذا المعدل المنخفض للتغيير المستضدي، جنبا إلى جنب مع مجموعة المضيف المحدودة (تثبيط انتقال الأنواع عبر المستضد)، وبالتالى نضمن بذلك عدم حدوث جوائح الإنفلونزا ب.[42][45][46][47][48][49]
فيروس إنفلونزا ج
إنفلونزا سي، الذي يصيب البشر والكلاب والخنازير، وأحيانا يسبب المرض الشديد والأوبئة المحلية. ومع ذلك، فإن الإنفلونزا ج أقل شيوعا من الأنواع الأخرى وعادة ما تسبب فقط مرضا خفيفا لدى الأطفال.[50][51][52][53]
هيكل وخصائص الفيروس
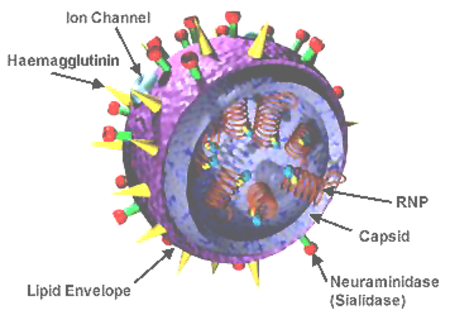
يتشابه فيروس أنفلونزا أ، ب، ج في الهيكل العام. قطر الجسيمات الفيروسية 80-120 نانومتر وعادة ما تكون كروية في الشكل، وتوجد بعض الأشكال الخيطية لها أيضاً. هذه الأشكال الخيطية أكثر شيوعا في الإنفلونزا ج، والتي يمكن أن تشكل هياكل كوردليك التي تصل إلى 500 ميكرومتر على أسطح الخلايا المصابة.ومع ذلك، على الرغم من هذه الأشكال المتنوعة، تعتبر الجسيمات الفيروسية من فيروسات الأنفلونزا المختلفة متشابهة في التكوين. هيكل الفيروس يتكون من غلاف الفيروس الذي يحتوي على نوعين رئيسيين من البروتينات السكرية، ملفوفة حول جوهر مركزي. يحتوي القلب المركزي على الجينوم الفيروسي وهو الحمض النووي الريبوزي والبروتينات الفيروسية الأخرى التي تحمي هذا الحمض النووي الريبوزي.[54][55][56][57] يعتبر الجينوم ليس قطعة واحدة من الحمض النووي؛ بل يحتوي على سبع أو ثماني قطع من الحمض النووي الريبي مجزأة كل قطعة من الحمض النووي الريبي تحتوي على واحد أو اثنين من الجينات، التي ترمز للمنتج الجيني (البروتين). على سبيل المثال، يحتوي جينوم الإنفلونزا أ على 11 جين على ثماني قطع من الحمض النووي الريبي، يرمز لأـ 11 بروتين : هيماغلوتينين HA، نيورامينيداز NA، بروتين نووي NP و، M1، M2، NS1، NS2 ، و PB1 (البلمرة الأساسية 1)، PB1-F2 وPB2.[56][58]
هيماغلوتينين (HA) والنيورامينيداز (NA) هما بروتين سكري كبير على الجزء الخارجي من الجسيمات الفيروسية. HA هو ليتين الذي يتوسط ربط الفيروس لاستهداف الخلايا ودخول الجينوم الفيروسي في الخلية المستهدفة، في حين أن NA تشارك في الإفراج عن فيروس النسل من الخلايا المصابة. تعمل الأدوية المضادة للفيروسات على تلك الأنواع من البروتين حتى تقضى على الفيروس. تصنف فيروسات الأنفلونزا أ إلى أنواع فرعية استنادا إلى استجابات الأجسام المضادة ل HA و NA. هذه الأنواع المختلفة من HA و NA تشكل أساس الفروق، على سبيل المثال : هناك 16 H و 9 N في فيروس H5N1 في الأنواع الفرعية المعروفة، ولكن يوجد فقط H 1 و N 1 في البشر.[59][60][61][62]
تضاعف الفيروس
تتضاعف الڤيروسات فقط في الخلايا الحية. عدوى الأنفلونزا وتكرارها هي عملية متعددة الخطوات : أولا، يجب أن يرتبط الفيروس بدخول الخلية، ثم يتم تسليم الجينوم إلى موقع حيث يمكن أن يقوم بانتاج نسخ جديدة من البروتينات الفيروسية يبدأ الحمض النووي الريبوزي الخاص بالفيروس بالتضاعف ويتم تجميع هذه المكونات إلى جسيمات فيروسية جديدة، وأخيرا، الخروج من الخلية المضيفة.[56][63]
ترتبط فيروسات الأنفلونزا من خلال الهيماجلوتينين على سكريات حمض السياليك على أسطح الخلايا الظهارية، وعادة ما يكون في الأنف والحلق والرئتين من الثدييات، والأمعاء من الطيور (المرحلة 1 للعدوى). بعد أن يتم تشقق الهيماغلوتينين بواسطة بروتياز، تستورد الخلية الفيروس عن طريق الإدخال الخلوي.[64][65]
الظروف الحمضية في إندوسوم (endosome) تسبب حدثين : أولا، يقوم جزء من بروتين هيماغلوتينين بلصق صمامات المغلف الفيروسي مع الغشاء الفيروسي، ثم تسمح قناة أيون M2 البروتونات والحمض النووي الخاص بالفيروس بالتحرك من خلال المغلف الفيروسي، هذه العملية يحدث فيها تفكيك للنواة وإطلاق الحمض النووي الريبي الفيروسي والبروتينات الأساسية للفيروس. ثم تخرج جزيئات الحمض النووي الريبي الفيروسي (vRNA)، وبروتون وبوليميراز الآر إن إيه المعتمد على الآر إن إيه في السيتوبلازم (المرحلة 2). يتم غلق قناة أيون M2 بواسطة الأدوية مثل أمانتادين وبالتالي يتم منع العدوى بوقف انتشار الفيروس.[56][66][67]
تشكل البروتينات الأساسية و (vRNA) مركب معقد يتم نقله إلى نواة الخلية، حيث يبدأ الحمض النووي الريبي التي يعتمد على بوليميراز الحمض النووي الريبي النسخ التكميلي للحمض النووي الريبي الإيجابي الفردي (الخطوة 3 ). يخرج (vRNA) إلى السيتوبلازم ويتم ترجمته (الخطوة 4) أو يظل موجوداً في النواة. يتم إفراز البروتينات الفيروسية المصنعة حديثا من خلال جهاز غولجي على سطح الخلية أو نقلها مرة أخرى إلى النواة لربط (vRNA) وتشكيل الجسيمات الجينومية الفيروسية الجديدة (الخطوة 5 أ). البروتينات الفيروسية الأخرى لها إجراءات متعددة في الخلية المضيفة، بما في ذلك استخدام النوكليوتيدات لـ ترجمة ال (vRNA).[68][69]
يتم تجميع vRNAs السلبية التي تعمل على تكوين جينومات فيروسات المستقبل، بينما يعتمد RNA على بوليميراز الحمض النووي الريبي، والبروتينات الفيروسية الأخرى في فيريون. هيماغلوتينين وجزيئات نيورامينيداس تتجمع في انتفاخ في غشاء الخلية. وvRNAs والبروتينات الأساسية الفيروسية تترك النواة وتدخل نتوء الغشاء (الخطوة 6). تبدأ براعم الفيروس الناضجة من الخلية في مجال غشاء فوسفاتيبي لخلية المضيف، ويتم الحصول على هيماغلوتينين والنورامينيداز من الغشاء (الخطوة 7). تبدأ الفيروسات الناضجة بالفصل من بقايا حمض سياليك من الخلية المضيفة. بعد إطلاق فيروسات الأنفلونزا الجديدة، تموت الخلية المضيفة.[65][70]
وبسبب عدم وجود إنزيمات تصحيح الحمض النووي الريبي RNA، فإن بوليميراز الآر إن إيه المعتمد على الآر إن إيه يقوم بنسخ الجينوم الفيروسي لكل 10 آلاف نيوكليوتيدات تقريبا، وهو الطول التقريبي للأنفلونزا. وبالتالي، فإن غالبية فيروسات الأنفلونزا المصنعة حديثا تسبب الانجراف المستضدي، وهو تغيير بطيء في المستضدات على السطح الفيروسي مع مرور الوقت. وتسمح هذه التغيرات الكبيرة المفاجئة للفيروس بأن يصيب أنواع مضيفة جديدة وأن يتغلب بسرعة على المناعة الوقائية. وهذا أمر مهم في ظهور الأوبئة، على النحو المبين أدناه في الفرع المتعلق بعلم الأوبئة.[61][71]
انتقال الفيروس
عندما يعطس الشخص المصاب أو يسعل ينتشر أكثر من نصف مليون من جسيمات فيروس في الهواء. يزيد إصابة الأشخاص بفيروسات الأنفلونزا بشكل حاد من نصف إلى يوم واحد بعد العدوى (الوقت الذي قد يكون فيه الشخص معديا لشخص آخر)، وتصل أعلى نسبة لإصابة شخص أخر في اليوم الثانى من المرض ويستمر لمتوسط مدة إجمالية قدرها 5 أيام، ويمكن أن تستمر لمدة 9 أيام. في أولئك الذين يتطورون من أعراض العدوى التجريبية (67% فقط من الأفراد المصابين بصحة تجريبيا)، تظهر الأعراض على هيئة نمط مماثل. الأطفال أكثر عدوى بكثير من البالغين ويظل الفيروس لمدة أسبوعين تقريبا في أجسامهم أما بالنسبة للأشخاص الذين يعانون من نقص المناعة، يمكن أن يستمر الفيروس لمدة أطول من أسبوعين.[72][73][74][75]
يمكن أن تنتشر الأنفلونزا بثلاث طرق رئيسية : عن طريق الإرسال المباشر (عندما يعط الشخص المصاب المخاط مباشرة في عيون أو أنف أو فم شخص آخر). (عندما يستنشق شخص ما الهواء الذي أنتجة الشخص المصاب بالسعال أو العطس أو البصق) ومن خلال نقله من جهة إلى أخرى أو من ناحية إلى الأنف أو من جهة الفم إما من الأسطح الملوثة أو من الاتصال المباشر مثل المصافحة. تسهم تلك الطرق الثلاث في انتشار الفيروس. استنشاق قطرة واحدة فقط من الفيروس في الجو قد يكون كافيا ليسبب العدوى. على الرغم من أن العطسة الواحدة تطلق ما يصل إلى 40.000 قطرة. معظم هذه القطرات كبيرة جدا وسوف تستقر بسرعة من الهواء. مدة قطرات إنفلونزا الطيور في الجو تتأثر بمستويات الرطوبة والأشعة فوق البنفسجية، وبالتالي مع انخفاض الرطوبة ونقص أشعة الشمس في الشتاء تساعد على بقائها لفترة أطول.[6][76][76][77][78]
وبما أن فيروس الإنفلونزا يمكن أن يعيش لفترة خارج الجسم، فإنه يمكن أن ينتقل أيضا من خلال الأسطح الملوثة مثل الأوراق النقدية، مقابض الأبواب، مفاتيح الإضاءة وغيرها من الأدوات المنزلية. طول الفترة الزمنية التي سيستمر فيها الفيروس على سطح يختلف على قيد الحياة تقدر ما بين يوم إلى يومين على الأسطح الصلبة غير المسامية مثل البلاستيك أو المعدن، ولمدة 15 دقيقة على أنسجة الورق الجاف، وخمس دقائق فقط على الجلد. ومع ذلك، إذا كان الفيروس موجودا في المخاط، وهذا يحمي الفيروس لفترات أطول (تصل إلى 17 يوما على الأوراق النقدية). يمكن لفيروسات أنفلونزا الطيور البقاء على قيد الحياة إلى أجل غير مسمى عند تجميدها. يتم تعطيل الفيروس وقتله عن طريق التسخين إلى 56 درجة مئوية (133 درجة فهرنهايت) لمدة لا تقل عن 60 دقيقة، وكذلك في الأحماض (في درجة الحموضة <2)[17][76][79][79][80][80][81]
الفيزيولوجيا المرضية
درست الآليات التي تسبب فيها عدوى الأنفلونزا أعراض في البشر بشكل مكثف. ويعتقد أن إحدى الآليات هي تثبيط هرمون القشرة الكظرية (ACTH) مما يؤدي إلى انخفاض مستويات الكورتيزول. معرفة الجينات التي تحملها سلالة معينة يمكن أن يساعد في التنبؤ بكيفية إصابتها بالعدوى البشرية ومدى خطورة هذه العدوى (أي التنبؤ بالفيزيولوجيا المرضية للسلالة).[52][82][83]
على سبيل المثال، جزء من العملية التي تسمح لفيروسات الأنفلونزا بغزو الخلايا هو انشقاق بروتين هيماغلوتينين الفيروسي من قبل بروتيز الشخص المصاب، في الفيروسات المعتدلة فإن بنية هيماغلوتينين لا يمكن إلا أن تنشق بواسطة بروتياز الحلق والرئتين، وبالتالي فإن هذه الفيروسات لا يمكن أن تصيب الأنسجة الأخرى. ومع ذلك، في سلالات شديدة الضراوة، مثل H5N1، يمكن أن يكون الانشقاق الخاص بهيماغلوتينين من قبل مجموعة واسعة من البروتياز، مما يسمح للفيروس أن ينتشر في جميع أنحاء الجسم.[64][82]
بروتين هيماجلوتينين الفيروسي هو المسؤول عن تحديد الأنواع التي يمكن أن تصيبها السلالة، السلالات التي تنتقل بسهولة بين الناس لديها بروتينات هيماغلوتينين ترتبط بمستقبلات في الجزء العلوي من الجهاز التنفسي، كما هو الحال في الأنف والحنجرة والفم. في المقابل، فإن سلالة H5N1 الفتاكة للغاية ترتبط بمستقبلات توجد في الغالب في الرئتين ( في الجزء العميق منه). هذا الاختلاف في موقع العدوى قد يكون جزءا من السبب في أن سلالة H5N1 تسبب الالتهاب الرئوي الفيروسي الشديد في الرئتين، ولكن لا ينتقل بسهولة من قبل الناس بالسعال أوبالعطس.[84][85][86][87]
الأعراض الشائعة للإنفلونزا هي : الحمى والصداع والتعب نتيجة لكميات ضخمة من السيتوكين والكيموكين و الإنترفيرون أو عامل نخر الورم ألفا المنتجة من الخلايا المصابة بالأنفلونزا. على النقيض من فيروس الأنف الذي يسبب نزلات البرد، فإن الأنفلونزا لا تسبب تلف الأنسجة. الاستجابة المناعية الهائلة قد تنتج عاصفة من السيتوكين المهددة للحياة. وقد اُقترح أن يكون هذا التأثير هو سبب الفتك غير العادي لكل من إنفلونزا الطيور H5N1، والسلالة الجائحة لعام 1918. ومع ذلك، هناك احتمال آخر هو أن هذه الكميات الكبيرة من السيتوكينات هي مجرد نتيجة لمستويات هائلة من تكاثر الفيروس التي تنتجها هذه السلالات، والاستجابة المناعية لا تساهم في حد ذاته في هذا المرض.[23][88][89][90][91][92][93]
الوقاية
التطعيم
أوصت منظمة الصحة العالمية ومراكز الولايات المتحدة من مكافحة الأمراض والوقاية منها ب لقاح الإنفلونزا للفئات المعرضة للخطر، مثل الأطفال والمسنين والعاملين في مجال الرعاية الصحية والأشخاص الذين يعانون من أمراض مزمنة مثل الربو والسكري وأمراض القلب، أما بالنسبة لتلقيح البالغين الأصحاء يكون التلقيح فعالا بشكل متواضع في خفض كمية الأعراض الشبيهة بالأنفلونزا. الأدلة تدعم انخفاض معدل الإنفلونزا لدى الأطفال الذين تزيد أعمارهم عن سنتين. في أولئك الذين يعانون من التطعيم يقلل مرض الانسداد الرئوي المزمن من التفاقم. ولكن ذلك التلقيح ليس من الواضح ما إذا كان يقلل من تفاقم الربو.[94][95][96][97][98][99] الأدلة تدعم انخفاض معدل الأمراض الشبيهة بالأنفلونزا في العديد من المجموعات التي تعاني من نقص المناعة مثل : فيروس نقص المناعة البشرية / الإيدز، والسرطان، وزرع الأعضاء. في أولئك الذين يعانون من التحصين عالية المخاطر قد يقلل من خطر الإصابة بأمراض القلب. تحصين العاملين في مجال الرعاية الصحية يؤثر على نتائج المرضى أمر مثير للجدل ولا توجد أدلة علمية كافية بعد.[100][101][102][103][104][105]
وبسبب معدل التحور العالي للفيروس، فإن لقاح الأنفلونزا المعين عادة ما يوفر الحماية لمدة لا تزيد عن بضع سنوات. وتتوقع منظمة الصحة العالمية كل عام أن تكون سلالات الفيروس أكثر انتشارا في العام المقبل (انظر التعديلات السنوية التاريخية للقاح الأنفلونزا)، مما يسمح لشركات الأدوية بتطوير لقاحات من شأنها أن توفر أفضل حصانة ضد هذه السلالات. يتم إعادة صياغة اللقاح في كل موسم لعدد قليل من سلالات الأنفلونزا المحددة ولكن لا يشمل جميع السلالات النشطة في العالم خلال هذا الموسم. ويستغرق الأمر حوالي ستة أشهر لكي يقوم المصنعون بصياغة وإنتاج ملايين الجرعات اللازمة للتعامل مع الأوبئة الموسمية؛ في بعض الأحيان، تصبح سلالة جديدة بارزة خلال تلك الفترة. ومن الممكن أيضا أن يصاب الشخص بالعدوى قبل التطعيم ويصاب بالمرض بالسلالة التي يفترض أن يمنعها اللقاح، حيث يستغرق اللقاح حوالي أسبوعين ليصبح فعالا.[106][107][108]
تسبب اللقاحات نشاط للجهاز المناعي للرد كما لو كان الجسم مصابا بالفعل، وأعراض العدوى العامة يمكن أن تظهر، على الرغم من أن هذه الأعراض عادة ليست خطيرة أو طويلة الأمد كما في الأنفلونزا . إن التأثير السلبي الأكثر خطورة هو رد فعل تحسسي شديد إما على مادة الفيروس نفسها، ومع ذلك فإن هذه التفاعلات نادرة للغاية.[109]
وقد تم تقييم فعالية التطعيم الموسمية للإنفلونزا على نطاق واسع لمجموعات مختلفة وفي بيئات مختلفة. وقد تبين عموما أنها ذو تدخل فعال من حيث التكلفة، وخاصة في الأطفال وكبار السن، إلا أن نتائج التقييمات الاقتصادية لتطعيم الأنفلونزا كثيرا ما تبين أنها تعتمد على الافتراضات الرئيسية.[110][111][112][113][114]
مكافحة العدوى
تشمل الطرق الفعالة للحد من انتقال الأنفلونزا عادات صحية وشخصية جيدة مثل : عدم لمس عينيك أو أنفك أو فمك؛ غسل اليدين بشكل متكرر في اليوم الواحد (بالصابون والماء، أو مع التدليك اليدوي القائم على الكحول)؛ تغطية الفم أثناء السعال والعطس. وتجنب الاتصال الوثيق مع المرضى؛ والبقاء في المنزل إذا كنت مريضا. ويوصى أيضا بتجنب البصق.[115][116][117] وعلى الرغم من أن أقنعة الوجه قد تساعد على منع انتقال المرض عند رعاية المرضى، إلى أن هناك أدلة مختلطة حول الآثار المفيدة في المجتمع. التدخين يثير خطر الإصابة بالإنفلونزا، فضلا عن إنتاج أعراض مرضية أكثر شدة.[118][119][120][121][122]
وبما أن الأنفلونزا تنتشر عبر كل من الهباء الجوي والاتصال بالأسطح الملوثة، فإن تعقيم السطح قد يساعد على منع العدوى. الكحول هو مطهر فعال ضد فيروسات الأنفلونزا، في حين أن مركبات الأمونيوم الرباعية يمكن استخدامها مع الكحول بحيث يستمر تأثير التعقيم لفترة أطول. في المستشفيات، تستخدم مركبات الأمونيوم الرباعية والتبييض لتعقيم الغرف أو المعدات التي تم استخدامها من قبل المرضى الذين يعانون من أعراض الأنفلونزا. أما في المنزل، يمكن القيام بذلك بشكل فعال مع مبيض الكلور المخفف.[123][124][125]
وقد أدت التبديلات الاجتماعية المستخدمة خلال الأوبئة السابقة، مثل إغلاق المدارس والكنائس والمسارح، إلى إبطاء انتشار الفيروس ولكن لم يكن لها تأثير كبير على معدل الوفيات الإجمالي. ومن غير المؤكد أن تقليل التجمعات العامة، من خلال إغلاق المدارس وأماكن العمل مثلا، سيحد من انتقال المرض لأن الأشخاص المصابين بالأنفلونزا يمكن نقلهم من منطقة إلى أخرى؛ فإن من الصعب أيضا إنفاذ هذه التدابير وقد لا تحظى بشعبية. عندما يصاب عدد قليل من الناس، فإن عزل المرضى قد يقلل من خطر انتقال العدوى.[117][126][127]
العلاج
ينصح الناس المصابون بالإنفلونزا بالحصول على الكثير من الراحة، وشرب الكثير من السوائل، وتجنب استخدام المشروبات الكحولية والتبغ، وإذا لزم الأمر، تناول أدوية مثل الأسيتامينوفين (باراسيتامول) لتخفيف الحمى وآلام العضلات المرتبطة بالإنفلونزا. يجب على الأطفال والمراهقين الذين يعانون من أعراض الإنفلونزا (وخاصة الحمى) تجنب تناول الأسبرين خلال عدوى الأنفلونزا (وخاصة فيروس إنفلونزا ب)، لأن القيام بذلك يمكن أن يؤدي إلى متلازمة راي، وهو مرض نادر ولكنه يحتمل أن يكون مميتا لأنه يصيب الكبد. وبما أن الأنفلونزا سببها فيروس، فإن المضادات الحيوية ليس لها أي تأثير على العدوى؛ ما لم ينص على الالتهابات الثانوية مثل الالتهاب الرئوي الجرثومي. قد يكون الدواء المضاد للفيروسات فعالا، إذا أعطي في وقت مبكر، ولكن بعض سلالات الأنفلونزا يمكن أن تظهر مقاومة للأدوية المضادة للفيروسات القياسية وهناك قلق بشأن جودة البحث.[128][129][130]
الأدوية المضادة للفيروسات
يوجد فئتان من الأدوية المضادة للفيروسات المستخدمة ضد الإنفلونزا هي مثبطات نورامينيداز (أوسيلتاميفير و زاناميفير) ومثبطات البروتين M2 (مشتقات أدامانتان).
مثبطات النيورامينيداز
فوائد مثبطات النيورامينيداز عموما في الأشخاص الأصحاء لا يبدو أن تكون أكبر من مخاطرها. في أولئك المصابون بالإنفلونزا، تعمل تلك الأدوية على خفض طول مدة الأعراض ولكن لا يبدو أنها تؤثر على خطر حدوث مضاعفات مثل الحاجة إلى دخول المستشفى أو الالتهاب الرئوي. قبل عام 2013 كانت الفوائد غير واضحة لأن الشركة المصنعة (Roche) رفضت الإفراج عن بيانات المحاكمة لتحليل مستقل. وقد أدت المقاومة السائدة على نحو متزايد لمثبطات النيورامينيداز الباحثين إلى البحث عن أدوية بديلة مضادة للفيروسات مع آليات عمل مختلفة.[7][9][131][132]
مثبطات M2
الأدوية المضادة للفيروسات مثل أمانتادين وريمانتادين تمنع قناة أيون الفيروسية (بروتين M2)، وبالتالي تثبيط تضاعف فيروس الإنفلونزا أ. هذه الأدوية فعالة في بعض الأحيان ضد الإنفلونزا أ إذا أعطيت في وقت مبكر من العدوى ولكنها غير فعالة ضد فيروسات الأنفلونزا ب، وقد زادت المقاومة المقاسة لأمانتادين وريمانتادين في العزلات الأمريكية من فيروس H3N2 إلى 91% في عام 2005. هذا المستوى العالي من المقاومة قد يكون بسبب سهولة توافر الامانتادين كجزء من العلاجات الباردة دون وصفة طبية في بلدان مثل الصين وروسيا، واستخدامها لمنع تفشي الأنفلونزا في الدواجن المستزرعة. وأوصت CDC بعدم استخدام مثبطات M2 خلال موسم الإنفلونزا 2005-2006 بسبب مستويات عالية من مقاومة الدواء.[133][134][135][136][137][138]
تنبؤ الحالة الصحية
آثار الأنفلونزا أكثر شدة من البرد العادى كما تستمر لفترة أطول. معظم الناس تتعافى تماما في حوالي 1-2 أسابيع، ولكن البعض الاخر يتطور إلى المضاعفات التي تهدد الحياة (مثل الالتهاب الرئوي). وهكذا، يمكن أن تكون الأنفلونزا مميتة، خاصة بالنسبة للضعفاء، صغارا وكبارا، أو أصحاب الأمراض المزمنة. الأشخاص الذين يعانون من ضعف في الجهاز المناعي، مثل المصابين بفيروس نقص المناعة البشرية المتقدم أو المرضى الذين زرعوا عضو معين ( تم القضاء على أجهزة المناعة طبيا لمنع رفض الجهاز المزروع)، يعانون من المرض بشدة بشكل خاص. النساء الحوامل والأطفال الصغار هم أيضا في خطر كبير للمضاعفات.[61][139][140]
يمكن أن تؤدي الإنفلونزا إلى تفاقم المشاكل الصحية المزمنة. الناس الذين يعانون من انتفاخ الرئة، التهاب الشعب الهوائية المزمن أو الربو قد يعانون من ضيق في التنفس، كما تسبب الأنفلونزا تفاقم مرض القلب التاجي أو قصور القلب الاحتقاني. التدخين هو عامل خطر آخر يرتبط بأمراض أكثر خطورة ويسبب زيادة الوفيات من الأنفلونزا.[141][142]
وفقا لمنظمة الصحة العالمية: "كل شتاء، عشرات الملايين من الناس يصابون بالإنفلونزا، ومعظمهم يغيب من العمل لمدة أسبوع، كبار السن هم أكثر عرضة للوفاة من المرض، ونحن نعرف أن عدد القتلى في جميع أنحاء العالم يتجاوز بضع مئات لالاف الأشخاص سنويا، ولكن حتى في البلدان المتقدمة، فإن الأرقام غير مؤكدة، لأن السلطات الطبية لا تحقق عادة من مات فعلا من الأنفلونزا والذين ماتوا بسبب مرض يشبه الأنفلونزا ". يمكن أن تحدث مشاكل خطيرة من الأنفلونزا في أي سن. الناس على مدى 65 عاما، والنساء الحوامل والأطفال الصغار جدا والناس من جميع الفئات العمرية يعانون من أمراض مزمنة هم أكثر احتمالا للحصول على مضاعفات الأنفلونزا، مثل الالتهاب الرئوي والتهاب الشعب الهوائية، الجيوب الأنفية، والتهابات الأذن.[143][144]
في بعض الحالات، قد تسهم استجابة المناعة الذاتية لعدوى الأنفلونزا في تطور متلازمة غيلان باريه. ومع ذلك، فإن العديد من الإصابات الأخرى يمكن أن تزيد من خطر هذا المرض، قد تكون الأنفلونزا فقط سبب مهم خلال الأوبئة. ويعتقد أن هذه المتلازمة أيضا تأثير جانبي نادر للقاحات الأنفلونزا. ويظهر أحد الاستعراضات حدوث حالة واحدة لكل مليون من اللقاحات. الإصابة بعدوى الإنفلونزا نفسها يزيد كلا من خطر الموت (يصل إلى 1 في 10000).[145][146][147][147][148][149]
علم الأوبئة
التغيرات الموسمية
تصل الأنفلونزا إلى ذروتها في فصل الشتاء، ولأن نصف الكرة الشمالي والجنوبي له فصل الشتاء في أوقات مختلفة من السنة، فهناك في الواقع موسمان مختلفان للإنفلونزا كل عام. ولهذا تقدم منظمة الصحة العالمية (بمساعدة المراكز الوطنية للأنفلونزا) توصيات بشأن تركيبتين مختلفتين من اللقاحات كل عام؛ واحدة في الشمال، وواحدة لنصف الكرة الجنوبي.[108]
وهناك لغز طويل الأمد هو السبب في أن تفشي الأنفلونزا يحدث موسميا وليس موحدا على مدار السنة. أحد التفسيرات المحتملة هو أن الناس في كثير من الأحيان خلال فصل الشتاء، هم على اتصال وثيق في كثير من الأحيان، وهذا يعزز انتقال الفيروس من شخص لآخر. زيادة السفر بسبب موسم الشتاء في نصف الكرة الشمالي قد تلعب دوراً مهماً أيضا. عامل آخر هو أن درجات الحرارة الباردة تجعل الهواء أكثر جفافا، والتي قد تجفف المخاط، ومنع الجسم من طرد فعال لجزيئات الفيروس. كما يستمر الفيروس لفترة أطول على الأسطح في درجات حرارة أكثر برودة ويكون انتقال الهباء الجوي للفيروس أعلى في البيئات الباردة (أقل من 5 درجات مئوية) مع رطوبة نسبية منخفضة. ويبدو أن انخفاض رطوبة الهواء في الشتاء هو السبب الرئيسي لانتقال الأنفلونزا الموسمية في المناطق المعتدلة.[150][151][152][153]
ومع ذلك، تحدث التغيرات الموسمية في معدلات الإصابة أيضا في المناطق الاستوائية، وفي بعض البلدان ينظر إلى هذه القمم من العدوى بشكل رئيسي خلال موسم الأمطار. كما أن التغيرات الموسمية في معدلات الاتصال من الناحية المدرسية، والتي تعتبر عاملا رئيسيا في أمراض الطفولة الأخرى مثل الحصبة والسعال الديكي، قد تلعب أيضا دورا في الإنفلونزا. مزيج من هذه الآثار الموسمية الصغيرة يمكن تضخيمها بواسطة الرنين الديناميكي مع دورات المرض الذاتية.[154][155][156]
وهناك فرضية بديلة لشرح الموسمية في عدوى الأنفلونزا وهي تأثير مستويات فيتامين (د) على المناعة للڤيروس. اقترحت هذه الفكرة لأول مرة من روبرت إدغر هوب - سيمبسون في عام 1965. واقترح أن تكون أسباب وباء الأنفلونزا خلال فصل الشتاء مرتبطة بالتقلبات الموسمية لفيتامين (د)، الذي ينتج في الجلد تحت تأثير الأشعة فوق البنفسجية الشمسية (أو الاصطناعية). وقد يفسر ذلك سبب حدوث الإنفلونزا في الشتاء وأثناء موسم الأمطار الاستوائي، عندما يبقى الناس في الداخل، بعيدا عن الشمس، وتنخفض مستويات فيتامين (د) لديهم مما يسهل من انتشار الفيروس.[157][158]
الأوبئة وانتشار الفيروس
سبب فيروس الإنفلونزا عبارة عن مجموعة متنوعة من أنواع وسلالات من الفيروسات، في أي سنة من السنوات بعض السلالات يمكن أن تنقرض في حين يتم خلق جيل اخر، ويمكن أن تسبب تلك السلالة الجديدة وباء عالميا. السلالة الجديدة من الفيروس يكون في مواسم عادية في السنة، اثنين سلالات الإنفلونزا (واحد لكل نصف الكرة الأرضية)، وهناك ما بين ثلاثة وخمسة ملايين حالة مرض شديدة وحول 500.000 حالة وفاة في جميع أنحاء العالم. على الرغم من أن الإصابة بالأنفلونزا يمكن أن تختلف على نطاق واسع بين السنوات، وترتبط حوالي 36.000 حالة وفاة وأكثر من 200.000 المستشفيات مباشرة مع الإنفلونزا كل عام في الولايات المتحدة. وأنتجت إحدى طرق حساب وفيات الأنفلونزا تقديرات تقدر ب 41.400 حالة وفاة سنويا في الولايات المتحدة بين عامي 1979 و 2001. وأفادت طرق مختلفة في عام 2010 من قبل مراكز السيطرة على الأمراض والوقاية منها (CDC) مجموعة من انخفاض من حوالي 3300 حالة وفاة إلى 49.000 حالة في السنة.[159][160][161][162][163][164]
يحدث الوباء ما يقرب من ثلاث مرات في القرن، ويصيب نسبة كبيرة من سكان العالم، ويمكن أن يقتل عشرات الملايين من الناس (انظر قسم الأوبئة). وقدرت إحدى الدراسات أنه في حالة ظهور سلالة مماثلة لانفلونزا 1918 اليوم، فإنها يمكن أن تقتل ما بين 50 و 80 مليون شخص.[165]
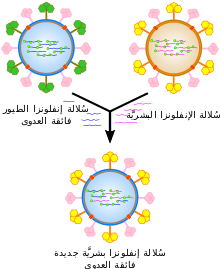
إن فيروسات الأنفلونزا الجديدة تتطور باستمرار عن طريق الطفرات التي تحدث لها أو عن طريق إعادة التكهن. الطفرات يمكن أن تسبب تغيرات صغيرة في مستضدات هيماغلوتينين ونورامينيداز على سطح الفيروس. وهذا ما يسمى الانجراف المستضدي، الذي يخلق ببطء مجموعة متزايدة من سلالات حتى يتم خلق سلالة جديدة تماماً يمكن أن تصيب الناس الذين هم في مأمن من سلالات كانت موجودة من قبل. هذا البديل الجديد يحل محل السلالات القديمة كما أنها تجتاح بسرعة العديد من السكان، مما تسبب الوباء. ومع ذلك، بما أن السلالات الناتجة عن الانجراف لا تزال مماثلة إلى حد معقول للسلالات القديمة، فإن بعض الناس لا يزالون في مأمن لهم. وعلى النقيض من ذلك، عندما تتكاثر فيروسات الأنفلونزا، فإنها تكتسب مستضدات جديدة تماما - على سبيل المثال عن طريق إعادة التكاثر بين سلالات الطيور والسلالات البشرية؛ وهذا ما يسمى التحول المستضدي. إذا تم إنتاج فيروس الأنفلونزا البشرية التي لديها مستضدات جديدة تماما، سوف يكون الجميع عرضة لهذا الفيروس الجديد، وسوف تنتشر الأنفلونزا بحيث لا يمكن السيطرة عليها، مما تسبب في حدوث الوباء. وعلى النقيض من هذا النموذج من الأوبئة القائمة على الانجراف والتحول المستضدي، اقترحت مقاربة بديلة حيث تنتج الأوبئة الدورية عن طريق تفاعلات مجموعة ثابتة من السلالات الفيروسية مع مجموعة بشرية مع مجموعة متغيرة باستمرار من الحصانات لمختلف السلالات الفيروسية.[42][166][167][168]
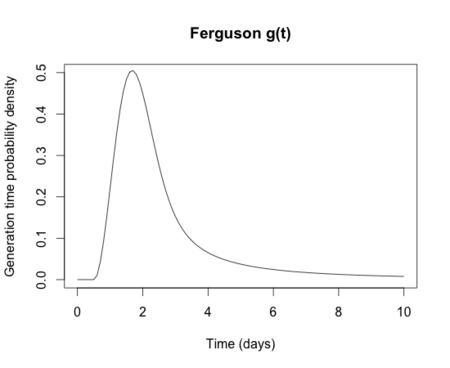
ومن وجهة نظر الصحة العامة، انتشرت أوبئة الإنفلونزا بسرعة وأصبح من الصعب جدا السيطرة عليها. معظم سلالات فيروس الإنفلونزا ليست معدية جدا وكل فرد مصاب سوف يصيب واحد أو اثنين من الأفراد الآخرين (عدد التكاثر الأساسي للأنفلونزا عموما حوالي 1.4). ومع ذلك، فإن وقت التوليد للأنفلونزا قصير للغاية : الوقت الذي يستغرقه الشخص المصاب لكى يصيب شخص أخر سليم هو يومين فقط. ويعني وقت التوليد القصير أن أوبئة الأنفلونزا ترتفع عموما في حوالي شهرين وتحترق بعد 3 أشهر، ولذلك يجب اتخاذ قرار التدخل في وباء الأنفلونزا في وقت مبكر، وبالتالي فإن القرار غالبا ما يتخذ على خلفية البيانات غير المكتملة. وهناك مشكلة أخرى هي أن الأفراد يصبحون معديين قبل أن تظهر أعراض المرض عليهم، مما يعني أن وضع الناس في الحجر الصحي بعد إصابتهم بالمرض ليس تدخلا فعالا في الصحة العامة.[15][169]
تاريخ الفيروس
كلمة الإنفلونزا تأتي من اللغة الإيطالية بمعنى "النفوذ" وتشير إلى سبب المرض. أدت التغيرات في الفكر الطبي إلى تعديله إلى إنفلونزا ديل فريدو، بمعنى "تأثير البرد". وقد استخدمت كلمة الإنفلونزا لأول مرة في اللغة الإنجليزية للإشارة إلى المرض الذي نعرفه اليوم في عام 1703 من قبل ج. هاجر من جامعة ادنبره في أطروحته دي كاتارهو أوبديميو، فيل إنفلنزا، بروت في الهند أوتشيدنتالي سيس أوستنديت. المصطلحات القديمة للأنفلونزا تشمل الوباء الوبائي، والتعرق المرضي، والحمى الإسبانية (وخاصة بالنسبة لسلالة الأنفلونزا الجائحة لعام 1918).[170][171][172][173]
تفشي الوباء

كانت أعراض الأنفلونزا البشرية موضحة بوضوح من قبل أبقراط قبل حوالي 2400 سنة. على الرغم من أن الفيروس تسبب في انتشار الأوبئة عبر تاريخ البشرية، إلا أن البيانات التاريخية عن الأنفلونزا يصعب تفسيرها، لأن الأعراض يمكن أن تكون مشابهة لأعراض أمراض الجهاز التنفسي الأخرى. انتشر المرض من أوروبا إلى الأمريكتين في وقت مبكر من الاستعمار الأوروبي للأمريكتين. حيث أن معظم السكان الأصليين في جزر الأنتيل قتلوا بسبب وباء يشبه الإنفلونزا الذي اندلع في عام 1493، بعد وصول كريستوفر كولومبوس.[175][176][177][178][179][180]
كان أول وباء للأنفلونزا في عام 1580، والذي بدأ في روسيا وانتشر إلى أوروبا عبر أفريقيا. وفي روما، قتل أكثر من 8000 شخص، وتم القضاء على العديد من المدن الإسبانية تقريبا. واستمرت الأوبئة بشكل متقطع طوال القرنين السابع عشر والثامن عشر، مع انتشار وباء 1830-1833 على نطاق واسع؛ فقد أصيب حوالي ربع الأشخاص المعرضين للفيروس.[177]
كان الوباء الأكثر شهرة وأكثر فتكا بالبشر عام 1918 (وباء الإنفلونزا الأسبانية - جائحة إنفلونزا 1918) (نوع الإنفلونزا : فيروس الإنفلونزا أ H1N1 )، التي استمرت من 1918 إلى 1919. عدد الأشخاص الذين قتلوا غير معروف، ولكن التقديرات تتراوح من خمسين حتى مائة مليون من القتلى.[174][177][181][182] وقد وصف هذا الوباء بأنه "أكبر محرقة طبية في التاريخ" وربما قتل العديد من الناس مثل الموت الأسود. وقد تسبب هذا العدد الكبير من القتلى في ارتفاع معدل الإصابة بنسبة تصل إلى 50%. كانت الأعراض في عام 1918 غير عادية لدرجة أن الأنفلونزا في البداية كانت تشخص خطأ على أنها حمى الضنك والكوليرا أو التيفوئيد. كتب أحد المراقبين، "كان واحدا من المضاعفات الأكثر لفتا هو : النزف من الأغشية المخاطية، وخاصة من الأنف والمعدة والأمعاء. نزيف من الأذنين ونزيف دموي صغير في الجلد أيضا". غالبية الوفيات كانت من الالتهاب الرئوي الجرثومي، وهو عدوى ثانوية تسببها الأنفلونزا، ولكن الفيروس أيضا قتل الناس بشكل مباشر.[181][182][183]
كان وباء انفلونزا عام 1918 عالميا حقا، حيث انتشر حتى القطب الشمالي والجزر النائية في المحيط الهادئ. وأدى المرض الشاذ بشكل غير عادي إلى مقتل ما بين اثنين وعشرين بالمائة من المصابين، بدلا من معدل وفيات الوباء الأنفلونزا المعتاد بنسبة 0.1%. وكانت ميزة أخرى غير عادية من هذا الوباء أن معظم القتلى معظمهم شباب، مع 99% من وفيات الإنفلونزا الوبائية التي تحدث في الناس تحت 65، وأكثر من النصف في الشباب 20-40 سنة. هذا أمر غير عادي لأن الإنفلونزا عادة ما تكون أكثر فتكا في الصغار جدا (تحت سن 2) والشيخوخة (فوق سن 70). ولا يعرف مجموع الوفيات الناجمة عن وباء 1918-1919، ولكن يقدر أن 2.5% إلى 5% من سكان العالم قد قتلوا. وقد يكون قد قتل 25 مليونا في الأسابيع ال 25 الأولى؛ في المقابل، قتل فيروس نقص المناعة البشرية / الإيدز 25 مليونا في السنوات ال 25 الأولى.[174][181][181][184]
لم تكن جائحات الإنفلونزا مدمرة جدا بعد ذلك. وشملت هذه الأنواع : 1957 الأنفلونزا الآسيوية (فيروس الإنفلونزا أ H2N2) وإنفلونزا هونغ كونغ عام 1968 (فيروس الإنفلونزا أ - H3N2 )، ولكن حتى هذه الفاشيات الصغيرة قتلت الملايين من الناس. في جائحات في وقت لاحق كانت المضادات الحيوية المتاحة للسيطرة على الالتهابات الثانوية قد ساعدت على خفض الوفيات مقارنة مع الإنفلونزا الأسبانية عام 1918.[174]
| اسم الوباء | التاريخ | عدد الوفيات | معدل إماتة الحالة | السلالة | مؤشر شدة الجوائح |
|---|---|---|---|---|---|
| وباء انفلونزا 1889-1890
(الإنفلونزا الآسيوية أو الروسية)[185] |
1889–1890 | 1 مليون | 0.15% | قد يكون فيروس الإنفلونزا أ H3N8 أو فيروس الإنفلونزا أ H2N2 |
N/A |
| جائحة إنفلونزا 1918 (الإنفلونزا الأسبانية)[186] |
1918–1920 | من 20 لـ 100 مليون | 2% | فيروس الإنفلونزا أ H1N1 | 5 |
| فيروس الإنفلونزا أ H2N2 | 1957–1958 | من 1 إلى 1 ونص مليون | 0.13% | فيروس الإنفلونزا أ H2N2 | 2 |
| فيروس الإنفلونزا أ H3N2 | 1968–1969 | من 0.75 إلى 1 مليون | <0.1% | فيروس الإنفلونزا أ H3N2 | 2 |
| فيروس الإنفلونزا أ H1N1 | 1977–1978 | - | N/A | فيروس الإنفلونزا أ H1N1 | N/A |
| جائحة إنفلونزا الخنازير 2009[187] | 2009–2010 | 105,700–395,600[188] | 0.03% | فيروس الإنفلونزا أ H1N1 | N/A |
كان أول فيروس إنفلونزا معزول من الدواجن، تم ذلك في عام 1901 بتمرير العامل الذي يسبب مرضا يسمى "طاعون الطيور" من خلال مرشحات تشامبرلاند، التي لها مسام صغيرة جدا للبكتيريا لتمريرها. تم اكتشاف السبب المسبب للإنفلونزا، عائلة أورثوميكسوفيريداي من الفيروسات، لأول مرة في الخنازير التي كتبها ريتشارد شوب في عام 1931. وتبع هذا الاكتشاف بفترة قصيرة عزل الفيروس من البشر من قبل مجموعة برئاسة باتريك ليدلاو في مجلس البحوث الطبية في المملكة المتحدة في عام 1933.[189][190][191]
كانت أول خطوة هامة نحو الوقاية من الأنفلونزا هي تطوير لقاح للفيروسات القاتلة في عام 1944 من قبل توماس فرانسيس. وهذا مبني على عمل فرانك ماكفارلين بورنيت الأسترالي الذي أظهر أن الفيروس فقد الفوعة عندما تم تربيته في الدجاجة المخصبة. طبق فرانسيس هذه الملاحظة حيث سمح له مجموعة من الباحثين في جامعة ميشيغان لتطوير أول لقاح للأنفلونزا، بدعم من الجيش الأمريكي. وكان الجيش مشاركا عميقا في هذا البحث بسبب تجربته في الإنفلونزا في الحرب العالمية الأولى، عندما قتل الآلاف من الجنود بالفيروس في غضون أشهر. وبالمقارنة مع اللقاحات، كان تطوير العقاقير المضادة للإنفلونزا أبطأ، مع ترخيص أمانتادين في عام 1966، وبعد ثلاثين عاما تقريبا، تم تطوير الفئة التالية من العقاقير (مثبطات نورامينيداز). فرانك ماكفارلين بورنيت.[59][181][193][194]
المجتمع والثقافة
تسبب الأنفلونزا تكاليف مباشرة بسبب فقدان الإنتاجية والعلاج الطبي المرتبط بها، فضلا عن التكاليف غير المباشرة للتدابير الوقائية. أما في الولايات المتحدة، فإن الإنفلونزا مسؤولة عن تكلفة إجمالية تزيد عن 10 مليارات دولار سنويا، في حين يقدر أن الجائحة المقبلة قد تسبب مئات المليارات من الدولارات في التكاليف المباشرة وغير المباشرة. ومع ذلك، لم يتم دراسة الآثار الاقتصادية للأوبئة الماضية بشكل مكثف، وقد اقترح بعض المؤلفين أن الإنفلونزا الإسبانية كان لها في الواقع تأثير إيجابي طويل الأجل على نمو الدخل الفردي، على الرغم من انخفاض كبير في عدد السكان العاملين، وقد حاولت دراسات أخرى التنبؤ بتكاليف وباء خطير مثل الإنفلونزا الإسبانية عام 1918 في الاقتصاد الأمريكي، حيث أصبح 30% من جميع العمال مرضى، وقُتل 2.5%. ومن شأن معدل المرض بنسبة 30 في المائة وطول المرض لمدة ثلاثة أسابيع أن يخفض الناتج المحلي الإجمالي بنسبة 5 في المائة. وستأتي تكاليف إضافية من العلاج الطبي الذي يتراوح بين 18 مليون و 45 مليون نسمة، وستبلغ التكاليف الاقتصادية الإجمالية 700 بليون دولار تقريبا.[195][196][197]
كما أن التكاليف الوقائية مرتفعة أيضا. حيث أنفقت الحكومات في جميع أنحاء العالم مليارات الدولارات الأمريكية على الإعداد والتخطيط لوباء إنفلونزا الطيور H5N1 المحتمل، مع التكاليف المرتبطة بشراء الأدوية واللقاحات، فضلا عن تطوير تدريبات الكوارث واستراتيجيات لتحسين مراقبة الحدود. وفي 1 تشرين الثاني / نوفمبر 2005، كشف الرئيس الأمريكي جورج دبليو بوش عن الاستراتيجية الوطنية للوقاية من خطر الإنفلونزا الجائحة ، مدعومة بطلب من الكونغرس بمبلغ 7.1 بليون دولار لبدء تنفيذ الخطة. وعلى الصعيد الدولي، في 18 كانون الثاني / يناير 2006، تعهدت الدول المانحة بتقديم 2 بليون دولار من دولارات الولايات المتحدة لمكافحة انفلونزا الطيور في المؤتمر الدولي لإعلان التبرعات بشأن انفلونزا الطيور والإنسان الذي عقد لمدة يومين في الصين.[196][198][199][200]
وفي تقييم لوباء H1N1 لعام 2009 في بلدان مختارة في نصف الكرة الجنوبي، تشير البيانات إلى أن جميع البلدان شهدت بعض الآثار الاجتماعية / الاقتصادية المعزولة زمنيا وانخفاضا مؤقتا في السياحة على الأرجح بسبب الخوف من مرض H1N1 2009 . ولا يزال من السابق لأوانه تحديد ما إذا كان وباء H1N1 قد تسبب في أي آثار اقتصادية طويلة الأجل.[201]
أبحاث
شملت البحوث المتعلقة بالإنفلونزا دراسات عن الفيروسات الفيروسية الجزيئية، وكيف ينتج الفيروس المرض والاستجابات المناعية المضيفة، وعلم الجينوم الفيروسي، وكيف ينتشر الفيروس (علم الأوبئة). وساعدت هذه الدراسات في تطوير التدابير المضادة للأنفلونزا؛ على سبيل المثال، فهم أفضل لاستجابة الجهاز المناعي في الجسم ساعد على تطوير اللقاح، وصورة مفصلة لخلايا الفيروس سهلت تطوير العقاقير المضادة للفيروسات. ومن بين البرامج البحثية الأساسية الهامة مشروع تسلسل الجينوم في الأنفلونزا، الذي يقوم بإنشاء مكتبة لتسلسل الأنفلونزا؛ ينبغي لهذه المكتبة أن تساعد في توضيح العوامل التي تجعل سلالة واحدة أكثر فتكا من غيرها، والتي تؤثر أكثر على الجهاز المناعي، وكيف يتطور الفيروس مع مرور الوقت.[202]
وللبحوث في اللقاحات الجديدة أهمية خاصة، حيث أن اللقاحات الحالية بطيئة جدا ومكلفة، ويجب إعادة صياغتها كل عام. وقد يؤدي تسلسل جينوم الإنفلونزا وتكنولوجيا الحمض النووي المؤتلف إلى تسريع توليد سلالات لقاح جديدة من خلال السماح للعلماء باستبدال المستضدات الجديدة بسلالة لقاح تم تطويره سابقا. ويجري أيضا تطوير تكنولوجيات جديدة لزراعة فيروسات في زراعة الخلايا، مما يعد بتحقيق عوائد أعلى، وتكلفة أقل، ونوعية أفضل، وزيادة في القدرات. يجري الآن بحث عن لقاح عالمي ضد مرض الأنفلونزا، يستهدف المجال الخارجي من الغشاء الفيروسي للبروتين M2 (M2e)، ويجري في جامعة غنت من قبل والتر فيرس، كسافير سايلنز وفريقهم.[203][204][205][206] و قد اختتمت بنجاح المرحلة الأولى في التجارب السريرية. كان هناك بعض النجاح البحثي نحو "لقاح الإنفلونزا العالمي" الذي ينتج أجسام مضادة ضد البروتينات على المعطف الفيروسي الذي يتحول بسرعة أقل، وبالتالي فإن طلقة واحدة يمكن أن توفر حماية أطول مدى.[207][208][209][210]
ويجري أيضا التحقيق في عدد من مستحضرات دوائية حيوية واللقاحات العلاجية والمناعية من أجل علاج العدوى التي تسببها الفيروسات. تم تصميم البيولوجيا العلاجية لتفعيل الاستجابة المناعية للفيروسات أو المستضدات. عادة، البيولوجية لا تستهدف مسارات الأيض مثل العقاقير المضادة للفيروسات، ولكن تعمل على تحفيز الخلايا المناعية مثل الخلايا الليمفاوية، الضامة، و / أو خلايا مقدمة للمستضد، في محاولة لدفع استجابة مناعية تجاه خلايا الفيروس. نماذج الأنفلونزا، مثل أنفلونزا الفئران، هي نماذج مريحة لاختبار آثار البيولوجيا الوقائية والعلاجية. على سبيل المثال، اللمفاويات (تي) وهي خلية مناعية تمنع النمو الفيروسي في نموذج الفئران من الأنفلونزا.[211]
حيوانات
تصيب الأنفلونزا العديد من الأنواع الحيوانية، ويمكن أن يحدث نقل السلالات الفيروسية بين الأنواع. ويعتقد أن الطيور هي الخزانات الحيوانية الرئيسية لڤيروسات الأنفلونزا. وقد تم تحديد ستة عشر شكل من هيماجلوتينين وتسعة أشكال من النيورامينيداز. جميع الأنواع الفرعية المعروفة (HxNy) موجودة في الطيور، ولكن العديد من الأنواع الفرعية متوطنة في البشر والكلاب والخيول والخنازير. بينما الإبل والقطط والأختام والمنك والحيتان تظهر أيضا أدلة على الإصابة المسبقة أو التعرض للأنفلونزا. وتسمى أحيانا أنواع فيروس الإنفلونزا وفقا للأنواع المتوطنة في السلالة. المتغيرات الرئيسية المسماة باستخدام هذه الاتفاقية هي: انفلونزا الطيور والإنفلونزا البشرية وانفلونزا الخنازير وانفلونزا الحصان وانفلونزا الكلاب. (إنفلونزا القطط يشار اليها بالتهاب الأنف وفيروسات القطط الفيروسي أو فيروس كاليسيف القطط وليس العدوى من فيروس الأنفلونزا.) في الخنازير والخيول والكلاب، أعراض الأنفلونزا تشبه البشر، مع السعال والحمى وفقدان الشهية. لم يتم دراسة تواتر الأمراض الحيوانية بشكل جيد كعدوى بشرية، ولكن اندلاع الأنفلونزا في أختام الميناء تسبب في وفاة حوالي 500 ختم من ساحل نيو إنجلاند في 1979-1980.غير أن الفاشيات في الخنازير شائعة ولا تسبب وفيات شديدة. كما تم تطوير لقاحات لحماية الدواجن من انفلونزا الطيور. هذه اللقاحات يمكن أن تكون فعالة ضد سلالات متعددة وتستخدم كجزء من استراتيجية وقائية.[46][212][213][214]
إنفلونزا الطيور
أعراض الإنفلونزا في الطيور متغيرة ويمكن أن تكون غير محددة. قد تكون الأعراض التالية للإصابة بالأنفلونزا الطيرية منخفضة الإمراض مثل الريش المتضخم، أو انخفاض طفيف في إنتاج البيض، أو فقدان الوزن جنبا إلى جنب مع أمراض الجهاز التنفسي البسيطة. وبما أن هذه الأعراض الخفيفة يمكن أن تجعل التشخيص في الميدان صعبا، فإن تتبع انتشار أنفلونزا الطيور يتطلب إجراء فحوص مخبرية لعينات من الطيور المصابة. بعض السلالات مثل H9N2 الآسيوية هي شديدة الفوعة للدواجن وقد تسبب أعراض أكثر تطرفا ووفيات كبيرة. في شكله الأكثر إمراضا، تنتج الأنفلونزا في الدجاج والديك الرومي ظهور مفاجئ لأعراض حادة و 100% تقريبا من الوفيات خلال يومين. كما ينتشر الفيروس بسرعة في الظروف المزدحمة التي ينظر إليها في الزراعة المكثفة للدجاج والديك الرومي، وهذه الفاشيات يمكن أن يسبب خسائر اقتصادية كبيرة لمربي الدواجن.[215][216][217][218]
إن سلالة فيروس H5N1، التي تتكيف مع الطيور، شديدة الإمراض، وتسمى HPAI H5N1، "فيروس إنفلونزا الطيور شديد العدوى من النوع أ من النوع الفرعي H5N1" المعروف باسم "إنفلونزا الطيور" وهو متوطن في العديد من الطيور، وخاصة في جنوب شرق آسيا. سلالة النسب الآسيوية من HPAI H5N1 منتشر على الصعيد العالمي. وهو مرض إبيزوتي (وباء في غير البشر) و بانزوتيك (مرض يؤثر على الحيوانات في العديد من الأنواع، وخاصة على مساحة واسعة)، مما أسفر عن مقتل عشرات الملايين من الطيور وتحفيز إعدام مئات الملايين من الطيور الأخرى في محاولة للسيطرة على انتشاره. معظم الإشارات في وسائل الإعلام إلى "انفلونزا الطيور" ومعظم الإشارات إلى H5N1 هي حول هذه السلالة المحددة.[219][220]
وفي الوقت الحاضر، فإن مرض إنفلونزا الطيور H-H1N A5 هو مرض طيور، وليس هناك أي دليل يشير إلى انتقال فيروس HPAI H5N1 الفعال من إنسان إلى إنسان. في جميع الحالات تقريبا، كان المصابون لديهم اتصال جسدي واسع النطاق مع الطيور المصابة. وفي المستقبل، قد يتحول الفيروس H5N1 أو ينتقل إلى سلالة قادرة على انتقال الفيروس من إنسان إلى آخر. التغييرات الدقيقة المطلوبة لتحقيق ذلك ليست مفهومة جيدا. ومع ذلك، وبسبب الفتك القوى من H5N1، وجوده المتوطن، وخزان المضيف البيولوجي الكبير والمتزارع، كان فيروس H5N1 هو تهديد العالم للجائحة في موسم الإنفلونزا 2006-2007، ويجري جمع مليارات الدولارات وإنفاقها لإجراء أبحاث عن H5N1 والتحضير لوباء إنفلونزا محتمل.[200][221][222]
في مارس 2013، أبلغت الحكومة الصينية عن ثلاث حالات من عدوى الأنفلونزا H7N9 في البشر. توفي اثنان منهم والثالث كان مريضا للغاية. على الرغم من أن سلالة الفيروس لا يعتقد أنها تنتشر بكفاءة بين البشر، بحلول منتصف أبريل، ما لا يقل عن 82 شخصا قد أصيبوا بالمرض من H7N9، منهم 17 قد توفوا. وتشمل هذه الحالات ثلاث مجموعات عائلية صغيرة في شنغهاي، ومجموعة واحدة بين فتاة وصبي مجاور في بيجين، مما يرفع احتمال انتقال الفيروس من إنسان إلى آخر على الأقل. وتشير منظمة الصحة العالمية إلى أن مجموعة واحدة لم يكن لديها اثنان من مختبرات الحالات المؤكدة، وتشير كذلك، كمعلومات أساسية، إلى أن بعض الفيروسات قادرة على إحداث انتقال محدود من إنسان إلى إنسان في ظل ظروف اتصال وثيق ولكنها ليست قابلة للانتقال وهو ما يكفي لتسبب تفشي كبير في المجتمعات.[223][224][225][226]
انفلونزا الخنازير
تنتج أنفلونزا الخنازير الحمى والخمول والعطس والسعال وصعوبة في التنفس وانخفاض الشهية. في بعض الحالات يمكن أن يسبب العدوى الإجهاض. وعلى الرغم من أن معدل الوفيات منخفض عادة، إلا أن الفيروس يمكن أن يؤدي إلى فقدان الوزن وضعف النمو، مما يسبب خسارة اقتصادية للمزارعين. الخنازير المصابة يمكن أن تفقد ما يصل إلى 12 رطلا من وزن الجسم على مدى 3-4 أسابيع. من الممكن أحيانا نقل فيروس الأنفلونزا من الخنازير إلى البشر مباشرة (وهذا ما يسمى انفلونزا الخنازير الحيوانية المنشأ). من المعروف أن 50 حالة إنسانية قد حدثت منذ اكتشاف الفيروس في منتصف القرن العشرين، مما أدى إلى وفاة ستة أشخاص.[227][228]
في عام 2009، تسببت سلالة فيروس H1N1 من أصل الخنازير التي يشار إليها عادة باسم "انفلونزا الخنازير" في وباء إنفلونزا 2009، ولكن لا يوجد دليل على أنه متوطن للخنازير أى انتقال الفيروس من الخنازير إلى الناس، بدلا من ذلك قد ينتشر الفيروس من شخص لآخر. هذه السلالة هي إعادة تكوين عدة سلالات من H1N1 التي عادة ما توجد بشكل منفصل، في البشر والطيور والخنازير.[229][230][231]
مراجع
- معرف أنطولوجية المرض: http://www.disease-ontology.org/?id=DOID:8469 — تاريخ الاطلاع: 15 مايو 2019 — الاصدار 2019-05-13
- "Influenza (Seasonal) Fact sheet N°211". who.int. March 201425 نوفمبر 2014. نسخة محفوظة 21 أبريل 2018 على موقع واي باك مشين.
- "Key Facts about Influenza (Flu) & Flu Vaccine". cdc.gov. 9 September 201426 نوفمبر 2014. نسخة محفوظة 28 أبريل 2019 على موقع واي باك مشين.
- Duben-Engelkirk، Paul G. Engelkirk, Janet (2011). Burton's microbiology for the health sciences (الطبعة 9th). Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. صفحة 314. ISBN . نسخة محفوظة 03 ديسمبر 2016 على موقع واي باك مشين.
- Longo، Dan L. (2012). "187: Influenza". Harrison's principles of internal medicine. (الطبعة 18th). New York: McGraw-Hill. ISBN .
- Brankston G، Gitterman L، Hirji Z، Lemieux C، Gardam M (April 2007). "Transmission of influenza A in human beings". Lancet Infect Dis. 7 (4): 257–65. PMID 17376383. doi:10.1016/S1473-3099(07)70029-4. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Michiels، B؛ Van Puyenbroeck, K؛ Verhoeven, V؛ Vermeire, E؛ Coenen, S (2013). "The value of neuraminidase inhibitors for the prevention and treatment of seasonal influenza: a systematic review of systematic reviews.". PLoS ONE. 8 (4): e60348. PMC 3614893
 . PMID 23565231. doi:10.1371/journal.pone.0060348. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
. PMID 23565231. doi:10.1371/journal.pone.0060348. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Jefferson T، Del Mar CB، Dooley L، وآخرون. (2011). "Physical interventions to interrupt or reduce the spread of respiratory viruses". Cochrane Database Syst Rev (7): CD006207. PMID 21735402. doi:10.1002/14651858.CD006207.pub4. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Ebell، MH؛ Call, M؛ Shinholser, J (April 2013). "Effectiveness of oseltamivir in adults: a meta-analysis of published and unpublished clinical trials.". Family practice. 30 (2): 125–33. PMID 22997224. doi:10.1093/fampra/cms059. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- "Ten things you need to know about pandemic influenza". World Health Organization. 14 October 2005. تمت أرشفته من الأصل في 8 October 200926 سبتمبر 2009. نسخة محفوظة 02 سبتمبر 2011 على موقع واي باك مشين.
- World Health Organization. World now at the start of 2009 influenza pandemic. http://www.who.int/mediacentre/news/statements/2009/h1n1_pandemic_phase6_20090611/en/index.html
- Palmer، S. R. (2011). Oxford textbook of zoonoses : biology, clinical practice, and public health control (الطبعة 2.). Oxford u.a.: Oxford Univ. Press. صفحة 332. ISBN . نسخة محفوظة 03 ديسمبر 2016 على موقع واي باك مشين.
- Centers for Disease Control and Prevention > Influenza Symptoms Page last updated 16 November 2007. Retrieved 28 April 2009. نسخة محفوظة 18 ديسمبر 2016 على موقع واي باك مشين.
- Call S، Vollenweider M، Hornung C، Simel D، McKinney W (2005). "Does this patient have influenza?". JAMA. 293 (8): 987–97. PMID 15728170. doi:10.1001/jama.293.8.987. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Time Lines of Infection and Disease in Human Influenza: A Review of Volunteer Challenge Studies, American Journal of Epidemiology, Carrat, Vergu, Ferguson, et al., 167 (7): 775–785, 2008. "... In almost all studies, participants were individually confined for 1 week ..." See especially Figure 5 which shows that virus shedding tends to peak on day 2 whereas symptoms tend to peak on day 3. نسخة محفوظة 18 أكتوبر 2015 على موقع واي باك مشين.
- Suzuki E، Ichihara K، Johnson AM (January 2007). "Natural course of fever during influenza virus infection in children". Clin Pediatr (Phila). 46 (1): 76–9. PMID 17164515. doi:10.1177/0009922806289588. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- "Influenza: Viral Infections: Merck Manual Home Edition". Merck15 مارس 2008. نسخة محفوظة 05 نوفمبر 2010 على موقع واي باك مشين.
- Silva ME، Cherry JD، Wilton RJ، Ghafouri NM، Bruckner DA، Miller MJ (August 1999). "Acute fever and petechial rash associated with influenza A virus infection". Clinical Infectious Diseases. 29 (2): 453–4. PMID 10476766. doi:10.1086/520240. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Kerr AA، McQuillin J، Downham MA، Gardner PS (1975). "Gastric 'flu influenza B causing abdominal symptoms in children". Lancet. 1 (7902): 291–5. PMID 46444. doi:10.1016/S0140-6736(75)91205-2. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Richards S (2005). "Flu blues". Nurs Stand. 20 (8): 26–7. PMID 16295596. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Heikkinen T (July 2006). "Influenza in children". Acta Paediatr. 95 (7): 778–84. PMID 16801171. doi:10.1080/08035250600612272. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Hui DS (March 2008). "Review of clinical symptoms and spectrum in humans with influenza A/H5N1 infection". Respirology. 13 Suppl 1: S10–3. PMID 18366521. doi:10.1111/j.1440-1843.2008.01247.x. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Eccles، R (2005). "Understanding the symptoms of the common cold and influenza". Lancet Infect Dis. 5 (11): 718–25. PMID 16253889. doi:10.1016/S1473-3099(05)70270-X. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Rothberg M، Bellantonio S، Rose D (2 September 2003). "Management of influenza in adults older than 65 years of age: cost-effectiveness of rapid testing and antiviral therapy" (PDF). Annals of Internal Medicine. 139 (5 Pt 1): 321–9. PMID 12965940. doi:10.7326/0003-4819-139-5_part_1-200309020-00007. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Smith K، Roberts M (2002). "Cost-effectiveness of newer treatment strategies for influenza". Am J Med. 113 (4): 300–7. PMID 12361816. doi:10.1016/S0002-9343(02)01222-6. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Monto A، Gravenstein S، Elliott M، Colopy M، Schweinle J (2000). "Clinical signs and symptoms predicting influenza infection" (PDF). Arch Intern Med. 160 (21): 3243–7. PMID 11088084. doi:10.1001/archinte.160.21.3243. نسخة محفوظة 02 أبريل 2012 على موقع واي باك مشين.
- "Rapid Diagnostic Testing for Influenza: Information for Clinical Laboratory Directors". مراكز مكافحة الأمراض واتقائها. 13 October 201502 فبراير 2016. نسخة محفوظة 06 أبريل 2019 على موقع واي باك مشين.
- Centers for Disease Control and Prevention. Lab Diagnosis of Influenza. Retrieved 1 May 2009 نسخة محفوظة 17 ديسمبر 2017 على موقع واي باك مشين.
- Report Finds Swine Flu Has Killed 36 Children, New York Times, DENISE GRADY, 3 September 2009. نسخة محفوظة 27 يونيو 2017 على موقع واي باك مشين.
- Transcript of virtual press conference with Gregory Hartl, Spokesperson for H1N1, and Dr Nikki Shindo, Medical Officer, Global Influenza Programme, World Health Organization, 12 November 2009. نسخة محفوظة 16 أكتوبر 2012 على موقع واي باك مشين.
- Hospitalized Patients with 2009 H1N1 Influenza in the United States, April–June 2009, New England Journal of Medicine, Jain, Kamimoto, et al., 12 November 2009. نسخة محفوظة 04 سبتمبر 2017 على موقع واي باك مشين.
- Kawaoka Y (editor) (2006). Influenza Virology: Current Topics. Caister Academic Press. ISBN . نسخة محفوظة 06 أكتوبر 2016 على موقع واي باك مشين.
- Hall CB (June 2001). "Respiratory syncytial virus and parainfluenza virus". N. Engl. J. Med. 344 (25): 1917–28. PMID 11419430. doi:10.1056/NEJM200106213442507. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Vainionpää R، Hyypiä T (April 1994). "Biology of parainfluenza viruses". Clin. Microbiol. Rev. 7 (2): 265–75. PMC 358320
 . PMID 8055470. doi:10.1128/CMR.7.2.265. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
. PMID 8055470. doi:10.1128/CMR.7.2.265. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Hause BM، Collin EA، Liu R، Huang B، Sheng Z، Lu W، Wang D، Nelson EA، Li F (2014). "Characterization of a novel influenza virus in cattle and swine: proposal for a new genus in the Orthomyxoviridae family". MBio. 5 (2): e00031–14. doi:10.1128/mBio.00031-14. نسخة محفوظة 4 أبريل 2020 على موقع واي باك مشين.
- Collin EA، Sheng Z، Lang Y، Ma W، Hause BM، Li F (2015). "Cocirculation of two distinct genetic and antigenic lineages of proposed influenza D virus in cattle". J Virol. 89 (2): 1036–1042. PMC 4300623
 . PMID 25355894. doi:10.1128/JVI.02718-14. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
. PMID 25355894. doi:10.1128/JVI.02718-14. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Ducatez MF، Pelletier C، Meyer G (2015). "Influenza D virus in cattle, France, 2011-2014". Emerg Infect Dis. 21 (2): 368–371. doi:10.3201/eid2102.141449. نسخة محفوظة 12 أكتوبر 2019 على موقع واي باك مشين.
- Song H، Qi J، Khedri Z، Diaz S، Yu H، Chen X، Varki A، Shi Y، Gao GF (2016). "An open receptor-binding cavity of hemagglutinin-esterase-fusion glycoprotein from newly-identified Influenza D Virus: Basis for its broad cell tropism". PLoS Pathog. 12 (1): e1005411. doi:10.1371/journal.ppat.1005411. نسخة محفوظة 6 أبريل 2020 على موقع واي باك مشين.
- Sheng Z، Ran Z، Wang D، Hoppe AD، Simonson R، Chakravarty S، Hause BM، Li F (2014). "Genomic and evolutionary characterization of a novel influenza-C-like virus from swine". Arch Virol. 159 (2): 249–255. doi:10.1007/s00705-013-1815-3. نسخة محفوظة 20 أكتوبر 2019 على موقع واي باك مشين.
- Quast M، Sreenivasan C، Sexton G، Nedland H، Singrey A، Fawcett L، Miller G، Lauer D، Voss S، Pollock S، Cunha CW، Christopher-Hennings J، Nelson E، Li F (2015). "Serological evidence for the presence of influenza D virus in small ruminants". Vet Microbiol. 180 (3–4): 281–285. doi:10.1016/j.vetmic.2015.09.005. نسخة محفوظة 4 أبريل 2020 على موقع واي باك مشين.
- Smith DB، Gaunt ER، Digard P، Templeton K، Simmonds P (2016). "Detection of influenza C virus but not influenza D virus in Scottish respiratory samples". J Clin Virol. 74: 50–53. doi:10.1016/j.jcv.2015.11.036.
- Hay، A؛ Gregory V؛ Douglas A؛ Lin Y (29 December 2001). "The evolution of human influenza viruses". Philosophical Transactions of the Royal Society B. 356 (1416): 1861–70. PMC 1088562
 . PMID 11779385. doi:10.1098/rstb.2001.0999. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
. PMID 11779385. doi:10.1098/rstb.2001.0999. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Klenk, Hans-Dieter؛ Matrosovich, Mikhail؛ Stech, Jürgen (2008). "Avian Influenza: Molecular Mechanisms of Pathogenesis and Host Range". Animal Viruses: Molecular Biology. Caister Academic Press. ISBN . نسخة محفوظة 20 أغسطس 2016 على موقع واي باك مشين.
- Fouchier، RAM؛ Schneeberger، PM؛ Rozendaal، FW؛ Broekman، JM؛ Kemink، SA؛ Munster، V؛ Kuiken، T؛ Rimmelzwaan، GF؛ وآخرون. (2004). "Avian influenza A virus (H7N7) associated with human conjunctivitis and a fatal case of acute respiratory distress syndrome" (PDF). Proceedings of the National Academy of Sciences. 101 (5): 1356–61. Bibcode:2004PNAS..101.1356F. PMC 337057
 . PMID 14745020. doi:10.1073/pnas.0308352100. نسخة محفوظة 25 يناير 2016 على موقع واي باك مشين.
. PMID 14745020. doi:10.1073/pnas.0308352100. نسخة محفوظة 25 يناير 2016 على موقع واي باك مشين.
- Zambon، M (November 1999). "Epidemiology and pathogenesis of influenza" (PDF). J Antimicrob Chemother. 44 Suppl B (90002): 3–9. PMID 10877456. doi:10.1093/jac/44.suppl_2.3. نسخة محفوظة 31 مايو 2013 على موقع واي باك مشين.
- R، Webster؛ Bean W؛ Gorman O؛ Chambers T؛ Kawaoka Y (1992). "Evolution and ecology of influenza A viruses". Microbiol Rev. 56 (1): 152–79. PMC 372859
 . PMID 1579108. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
. PMID 1579108. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Jakeman KJ، Tisdale M، Russell S، Leone A، Sweet C (August 1994). "Efficacy of 2'-deoxy-2'-fluororibosides against influenza A and B viruses in ferrets". Antimicrob. Agents Chemother. 38 (8): 1864–7. PMC 284652
 . PMID 7986023. doi:10.1128/aac.38.8.1864. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
. PMID 7986023. doi:10.1128/aac.38.8.1864. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Osterhaus، A؛ Rimmelzwaan G؛ Martina B؛ Bestebroer T؛ Fouchier R (2000). "Influenza B virus in seals". Science. 288 (5468): 1051–3. Bibcode:2000Sci...288.1051O. PMID 10807575. doi:10.1126/science.288.5468.1051. نسخة محفوظة 02 سبتمبر 2017 على موقع واي باك مشين.
- Nobusawa، E؛ Sato K (April 2006). "Comparison of the mutation rates of human influenza A and B viruses". J Virol. 80 (7): 3675–8. PMC 1440390
 . PMID 16537638. doi:10.1128/JVI.80.7.3675-3678.2006. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
. PMID 16537638. doi:10.1128/JVI.80.7.3675-3678.2006. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Matsuzaki، Y؛ Katsushima N؛ Nagai Y؛ Shoji M؛ Itagaki T؛ Sakamoto M؛ Kitaoka S؛ Mizuta K؛ Nishimura H (1 May 2006). "Clinical features of influenza C virus infection in children". J Infect Dis. 193 (9): 1229–35. PMID 16586359. doi:10.1086/502973. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Katagiri، S؛ Ohizumi A؛ Homma M (July 1983). "An outbreak of type C influenza in a children's home". J Infect Dis. 148 (1): 51–6. PMID 6309999. doi:10.1093/infdis/148.1.51. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Taubenberger, JK; Morens, DM (2008). "The pathology of influenza virus infections". Annu Rev Pathol. 3: 499–522. doi:10.1146/annurev.pathmechdis.3.121806.154316. PMC . PMID 18039138.
- Matsuzaki، Y؛ Sugawara K؛ Mizuta K؛ Tsuchiya E؛ Muraki Y؛ Hongo S؛ Suzuki H؛ Nakamura K (2002). "Antigenic and genetic characterization of influenza C viruses which caused two outbreaks in Yamagata City, Japan, in 1996 and 1998". J Clin Microbiol. 40 (2): 422–9. PMC 153379
 . PMID 11825952. doi:10.1128/JCM.40.2.422-429.2002. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
. PMID 11825952. doi:10.1128/JCM.40.2.422-429.2002. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- International Committee on Taxonomy of Viruses. "The Universal Virus Database, version 4: Influenza A". تمت أرشفته من الأصل في 14 October 2006. نسخة محفوظة 07 مارس 2010 على موقع واي باك مشين.
- Lamb RA، Choppin PW (1983). "The gene structure and replication of influenza virus". Annu. Rev. Biochem. 52: 467–506. PMID 6351727. doi:10.1146/annurev.bi.52.070183.002343. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Bouvier NM, Palese P (September 2008). "The biology of influenza viruses". Vaccine. 26 Suppl 4: D49–53. doi:10.1016/j.vaccine.2008.07.039. PMC . PMID 19230160.
- International Committee on Taxonomy of Viruses descriptions of:Orthomyxoviridae,Influenzavirus B and Influenzavirus C
- Ghedin، E؛ Sengamalay، NA؛ Shumway، M؛ Zaborsky، J؛ Feldblyum، T؛ Subbu، V؛ Spiro، DJ؛ Sitz، J؛ وآخرون. (October 2005). "Large-scale sequencing of human influenza reveals the dynamic nature of viral genome evolution". نيتشر (مجلة). 437 (7062): 1162–6. Bibcode:2005Natur.437.1162G. PMID 16208317. doi:10.1038/nature04239. نسخة محفوظة 23 أكتوبر 2018 على موقع واي باك مشين.
- Lynch JP، Walsh EE (April 2007). "Influenza: evolving strategies in treatment and prevention". Semin Respir Crit Care Med. 28 (2): 144–58. PMID 17458769. doi:10.1055/s-2007-976487. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Wilson، J؛ von Itzstein M (July 2003). "Recent strategies in the search for new anti-influenza therapies". Curr Drug Targets. 4 (5): 389–408. PMID 12816348. doi:10.2174/1389450033491019. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Hilleman, M (19 August 2002). "Realities and enigmas of human viral influenza: pathogenesis, epidemiology and control". Vaccine. 20 (25–26): 3068–87. doi:10.1016/S0264-410X(02)00254-2. PMID 12163258.
- Suzuki، Y (2005). "Sialobiology of influenza: molecular mechanism of host range variation of influenza viruses". Biol Pharm Bull. 28 (3): 399–408. PMID 15744059. doi:10.1248/bpb.28.399. نسخة محفوظة 05 2يناير9 على موقع واي باك مشين.
- Smith AE, Helenius A (April 2004). "How viruses enter animal cells". Science. 304 (5668): 237–42. Bibcode:2004Sci...304..237S. doi:10.1126/science.1094823. PMID 15073366.
- Steinhauer DA (May 1999). "Role of hemagglutinin cleavage for the pathogenicity of influenza virus". Virology. 258 (1): 1–20. doi:10.1006/viro.1999.9716. PMID 10329563.
- Wagner, R; Matrosovich M; Klenk H (May–June 2002). "Functional balance between haemagglutinin and neuraminidase in influenza virus infections". Rev Med Virol. 12 (3): 159–66. doi:10.1002/rmv.352. PMID 11987141.
- Pinto LH, Lamb RA (April 2006). "The M2 proton channels of influenza A and B viruses". J. Biol. Chem. 281 (14): 8997–9000. doi:10.1074/jbc.R500020200. PMID 16407184.
- Lakadamyali, M; Rust M; Babcock H; Zhuang X (5 August 2003). "Visualizing infection of individual influenza viruses". Proc Natl Acad Sci USA. 100 (16): 9280–5. Bibcode:2003PNAS..100.9280L. doi:10.1073/pnas.0832269100. PMC . PMID 12883000.
- Kash, J; Goodman A; Korth M; Katze M (July 2006). "Hijacking of the host-cell response and translational control during influenza virus infection". Virus Res. 119 (1): 111–20. doi:10.1016/j.virusres.2005.10.013. PMID 16630668.
- Cros, J; Palese P (September 2003). "Trafficking of viral genomic RNA into and out of the nucleus: influenza, Thogoto and Borna disease viruses". Virus Res. 95 (1–2): 3–12. doi:10.1016/S0168-1702(03)00159-X. PMID 12921991.
- Nayak, D; Hui E; Barman S (December 2004). "Assembly and budding of influenza virus". Virus Res. 106 (2): 147–65. doi:10.1016/j.virusres.2004.08.012. PMID 15567494.
- Drake, J (1 May 1993). "Rates of spontaneous mutation among RNA viruses". Proc Natl Acad Sci USA. 90 (9): 4171–5. Bibcode:1993PNAS...90.4171D. doi:10.1073/pnas.90.9.4171. PMC . PMID 8387212.
- Gooskens, Jairo; Jonges, Marcel; Claas, Eric C. J.; Meijer, Adam; Kroes, Aloys C. M. (15 May 2009). "Prolonged Influenza Virus Infection during Lymphocytopenia and Frequent Detection of Drug‐Resistant Viruses". The Journal of Infectious Diseases. 199 (10): 1435–1441. doi:10.1086/598684. PMID 19392620.
- Carrat, F.; Vergu, E.; Ferguson, N. M.; Lemaitre, M.; Cauchemez, S.; Leach, S.; Valleron, A.-J. (14 March 2008). "Time Lines of Infection and Disease in Human Influenza: A Review of Volunteer Challenge Studies". American Journal of Epidemiology. 167 (7): 775–785. doi:10.1093/aje/kwm375. PMID 18230677.
- Mitamura K, Sugaya N (2006). "[Diagnosis and Treatment of influenza—clinical investigation on ذرف الفيروس in children with influenza]". Uirusu. 56 (1): 109–16. doi:10.2222/jsv.56.109. PMID 17038819.
- Sherman, Irwin W. (2007). Twelve diseases that changed our world. Washington, DC: ASM Press. صفحة 161. .
- Weber TP, Stilianakis NI (November 2008). "Inactivation of influenza A viruses in the environment and modes of transmission: a critical review". J. Infect. 57 (5): 361–73. doi:10.1016/j.jinf.2008.08.013. PMID 18848358.
- Cole E, Cook C (1998). "Characterization of infectious aerosols in health care facilities: an aid to effective engineering controls and preventive strategies". Am J Infect Control. 26 (4): 453–64. doi:10.1016/S0196-6553(98)70046-X. PMID 9721404.
- Hall CB (August 2007). "The spread of influenza and other respiratory viruses: complexities and conjectures" ( كتاب إلكتروني PDF ). Clin. Infect. Dis. 45 (3): 353–9. doi:10.1086/519433. PMID 17599315. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 25 يناير 2016.
- "Influenza Factsheet" ( كتاب إلكتروني PDF ). Center for Food Security and Public Health, Iowa State University. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 02 مايو 2019. p. 7
- Thomas Y, Vogel G, Wunderli W, et al. (May 2008). "Survival of influenza virus on banknotes". Appl. Environ. Microbiol. 74 (10): 3002–7. doi:10.1128/AEM.00076-08. PMC . PMID 18359825.
- Bean B, Moore BM, Sterner B, Peterson LR, Gerding DN, Balfour HH (July 1982). "Survival of influenza viruses on environmental surfaces". J. Infect. Dis. 146 (1): 47–51. doi:10.1093/infdis/146.1.47. PMID 6282993.
- Korteweg C, Gu J (May 2008). "Pathology, molecular biology, and pathogenesis of avian influenza A (H5N1) infection in humans". Am. J. Pathol. 172 (5): 1155–70. doi:10.2353/ajpath.2008.070791. PMC . PMID 18403604.
- Jefferies WM, Turner JC, Lobo M, Gwaltney JM (1998). "Low plasma levels of adrenocorticotropic hormone in patients with acute influenza" ( كتاب إلكتروني PDF ). Clin Infect Dis. 26 (3): 708–10. doi:10.1086/514594. PMID 9524849. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 25 يناير 2016.
- Shinya K, Ebina M, Yamada S, Ono M, Kasai N, Kawaoka Y (March 2006). "Avian flu: influenza virus receptors in the human airway". Nature. 440 (7083): 435–6. Bibcode:2006Natur.440..435S. doi:10.1038/440435a. PMID 16554799.
- van Riel D, Munster VJ, de Wit E, et al. (October 2007). "Human and avian influenza viruses target different cells in the lower respiratory tract of humans and other mammals". Am. J. Pathol. 171 (4): 1215–23. doi:10.2353/ajpath.2007.070248. PMC . PMID 17717141.
- van Riel D, Munster VJ, de Wit E, et al. (April 2006). "H5N1 Virus Attachment to Lower Respiratory Tract". Science. 312 (5772): 399. doi:10.1126/science.1125548. PMID 16556800.
- Nicholls JM, Chan RW, Russell RJ, Air GM, Peiris JS (April 2008). "Evolving complexities of influenza virus and its receptors". Trends Microbiol. 16 (4): 149–57. doi:10.1016/j.tim.2008.01.008. PMID 18375125.
- Beigel J, Bray M (April 2008). "Current and future antiviral therapy of severe seasonal and avian influenza". Antiviral Res. 78 (1): 91–102. doi:10.1016/j.antiviral.2008.01.003. PMC . PMID 18328578.
- Kash JC, Tumpey TM, Proll SC, et al. (October 2006). "Genomic analysis of increased host immune and cell death responses induced by 1918 influenza virus". Nature. 443 (7111): 578–81. Bibcode:2006Natur.443..578K. doi:10.1038/nature05181. PMC . PMID 17006449.
- Kobasa D, Jones SM, Shinya K, et al. (January 2007). "Aberrant innate immune response in lethal infection of macaques with the 1918 influenza virus". Nature. 445 (7125): 319–23. Bibcode:2007Natur.445..319K. doi:10.1038/nature05495. PMID 17230189.
- Cheung CY, Poon LL, Lau AS, et al. (December 2002). "Induction of proinflammatory cytokines in human macrophages by influenza A (H5N1) viruses: a mechanism for the unusual severity of human disease?". Lancet. 360 (9348): 1831–7. doi:10.1016/S0140-6736(02)11772-7. PMID 12480361.
- Schmitz N, Kurrer M, Bachmann M, Kopf M (2005). "Interleukin-1 is responsible for acute lung immunopathology but increases survival of respiratory influenza virus infection". J Virol. 79 (10): 6441–8. doi:10.1128/JVI.79.10.6441-6448.2005. PMC . PMID 15858027.
- Winther B, Gwaltney J, Mygind N, Hendley J (1998). "Viral-induced rhinitis". Am J Rhinol. 12 (1): 17–20. doi:10.2500/105065898782102954. PMID 9513654.
- "Vaccine use". World Health Organization. مؤرشف من الأصل في 18 أبريل 201906 ديسمبر 2012.
- Smith NM, Bresee JS, Shay DK, Uyeki TM, Cox NJ, Strikas RA (July 2006). "Prevention and Control of Influenza: recommendations of the Advisory Committee on Immunization Practices (ACIP)" ( كتاب إلكتروني PDF ). MMWR Recomm Rep. 55 (RR–10): 1–42. PMID 16874296. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 2 مايو 2019.
- Cates, CJ; Rowe, BH (28 February 2013). "Vaccines for preventing influenza in people with asthma". The Cochrane database of systematic reviews. 2: CD000364. doi:10.1002/14651858.CD000364.pub4. PMID 23450529.
- Jefferson T, Rivetti A, Di Pietrantonj C, Demicheli V, Ferroni E (2012). "Vaccines for preventing influenza in healthy children". Cochrane Database Syst Rev. 8: CD004879. doi:10.1002/14651858.CD004879.pub4. PMID 22895945.
- Jefferson, T; Di Pietrantonj, C; Rivetti, A; Bawazeer, GA; Al-Ansary, LA; Ferroni, E (13 March 2014). "Vaccines for preventing influenza in healthy adults". The Cochrane database of systematic reviews. 3: CD001269. doi:10.1002/14651858.CD001269.pub5. PMID 24623315.
- Thomas, RE; Jefferson, T; Lasserson, TJ (22 July 2013). "Influenza vaccination for healthcare workers who care for people aged 60 or older living in long-term care institutions". The Cochrane database of systematic reviews. 7: CD005187. doi:10.1002/14651858.CD005187.pub4. PMID 23881655.
- Ahmed, F; Lindley, MC; Allred, N; Weinbaum, CM; Grohskopf, L (13 November 2013). "Effect of Influenza Vaccination of Healthcare Personnel on Morbidity and Mortality Among Patients: Systematic Review and Grading of Evidence". Clinical Infectious Diseases. 58 (1): 50–7. doi:10.1093/cid/cit580. PMID 24046301.
- Dolan, GP; Harris, RC; Clarkson, M; Sokal, R; Morgan, G; Mukaigawara, M; Horiuchi, H; Hale, R; Stormont, L; Béchard-Evans, L; Chao, YS; Eremin, S; Martins, S; Tam, J; Peñalver, J; Zanuzadana, A; Nguyen-Van-Tam, JS (September 2013). "Vaccination of healthcare workers to protect patients at increased risk of acute respiratory disease: summary of a systematic review". Influenza and other respiratory viruses. 7 Suppl 2: 93–6. doi:10.1111/irv.12087. PMID 24034492.
- Beck, CR; McKenzie, BC; Hashim, AB; Harris, RC; University of Nottingham Influenza and the ImmunoCompromised (UNIIC) Study Group; Nguyen-Van-Tam, JS (October 2012). "Influenza vaccination for immunocompromised patients: systematic review and meta-analysis by etiology". The Journal of Infectious Diseases. 206 (8): 1250–9. doi:10.1093/infdis/jis487. PMID 22904335.
- Udell, JA.; Zawi, R.; Bhatt, DL.; Keshtkar-Jahromi, M.; Gaughran, F.; Phrommintikul, A.; Ciszewski, A.; Vakili, H.; et al. (Oct 2013). "Association between influenza vaccination and cardiovascular outcomes in high-risk patients: a meta-analysis". JAMA. 310 (16): 1711–20. doi:10.1001/jama.2013.279206. PMID 24150467.
- Poole PJ, Chacko E, Wood-Baker RW, Cates CJ (2006). "Influenza vaccine for patients with chronic obstructive pulmonary disease". Cochrane Database Syst Rev (1): CD002733. doi:10.1002/14651858.CD002733.pub2. PMID 16437444.
- Abramson ZH (2012). "What, in Fact, Is the Evidence That Vaccinating Healthcare Workers against Seasonal Influenza Protects Their Patients? A Critical Review". Int J Family Med. 2012: 205464. doi:10.1155/2012/205464. PMC . PMID 23209901.
- Key Facts about Influenza (Flu) Vaccine CDC publication. Published 17 October 2006. Retrieved 18 October 2006. نسخة محفوظة 28 فبراير 2018 على موقع واي باك مشين.
- Holmes E, Ghedin E, Miller N, Taylor J, Bao Y, St George K, Grenfell B, Salzberg S, Fraser C, Lipman D, Taubenberger J (September 2005). "Whole-genome analysis of human influenza A virus reveals multiple persistent lineages and reassortment among recent H3N2 viruses". PLoS Biol. 3 (9): e300. doi:10.1371/journal.pbio.0030300. PMC . PMID 16026181.
- "Recommended composition of influenza virus vaccines for use in the 2006–2007 influenza season" ( كتاب إلكتروني PDF ). WHO Report. 14 February 2006. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 14 أبريل 201628 ديسمبر 2016.
- Questions & Answers: Flu Shot CDC publication updated 24 July 2006. Retrieved 19 October 2006. نسخة محفوظة 28 فبراير 2018 على موقع واي باك مشين.
- Newall, Anthony T.; Dehollain, Juan Pablo; Creighton, Prudence; Beutels, Philippe; Wood, James G. (4 May 2013). "Understanding the Cost-Effectiveness of Influenza Vaccination in Children: Methodological Choices and Seasonal Variability". PharmacoEconomics. 31 (8): 693–702. doi:10.1007/s40273-013-0060-7. PMID 23645539.
- Newall, Anthony T.; Kelly, Heath; Harsley, Stuart; Scuffham, Paul A. (1 June 2009). "Cost Effectiveness of Influenza Vaccination in Older Adults". PharmacoEconomics. 27 (6): 439–450. doi:10.2165/00019053-200927060-00001. PMID 19640008.
- Jit, Mark; Newall, Anthony T.; Beutels, Philippe (1 April 2013). "Key issues for estimating the impact and cost-effectiveness of seasonal influenza vaccination strategies". Human vaccines & immunotherapeutics. 9 (4): 834–840. doi:10.4161/hv.23637. PMC . PMID 23357859.
- Postma, Maarten J; Baltussen, Rob PM; Palache, Abraham M; Wilschut, Jan C (1 April 2006). "Further evidence for favorable cost-effectiveness of elderly influenza vaccination". Expert Review of Pharmacoeconomics & Outcomes Research. 6 (2): 215–227. doi:10.1586/14737167.6.2.215. PMID 20528557.
- Newall, Anthony T.; Jit, Mark; Beutels, Philippe (1 August 2012). "Economic Evaluations of Childhood Influenza Vaccination". PharmacoEconomics. 30 (8): 647–660. doi:10.2165/11599130-000000000-00000. PMID 22788257.
- Interim Guidance for the Use of Masks to Control Influenza Transmission Coordinating Center for Infectious Diseases (CCID) 8 August 2005 نسخة محفوظة 21 فبراير 2018 على موقع واي باك مشين.
- Grayson ML, Melvani S, Druce J, et al. (February 2009). "Efficacy of soap and water and alcohol-based hand-rub preparations against live H1N1 influenza virus on the hands of human volunteers". Clin. Infect. Dis. 48 (3): 285–91. doi:10.1086/595845. PMID 19115974.
- Aledort JE, Lurie N, Wasserman J, Bozzette SA (2007). "Non-pharmaceutical public health interventions for pandemic influenza: an evaluation of the evidence base". BMC Public Health. 7: 208. doi:10.1186/1471-2458-7-208. PMC . PMID 17697389.
- Murin, Susan; Kathryn Smith Bilello (2005). "Respiratory tract infections: another reason not to smoke". Cleveland Clinic Journal of Medicine. 72 (10): 916–920. doi:10.3949/ccjm.72.10.916. PMID 16231688.
- Kark, J D; M Lebiush; L Rannon (1982). "Cigarette smoking as a risk factor for epidemic a(h1n1) influenza in young men". The New England Journal of Medicine. 307 (17): 1042–1046. doi:10.1056/NEJM198210213071702. ISSN 0028-4793. PMID 7121513.
- Bridges CB, Kuehnert MJ, Hall CB (October 2003). "Transmission of influenza: implications for control in health care settings". Clin. Infect. Dis. 37 (8): 1094–101. doi:10.1086/378292. PMID 14523774.
- MacIntyre CR, Cauchemez S, Dwyer DE, et al. (February 2009). "Face mask use and control of respiratory virus transmission in households" ( كتاب إلكتروني PDF ). Emerging Infect. Dis. 15 (2): 233–41. doi:10.3201/eid1502.081167. PMC . PMID 19193267. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 15 يوليو 2011.
- Centers for Disease Control and Prevention: "QUESTIONS & ANSWERS: Novel H1N1 Flu (Swine Flu) and You". Retrieved 15 December 2009. نسخة محفوظة 22 فبراير 2018 على موقع واي باك مشين.
- "Chlorine Bleach: Helping to Manage the Flu Risk". Water Quality & Health Council. April 2009. مؤرشف من الأصل في 03 مايو 201912 مايو 2009.
- McDonnell G, Russell A (1 January 1999). "Antiseptics and disinfectants: activity, action, and resistance" ( كتاب إلكتروني PDF ). Clin Microbiol Rev. 12 (1): 147–79. PMC . PMID 9880479. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 25 يوليو 2011.
- Hota B; Hota, B. (2004). "Contamination, disinfection, and cross-colonization: are hospital surfaces reservoirs for nosocomial infection?". Clin Infect Dis. 39 (8): 1182–9. doi:10.1086/424667. PMID 15486843.
- Bootsma MC, Ferguson NM (2007). "The effect of public health measures on the 1918 influenza pandemic in U.S. cities" ( كتاب إلكتروني PDF ). Proc Natl Acad Sci U S A. 104 (18): 7588–7593. Bibcode:2007PNAS..104.7588B. doi:10.1073/pnas.0611071104. PMC . PMID 17416677. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 24 سبتمبر 2015.
- Hatchett RJ, Mecher CE, Lipsitch M (2007). "Public health interventions and epidemic intensity during the 1918 influenza pandemic" ( كتاب إلكتروني PDF ). Proc Natl Acad Sci U S A. 104 (18): 7582–7587. Bibcode:2007PNAS..104.7582H. doi:10.1073/pnas.0610941104. PMC . PMID 17416679. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 13 ديسمبر 2015.
- Hurt AC, Ho HT, Barr I (October 2006). "Resistance to anti-influenza drugs: adamantanes and neuraminidase inhibitors". Expert Rev Anti Infect Ther. 4 (5): 795–805. doi:10.1586/14787210.4.5.795. PMID 17140356.
- Glasgow, J; Middleton B (2001). "Reye syndrome — insights on causation and prognosis" ( كتاب إلكتروني PDF ). Arch Dis Child. 85 (5): 351–3. doi:10.1136/adc.85.5.351. PMC . PMID 11668090. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 2 يونيو 2016.
- "Flu: MedlinePlus Medical Encyclopedia". U.S. National Library of Medicine. مؤرشف من الأصل في 04 يوليو 201607 فبراير 2010.
- Moscona, Anne (5 March 2009). "Global Transmission of Oseltamivir-Resistant Influenza". New England Journal of Medicine. 360 (10): 953–956. doi:10.1056/NEJMp0900648. ISSN 0028-4793. PMID 19258250. مؤرشف من الأصل في 06 مارس 2020.
- Jefferson T, Jones MA, Doshi P, et al. (2012). "Neuraminidase inhibitors for preventing and treating influenza in healthy adults and children". Cochrane Database Syst Rev. 1: CD008965. doi:10.1002/14651858.CD008965.pub3. PMID 22258996.
- "CDC Recommends against the Use of Amantadine and Rimantadine for the Treatment or Prophylaxis of Influenza in the United States during the 2005–06 Influenza Season". Centers for Disease Control and Prevention. 14 January 2006. مؤرشف من الأصل في 31 ديسمبر 201828 ديسمبر 2016.
- Ilyushina NA, Govorkova EA, Webster RG (October 2005). "Detection of amantadine-resistant variants among avian influenza viruses isolated in North America and Asia" ( كتاب إلكتروني PDF ). Virology. 341 (1): 102–6. doi:10.1016/j.virol.2005.07.003. PMID 16081121. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 3 نوفمبر 2013.
- Bright, Rick A; Medina, Marie-jo; Xu, Xiyan; Perez-Oronoz, Gilda; Wallis, Teresa R; Davis, Xiaohong M; Povinelli, Laura; Cox, Nancy J; Klimov, Alexander I (2005). "Incidence of adamantane resistance among influenza A (H3N2) viruses isolated worldwide from 1994 to 2005: a cause for concern". The Lancet. 366 (9492): 1175–81. doi:10.1016/S0140-6736(05)67338-2. PMID 16198766.
- Parry J (July 2005). "Use of antiviral drug in poultry is blamed for drug resistant strains of avian flu". BMJ. 331 (7507): 10. doi:10.1136/bmj.331.7507.10. PMC . PMID 15994677.
- Centers for Disease Control and Prevention (CDC) (2006). "High levels of adamantane resistance among influenza A (H3N2) viruses and interim guidelines for use of antiviral agents — United States, 2005–06 influenza season" ( كتاب إلكتروني PDF ). MMWR Morb Mortal Wkly Rep. 55 (2): 44–6. PMID 16424859. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 2 مايو 2019.
- Stephenson, I; Nicholson K (1999). "Chemotherapeutic control of influenza" ( كتاب إلكتروني PDF ). J Antimicrob Chemother. 44 (1): 6–10. doi:10.1093/jac/44.1.6. PMID 10459804. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 25 يناير 2016.
- Whitley RJ, Monto AS (2006). "Prevention and treatment of influenza in high-risk groups: children, pregnant women, immunocompromised hosts, and nursing home residents" ( كتاب إلكتروني PDF ). J Infect Dis. 194 S2: S133–8. doi:10.1086/507548. PMID 17163386. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 25 يناير 2016.
- Hayden FG (March 1997). "Prevention and treatment of influenza in immunocompromised patients". Am. J. Med. 102 (3A): 55–60, discussion 75–6. doi:10.1016/S0002-9343(97)80013-7. PMID 10868144.
- Murin S, Bilello K (2005). "Respiratory tract infections: another reason not to smoke". Cleve Clin J Med. 72 (10): 916–20. doi:10.3949/ccjm.72.10.916. PMID 16231688.
- Angelo SJ, Marshall PS, Chrissoheris MP, Chaves AM (April 2004). "Clinical characteristics associated with poor outcome in patients acutely infected with Influenza A". Conn Med. 68 (4): 199–205. PMID 15095826.
- People at High Risk of Developing Flu–Related Complications CDC publication. Published 26 August 2016. Retrieved 20 March 2017. نسخة محفوظة 25 فبراير 2018 على موقع واي باك مشين.
- Sandman, Peter M; Lanard, Jody (2005). "Bird Flu: Communicating the Risk" ( كتاب إلكتروني PDF ). Perspectives in Health Magazine. 10 (2): 1–6. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 25 أبريل 2018.
- Stowe J, Andrews N, Wise L, Miller E (February 2009). "Investigation of the temporal association of Guillain–Barré syndrome with influenza vaccine and influenzalike illness using the United Kingdom General Practice Research Database" ( كتاب إلكتروني PDF ). Am. J. Epidemiol. 169 (3): 382–8. doi:10.1093/aje/kwn310. PMID 19033158. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 4 أبريل 2020.
- Sivadon-Tardy V, Orlikowski D, Porcher R, et al. (January 2009). "Guillain–Barré syndrome and influenza virus infection" ( كتاب إلكتروني PDF ). Clin. Infect. Dis. 48 (1): 48–56. doi:10.1086/594124. PMID 19025491. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 4 أبريل 2020.
- Sivadon-Tardy V, Orlikowski D, Porcher R, et al. (January 2009). "Guillain–Barré syndrome and influenza virus infection". Clin. Infect. Dis. 48 (1): 48–56. doi:10.1086/594124. PMID 19025491.
- Jacobs BC, Rothbarth PH, van der Meché FG, et al. (October 1998). "The spectrum of antecedent infections in Guillain–Barré syndrome: a case-control study". Neurology. 51 (4): 1110–5. doi:10.1212/wnl.51.4.1110. PMID 9781538.
- Vellozzi C, Burwen DR, Dobardzic A, Ball R, Walton K, Haber P (March 2009). "Safety of trivalent inactivated influenza vaccines in adults: Background for pandemic influenza vaccine safety monitoring". Vaccine. 27 (15): 2114–2120. doi:10.1016/j.vaccine.2009.01.125. PMID 19356614.
- Shaman J, Kohn M (March 2009). "Absolute humidity modulates influenza survival, transmission, and seasonality". Proc. Natl. Acad. Sci. U.S.A. 106 (9): 3243–8. Bibcode:2009PNAS..106.3243S. doi:10.1073/pnas.0806852106. PMC . PMID 19204283.
- Shaman J, Pitzer VE, Viboud C, Grenfell BT, Lipsitch M (February 2010). Ferguson NM (المحرر). "Absolute humidity and the seasonal onset of influenza in the continental United States". PLoS Biol. 8 (2): e1000316. doi:10.1371/journal.pbio.1000316. PMC . PMID 20186267.
- Weather and the Flu Season NPR Day to Day, 17 December 2003. Retrieved, 19 October 2006 نسخة محفوظة 24 يونيو 2017 على موقع واي باك مشين.
- Lowen, AC; Mubareka, S; Steel, J; Palese, P (October 2007). "Influenza virus transmission is dependent on relative humidity and temperature". PLoS Pathogens. 3 (10): e151. doi:10.1371/journal.ppat.0030151. PMC . PMID 17953482. مؤرشف من الأصل في 15 ديسمبر 2014.
- Dushoff, J; Plotkin, JB; Levin, SA; Earn, DJ (2004). "Dynamical resonance can account for seasonality of influenza epidemics". Proceedings of the National Academy of Sciences of the United States of America. 101 (48): 16915–6. Bibcode:2004PNAS..10116915D. doi:10.1073/pnas.0407293101. PMC . PMID 15557003.
- "WHO Confirmed Human Cases of H5N1". WHO Epidemic and Pandemic Alert and Response (EPR). مؤرشف من الأصل في 16 نوفمبر 201628 ديسمبر 2016.
- Shek, LP; Lee, BW (2003). "Epidemiology and seasonality of respiratory tract virus infections in the tropics". Paediatric respiratory reviews. 4 (2): 105–11. doi:10.1016/S1526-0542(03)00024-1. PMID 12758047.
- HOPE-SIMPSON, R (1965). "The nature of herpes zoster: a long-term study and a new hypothesis". Proceedings of the Royal Society of Medicine. 58: 9–20. PMC . PMID 14267505.
- Cannell, J; Vieth R; Umhau J; Holick M; Grant W; Madronich S; Garland C; Giovannucci E (2006). "Epidemic influenza and vitamin D". Epidemiol Infect. 134 (6): 1129–40. doi:10.1017/S0950268806007175. PMC . PMID 16959053.
- Julie Steenhuysen (26 August 2010). "CDC backs away from decades-old flu death estimate". Reuters. مؤرشف من الأصل في 11 أكتوبر 201013 سبتمبر 2010.
Instead of the estimated 36,000 annual flu deaths in the United States ... the actual number in the past 30 years has ranged from a low of about 3,300 deaths to a high of nearly 49,000, the CDC said on Thursday
- Jonathan Dushoff; Plotkin, JB; Viboud, C; Earn, DJ; Simonsen, L (2006). "Mortality due to Influenza in the United States — An Annualized Regression Approach Using Multiple-Cause Mortality Data". المجلة الأمريكية لعلم الأوبئة. 163 (2): 181–7. doi:10.1093/aje/kwj024. PMID 16319291. مؤرشف من الأصل في 07 مارس 201029 أكتوبر 2009.
The regression model attributes an annual average of 41,400 (95% confidence interval: 27,100, 55,700) deaths to influenza over the period 1979–2001
نسخة محفوظة 7 مارس 2010 على موقع واي باك مشين. - Thompson, W; Shay D; Weintraub E; Brammer L; Cox N; Anderson L; Fukuda K (2003). "Mortality associated with influenza and respiratory syncytial virus in the United States" ( كتاب إلكتروني PDF ). JAMA. 289 (2): 179–86. doi:10.1001/jama.289.2.179. PMID 12517228. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 18 يناير 2012.
- Thompson, W; Shay D; Weintraub E; Brammer L; Bridges C; Cox N; Fukuda K (2004). "Influenza-associated hospitalizations in the United States". JAMA. 292 (11): 1333–40. doi:10.1001/jama.292.11.1333. PMID 15367555.
- Influenza WHO Fact sheet No. 211 revised March 2003. Retrieved 22 October 2006. نسخة محفوظة 28 أغسطس 2017 على موقع واي باك مشين.
- Lozano, R (15 December 2012). "Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010". Lancet. 380 (9859): 2095–128. doi:10.1016/S0140-6736(12)61728-0. PMID 23245604.
- Murray CJ, Lopez AD, Chin B, Feehan D, Hill KH (December 2006). "Estimation of potential global pandemic influenza mortality on the basis of vital registry data from the 1918–20 pandemic: a quantitative analysis". Lancet. 368 (9554): 2211–8. doi:10.1016/S0140-6736(06)69895-4. PMID 17189032.
- Recker M, Pybus OG, Nee S, Gupta S (2007). "The generation of influenza outbreaks by a network of host immune responses against a limited set of antigenic types" ( كتاب إلكتروني PDF ). Proc Natl Acad Sci U S A. 104 (18): 7711–16. Bibcode:2007PNAS..104.7711R. doi:10.1073/pnas.0702154104. PMC . PMID 17460037. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 24 سبتمبر 2015.
- Parrish, C; Kawaoka Y (2005). "The origins of new pandemic viruses: the acquisition of new host ranges by canine parvovirus and influenza A viruses". Annu Rev Microbiol. 59: 553–86. doi:10.1146/annurev.micro.59.030804.121059. PMID 16153179.
- Wolf, Yuri I; Viboud, C; Holmes, EC; Koonin, EV; Lipman, DJ (2006). "Long intervals of stasis punctuated by bursts of positive selection in the seasonal evolution of influenza A virus". Biol Direct. 1 (1): 34. doi:10.1186/1745-6150-1-34. PMC . PMID 17067369.
- Ferguson, NM; Cummings DA; Cauchemez S; Fraser C; Riley S; Meeyai A; Iamsirithaworn S; Burke DS (2005). "Strategies for containing an emerging influenza pandemic in Southeast Asia". Nature. 437 (7056): 209–14. Bibcode:2005Natur.437..209F. doi:10.1038/nature04017. PMID 16079797.
- Smith, P (2009). "Swine Flu". Croatian Medical Journal. 50 (4): 412–5. doi:10.3325/cmj.2009.50.412. PMC . PMID 19673043.
- Influenza, قاموس أكسفورد الإنجليزي, second edition.
- Potter, CW (2001). "A history of influenza". Journal of applied microbiology. 91 (4): 572–579. doi:10.1046/j.1365-2672.2001.01492.x. PMID 11576290.
- Creighton, Charles (1965): A History Of Epidemics In Britain, With Additional Material By D.E.C. Eversley
- Taubenberger, J; Morens D (2006). "1918 Influenza: the mother of all pandemics". Emerg Infect Dis. 12 (1): 15–22. doi:10.3201/eid1201.050979. PMC . PMID 16494711.
- Guerra, Francisco (1988). "The Earliest American Epidemic: The Influenza of 1493". Social Science History. 12 (3): 305–325. doi:10.2307/1171451. JSTOR 1171451. PMID 11618144. (only the first page can be read for free, but that has enough information about influenza being the main disease brought by Columbus killing 90 % of the indigenous population)
- Guerra, F (1993). "The European-American exchange". History and Philosophy of the Life Sciences. 15 (3): 313–327. PMID 7529930.
- Potter CW (October 2001). "A History of Influenza". Journal of Applied Microbiology. 91 (4): 572–579. doi:10.1046/j.1365-2672.2001.01492.x. PMID 11576290.
- Beveridge, W I (1991). "The chronicle of influenza epidemics". History and Philosophy of the Life Sciences. 13 (2): 223–234. PMID 1724803.
- Martin, P; Martin-Granel E (June 2006). "2,500-year evolution of the term epidemic". Emerg Infect Dis. 12 (6): 976–80. doi:10.3201/eid1206.051263. PMC . PMID 16707055. مؤرشف من الأصل في 30 أبريل 2011.
- Hippocrates. "Of the Epidemics, c. 400 BCE". فرنسيس آدامز (لغوي) (transl.). مؤرشف من الأصل في 18 أغسطس 201818 أكتوبر 2006.
- Knobler S, Mack A, Mahmoud A, Lemon S (المحررون). "1: The Story of Influenza". The Threat of Pandemic Influenza: Are We Ready? Workshop Summary (2005). Washington, D.C.: The National Academies Press. صفحات 60–61.
- Patterson, KD; Pyle GF (Spring 1991). "The geography and mortality of the 1918 influenza pandemic". Bull Hist Med. 65 (1): 4–21. PMID 2021692.
- Taubenberger JK, Reid AH, Janczewski TA, Fanning TG (December 2001). "Integrating historical, clinical and molecular genetic data in order to explain the origin and virulence of the 1918 Spanish influenza virus". Philosophical Transactions of the Royal Society B. 356 (1416): 1829–39. doi:10.1098/rstb.2001.1020. PMC . PMID 11779381.
- Simonsen, L; Clarke M; Schonberger L; Arden N; Cox N; Fukuda K (July 1998). "Pandemic versus epidemic influenza mortality: a pattern of changing age distribution". J Infect Dis. 178 (1): 53–60. doi:10.1086/515616. PMID 9652423.
- Valleron AJ, Cori A, Valtat S, Meurisse S, Carrat F, Boëlle PY (May 2010). "Transmissibility and geographic spread of the 1889 influenza pandemic". Proc. Natl. Acad. Sci. U.S.A. 107 (19): 8778–81. Bibcode:2010PNAS..107.8778V. doi:10.1073/pnas.1000886107. PMC . PMID 20421481.
- Mills CE, Robins JM, Lipsitch M (December 2004). "Transmissibility of 1918 pandemic influenza". Nature. 432 (7019): 904–6. Bibcode:2004Natur.432..904M. doi:10.1038/nature03063. PMID 15602562.
- Donaldson LJ, Rutter PD, Ellis BM, et al. (2009). "Mortality from pandemic A/H1N1 2009 influenza in England: public health surveillance study". BMJ. 339: b5213. doi:10.1136/bmj.b5213. PMC . PMID 20007665.
- Fatimah S Dawood, A Danielle Iuliano, Carrie Reed, Martin I Meltzer, David K Shay, Po-Yung Cheng, Don Bandaranayake, Robert F Breiman, W Abdullah Brooks, Philippe Buchy, Daniel R Feikin, Karen B Fowler, Aubree Gordon, Nguyen Tran Hien, Peter Horby, Q Sue Huang, Mark A Katz, Anand Krishnan, Renu Lal, Joel M Montgomery, Kåre Mølbak, Richard Pebody, Anne M Presanis, Hugo Razuri, Anneke Steens, Yeny O Tinoco, Jacco Wallinga, Hongjie, Sirenda Vong, Joseph Bresee, Marc-Alain Widdowson (26 June 2012). "Estimated global mortality associated with the first 12 months of 2009 pandemic influenza A H1N1 virus circulation: a modelling study". The Lancet Infectious Diseases. 12 (9): 687–95. doi:10.1016/S1473-3099(12)70121-4. PMID 22738893. مؤرشف من الأصل في 7 فبراير 201819 مارس 2014.
- Smith, W; Andrewes CH; Laidlaw PP (1933). "A virus obtained from influenza patients". Lancet. 2 (5732): 66–68. doi:10.1016/S0140-6736(00)78541-2.
- Heinen PP (15 September 2003). "Swine influenza: a zoonosis". Veterinary Sciences Tomorrow. ISSN 1569-0830. مؤرشف من الأصل في 11 فبراير 200728 ديسمبر 2016.
- Shimizu, K (October 1997). "History of influenza epidemics and discovery of influenza virus". Nippon Rinsho. 55 (10): 2505–201. PMID 9360364.
- Palese P (December 2004). "Influenza: old and new threats". Nat. Med. 10 (12 Suppl): S82–7. doi:10.1038/nm1141. PMID 15577936.
- "Sir Frank Macfarlane Burnet: Biography". The مؤسسة نوبل. Retrieved 22 October 2006. نسخة محفوظة 21 أغسطس 2017 على موقع واي باك مشين.
- Kendall, H (2006). "Vaccine Innovation: Lessons from World War II". Journal of Public Health Policy. 27 (1): 38–57. doi:10.1057/palgrave.jphp.3200064. PMID 16681187.
- Poland G (2006). "Vaccines against avian influenza—a race against time". N Engl J Med. 354 (13): 1411–3. doi:10.1056/NEJMe068047. PMID 16571885. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 3 مايو 2019.
- "Statement from President George W. Bush on Influenza". مؤرشف من الأصل في 9 يناير 200926 أكتوبر 2006.
- Brainerd, E. and M. Siegler (2003), "The Economic Effects of the 1918 Influenza Epidemic", CEPR Discussion Paper, no. 3791.
- Donor Nations Pledge $1.85 Billion to Combat Bird Flu - تصفح: نسخة محفوظة 17 May 2008 على موقع واي باك مشين. Newswire Retrieved 26 October 2006.
- Bush Outlines $7 Billion Pandemic Flu Preparedness Plan US Mission to the EU. Retrieved 12 December 2009. نسخة محفوظة 17 مارس 2020 على موقع واي باك مشين.
- Rosenthal, E; Bradsher, K (16 March 2006). "Is Business Ready for a Flu Pandemic?". نيويورك تايمز. مؤرشف من الأصل في 06 أبريل 201617 أبريل 2006.
- Assessment of the 2009 Influenza A (H1N1) Outbreak on Selected Countries in the Southern Hemisphere. 2009. "Archived copy". مؤرشف من الأصل في 24 سبتمبر 200921 سبتمبر 2009.
- Influenza A Virus Genome Project at The Institute of Genomic Research. Retrieved 19 October 2006 نسخة محفوظة 07 20أغسطس على موقع واي باك مشين.
- Fiers W, Neirynck S, Deroo T, Saelens X, Jou WM (December 2001). "Soluble recombinant influenza vaccines". Philosophical Transactions of the Royal Society B. 356 (1416): 1961–3. doi:10.1098/rstb.2001.0980. PMC . PMID 11779398.
- Subbarao K, Katz J (2004). "Influenza vaccines generated by reverse genetics". Curr Top Microbiol Immunol. 283: 313–42. doi:10.1007/978-3-662-06099-5_9. PMID 15298174.
- Fiers W, De Filette M, Birkett A, Neirynck S, Min Jou W (July 2004). "A "universal" human influenza A vaccine". Virus Res. 103 (1–2): 173–6. doi:10.1016/j.virusres.2004.02.030. PMID 15163506.
- Bardiya N, Bae J (2005). "Influenza vaccines: recent advances in production technologies". Appl Microbiol Biotechnol. 67 (3): 299–305. doi:10.1007/s00253-004-1874-1. PMID 15660212. مؤرشف من الأصل في 26 مارس 2020.
- Petsch B, Schnee M, Vogel AB, et al. (November 2012). "Protective efficacy of in vitro synthesized, specific mRNA vaccines against influenza A virus infection". Nat. Biotechnol. 30 (12): 1210–6. doi:10.1038/nbt.2436. PMID 23159882.
- Stephen Adams (8 July 2011). "Universal flu vaccine a step closer". The Telegraph. مؤرشف من الأصل في 02 ديسمبر 2014.
- Ekiert, DC; Friesen, RHE; Bhabha, G; Kwaks, T; Jongeneelen, M; Yu, W; Ophorst, C; Cox, F; et al. (2011). "A Highly Conserved Neutralizing Epitope on Group 2 Influenza a Viruses". Science. 333 (6044): 843–50. Bibcode:2011Sci...333..843E. doi:10.1126/science.1204839. PMC . PMID 21737702.
- Neirynck S, Deroo T, Saelens X, Vanlandschoot P, Jou WM, Fiers W (October 1999). "A universal influenza A vaccine based on the extracellular domain of the M2 protein". Nat. Med. 5 (10): 1157–63. doi:10.1038/13484. PMID 10502819.
- Gingerich, DA (2008). "Lymphocyte T-Cell Immunomodulator: Review of the ImmunoPharmacology of a new Veterinary Biologic" ( كتاب إلكتروني PDF ). Journal of Applied Research in Veterinary Medicine. 6 (2): 61–68. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 23 أبريل 201605 ديسمبر 2010.
- Capua, I; Alexander D (2006). "The challenge of avian influenza to the veterinary community". Avian Pathol. 35 (3): 189–205. doi:10.1080/03079450600717174. PMID 16753610. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 3 مايو 2019.
- Hinshaw V, Bean W, Webster R, Rehg J, Fiorelli P, Early G, Geraci J, St Aubin D (1984). "Are seals frequently infected with avian influenza viruses?". J Virol. 51 (3): 863–5. PMC . PMID 6471169.
- Gorman O, Bean W, Kawaoka Y, Webster R (1990). "Evolution of the nucleoprotein gene of influenza A virus". J Virol. 64 (4): 1487–97. PMC . PMID 2319644.
- Swayne D, Suarez D (2000). "Highly pathogenic avian influenza". Rev Sci Tech. 19 (2): 463–82. PMID 10935274.
- Bano S, Naeem K, Malik S (2003). "Evaluation of pathogenic potential of avian influenza virus serotype H9N2 in chickens". Avian Dis. 47 (3 Suppl): 817–22. doi:10.1637/0005-2086-47.s3.817. PMID 14575070.
- Elbers A, Koch G, Bouma A (2005). "Performance of clinical signs in poultry for the detection of outbreaks during the avian influenza A (H7N7) epidemic in The Netherlands in 2003". Avian Pathol. 34 (3): 181–7. doi:10.1080/03079450500096497. PMID 16191700.
- Capua, I; Mutinelli, F (2001). "Low pathogenicity (LPAI) and highly pathogenic (HPAI) avian influenza in turkeys and chicken". A Colour Atlas and Text on Avian Influenza. Bologna: Papi Editore. صفحات 13–20. . مؤرشف من الأصل في 2 مايو 2019.
- Li K, Guan Y, Wang J, Smith G, Xu K, Duan L, Rahardjo A, Puthavathana P, Buranathai C, Nguyen T, Estoepangestie A, Chaisingh A, Auewarakul P, Long H, Hanh N, Webby R, Poon L, Chen H, Shortridge K, Yuen K, Webster R, Peiris J (2004). "Genesis of a highly pathogenic and potentially pandemic H5N1 influenza virus in eastern Asia". Nature. 430 (6996): 209–13. Bibcode:2004Natur.430..209L. doi:10.1038/nature02746. PMID 15241415.
- Li KS, Guan Y, Wang J, Smith GJ, Xu KM, Duan L, Rahardjo AP, Puthavathana P, Buranathai C, Nguyen TD, Estoepangestie AT, Chaisingh A, Auewarakul P, Long HT, Hanh NT, Webby RJ, Poon LL, Chen H, Shortridge KF, Yuen KY, Webster RG, Peiris JS. "The Threat of Pandemic Influenza: Are We Ready?" Workshop Summary The National Academies Press (2005) "Today's Pandemic Threat: Genesis of a Highly Pathogenic and Potentially Pandemic H5N1 Influenza Virus in Eastern Asia", pages 116–130 نسخة محفوظة 26 مارس 2020 على موقع واي باك مشين.
- Salomon R, Webster RG (February 2009). "The influenza virus enigma". Cell. 136 (3): 402–10. doi:10.1016/j.cell.2009.01.029. PMC . PMID 19203576.
- Liu J (2006). "Avian influenza—a pandemic waiting to happen?". J Microbiol Immunol Infect. 39 (1): 4–10. PMID 16440117. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 25 يوليو 2019.
- Deadly Bird Flu Spreading in China, Unclear How, ABC News, Katie Moisse, 18 April 2013. نسخة محفوظة 22 يونيو 2017 على موقع واي باك مشين.
- Background and summary of human infection with influenza A(H7N9) virus– as of 5 April 2013, World Health Organization. نسخة محفوظة 14 فبراير 2014 على موقع واي باك مشين.
- H7N9 avian influenza human infections in China, World Health Organization, 1 April 2013. "... So far no further cases have been identified among the 88 identified contacts under follow up." نسخة محفوظة 27 يونيو 2013 على موقع واي باك مشين.
- 2 Men in China Die of Lesser-Known Strain of Bird Flu, New York Times, DAVID BARBOZA, 31 March 2013. نسخة محفوظة 03 يوليو 2017 على موقع واي باك مشين.
- Myers KP, Olsen CW, Gray GC (April 2007). "Cases of swine influenza in humans: a review of the literature". Clin. Infect. Dis. 44 (8): 1084–8. doi:10.1086/512813. PMC . PMID 17366454.
- Kothalawala H, Toussaint MJ, Gruys E (June 2006). "An overview of swine influenza". Vet Q. 28 (2): 46–53. doi:10.1080/01652176.2006.9695207. PMID 16841566.
- McNeil Jr, Donald G (1 May 2009). "Virus's Tangled Genes Straddle Continents, Raising a Mystery About Its Origins". نيويورك تايمز. مؤرشف من الأصل في 16 فبراير 201831 مارس 2010.
- Maria Zampaglione (29 April 2009). "Press Release: A/H1N1 influenza like human illness in Mexico and the USA: OIE statement". المنظمة العالمية لصحة الحيوان. مؤرشف من الأصل في 30 أبريل 200929 أبريل 2009.
- Grady, Denise (1 May 2009). "W.H.O. Gives Swine Flu a Less Loaded, More Scientific Name". نيويورك تايمز. مؤرشف من الأصل في 27 يونيو 201731 مارس 2010.
للمزيد من القراءة
"عام"
|
طريقة تطور المرض
|