لاكوساميد (Lacosamide) (اسم دولي غير مسجل الملكية INN، معروف سابقاً باسم إرلوساميد erlosamide، هاركيروسايد harkeroside، إس بي أم SPM 927، أو ADD 234037) هو دواء اكتشفه الدكتور هارولد كون (Dr. Harold Kohn) [2] بينما كان في جامعة هيوستن وطوّرته شركة الاتحاد الكيميائي البلجيكي "(يو سي بي)" ((بالفرنسية: Union Chimique Belge) UCB) المختصة بالمستحضرات الدوائية الحيوية ويستعمل للمُعالَجَةِ المُساعِدَةِ للصرع الجزئي واعتلال الأعصاب السكري، وتم تسويق الدواء تحت الاسم التجاري "ڤيمبات Vimpat".
| لاكوساميد | |
|---|---|
| الاسم النظامي | |
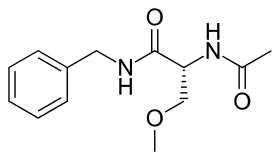
| N2-acetyl-N-benzyl-D-homoserinamide | |
| يعالج | |
| اعتبارات علاجية | |
| اسم تجاري | فيمبات Vimpat |
| مرادفات | (2R)-2-(acetylamino)-N-benzyl-3-methoxypropanamide |
| ASHPDrugs.com | أفرودة |
| مدلاين بلس | a609028 |
| فئة السلامة أثناء الحمل | C |
| طرق إعطاء الدواء | عن طريق الفم، وعن طريق الوريد |
| بيانات دوائية | |
| توافر حيوي | عالي |
| عمر النصف الحيوي | 13 ساعة |
| إخراج (فسلجة) | كلوي |
| معرّفات | |
| CAS | 175481-36-4  |
| ك ع ت | N03N03AX18 AX18 |
| بوب كيم | CID 219078 |
| IUPHAR | 7472 |
| ECHA InfoCard ID | 100.112.805 |
| درغ بنك | 06218 |
| كيم سبايدر | 189902  |
| المكون الفريد | 563KS2PQY5  |
| كيوتو | D07299  |
| ChEMBL | CHEMBL58323  |
| ترادف | (2R)-2-(acetylamino)-N-benzyl-3-methoxypropanamide |
| بيانات كيميائية | |
| الصيغة الكيميائية | C13H18N2O3 |
| الكتلة الجزيئية | 250.294 g/mol |
الموافقات والمؤشرات
لاكوساميد مركّب مضاد للاختلاج مٌعتمد للعلاج المرافق (adjunctive treatment).
يُستخدم لاكوساميد أيضاً للتحول إلى معالجة أحادية الدواء (monotherapy treatment) لعلاج الصرع الجزئي (partial-onset seizures) وألم الاعتلال العصبي (neuropathic pain) (ليس معتمداً من إدارة الغذاء والدواء الأمريكية FDA).
قبلت إدارة الغذاء والدواء الأمريكية (FDA) طلب التماس الدواء الجديد لاكوساميد من شركة "يو سي بي" (UCB) في 29 نوفمبر 2007، وبدأت عملية الموافقة على الدواء [3][4]. كما قدمت شركة "يو سي بي" (UCB) أيضا للموافقة على التسويق في الاتحاد الأوروبي. قبلت وكالة الأدوية الأوروبية طلب التسويق للمراجعة والفحص في مايو 2007 [3][5].
تمت الموافقة على الدواء في الاتحاد الأوروبي يوم 3 سبتمبر، 2008 [6]. وقد تم التصديق عليه في الولايات المتحدة في 29 أكتوبر 2008 [7]. تأخر الترويج للاكوساميد بسبب اعتراض حول تصنيف الدواء في الجدول الخامس (schedule V) من قانون المواد الخاضعة للرقابة. أصدرت إدارة الغذاء والدواء الأمريكية الحكم النهائي بإقرار وضع الدواء في الجدول الخامس في 22 يونيو 2009 [8].
الاكتشاف
اكتشف لاكوساميد الدكتور هارولد كون وزملاؤه في جامعة هيوستن عام 1996.[9] فقد افترضوا أن الأحماض الأمينية المعدّلة قد تكون مفيدة علاجياً في علاج داء الصرع. فتم توليف بضع مئات من مثل هذه الجزيئات على مدى عدة سنوات، وتم اختبارها ظاهرياً على نموذج مرض الصرع جرى تطبيقه على الفئران. وُجد أن (N-benzyl-2-acetamido-3-methoxypropionamide) فعال للغاية في هذا النموذج، مع تتبع النشاط البيولوجي خصيصا إلى جزئ R بها [9]. وأصبح هذا المركّب اسمه لاكوساميد بعد الحصول على ترخيص من قبل شركة شفارتز فارما (Schwarz Pharma)، التي أنجزت التطوير ما قبل السريري والسريري المبكّر لها. في عام 2006 اشترت شركة "'يو سي بي'" (UCB) شركة شفارتز فارما، وأكملت برنامج التطوير السريري وحصلت على الموافقة بتسويق لاكوساميد. ومن المثير للاهتمام أن آلية عملها كانت غير معروفة في وقت الحصول على الموافقة بالترخيص.[10]
آلية العمل والديناميكا الدوائية
لاكوساميد حمض أميني مٌفعّل يُنتج نشاط في اختبار صرع الصدمة الكهربائية القصوى (Maximal Electroshock Seizure) (MES)، وهو، مثله كمثل بعض العقاقير الأخرى المضادة للصرع، يُعتقد أنه يعمل من خلال قنوات الصوديوم التي تفتح وتغلق بواباتها بالجهد الكهربي للصوديوم (voltage-gated sodium channels).[10]
يعزز لاكوساميد التعطيل البطيء لقنوات الصوديوم المُبوّبة بالجهد الكهربي (الفولت) دون التأثير على التثبيط السريع لقنوات الصوديوم المُبوّبة بالجهد الكهربى. هذا التعطيل يمنع القناة من أن تفتح، مما يساعد على إنهاء جهد الفعل (action potential). العديد من الأدوية المضادة للصرع، مثل كاربامازيبين أو لاموتريجين، تبطئ التعافي من عملية التثبيط، وبالتالي تقلل من قدرة الخلايا العصبية على إطلاق جهود الفعل. يحدث التثبيط فقط في الخلايا العصبية التي تطلق جهود الفعل، وهذا يعني أن الأدوية التي تعدّل التعطيل السريع بشكل انتقائي تقلل الإطلاق في الخلايا النشطة، والتعطيل البطئ مماثل ولكن لا ينتج منع كامل لقنوات الصوديوم المُبوّبة بالجهد الكهربي، وذلك مع حدوث التفعيل والتعطيل على مدى المئات من الميلّي ثانية أو أكثر. يجعل لاكوساميد هذا التعطيل يحدث في الجهد عبر الغشائي الأقل استقطاباً، وهذا يعني أن لاكوساميد يؤثر فقط على الخلايا العصبية غير المستقطبة (depolarized) أو النشطة لفترات طويلة من الزمن، وهو يطابق الخلايا العصبية في بؤرة الصرع.[11]
جاءت نتائج تعاطي لاكوساميد في تثبيط الإطلاق المتكرر للخلايا العصبية، حيث أنها تحقق الاستقرار في أغشية الخلايا العصبية الشديدة الاستثارة، وتحد من توافر القنوات على المدى الطويل، ولكن بدون التأثير على الوظيفة الفسيولوجية.[12] كما أن للاكوساميد آلية مزدوجة في العمل، فهو ينظم أيضا استجابة كولابسين البروتين الوسيط 2 (CRMP-2) (collapsin response mediator protein 2)، مانعاً بذلك تشكيل اتصالات عصبية غير طبيعية في المخ.[13]
لا يؤثر لاكوساميد على مستقبلات AMPA، kainate، NMDA، GABAA، GABAB، ولا على مجموعة متنوعة متعلقة بمستقبلات الدوبامين (Dopaminergic) أو والسيروتونين (Serotonergic) أو الأدرينالين (Adrenergic) أو المسكارين (muscarinic) أو الكانابينويد (cannabinoid)، ولا يمنع تيارات البوتاسيوم أو الكالسيوم.[14] لا يعدّل لاكوساميد اسْتِرْداد (reuptake) النواقل العصبية بما في ذلك النورإبينفرين والدوبامين والسيروتونين.[15] وبالإضافة إلى ذلك، فإنه لا يثبط ناقلة GABA.[16]
الحرائك الدوائية
عندما تناول الأفراد الأصحاء لاكوساميد عن طريق الفم، يُمتص لاكوساميد سريعاً من خلال الجهاز الهضمي. يتم فقدان القليل من الدواء بسبب تأثير المرور الأولي، وبالتالي فإن التوافر البيولوجي للاكوساميد عن طريق الفم يقارب 100٪.[17] ينخفض ارتباط لاكوساميد مع بروتين البلازما في البالغين لأقل من <15، مما يقلل من إمكانية التفاعل مع أدوية أخرى، ويظل تركيز لاكوساميد أعلى ما يكون في بلازما الدم ما يقرب من 1 إلى 4 ساعات بعد تناوله عن طريق الفم. عمر النصف للاكوساميد حوالي 12-16 ساعة، ويظل بدون تغيير إذا كان المريض يتعاطى أيضا محرضات الإنزيم. ونتيجة لذلك، يُتناول لاكوساميد مرتين يوميا، مرة كل 12 ساعة. يُفصل الدواء من الجسم عن طريق الكلى ويُطرح في البول بنسبة 95٪.[18] يظل 40٪ من المركّب كما هو من دون تغيير البناء الدوائي الأصلي، في حين أن بقية المركّب يتكون من ناتج عمليّة تّمثيل لاكوساميد (الأيض). يتم طرح 0.5٪ فقط من الدواء في البراز.[19]. المسار الأيضي الرئيسي للاكوساميد هو CYP2C9، CY2C19، وإزالة مجموعة الميثيل (CH3) بوساطة CYP3A4 [20]
منحنى الجرعة والاستجابة للاكوساميد خطّي ومتناسب مع الجرعات عن طريق الفم حتي 800 ملغ، والجرعات الوريدية حتى 300 ملغ.[21] احتمالية تفاعل لاكوساميد مع الأدوية الأخرى منخفضة، ولم يتم العثور على تفاعلات دوائية تحدث مع الأدوية الأخرى من مضادات الاختلاج (AEDs) التي تعمل على قنوات الصوديوم.[22] أظهرت دراسة على ارتباط لاكوساميد مع CRMP-2 في بويضات حيوان القيطم (جنس من البرمائيات يتبع فصيلة الضفادع العديمة اللسان) أن الارتباط تنافسي (competitive binding) ومُحَدّد (specific binding). لدى لاكوساميد قيمة Kd أقل بقليل من 5μM، وقيمة Bmax حوالي 200 جزء في المليون/ملغ (pM/mg).[23] حجم توزيع لاكوساميد في البلازما (Vd) هو 0.6 لتر/كجم (L/kg)، وهي قريبة من الحجم الكلي للماء.
إن لاكوساميد مزدوج الألفة (محب للدهون والماء - ampiphilic) وبالتالي فهو محب للماء وأيضا محب للدهون بالقدر الكافي لعبور الحاجز الدموي الدماغي.[24]
الجرعة
يوصف لاكوساميد في البداية على جرعات فموية من 50 ملغ مرتين يوميا، بجرعة مجموعها 100 ملغ يومياً. يمكن زيادة الجرعات بمقدار 100 ملغ/يوم عن طريق جرعتين يوميا تصل إلى ما مجموعه 200-400 ملغ/يوم. أظهرت التجارب السريرية أن جرعة 600 ملغ/يوم لم تكن أكثر فعالية من جرعة 400 ملغ/يوم، ولكن أدت إلى المزيد من ردود الفعل السلبية. يُعطى لاكوساميد فموياً من خلال أقراص مغلفة من 50 ملغ (لونها وردي)، و100 ملغ (لونها أصفر غامق)، و150 ملغ (لونها سلموني)، و200 ملغ (لونها أزرق). ويمكن أيضا أن تُعطى عن طريق الحقن بتركيز 200 مجم/20 مل أو حل عن طريق الفم بتركيز 10 ملغ/مل.[25]
التجارب قبل السريرية
في التجارب قبل السريرية، تم اختبار تأثير لاكوساميد على نماذج صرع حيوانية باستخدام نموذج فأر فرينجز (Frings) لصَرْعٌ سَمْعِيُّ المَنْشَأ (audiogenic seizures AGS) الذي هو حساس لنوبة صرع مع جرعة فعالة (أو ED50) قيمتها 0.63 ملغ/كغ داخل الغشاء المصلي البطني.
تم أيضا تقييم تأثير لاكوساميد باستخدام اختبار صرع الصدمة الكهربائية القصوى ((Maximal Electroshock Seizure) MES) للكشف عن تثبيط انتشار النوبة.[26][27] وكان تعاطي لاكوساميد ناجحاً في منع انتشار النوبة الصرعية المُستحثة بالصدمة الكهربائية القصوى MES في الفئران (ED50 = 4.5 ملغ/كغ، داخل الغشاء المصلي البطني) والجرذان (ED50 = 3.9 ملغ/كغ، عن طريق الفم).[28] في التجارب قبل السريرية، تبين أن تعاطي لاكوساميد في تركيبة مع أدوية أخرى مضادة للصرع أنتجت آثرا متآزرا مضادا للصرع. أنتج لاكوساميد آثارا في نماذج حيوانية تعاني من رعاش مجهول السبب وخلل الحركة المتأخر والفصام والقلق.[29] وقد وجدت التجارب قبل السريرية أن المتماكب الفراغي S (دوران عكس عقارب الساعة) S-stereoisomer أقل قوة من المتماكب الفراغي R (دوران مع عقارب الساعة) R-stereoisomer في علاج النوبات.[30]
التجارب السريرية
النوبة الجزئية
تم اختبار لاكوساميد في ثلاث دراسات منضبطة بالعلاج الممّوه (Placebo-controlled study) ومزدوجة التعمية وعشوائية على أكثر من 1300 مريض.[31] في مراكز متعددة، وفي دول متعددة، أُجريت تجارب سريرية منضبطة بالعلاج المموه وهمي ومزدوجة التعمية (لا يعلم المرضى أو المعالجون ماهية الدواء) وعشوائية لتحديد مدى فعالية وسلامة جرعات مختلفة من لاكوساميد على أفراد يشتكون ضعف السيطرة على نوبات الصرع الجزئية (poorly controlled partial-onset seizures)، حيث وُجد أن لاكوساميد أحدث انخفاضاً كبيراً ذا دلالة إحصائية في وتيرة حدوث النوبات عندما تعطى للمريض بالإضافة إلى مضادات الصرع الأخرى، في جرعات من 400 و600 ملليغرام في اليوم.[32]
الاعتلال العصبي السكري
في دراسة أصغر على المرضى الذين يعانون من اعتلال الأعصاب السكري، أحدث لاكوساميد أيضا سيطرة على الألم أفضل بشكل ملحوظ مقارنة مع الدواء الوهمي.[33] عندما أٌعطي لاكوساميد في تركيبة بنسبة 1-3 مع أدوية أخرى مضادة للصرع كان ذلك جيد التحمّل بالنسبة للمرضى.
وُجد أن اعطاء المريض 400 ملغ/اليوم لاكوساميد يخفض بشكل كبير من الألم في المرضى الذين يعانون من اعتلال الأعصاب السكري، وذلك من خلال دراسة أجريت في مراكز متعددة، تجربة مزدوجة التعمية ومنضبطة بإيحاء وهمي، في المرحلة الثالثة من التجارب، مع مدة علاج 18 أسبوعا.[34]
المداواة
لاكوساميد مركّب مضاد للاختلاج معتمد للمعالجة بشكل إضافي للصرع الجزئي وألم الاعتلال العصبي. التجارب السريرية جارية حاليا لاستخدام لاكوساميد كعلاج وحيد لنوبات الصرع الجزئي.[31] وليس هناك دليل على أن لاكوساميد يوفر قيمة إضافية على أدوية معالجة الصرع الحالية التي تعالج نوبات الصرع الجزئية، ولكنها قد توفر ميزة أمان.[22] وُجد أن أدوية الصرع الحديثة، بما في ذلك لاكوساميد، وفيجابارتين وفيلباميت وغابابنتين وتياجابين وروفينامايد أكثر أماناً وأكثر إمكانية للتحمل، من الأدوية القديمة مثل كاربامازيبين وفينيتوين والفالبروات.[35]
الآثار الجانبية وقابلية الاحتمال
كان لاكوساميد جيد التحمل عموما في البالغين المرضى بنوبات جزئية الظهور (partial-onset seizures).[36]. الآثار الجانبية الأكثر شيوعا المؤدية إلى إيقاف الدواء كانت حدوث: دوخة ورنح وتقيؤ وازدواج الرؤية وغثيان ودوار وعدم وضوح الرؤية. وقد لوحظت ردود الفعل السلبية هذه في ما لا يقل عن 10٪ من المرضى.[25] وتشمل الآثار الجانبية الأقل شيوعاً: النسيان والإحباط ومشاعر الحزن وفقدان الشهية.
الجهاز الهضمي
الجهاز العصبي المركزي
كانت الدوخة هي العرض السلبي الأكثر شيوعا. آثار الجهاز العصبي المركزي الأخرى هي: الصداع والنعاس وعدم وضوح الرؤية وحركات لا إرادية والضعف والتعب ومشاكل في الذاكرة وازدواج الرؤية وارتجاف أو اهتزاز اليدين وعدم الثباتوالترنح.
تأثيرات نفسية
نوبات الذعر، الانفعال أو السأم، التهيج والعدوان والقلق أو الاكتئاب، الانتحار، الأرق والهوس، تغير المزاج، شعور زائف وغير عادي بالسعادة والرفاهية.
القلب والأوعية الدموية
انخفاض ضغط الدم الوضعي وعدم انتظام ضربات القلب.
الحساسية
تحذيرات
لوحظ أن السلوك الانتحاري والفكر الانتحاري قد بدئا في أقرب وقت بعد أسبوع من بدء العلاج بلاكوساميد، وهو أثر ضائر يحدث من استخدام معظم الأدوية المضادة للصرع. في التجارب السريرية مع مدة علاج 12 أسبوعاً في المُتَوَسّط، كانت نسبة التفكير في الانتحار 0.43٪ من بين 27863 مريضاً في مقابل 0.24٪ بين 16029 مريضاً عولجوا بدواء وهمي. وقد شوهد السلوك الانتحاري في مريض واحد (1) من كل 530 مريضاً عولجوا.[25]
في الحمل
في دراسة أجريت على الأدوية المضادة للصرع لتقييم احتمالية حدوث مسخ في جنين أسماك الزرد (من أسماك المياه العذبة الاستوائية الصغيرة التي يشيع استخدامها بوصفها كائن نموذج)، وٌجد أن مؤشر المسخية للاكوساميد أعلى منه بالنسبة إلى لاموتريجين وليفيتيراسيتام وإيثوسوكسيميد. أسفر تعاطي لاكوساميد عن تشوهات مختلفة في أسماك الزرد حديثي الولادة، تختف باختلاف قيمة الجرعة.[38]
حددت إدارة الغذاء والدواء الأمريكية مكان دواء لاكوساميد تحت فئة "الحمل ج". وأفادت الدراسات على الحيوان حالات وفيات الأجنة ونقص النمو. لم يتم اختبار لاكوساميد خلال فترة الحمل البشري، وينبغي تعاطيه بحذر. وبالإضافة إلى ذلك، لم يُحدد بعد ما إذا كان إفراز لاكوساميد يظهر في حليب الثدي.[39]
استخدامات أخرى
قد يكون للاكوساميد مجموعة متنوعة من الاستخدامات الأخرى، بما في ذلك معالجة الألم وعلاج اضطرابات الصحة العقلية. وقد استخدم لاكوساميد وأدوية أخرى مضادة للصرع في معالجة الاضطراب ثنائي القطب (الهوس الاكتئابي) وإدمان الكوكايين والخرف والاكتئاب واعتلال الأعصاب المحيطية السكري ومتلازمة الألم العضلي المتفشي والصداع والفواق وداء هنتنغتون والهوس والصداع النصفي والوسواس القهري واضطرابات الهلع ومتلازمة تململ الساقين وطنين الأذن.
غالبا ما تُستخدم مجموعات متعددة من الأدوية المضادة للصرع معاً للحد من نوبة الصرع. هناك دراسات تُجرى حالياً على استخدام لاكوساميد كدواء واحد لنوبات الصرع الجزئية والاعتلال العصبي السكري والألم العضلي الليفي (الفيبروميالغيا).[22]
الكيمياء
لاكوساميد مسحوق مركّب بلوري، لونه أبيض إلى أصفر فاتح. الاسم الكيميائي للاكوساميد هو (R)-2-acetamido-N-benzyl-3-methoxypropionamide، واسمه النظامي هو N2-Acetyl-N-benzyl-O-methyl-D-serinamide.[15][15]
لاكوساميد جزيء حمض أميني مُفعَّل، لديه قابلية عالية للذوبان في الماء وثنائي ميثيل السلفوكسيد(DMSO)، مع قابلية ذوبان 20.1 ملغ/مل في محلول منظم من الفوسفات المِلْحِيّ (PBS، ودرجة حموضة PH 7.5، ودرجة حرارة 25°).[15][40] والجزيء له ستة روابط قابلة للدوران وحلقة واحدة عطرية. يذوب لاكوساميد في 143-144 درجة حرارة مئوية، ويغلي عند 536.447 درجة حرارة مئوية تحت ضغط 760 ملم زئبق.[41][42]
التخليق
تم اقتراح الخطوات الثلاث الآتية لتصنيع لاكوساميد في عام 1996.
يُعالج حمض R)-2-amino-3-hydroxypropanoic) بأنهيدريد الخليك وحمض الخليك. ثم يُعالج الناتج بـ N-methylmorpholine، وisobutyl chloroformate، وبنزيل أمين أولاً. ثم يُعالج ثانياً بالميثيل يوديد (Methyl iodide) وأكسيد الفضة الأحادية ليكوّن اللاكوساميد. وقد اقتُرحت طرق أكثر كفاءة للتركيب في السنوات الأخيرة، منها ما يلي:[43][44]
العلامات التجارية في بلدان أخرى
في باكستان، يتم تسويق لاكوساميد من قبل شركة سيرل المحدودة (The Searle Company Limited) تحت اسم لاكوليت (Lakolit).
مقالات ذات صلة
مراجع
- https://dx.doi.org/10.5281/ZENODO.1435999
- WO2000000463A1 - Anticonvulsant enantiomeric amino acid derivatives - Google Patents - تصفح: نسخة محفوظة 26 أكتوبر 2016 على موقع واي باك مشين.
- "UCB Announces FDA Filing for lacosamide in the Treatment of Diabetic Neuropathic Pain" (Press release). UCB. 2007-11-29. مؤرشف من الأصل في 25 سبتمبر 200829 نوفمبر 2007.
- "UCB Announces FDA Filing for lacosamide in the Treatment of Partial Onset Seizures in Adults with Epilepsy" (Press release). UCB. 2007-11-29. مؤرشف من الأصل في 25 سبتمبر 200829 نوفمبر 2007.
- Wan, Yuet (17 أغسطس 2007). "Marketing application for lacosamide (Vimpat) filed in EU for treatment of diabetic neuropathic pain". PharmaTimes through the UK National electronic Library for Medicines30 نوفمبر 2007.
- "Vimpat Approved in Europe" (Press release). UCB. 2008-09-03. مؤرشف من الأصل في 19 سبتمبر 200817 سبتمبر 2008.
- "UCB's Vimpat approved by U.S. FDA as adjunctive therapy for partial onset seizures in adults" (Press release). UCB. 2008-10-29. مؤرشف من الأصل في 4 مارس 201625 نوفمبر 2008.
- "FDA places lacosamide in Schedule V" (Press release). FDA. 2009-06-22. مؤرشف من الأصل في 8 يوليو 201128 يونيو 2009.
- Choi, D; Stables, JP; Kohn, H (أبريل 26, 1996). "Synthesis and anticonvulsant activities of N-Benzyl-2-acetamidopropionamide derivatives". Journal of Medicinal Chemistry. 39 (9): 1907–16. doi:10.1021/jm9508705. PMID 8627614.
- Michael A. Rogawski; Azita Tofighy; H. Steve White; Alain Matagne; Christian Wolff (2015). "Current understanding of the mechanism of action of the antiepileptic drug lacosamide". Epilepsy Research. 110: 189–205. doi:10.1016/j.eplepsyres.2014.11.021. PMID 25616473. مؤرشف من الأصل في 12 مايو 2019.
- Errington AC, Stöhr T, Heers C, Lees G (يناير 2008). "The investigational anticonvulsant lacosamide selectively enhances slow inactivation of voltage-gated sodium channels". Molecular Pharmacology. 73 (1): 157–69. doi:10.1124/mol.107.039867. PMID 17940193.
- Doty, P; Hebert D; Mathy FX; Byrnes W; Zackheim J; Simontacchi K (2013). "Development of lacosamide for the treatment of partial-onset seizures". Ann N Y Acad Sci. 1291: 56–68. doi:10.1111/nyas.12213. PMC . PMID 23859801.
- "SCHWARZ PHARMA Highlights the Results of 13 Lacosamide Data Presentations at North American Regional Epilepsy Congress in San Diego". Schwarz Pharma. 5 ديسمبر 1996. مؤرشف من الأصل في 25 يونيو 20162 أبريل 2014.
- Errington AC, Coyne L, Stöhr T, Selve N, Lees G (يونيو 2006). "Seeking a mechanism of action for the novel anticonvulsant lacosamide". Neuropharmacology. 50 (8): 1016–29. doi:10.1016/j.neuropharm.2006.02.002. PMID 16620882.
- Beyreuther, BK; Freitag, J; Heers, C; Krebsfänger, N; Scharfenecker, U; Stöhr, T (Spring 2007). "Lacosamide: a review of preclinical properties". CNS Drug Reviews. 13 (1): 21–42. doi:10.1111/j.1527-3458.2007.00001.x. PMID 17461888.
- Errington, AC; Coyne, L; Stöhr, T; Selve, N; Lees, G (يونيو 2006). "Seeking a mechanism of action for the novel anticonvulsant lacosamide". Neuropharmacology. 50 (8): 1016–29. doi:10.1016/j.neuropharm.2006.02.002. PMID 16620882.
- Hovinga, CA (2003). "SPM-927 (Schwarz Pharma)". IDrugs. 6 (5): 479–85. PMID 12789603. مؤرشف من الأصل في 25 أغسطس 20182 أبريل 2014.
- Italiano, D; Perucca E (2013). "Clinical pharmacokinetics of new-generation antiepileptic drugs at the extremes of age: an update". Clin Pharmacokinet. 52 (8): 627–45. doi:10.1007/s40262-013-0067-4. PMID 23640503. مؤرشف من الأصل في 25 أغسطس 20182 أبريل 2014.
- "Lacosamide". DrugBank. مؤرشف من الأصل في 26 مارس 20192 أبريل 2014.
- Abou-Khalil, BW (2009). "Lacosamide: what can be expected from the next new antiepileptic drug?". Epilepsy Curr. 9 (5): 133–4. doi:10.1111/j.1535-7511.2009.01317.x. PMC . PMID 19826503.
- Bialer, M; Johannessen SI; Kupferberg HJ; Levy RH; Perucca E; Tomson T (2004). "Progress report on new antiepileptic drugs: a summary of the Seventh Eilat Conference (EILAT VII)". Epilepsy Res. 61 (1–3): 1–48. doi:10.1016/j.eplepsyres.2004.07.010. PMID 15570674.
- "Therapeutic Class Review" ( كتاب إلكتروني PDF ). RegenceRx. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 11 ديسمبر 20152 أبريل 2014.
- "Method for identifying CRMP modulators". مؤرشف من الأصل في 20 أكتوبر 20162 أبريل 2014.
- Stoht, T; Kupferberg HJ; Stables JP; Choi D; Kohn H; Walton N; White HS (2007). "Lacosamide, a novel anti-convulsant drug, shows efficacy with a wide safety margin in rodent models for epilepsy". Epilepsy Res. 74 (2–3): 147–54. doi:10.1016/j.eplepsyres.2007.03.004. PMID 17433624. مؤرشف من الأصل في 25 أغسطس 20182 أبريل 2014.
- "Highlights of Prescribing Information" ( كتاب إلكتروني PDF ). Vimpat. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 3 مارس 20162 أبريل 2014.
- Borowicz, KK; Gaisor M; Kleinrok Z; Czuczwar SJ (1997). "Influence of isradipine, niguldipine and dantrolene on the anticonvulsive action of conventional antiepileptics in mice". Eur J Pharmacol. 323 (1): 45–51. doi:10.1016/s0014-2999(97)00020-4. PMID 9105875. مؤرشف من الأصل في 25 أغسطس 20182 أبريل 2014.
- Swinyard, EA; Brown WC; Godman LS (1952). "Comparative assays of antiepileptic drugs in mice and rats". J Pharmacol Exp Ther. 106 (3): 319–20. PMID 13000628.
- Beyreuther, BK; Freitag J; Heers C; Krebsfanger N; Scharfenecker U; Stohr T (2007). "Lacosamide: a review of preclinical properties". CNS Drug Rev. 13 (1): 21–42. doi:10.1111/j.1527-3458.2007.00001.x. PMID 17461888. مؤرشف من الأصل في 25 أغسطس 20182 أبريل 2014.
- "SCHWARZ PHARMA Highlights the Results of 13 Lacosamide Data Presentations at North American Regional Epilepsy Congress in San Diego". Schwarz Pharma. 5 ديسمبر 2006. مؤرشف من الأصل في 27 أبريل 20202 أبريل 2014.
- LeTiran, A; Stables, JP; Kohn, H (أكتوبر 2001). "Functionalized amino acid anticonvulsants: synthesis and pharmacological evaluation of conformationally restricted analogues". Bioorganic & Medicinal Chemistry. 9 (10): 2693–708. doi:10.1016/s0968-0896(01)00204-8. PMID 11557357.
- Doty, P; Hebert, D; Mathy, FX; Byrnes, W; Zackheim, J; Simontacchi, K (يوليو 2013). "Development of lacosamide for the treatment of partial-onset seizures". Annals of the New York Academy of Sciences. 1291: 56–68. doi:10.1111/nyas.12213. PMC . PMID 23859801.
- Ben-Menachem E, Biton V, Jatuzis D, Abou-Khalil B, Doty P, Rudd GD (2007). "Efficacy and safety of oral lacosamide as adjunctive therapy in adults with partial-onset seizures". Epilepsia. 48 (7): 1308–17. doi:10.1111/j.1528-1167.2007.01188.x. PMID 17635557.
- Rauck RL, Shaibani A, Biton V, Simpson J, Koch B (2007). "Lacosamide in painful diabetic peripheral neuropathy: a phase 2 double-blind placebo-controlled study". Clin J Pain. 23 (2): 150–8. doi:10.1097/01.ajp.0000210957.39621.b2. PMID 17237664.
- "SCHWARZ PHARMA Highlights the Results of 13 Lacosamide Data Presentations at North American Regional Epilepsy Congress in San Diego". Schwarz Pharma. مؤرشف من الأصل في 25 يونيو 20162 أبريل 2014.
- "Antiepileptic drugs". مؤرشف من الأصل في 9 مايو 20152 أبريل 2014.
- Cross SA, Curran MP.[1]. Drugs 2009;69(4):449-459. doi:10.2165/00003495-200969040-00005. نسخة محفوظة 24 فبراير 2012 على موقع واي باك مشين.
- Vimpat Side Effects Center http://www.rxlist.com/vimpat-side-effects-drug-center.html
- Lee, SH; Kang, JW; Lin, T; Lee, JE; Jin, DI (2013). "Teratogenic potential of antiepileptic drugs in the zebrafish model". BioMed research international. 2013: 726478. doi:10.1155/2013/726478. PMC . PMID 24324971.
- "Lacosamide Pregnancy and Breastfeeding Warnings". Drugs.com. مؤرشف من الأصل في 2 أبريل 20192 أبريل 2014.
- Biton, V; Rosenfeld, WE; Whitesides, J; Fountain, NB; Vaiciene, N; Rudd, GD (مارس 2008). "Intravenous lacosamide as replacement for oral lacosamide in patients with partial-onset seizures". Epilepsia. 49 (3): 418–24. doi:10.1111/j.1528-1167.2007.01317.x. PMID 17888078.
- "Lacosamide". publisher=DrugBank|accessdate=2 أبريل 2014| وصلة مكسورة = yes | مسار الأرشيف = https://web.archive.org/web/20200427184440/https://www.drugbank.ca/drugs/DB06218%7C
- Kellinghaus, C (2009). "Lacosamide as treatment for partial epilepsy: mechanisms of action, pharmacology, effects, and safety". Therapeutics and clinical risk management. 5: 757–66. doi:10.2147/tcrm.s5189. PMC . PMID 19816574.
- Morieux, P; Stables, JP; Kohn, H (أكتوبر 1, 2008). "Synthesis and anticonvulsant activities of N-benzyl-(2R)-2-acetamido-3-oxysubstituted propionamide derivatives". Bioorganic & Medicinal Chemistry. 16 (19): 8968–75. doi:10.1016/j.bmc.2008.08.055. PMC . PMID 18789868.
- McIntyre, J.A.; Castaner, J. "2004". Drugs Future. 29 (992).