| Polycarbonate | |
| |
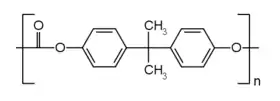
| Polycarbonate : -[CO-O-pPh-C(CH3)2-pPh-O]n | |
| Identification | |
|---|---|
| No CAS | |
| Propriétés physiques | |
| T° transition vitreuse | 140 °C (Tv car amorphe)[1] |
| Paramètre de solubilité δ | 20,3 J1/2·cm-3/2[2] |
| Masse volumique | 1,2 g·cm-3[1] - [3] |
| Conductivité thermique | 0,20 W·m-1·K-1[1] |
| Propriétés électroniques | |
| Constante diélectrique | 3,17 (60 Hz)[1] 2,92 (1 kHz, 23 °C) 2,8 (1 MHz, 23 °C)[4] |
| Propriétés optiques | |
| Indice de réfraction | 1,591 |
| Unités du SI et CNTP, sauf indication contraire. | |

| Couleur | |
|---|---|
| Usages |
Électronique Télécommunications Construction (d) DVD Disque Blu-ray |
| Date de découverte |
| Masse volumique |
1,2 gramme par centimètre cube |
|---|
| Module de Young |
2,3 gigapascals, 2,2 gigapascals |
|---|---|
| Résistance à la rupture |
65 mégapascal |
| Ténacité |
675 joule par mètre, 27,5 |
| Coefficient de Poisson |
0,37 |
| Conductivité thermique |
0,2 watt par mètre-kelvin |
|---|---|
| Capacité thermique |
1 250 joule par kilogramme-kelvin |
| Fabricant |
Mitsubishi, Hammerglass (d), Unigel (d), SABIC, Covestro, Quadrant Engineering Plastic (d) |
|---|---|
| Prix |
2,6 €, 2,8 € |
Le polycarbonate est une matière plastique disposant d'excellentes propriétés mécaniques et d'une résistance thermique permettant une utilisation entre −100 °C et 120 °C[3]. Ce polymère est issu de la polycondensation du bisphénol A (BPA) et d'un carbonate ou du phosgène, ou par transestérification.
Le matériau a été découvert en 1953 par trois chercheurs travaillant pour Bayer AG, Schnell, Bottenbruch et Krimm. Sa première mise sur le marché date de 1958. Il est commercialisé sous plusieurs noms : Makrolon de Covestro, Lexan de Sabic[5], Hammerglass, Xantar de Mitsubishi engineering plastics ou Durolon d'Unigel plasticos.
Propriétés physiques et applications
La très grande transparence de cette matière est exploitée pour la fabrication de verres optiques, des CD et DVD, des lentilles de caméras thermiques (caméras infrarouge) ou encore de vitres de phares automobiles. En forte épaisseur, il possède une légère teinte jaune.
Son excellente résistance aux chocs[3] en fait un matériau très approprié pour la fabrication de casques de moto ou de boucliers de police, mais aussi de mobilier ou de coques de smartphones.
L'innocuité physiologique du polycarbonate permet son utilisation dans le domaine médical pour la fabrication de matériel ou de prothèses. Sa sensibilité aux agents chimiques et aux ultraviolets limite toutefois son utilisation. On doit faire particulièrement attention lors de contacts prolongés avec l'eau, surtout à des températures supérieures à 60 °C, qui exposent au risque d'une forte hydrolyse. D'autre part la présence de particules de bisphénol A libérées peut rendre cette innocuité discutable[6].
À 20 °C, il est incompatible avec l'acétaldéhyde, l'acétate d'éthyle, l'acétone, l'acide acétique glacial, l'acide fluorhydrique à 48 %, l'acide nitrique à 70 %, l'acide perchlorique, l'acide sulfurique à 98 %, l'anhydride acétique, l'ammoniac, l'ammoniaque à 30 %, le benzène, le chloroforme, la diéthylamine, le diméthylsulfoxyde, l'éther éthylique, l'hydrazine, le nitrobenzène, le nitrométhane, le perchloroéthylène, la potasse concentrée, la soude à 50 %, le sulfure de carbone, le tétrachlorure de carbone, le trichloroéthane, le trichloroéthylène, l'urée, le xylène. Il n'est donc pas recommandé dans la confection de récipients.
Le polycarbonate est mal adapté aux fours à micro-ondes car il absorbe la chaleur.
Son indice de réfraction (dans le visible) est de 1,591.
Propriété dimensionnelle
Comme tous les polymères amorphes, le polycarbonate offre un retrait limité au démoulage (inférieur à 0,6 %). Sa faible reprise d'humidité lui assure une bonne stabilité dimensionnelle en ambiance humide. Il a une bonne tenue au fluage, surtout quand il est renforcé de fibres de verre.
À titre anecdotique, le polycarbonate peut exister sous forme cristalline : il est nécessaire de le refroidir très lentement (plusieurs jours) aux alentours de sa transition vitreuse et sous atmosphère inerte. On obtient alors un produit opaque, jaunâtre et très fragile. Il possède dans ce cas particulier un retrait important (de l'ordre de 10 %).
Forme
Le polycarbonate est commercialisé :
- soit sous forme de granulés (pour injection et extrusion) ;
- soit sous forme de demi-produit (pour usinage ou thermoformage).
Risques pour la santé
L'innocuité du polycarbonate est actuellement contestée en raison des particules de bisphénol A (BPA) qu'il peut libérer, notamment au contact des aliments[7]. Le polycarbonate était utilisé, entre autres, pour la fabrication de biberons en plastique mais interdit en France depuis 2010[7]. Les biberons en polycarbonate ont été retirés du marché en France car le BPA est un perturbateur endocrinien qui possède une forte homologie de structure avec les hormones endogènes de l'Homme, c'est d'ailleurs en tant qu'hormone que le BPA a été enregistré. Plus tard, voyant les possibilités que présentait le BPA dans la réalisation de matières plastiques, on a utilisé son produit de condensation (le polycarbonate) pour en fabriquer des produits de consommation courante. Le problème majeur est qu'au contact alimentaire et à la chaleur (en particulier aux micro-ondes) le polymère a tendance à se dépolymériser et à libérer des particules de BPA dans la nourriture. Les problèmes majeurs du BPA sont ses risques d'induction d'une hypofertilité (pour les adultes) et un mauvais développement des caractères sexuels (fœtus, enfants en particulier avec une non descente des testicules chez les petits garçons et des perturbations du cycle hormonal chez les filles).
Commerce
En 2014, la France est importatrice nette de polycarbonate, d'après les douanes françaises. Le prix moyen à la tonne à l'import était de 2 700 €[8].
Notes et références
- 1 2 3 4 (en) J. G. Speight, Norbert Adolph Lange, Lange's handbook of chemistry, McGraw-Hill, , 16e éd., 1623 p. (ISBN 0-07-143220-5), p. 2.758
- ↑ (en) Jozef Bicerano, Prediction of polymer properties, New York, Marcel Dekker, , 3e éd., 746 p. (ISBN 0-8247-0821-0), p. 196
- 1 2 3 « Plaque polycarbonate - Caractéristiques », sur plexiglass.fr.
- ↑ (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC Press Inc, , 90e éd., 2804 p., Relié (ISBN 978-1-4200-9084-0)
- ↑ Anciennement General Electric Plastic.
- ↑ « Polycarbonate », sur www.physique-et-matiere.com (consulté le )
- 1 2 Polycarbonate, inrs.fr d'octobre 2017, consulté le 28 novembre 2022
- ↑ « Indicateur des échanges import/export », sur Direction générale des douanes. Indiquer NC8=39074000 (consulté le ).
Voir aussi
Article connexe
- Bisphénol