| Sulfate de sodium | ||
| ||
 | ||
| Identification | ||
|---|---|---|
| No CAS | ||
| No ECHA | 100.028.928 | |
| No CE | 231-820-9 | |
| No RTECS | WE1650000 | |
| Code ATC | A12 | |
| PubChem | 24436 | |
| ChEBI | 32149 | |
| No E | E514 | |
| InChI | ||
| Apparence | solide blanc | |
| Propriétés chimiques | ||
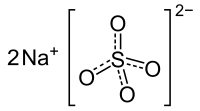
| Formule | Na2SO4 Heptahydrate : Na2SO4·7H2O Décahydrate : Na2SO4·10H2O |
|
| Masse molaire[1] | 142,042 ± 0,006 g/mol Na 32,37 %, O 45,06 %, S 22,58 %, |
|
| Propriétés physiques | ||
| T° fusion | 884 °C (anhydre) 32,38 °C (décahydrate) |
|
| Solubilité | 47,6 g·kg-1 (eau, 0 °C) 427 g·kg-1 (eau, 100 °C) pour la maille rhomboédrique |
|
| Masse volumique | 2,68 g·cm-3 (anhydre) | |
| Thermochimie | ||
| ΔfH0solide | 78,2 kJ/mol | |
| Cristallographie | ||
| Système cristallin | monoclinique, orthorhombique ou hexagonal | |
| Propriétés optiques | ||
| Indice de réfraction | polyaxe α=1,471, β=1,477, γ=1,484 |
|
| Précautions | ||
| SIMDUT[2] | ||
Produit non contrôlé |
||
| Peau | Irritant | |
| Unités du SI et CNTP, sauf indication contraire. | ||
Le sulfate de sodium est un composé chimique courant formé d'un ion sulfate et de deux ions sodium. Lorsqu'il est à l'état anhydre, il prend l'apparence d'un solide cristallin blanc de formule chimique Na2SO4 dont la forme naturelle est la thénardite des minéralogistes.
Ce sel était autrefois dénommé sel sec ou sel desséché de Glauber, car il provenait d'une lente dessication à l'étuve du sulfate de sodium décahydraté, Na2SO4·10H2O, connu sous le nom de sal mirabilis glauberi, simplifié en sel de Glauber par les anciens chimistes ou adapté plus tard par les minéralogistes en mirabilite pour désigner l'espèce minérale correspondante.
Parmi un grand nombre d'usages différents, les principales utilisations du sulfate de sodium concernent la fabrication de détergents et le procédé kraft de traitement de la pâte à papier. La moitié de la production mondiale provient de l'extraction de mirabilite ou de thénardite naturelles, et l'autre moitié de productions secondaires, notamment par sa récupération, dans des procédés de l'industrie chimique.
Histoire et description

Le sel naturel décahydraté du sulfate de sodium porte le nom de sel de Glauber, ou sal mirabilis. Il est baptisé par Johann Rudolf Glauber, qui le découvrit au XVIIe siècle en laboratoire. Cette matière minérale se présente sous la forme de cristaux blancs ou transparents, utilisés originellement comme laxatifs.
Propriétés physiques et chimiques
Le sulfate de sodium est très stable chimiquement, alors même qu'il existe sous diverses formes polymorphiques en général incolores : de maille rhomboédrique à température ambiante, monoclinique lentement à partir de 100 °C et surtout après 160 à 185 °C, enfin à structure hexagonale à plus haute température à partir de 241 °C et surtout au-dessus de 500 °C[3]. Il fond vers 884 °C sans se décomposer sous l'effet de la chaleur. Il est insensible aux agents oxydants (le soufre dans l'ion sulfate étant déjà à la valence VI, la plus élevée). Il ne réagit avec des réducteurs comme le carbone qu'à température très élevée (réduction thermochimique des sulfates dans le procédé kraft de purification de la pulpe à papier). À des températures élevées, au-delà de 730 °C, il peut néanmoins être réduit en sulfure de sodium.
Étant dérivé d'un acide fort (acide sulfurique H2SO4) et d'une base forte (hydroxyde de sodium NaOH ou bicarbonate de sodium), c'est un sel neutre dont la solution aqueuse est de pH 7.
Le sulfate de sodium peut réagir en solution aqueuse. Il réagit notamment avec une quantité équivalente d'acide sulfurique pour former un sel d'acide selon un équilibre chimique, comme indiqué ci-dessous :
- Na2SO4(aq) + H2SO4(aq) ⇔ 2 NaHSO4(aq).
Cet équilibre dépend des concentrations molaires en réactifs et produits ainsi que de la température.
Na2SO4 constitue typiquement un sulfate ionique. Une solution saturée précipite en formant le décahydrate de sulfate de sodium, appelé mirabilite ou sel de Glauber. La formation d'heptahydrate de sulfate de sodium est plus compliquée.
Il peut former des précipités en solution aqueuse lorsqu'il est combiné avec des sels de baryum ou de plomb qui forment des sulfates insolubles :
- Na2SO4(aq) + BaCl2(aq) → BaSO4(s) + 2 NaCl(aq).
L'évolution de la solubilité du sulfate de sodium dans l'eau en fonction de la température est assez inhabituelle, comme le montre la courbe ci-dessous (l'augmentation de pression nécessaire pour conserver l'eau à l'état liquide n'est pas indiquée sur le graphique). La solubilité croît de plus d'un facteur 10 entre 0 °C et 32,4 °C, température à laquelle elle atteint un maximum de 49,7 g/100 g d'eau (~ 497 g/L). À cette température, l'évolution de la courbe change brusquement et la solubilité devient presque indépendante de la température. La solubilité est nettement plus faible si l'on ajoute du chlorure de sodium dans la solution (régression de l'équilibre de dissolution vers la gauche par effet d'ion commun avec le cation Na+).
Cette évolution inhabituelle de la solubilité avec la température est à la base de l'utilisation du sulfate de sodium dans des systèmes passifs de chauffage solaire.
.png.webp)
Cette caractéristique de la solubilité du sulfate de sodium peut être expliquée par le fait que la valeur de 32,4 °C correspond à la température à laquelle le composé décahydratée du sulfate de sodium (sel de Glauber ou mirabilite naturelle) se décompose pour former une phase solide anhydre (thénardite) et un excédent d'eau liquide.
À 10 °C, la solubilité du sulfate de sodium est quatre fois plus faible que celle du chlorure de sodium. En cas de mélange en saumure sulfatée, l'écart est accru.
Le sulfate de sodium est soluble dans le glycérol. Il est soluble dans l'acide sulfurique dilué. Il est insoluble dans l'alcool.
Extraction
La moitié environ de la production mondiale provient de l'extraction de gisements naturels de roches évaporites naturelles, la thénardite, la glaubérite, etc., mais aussi le sel décahydratée, la mirabilite autrefois sel de Glauber, qui précipite en saison hivernale dans les lacs salés ou lagunes salées riches en sulfate[4]. Ces gisements minéraux d'évaporites sont souvent localisés et surtout formés dans des environnements arides.
En 1990, les principaux producteurs de sulfate de sodium naturel étaient le Mexique et l'Espagne (avec chacun environ 500 000 t) suivis par l'URSS, les États-Unis et le Canada (avec chacun environ 350 000 t).
Production industrielle
La seconde moitié de la production mondiale est issue essentiellement de récupérations diverses ou de synthèse via le chlorure de sodium NaCl. Il s'agit de productions ou d'issues secondaires de procédés de l'industrie chimique.
La plus importante survient lors de la production d'acide chlorhydrique à partir de chlorure de sodium et d'acide sulfurique selon le procédé Mannheim entre 800 et 900 °C. Le sulfate de sodium obtenu par synthèse directe est alors appelé « gâteau de sel ».
Il est produit également à partir de dioxyde de soufre, par une réaction plus lente, mais avec une meilleure efficacité à 650 °C, selon le procédé Hargreaves :
Mais il y a surtout les récupérations de diverses fabrications :
- il précipite facilement sous l'aspect de mirabilite dans les saumures ou solutions concentrées de chlorure de sodium, en particulier vers 10 °C ;
- il représente un coproduit de la synthèse du bichromate de potassium ;
- il apparaît nécessairement par rencontre de la base forte et de l'acide fort, les plus communément utilisées en chimie industrielle, soient respectivement la soude caustique et l'acide sulfurique ;
- il est un sous-produit de l'obtention de fibres synthétiques régénérées.
Aux États-Unis et au Royaume-Uni, l'une des principales sources de sulfate de sodium synthétique provient de la fabrication de dichromate de sodium. Il s'agit surtout d'un coproduit de l'obtention de bichromate de potassium.
- 2 Na2CrO4aq + 2 H2SO4aq + H2O → Na2Cr2O7aq. 2 H2O précipité+ Na2SO4aq
Il y a également un grand nombre de procédés industriels au cours desquels un excès d'acide sulfurique est neutralisé par de la soude, ce qui conduit à la production de sulfate de sodium. Cette méthode est également la technique de fabrication la plus aisée en laboratoire :
Le sulfate de sodium est généralement purifié via la forme décahydratée, la forme anhydre ayant tendance à réagir avec les composés à base de fer et avec les composés organiques. La forme anhydre est ensuite produite par chauffage modéré de la forme hydratée.
Utilisation
En 1995, le sulfate de sodium se vendait environ 70 $ la tonne aux États-Unis, ce qui en fait un composé chimique relativement bon marché. La première utilisation du sulfate de sodium à l'heure actuelle est probablement dans le domaine des détergents. Il s'agit à la fois d'une charge, d'un fluidisant et antimottant. C'est un véritable coproduit de tensio-actifs anioniques, une charge avec l'eau qui permet de solubiliser le détergent actif. Ainsi il est présent à hauteur de 25 à 40 % dans les diverses « poudres de machines à laver ».
La consommation totale en Europe était d'environ 1,6 million de tonnes en 2001, dont 80 % dans le domaine des détergents. Cependant, cet usage tend à diminuer avec l'utilisation croissante de détergents sous forme liquide qui ne contiennent pas de sulfate de sodium.
Une des autres applications majeures du sulfate de sodium, tout particulièrement aux États-Unis, est dans l'industrie de la pâte à papier, en particulier le procédé Kraft de traitement de la pâte à papier et les divers procédés de pâte à papier au sulfate, qui en réclame entre 20 et 30 kg·t-1 de pâte malgré les divers recyclages. En pratique, il permet l'obtention de sulfure de sodium Na2S, un réducteur et dépilatoire efficace. La réaction de réduction au carbone a lieu vers 750 °C. Na2SO4 + 2 C → Na2S + 2 CO2
Un litre d'une liqueur blanche industrielle, alcaline, possède entre 150 et 160 g d'alcalis actifs (par exemple 2/3 de soude caustique, moins d'1/3 de sulfure de sodium), 30 à 40 g de carbonate de sodium, 5 à 10 g de sulfate de sodium, 3 à 5 g de Na2S2O3, 0,5 g de Na2SO3.
Les composés organiques présents dans la « liqueur noire » formée au cours de ce procédé sont brûlés pour produire de la chaleur, avec en parallèle une réduction du sulfate de sodium en sulfure de sodium. Cependant, ce procédé a été remplacé dans une certaine mesure par un nouveau procédé, et l'utilisation du sulfate de sodium dans l'industrie papetière américaine a décru de 980 000 t en 1970 à 210 000 t en 1990.
L'industrie du verre, en particulier les verres d'oxydes, est également une grande utilisatrice de sulfate de sodium, avec une consommation d'environ 30 000 t en 1990 aux États-Unis (4 % de la consommation totale). Il est utilisé pour réduire la quantité de petites bulles d'air dans le verre fondu. Il contribue également à fluidifier le verre, et à prévenir la formation de mousse dans le verre fondu durant l'élaboration.
Le sulfate de sodium est utilisé dans l'industrie textile, en particulier au Japon. Il réduit la quantité de charges négatives sur les fibres ce qui facilite la pénétration des teintures. Contrairement au chlorure de sodium, il a l'avantage de ne pas corroder les instruments en acier inoxydable utilisés pour la teinture.
Comme charge blanche ou mate, voire comme fluidifiant et ajusteur de viscosité pratique, il est encore présent dans les encres et les colorants, ou les mélanges réfrigérants.
En laboratoire, le sulfate de sodium anhydre est utilisé comme agent de séchage pour les solutions organiques.
Le sel de Glauber, c'est-à-dire la mirabilite ou sulfate de sodium décahydratée, était utilisé dans le passé comme laxatif. Il a également été proposé pour stocker la chaleur dans des systèmes passifs de chauffage solaire. Cette utilisation profite de ses propriétés de solubilité inhabituelle, ainsi que de sa chaleur de cristallisation élevée (78,2 kJ·mol-1).
Il entre dans la composition des émulseurs anti-incendie AFFF (Agent Formant un Film Flottant), notamment pour les extincteurs à eau pulvérisée avec additif[5].
Précautions à prendre
Bien que le sulfate de sodium soit généralement considéré comme non toxique, il convient de le manipuler avec précaution. En effet, étant irritant, il convient de porter des gants et des lunettes de protection lors de sa manipulation.
Bibliographie
- Handbook of Chemistry and Physics, 71e éd., CRC Press, Ann Arbor, Michigan, 1990.
- The Merck Index, 71e éd., Merck & Co, Rahway, New Jersey, États-Unis, 1960.
- W. F. Linke, A. Seidell, Solubilities of Inorganic and Metal Organic Compounds, 4e éd., Van Nostrand, 1965.
- D. Butts, in Kirk-Othmer Encyclopedia of Chemical Technology, 4e éd., vol. 22, p. 403-411, 1997.
- H. Nechamkin, The Chemistry of the Elements, McGraw-Hill, New York, 1968.
- Maria Telkes, Improvements in or relating to a device and a composition of matter for the storage of heat, British Patent no GB694553, 1953.
- Robert Perrin, Jean-Pierre Scharff, Chimie industrielle, Masson, Paris, 1993, 1136 p. en deux tomes avec bibliographie et index (ISBN 978-2-225-84037-1) et (ISBN 978-2-225-84181-1)[6] pour la partie industrielle.
Notes et références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ « Sulfate de sodium » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 23 avril 2009
- ↑ Ce sont des températures de transition thermochimique, qui attestent des modifications structurales de l'état cristallin.
- ↑ La thénardite se transforme rapidement en mirabilite à l'air humide.
- ↑ « Fiche de données de sécurité Artic foam »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur Solbergfoam.com
- ↑ Jean-Pierre Scharff, Robert Perrin, Chimie industrielle, 2e édition, (ISBN 9782100067473)