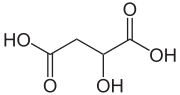
حمض التفاح (أو حمض الماليك) هو حمض عضوي ثنائي الكربوكسيل تنتجه جميع الكائنات الحية, وهو الذي يسبب الطعم الحامض للفواكه كما أنه يستخدم كمنكه للطعام. صيغته HO2CCH2CHOHCO2H. تعرف أملاح وإسترات حمض الماليك بالمالات, حيث يعتبر أنيون المالات وسيط في دورة حمض الستريك.
| حمض التفاح | |
|---|---|
DL-Malic acid
| |
| الاسم النظامي (IUPAC) | |
hydroxybutanedioic acid |
|
| أسماء أخرى | |
L-Malic acid |
|
| المعرفات | |
| رقم CAS | 6915-15-7  |
| بوب كيم (PubChem) | 525 |
| الخواص | |
| صيغة كيميائية | C4H6O5 |
| كتلة مولية | 134.09 غ.مول−1 |
| الكثافة | 1.609 g cm−3 |
| نقطة الانصهار | 130 °س، 403 °ك، 266 °ف |
| الذوبانية في الماء | 558 g/L (at 20 °C)[1] |
| حموضة (pKa) | pKa1 = 3.40, pKa2 = 5.20 [2] |
| مركبات متعلقة | |
| أنيونات أخرى | حمض التفاح |
| حمض كربوكسيليs ذات علاقة | حمض السكسينيك حمض الطرطريك حمض الفوماريك |
| مركبات ذات علاقة | ن-بوتانول ألدهيد البوتان crotonaldehyde مالات صوديوم |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
أهميته
يلعب المالات دوراً هاماً في الكيمياء الحيوية. ففي التمثيل ضوئي رباعي الكربون يعتبر هو مصدر ثاني أكسيد الكربون في دورة كلفن. وفي دورة حمض الستريك يمثل المالات وسيطاً عبر إضافة مجموعة هيدروكسيل إلى الفومارات.
ينتج المالات بوساطة كربكسلة حمض 2-فوسفونوكسي الأكرليك (الفوسفوينوبيروفيات) في الخلايا الحارسة لأوراق النباتات. ويقوم المالات كأنيون مزدوج بالارتباط بكاتيونات البوتاسيوم خلال دخول المذابات للخلايا الحارسة حتى يحافظ على الاتزان (التعادل) الكهربائي في الخلية. لكن تجمع المذابات في الخلايا الحارسة يؤدي لتقليل قدرة المذيب, مما يتيح للماء دخول الخلية وتوسعة الفوهات (الثقوب) على جدار الخلية.
حمض الماليك في الطعام
تم عزل حمض الماليك لأول مرة من عصير التفاح من قبل كارل فلهلم شيله في 1785, وقد اقترح أنطوان لافوازييه عام 1787 اسم حمض الماليك كاشتقاق من الكلمة اللاتينية "مالوم" والتي تعني التفاح. هذا ويعتبر حمض الماليك المسبب للطعم الحامض للتفاح الأخضر, كما أنه يتواجد في العنب والنبيذ بتركيز يصل إلى 5 جم/لتر. وتؤدي عملية التخمير المالولاكتيكي عمل تحويل حمض الماليك لحمض اللاكتيك الأقل حمضية. ينتج حمض الماليك طبيعياً في جميع الفواكه وعدة أنواع من الخضراوات؛ حيث ينتج من عمليات الأيض (عمليات البناء والهدم).
يستخدم حمض الماليك في صناعة السكاكر شديدة الحموضة مكان حمض الستريك, وتوجب القوانين العالمية وضع تحذير من الاستهلاك الشديد لهذه السكاكر بسبب تسبب كثرة حمض الماليك بتهيج الفم, ويوضع عليها الرقم E296. يعتبر حمض الماليك موافق عليه للاستخدام كمنكه للطعام في الاتحاد الأوروبي, الولايات المتحدة, أستراليا, ونيوزيلندا.
التصنيع والتفاعلات الرئيسة (الخواص الكيميائية)
ينتج حمض الماليك صناعياً بالهدرجة المزدوجة لأنهدريد المالايك. وقد وصل الإنتاج الأميركي عام 2000 إلى 5000 طن/سنة. هذا وينتج من هذا التفاعل ناتجين رئيسي وثانوي يتم فصلهما بوساطة تحليل كايرل.
كما أن التكثف الذاتي لحمض الماليك في وجود حمض الكبريتيك الدخاني (حمض الكبريتيك المؤكسد بوساطة تلامسه مع أكسجين الهواء الجوي) ينتج عنه حمض الكوماليك حسب التفاعل التالي:
وجديرُ بالذكر أنه كان لحمض الماليك دوراً هاماً في اكتشاف دورة والدن.
تنصهر أحماض التفاح عند درجة 100 مئوية ْ، وإذا سخنت حتى تصل إلى درجة 150 ْمئوية فإناه تفقد جزيئاً من الماء ليتحول إلى حمض الفوماريك, ويتحول من جراء حمض الآزوت إلى حمض الحماض. ويمتزج حمض التفاح مع القلويات مشكلا نوعين من الأملاح أحدهما معتدل والثاني حامض.
الاستخدام الصيدلاني
يُعتبر حمض المالئيك حمض خفيف في الأشكال الصيدلانية كما يُستخدم كمضاد للأكسدة و عامل مطعم و مفرز للعاب، كما أن لها بعض الاستخدامات العلاجية حيث يُستعمل كثيراً في الأشكال الصيدلانية لتحقيق درجات حموضة معينة ، كما أنه يمتلك نكهة التفاح لذلك فهو يدخل في الأشكال الصيدلانية كمطعم لتقنيع الطعم المر و إضفاء الطعم الحامض ، كما و يمكن له أن يحل مكان حمض الليمون في المساحيق الفوّارة و الغسولات الفموية و مضغوطات تنظيف الأسنان.
يملك حمض المالئيك خواصاً مُضادة للأكسدة حيث يُستخدم بالمشاركة مع بوتيل هيدروكسي تولوين لتدعيم الفعل المُضاد للأكسدة خاصة في الزيوت النباتية و المنتجات الغذائية، وغالباً ما يُضاف بتراكيز أعلى من 420 جزء من مليون جزء (420 ppm) .
علاجياً
يُطبق حمض المالئيك موضعياً مع حض البنزوئين و حمض الصفصاف لمعالجة الحروق و القروح و الجروح .
التأثير على صحة الجسم
لقد صنف حمض المالئيك عند استخدامه في المستحضرات الصيدلانية الفموية و الموضعية والحقنية و المنتجات الغذائية من فئة المواد غير السامّة و غير المخرشة إلا أن محاليله المركزة تُعتبر مخرشة للجلد و الأعين .
التنافرات
يمكن أن يتفاعل مع المؤكسدات.
طالع
- حمض الماليك
المصادر
- Handbook of Pharmaceutical Excipients SIXTH EDITION Edited by Raymond C Rowe BPharm, PhD, DSC, FRPharmS, FRSC, CPhys, MInstP Chief Scientist Intelligensys Ltd, Stokesley, North Yorkshire, UK Paul J Sheskey BSc, RPh Application Development Leader The Dow Chemical Company, Midland, MI, USA Marian E Quinn BSc, MSc Development Editor Royal Pharmaceutical Society of Great Britain, London, UK
المراجع
- chemBlink Online Database of Chemicals from Around the World - تصفح: نسخة محفوظة 30 أكتوبر 2013 على موقع واي باك مشين.
- Dawson, R. M. C. et al., Data for Biochemical Research, Oxford, Clarendon Press, 1959.