
Une réaction d'oxydoréduction ou réaction rédox est une réaction chimique au cours de laquelle se produit un transfert d'électrons. Elle consiste en une réaction oxydante couplée à une réaction réductrice. L'espèce chimique qui capte les électrons est l'oxydant et celle qui les cède, le réducteur. La réaction est caractérisée par une variation du nombre d'oxydation (n.o.) de chacune des espèces en jeu. Les réactions d’oxydoréduction peuvent libérer de l’énergie (réaction exergonique ou exothermique) ou en absorber (réaction endergonique ou endothermique).
Un exemple de réaction d'oxydoréduction est la formation de rouille, où le fer est le réducteur et l'oxygène l'oxydant :
La famille des réactions d'oxydoréduction est très large. Elles se produisent lors des combustions, pendant certains dosages métallurgiques, durant la corrosion des métaux, dans les phénomènes d'électrochimie, la respiration cellulaire et la photosynthèse. Cette diversité s'explique par la mobilité de l'électron, sa faible masse et son ubiquité dans la matière.
Définitions et histoire
Premières définitions
En 1772, Antoine Lavoisier met en évidence le rôle du dioxygène dans certaines réactions d'oxydoréduction à la suite d'expériences avec le mercure. Il pose les premières définitions[1] :
- l'oxydation signifie « combinaison avec l'oxygène ».
Dans le langage courant, l'oxydation est la réaction chimique dans laquelle un composé chimique (par exemple) se combine avec un ou plusieurs atomes d'oxygène, comme l'oxydation du fer (Fe) qui produit la rouille : 4 Fe + 3 O2 ⟶ 2 Fe2O3.
Ce n'est qu'au XXe siècle, après la découverte de l'électron par Joseph John Thomson (1897) et l'introduction du modèle atomique de Bohr (1913), que les réactions chimiques sont réexaminées à la lumière de ces nouveaux modèles et que des similitudes observées permettent de dégager progressivement le concept actuel d'oxydoréduction, soit des transferts d'électrons[2].
Les réactions d'oxydoréduction par voie sèche (échange de dioxygène) sont décrites par les diagrammes d'Ellingham.
En milieu aqueux, l'équation de Nernst est utilisée afin d'étudier les aspects thermodynamiques des réactions d'oxydoréduction et la relation de Butler-Volmer pour en étudier les aspects cinétiques.
Définitions plus modernes
Chaque atome d'un composé est associé à un nombre d'oxydation (n.o.), qui symbolise la valeur de la charge portée[3]. Par exemple, l'ion Fe2+, appelé ion ferreux « fer(II) », a un nombre d'oxydation égal à 2.
Une oxydation est une perte d'électrons (donc une augmentation du n.o., les électrons étant chargés négativement). Ce don d'électrons ne se produit que si un corps est susceptible de les recevoir.
Le phénomène inverse (acceptation des électrons) est la réduction. Une réduction est un gain d'électrons (donc une diminution du n.o.).
Les « combinaisons avec l'oxygène » ne sont qu'un cas particulier des réactions d'oxydoréduction, elles sont donc possibles sans oxygène.
Par exemple : Cu + Cl2 ⟶ CuCl2 combine le cuivre et le dichlore. Le chlore acquiert un électron dans le processus, c'est donc l'oxydant, et le cuivre perd ses électrons, c'est donc le réducteur[4].
Le chlore et l'oxygène ont un point commun : ce sont des éléments plus électronégatifs que le cuivre.
L'oxydation d'un corps s'accompagne toujours de la réduction d'un autre (les électrons ne peuvent pas circuler seuls et sont nécessairement captés), dans la réaction d'oxydoréduction. L'oxydation est une demi-réaction de l'oxydoréduction et la réduction est l'autre demi-réaction.
Occurrence
Les réactions d'oxydoréduction jouent un rôle important dans le domaine de la biologie, notamment dans la photosynthèse[5] et la respiration cellulaire[6]. Elles sont aussi fréquemment utilisées dans l'industrie métallurgique, l'oxydoréduction étant la base de l'extraction de la quasi-totalité des métaux[7], comme le fer ou l'aluminium (par exemple, la fonte est obtenue par réduction d'oxyde de fer, puis par oxydation pour former le fer et l'acier).
Principes
Couples oxydant-réducteur
Dans une réaction d'oxydoréduction, l'élément qui cède un ou des électron(s) est appelé « réducteur » et l'élément qui capte un ou des électron(s) est appelé « oxydant »[8].
Le « couple oxydant-réducteur » (aussi appelé « couple redox ») se compose de l'oxydant et du réducteur conjugué (l'oxydant réduit). Il est toujours noté sous la forme : « oxydant / réducteur ».
Oxydation
La réaction d'oxydation est notée Réd = Ox + n e−, Réd étant le réducteur et Ox l'oxydant de la réaction. Cette équation peut être notée avec une flèche (⟶) si la réaction est totale (c'est-à-dire si la constante d'équilibre K est supérieure à 10 000, K dépendant de la réaction).
L'oxydation est une demi-équation de l'oxydoréduction.
Réduction
La réaction de réduction est notée Ox + n e− = Réd, Réd étant le réducteur et Ox l'oxydant de la réaction). Cette équation peut être notée avec une flèche (⟶) si la réaction est totale (c'est-à-dire si K est supérieure à 10 000 (K dépend de la réaction)).
La réduction est une demi-équation de l'oxydoréduction.
Oxydoréduction

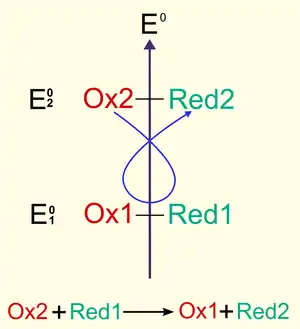
La réaction d'oxydoréduction est l'addition d'une oxydation et d'une réduction (de manière à simplifier les électrons). L'équation d'une oxydoréduction s'écrit de la manière suivante[9] :
- Ox1 + Réd2 = Ox2 + Réd1, avec Ox1 / Réd1 et Ox2 / Réd2 des couples oxydant-réducteur.
En biochimie, notamment à propos de la synthèse de molécules, les réactions se produisent dans une atmosphère oxydante, c'est-à-dire en présence d'oxygène, par opposition à une atmosphère réductrice, contenant par exemple du gaz carbonique.
Certains composés chimiques sont aussi bien des oxydants que des réducteurs. C'est notamment le cas de l'eau oxygénée, qui se dismute et qui ne peut être conservée longtemps :
soit finalement :
- 2 H2O2 ⟶ 2 H2O + O2.
Par exemple, les couples oxydant-réducteur Cu2+/Cu et Zn2+/Zn donnent la réaction en solution aqueuse :
Cette réaction peut se décomposer en une réduction de l'oxydant et une oxydation du réducteur :
- Zn(s) = Zn2+(aq) + 2 e− (oxydation) ;
- Cu2+(aq) + 2 e− = Cu(s) (réduction).
Les deux demi-équations d'oxydation et de réduction peuvent réellement être séparées dans certains cas (si elles sont suffisamment éloignées), ce qui permet de générer un courant électrique (processus à l'œuvre dans la pile électrique). Dans les autres cas, comme dans l'exemple donné, elles n'ont qu'un intérêt formel (les électrons libres n'existent pas dans l'eau).
Équilibre des équations de réaction
Une réaction d'oxydoréduction est équilibrée pour assurer un transfert exact des électrons en jeu. La rédaction de certaines réactions nécessite d'équilibrer les coefficients stœchiométriques des demi-équations pour retrouver le nombre exact des espèces chimiques mises en jeu. Il faut parfois pour cela ajouter des molécules ou des ions en solution (en fonction du milieu).
Par exemple, pour la réaction entre le permanganate de potassium (couple MnO4−/Mn2+) et une solution de fer (couple Fe3+/Fe2+), en milieu acide (présence d'ions H+) :
(Fe2+ = Fe3+ + e−) (oxydation)
(MnO4− + 8 H+ + 5 e− = Mn2+ + 4 H2O) (réduction)
MnO4− + H+ + Fe2+ = Mn2+ + H2O + Fe3+
L'équation est fausse car il y a une différence de 3 e− entre les deux parties. Il faut donc ajuster le nombre de molécules porteuses de ses charges :
- (Fe2+ = Fe3+ + e−) × 5 (oxydation) ;
- (MnO4− + 8 H+ + 5 e− = Mn2+ + 4 H2O) × 1 (réduction) ;
L'équation correcte est : MnO4− + 8 H+ + 5 Fe2+ = Mn2+ + 4 H2O + 5 Fe3+.
Pour équilibrer une équation d'oxydoréduction, il faut combiner linéairement les demi-réactions (oxydation et réduction) afin que le nombre d'électrons donnés soit exactement le nombre d'électrons acceptés : la réaction redox est un échange strict d'électrons (thermodynamiquement favorable).
Par exemple :
Dans ce cas, il faut trouver le plus petit commun multiple de 3 et de 4, soit 12, de manière à avoir un bilan d'échange strict : il faut donc combiner quatre fois la première demi-réaction (le fer va fournir 12 électrons) avec trois fois la seconde demi-réaction (le dioxygène va accepter 12 électrons), soit : 4 Fe + 3 O2 ⟶ 4 Fe3+ + 6 O2−. C'est l'échange d'électrons qui constitue le phénomène d'oxydoréduction.
Ensuite, il se produit une attraction électrostatique : les charges positives et les charges négatives s'attirent et se disposent de manière à former un cristal ionique neutre : 4 Fe3+ + 6 O2− ⟶ 2 Fe2O3.
Ce n'est pas une réaction chimique à proprement parler, mais une réécriture correspondant à l'attraction statique dans le cristal ionique (une hématite).
Potentiel d'oxydoréduction
Le caractère « oxydant » ou « réducteur » est relatif dans le cadre d'une réaction chimique. Un élément réducteur dans une réaction peut être oxydant dans une autre. Il est possible de construire une échelle de force oxydante (ou, dans l'autre sens, de force réductrice) : c'est le potentiel d'oxydoréduction, qui se mesure en volts. Ce potentiel peut dépendre du contexte chimique, notamment du pH, et du contexte physique : les effets de la lumière interviennent dans la photosynthèse et dans la photographie.
Principaux couples d'oxydants-réducteurs
Tous les couples d'oxydant-réducteur s'écrivent sous la forme Ox/Réd. Ils sont classés de l'oxydant le plus fort au plus faible, ou du réducteur le plus faible au plus fort, et on indique la valeur de leur potentiel en volts (à 25 °C et à 1 013 hPa).
| Oxydant/Réducteur | E0 (V) |
|---|---|
| F2 / F− | +2,87 |
| S2O82− / SO42− | +2,01 |
| H2O2 / H2O | +1,77 |
| MnO4− / MnO2 | +1,69 |
| MnO4− / Mn2+ | +1,51 |
| Au3+ / Au | +1,50 |
| PbO2 / Pb2+ | +1,45 |
| Cl2 / Cl− | +1,36 |
| Cr2O72− / Cr3+ | +1,33 |
| MnO2 / Mn2+ | +1,23 |
| O2 / H2O | +1,23 |
| Br2 / Br− | +1,08 |
| NO3− / NO | +0,96 |
| Hg2+ / Hg | +0,85 |
| NO3− / NO2− | +0,84 |
| Ag+ / Ag | +0,80 |
| Fe3+ / Fe2+ | +0,77 |
| O2 / H2O2 | +0,68 |
| I2 / I− | +0,62 |
| Cu2+ / Cu | +0,34 |
| CH3CHO / C2H5OH | +0,19 |
| SO42− / SO2 | +0,17 |
| S4O62− / S2O32− | +0,09 |
| H+ / H2 | +0,00 |
| CH3CO2H / CH3CHO | −0,12 |
| Pb2+ / Pb | −0,13 |
| Sn2+ / Sn | −0,14 |
| Ni2+ / Ni | −0,23 |
| Cd2+ / Cd | −0,40 |
| Fe2+ / Fe | −0,44 |
| Zn2+ / Zn | −0,76 |
| Al3+ / Al | −1,66 |
| Mg2+ / Mg | −2,37 |
| Na+ / Na | −2,71 |
| Ca2+ / Ca | −2,87 |
| K+ / K | −2,92 |
| Li+ / Li | −3,05 |
Le métabolisme cellulaire des organismes vivants repose sur des réactions d'oxydoréduction, que ce soit pour des processus de biosynthèse (des acides gras, de néoglucogenèse...), de dégradation de molécules biochimiques (glycolyse) ou de production d'énergie (chaîne respiratoire mitochondriale). Les couples les plus utilisés sont :
- NAD+ / NADH+H+ (Nicotinamide adénine dinucléotide) ;
- NADP+ / NADPH+H+ (Nicotinamide adénine dinucléotide phosphate) ;
- FAD / FADH2 (Flavine adénine dinucléotide).
Réactions d'oxydoréduction sans transfert évident d'électrons
La plupart des informations de cette section sont extraites de trois ouvrages cités dans la bibliographie :
- Paul Arnaud, Cours de chimie physique, 3e éd., Dunod ;
- Maurice Bernard, Cours de chimie minérale, 2e éd., Dunod ;
- pour les règles et les recommandations concernant la nomenclature : International Union of Pure and Applied Chemistry (IUPAC), Nomenclature of Inorganic Chemistry, Recommendations 1990, Blackwell Science.
Problématique
Dans certaines réactions d'oxydoréduction, notamment en phase sèche (c'est-à-dire en milieu non aqueux, souvent à haute température), il n'y a pas de transfert évident d'électrons. On peut citer par exemple le cas de la combustion de l'hydrogène dans l'oxygène de l'air : 2 H2 + O2 ⟶ 2 H2O.
Selon la définition ancienne, l'élément hydrogène, qui s'est combiné avec l'élément oxygène, a subi une oxydation.
Mais les réactifs H2 et O2 et le produit H2O sont des molécules ; aucun ion, qui permettrait une interprétation en termes de transfert d'électrons, n'est présent dans les espèces chimiques impliquées.
Généralisation de la notion de transfert d'électrons
Cela s'explique par l'électronégativité. Cette grandeur caractérise la capacité d'un atome de l'élément à capter un ou plusieurs électrons pour devenir un ion négatif. Dans les molécules, les atomes sont liés par des liaisons covalentes du fait de cette électronégativité.
Formation d'une liaison chimique et électronégativité
Atomes de même électronégativité : liaison covalente
Au sens strict, une liaison covalente résulte de la mise en commun d'une ou plusieurs paires d'électrons (doublets partagés ou doublets liants) entre deux atomes identiques (cas des liaisons entre atomes dans les molécules H2 et O2 de l'exemple précédent), donc de même électronégativité. Les doublets sont équitablement partagés entre les deux atomes : ceux-ci restent électriquement neutres.
- atomes séparés H • • H ;
- atomes liés H [:] H.
Le doublet liant [:] est (en moyenne) à égale distance des deux atomes H.
Atomes d'électronégativités différentes : liaisons ionique, covalente polarisée, iono-covalente
Transfert total d'électrons entre les atomes : formation d'une liaison ionique
Lorsque la différence d'électronégativité ΔEn entre les atomes est importante (typiquement ΔEn > 2), les électrons de liaison sont fortement déplacés vers l'atome le plus électronégatif, qui les accapare presque totalement. Ce transfert pratiquement total d'électrons fait de cet atome un ion négatif (ou anion) et de l'autre atome un ion positif (ou cation). Comme il n'y a plus à proprement parler de mise en commun d'électrons, il n'y a plus de liaison covalente. La liaison chimique est ici une liaison entre ions ou liaison ionique. Ce type de liaison est un cas limite, jamais atteint à 100 %.
Transfert électronique partiel : liaison covalente polarisée, liaison iono-covalente
Si la différence d'électronégativité est plus faible, le transfert d'électrons entre les deux atomes n'est plus total, mais le transfert partiel de charge négative vers l'atome le plus électronégatif produit un excédent de charge négative sur cet atome (qui porte alors une charge partielle négative, notée δ−) et un déficit de charge négative sur l'autre atome (qui porte alors une charge partielle positive, notée δ+) ; la liaison entre les atomes est une liaison covalente polarisée (lorsque la polarisation est modérée) ou iono-covalente (liaison au caractère « semi-ionique », lorsque la polarisation est notable, typiquement pour 1 < ΔEn < 2).
Cl est plus électronégatif que H : dans la molécule HCl, le doublet liant est décalé vers Cl :
H [:] Cl.
| Type de liaison | Transfert électronique entre atomes |
Position moyenne du doublet [:] = doublet liant |
Modèle (doublet liant = ——) |
|---|---|---|---|
| Covalente | aucun | H [:] H | H —— H |
| Covalente polarisée ou iono-covalente |
partiel | H [:] Cl | δ+H —— Clδ− |
| Ionique (attraction électrostatique) |
total | Na :Cl | Na+Cl− |
Transfert total d'électrons
Soit la combustion du sodium Na dans le dioxygène :
L'élément O est beaucoup plus électronégatif que l'élément Na : le transfert d'électrons est pratiquement total; on peut appliquer à Na2O le modèle ionique : ce composé est constitué d'ions Na+ et O2−.
L'interprétation de la réaction en termes d'oxydoréduction ne pose pas de problème :
Transfert total fictif (virtuel)
Par convention, on décide d'appliquer la même méthode aux composés covalents. Pour cela, on attribue d'une manière fictive tous les électrons de liaison à l'atome de l'élément le plus électronégatif. On est ainsi ramené au cas précédent : le transfert partiel d'électrons est fictivement considéré comme total.
Application à la réaction 2 H2 + O2 ⟶ 2 H2O
Dans la molécule d'eau, les électrons de liaison sont attribués à l'atome O, le plus électronégatif. L'eau devient un composé ionique fictif, constitué d'ions fictifs H+ et O2−. La réaction s'interprète alors comme dans le cas précédent :
Nombre d'oxydation d'un élément
Le nombre d'oxydation (n.o.) ou degré d'oxydation (d.o.) représente la charge de chaque ion fictif de l'élément dans l'espèce chimique considérée.
On l'exprime en chiffres romains pour le différencier de la charge d'un ion réel.
Dans la molécule H2O :
- le nombre d'oxydation de l'hydrogène, noté n.o.(H), correspond à la charge de l'ion fictif H+. On a donc : n.o.(H) = +I ;
- le nombre d'oxydation de l'oxygène, noté n.o.(O), correspond à la charge de l'ion fictif O2−. On a donc : n.o.(O) = –II.
Dans les molécules symétriques H2 et O2, la charge de chaque atome est nulle et le nombre d'oxydation de chaque élément est égal à zéro :
- n.o.(H2) = n.o.(O2) = 0 (il n'existe pas de chiffre romain pour représenter le zéro).
Au cours de la réaction :
- H est oxydé et son n.o. a augmenté de 0 à +I ;
- O est réduit et son n.o. a diminué de 0 à –II.
Généralisation de l'oxydoréduction
- Toute augmentation (en valeur algébrique) du n.o. est une oxydation.
- Toute diminution (en valeur algébrique) du n.o. est une réduction.
Cette définition est plus générale que celle se limitant à des échanges réels d'électrons. Elle est applicable aussi bien à un transfert partiel qu'à un transfert total d'électrons.
Utilisation des nombres d'oxydation
Reconnaître les réactions d'oxydoréduction
Si, au cours d'une réaction, on n'observe aucune variation des n.o. des éléments, cette réaction n'est pas une réaction d'oxydoréduction.
Exemple 1 : H2 (g) + Cl2 (g) ⟶ 2 HCl
- Réactifs (cas d'une molécule symétrique) :
- H2 n'est pas un composé ionique, donc n.o.(H) = 0 ;
- Cl2 n'est pas un composé ionique, donc n.o.(Cl) = 0.
- Produit : dans la molécule d'HCl, Cl est plus électronégatif que H (d'après le modèle ionique fictif de la molécule H+Cl−), on a donc :
- n.o.(Cl) = –I ;
- n.o.(H) = +I. Au cours de la réaction, le n.o.(H) augmente de 0 à +I et le n.o.(Cl) diminue de 0 à –I : cette réaction est une réaction d'oxydoréduction.
Exemple 2 : CaO + 2 HCl ⟶ CaCl2 + H2O
- D'après l'échelle d'électronégativité des éléments (échelle de Pauling) : χO > χCl > χCa > χH (l'électronégativité d'un élément se représentant par la lettre grecque χ).
- Réactifs (cas d'une molécule symétrique) :
- CaO est un composé ionique de modèle Ca2+O2−, donc n.o.(Ca) = +II et n.o.(O) = –II ;
- HCl est aussi un composé ionique de modèle H+Cl−, donc n.o.(H) = +I et n.o.(Cl) = –I.
- Produits : dans la molécule d'HCl, Cl est plus électronégatif que H (d'après le modèle ionique fictif de la molécule H+Cl−), on a donc :
- CaCl2 est un composé ionique de modèle Ca2+2Cl−, donc n.o.(Ca) = +II et n.o.(Cl) = –I ;
- H2O est également un composé ionique de modèle 2H+O2−, donc n.o.(H) = +I et n.o.(O) = –II. Au cours de la réaction, aucune variation de n.o. n'est observée : cette réaction n'est pas une réaction d'oxydoréduction.
Équilibrer les équations-bilans de réactions d'oxydoréduction
Les variations des n.o., notées « Δn.o. », correspondent à un transfert de charges des réducteurs vers les oxydants. La charge totale gagnée par les oxydants est donc égale à la charge totale cédée par les réducteurs.
Exemple
- Équilibrer l'équation suivante : a HCl + b O2 ⟶ c Cl2 + d H2O.
Pour la commodité des calculs, on peut provisoirement représenter les n.o. par des chiffres arabes. - Réactifs :
- HCl est un composé ionique de modèle H+Cl− : Donc n.o.(H) = 1 et n.o.(Cl) = –1 ;
- O2 n'est pas un composé ionique : Donc n.o.(O) = 0.
- Produits :
- Cl2 n'est pas un composé ionique, donc n.o.(Cl) = 0 ;
- H2O est un composé ionique de modèle 2H+O2−, donc n.o.(H) = 1 et n.o.(O) = –2.
- Au cours de la réaction :
- n.o.(H) ne varie pas : Δn.o.(H) = 0 ;
- n.o.(Cl) augmente, passant de –1 à 0 : Δn.o.(Cl) = 0 – (–1) = 1 ;
- n.o.(O) diminue, passant de 0 à –2 : Δn.o.(O) = –2 – 0 = -2. La charge totale cédée par les atomes de chlore Cl et celle captée par les atomes d'oxygène O doivent se compenser (conservation des charges pendant la réaction). Δn.o.(O) + Δn.o.(Cl) = –2 + 2 × 1 = 0. Donc une molécule de O2 est compensée par quatre molécules de HCl (a = 4 b).
- Il ne reste donc plus qu'à équilibrer les produits de manière à conserver tous les éléments.
- 4 HCl + O2 ⟶ 2 Cl2 + 2 H2O.
Remarque
Dans le cas général où les multiplicateurs a, b, c, d, etc. sont tous différents de 1, on calcule le plus petit commun multiple (ppcm) p de ces multiplicateurs.
On écrit ensuite : a ∨ b ∨ c ∨ d ∨ , etc. = p.
Nommer certains composés chimiques
L'écriture des formules et la dénomination des composés chimiques sont codifiées par l'UICPA.
Les n.o. sont utilisés dans la nomenclature principalement lorsqu'un élément peut présenter plusieurs états d'oxydation.
Quelques cas
Cations monoatomiques
On nomme les cations monoatomiques en ajoutant entre parenthèses, après le nom de l'élément, soit le nombre de charges approprié suivi du signe plus, soit le nombre d'oxydation (chiffre romain). Le nom est précédé du terme « ion » ou « cation ».
Exemple
- Les éléments sodium, calcium et aluminium ne présentent qu'un seul degré d'oxydation ; il n'y a donc pas d'ambiguïté sur la charge du cation, on peut l'omettre dans le nom :
- Na+ : ion sodium ; Ca2+ : ion calcium ; Al3+ : ion aluminium ;
- l'élément fer présente plusieurs degrés d'oxydation : Fe2+ appelé ion ferreux fer(II) et Fe3+ appelé ion ferrique fer(III).
Composés solides
D'une manière générale, les noms des composés chimiques sont basés sur les proportions de leurs constituants.
Cristaux ioniques
Remarque préliminaire : les proportions des ions constituant un cristal ionique sont déterminées par la condition de neutralité électrique de l'ensemble.
- CaCl2 (de modèle Ca2+2Cl−) est formé par un ion Ca2+ et deux ions Cl− : nom systématique = dichlorure de monocalcium.
Règle : le préfixe « mono- » est toujours omis, sauf pour éviter des confusions.
CaCl2 : dichlorure de calcium ; une deuxième simplification est encore envisageable :
Recommandation : si les composés contiennent des éléments tels qu'il n'est pas nécessaire de préciser les proportions, par exemple quand le degré d'oxydation est habituellement invariant, ces proportions n'ont pas besoin d'être fournies.
CaCl2 est le seul composé constitué des éléments Ca et Cl : nom = chlorure de calcium, préféré à dichlorure de calcium.
- NaCl (de modèle Na+Cl−) est le seul composé constitué des éléments Na et Cl : nom = chlorure de sodium.
Cristaux iono-covalents
- AlCl3 est le seul composé constitué des éléments Al et Cl : nom = chlorure d'aluminium.
- Oxydes de fer - Fe présente deux degrés d'oxydation (II et III) ; il existe trois oxydes différents : Fe2O3, FeO et Fe3O4.
| Formule de l'oxyde | Proportion des constituants | Nom | Modèle ionique fictif | Nom basé sur les n.o. de Fe |
|---|---|---|---|---|
| Fe2O3 | 3 atomes O pour 2 atomes Fe | trioxyde de difer | 2Fe3+3O2− | oxyde de fer(III) |
| FeO | 1 atome O pour 1 atome Fe | monoxyde de fer (comparer à CO : monoxyde de carbone) |
Fe2+O2− | oxyde de fer(II) |
| Fe3O4 | 4 atomes O pour 3 atomes Fe | tétraoxyde de trifer | Fe2+2Fe3+4O2− oxyde mixte |
oxyde de fer(II) et de fer(III) |
Notes et références
- ↑ « oxydoréduction », dictionnaire Larousse.
- ↑ Pierre-François Thomas, Précis de physique-chimie: cours et exercices, Bréal, (ISBN 978-2-7495-0591-6, lire en ligne), p. 69.
- ↑ « Oxydoréduction », sur www2.chm.ulaval.ca (consulté le ).
- ↑ Claudine Buess-Herman, Josette Dauchot-Weymeers et Thomas Doneux, Chimie analytique, De Boeck, (ISBN 978-2-8041-9071-2), p. 442.
- ↑ Jack Farineau et Jean-François Morot-Gaudry, La photosynthèse: Processus physiques, moléculaires et physiologiques, Quae, (ISBN 978-2-7592-2667-2, lire en ligne), p. 29.
- ↑ Hubert H. Girault, Électrochimie physique et analytique, PPUR presses polytechniques, (ISBN 978-2-88074-673-5, lire en ligne), p. 60.
- ↑ Brigitte Charpentier, Alain Harlay, Florence Hamon-Lorleac'h et Lionel Ridoux, Guide du préparateur en pharmacie, Elsevier Masson, (ISBN 978-2-294-70290-7, lire en ligne), p. 44.
- ↑ Un moyen mnémotechnique utilise les voyelles et les consonnes : réducteur = donneur, oxydant = accepteur.
- ↑ Futura, « Définition | Oxydoréduction - Rédox », sur Futura (consulté le ).
Bibliographie
- (en) Henry Guerlac, Lavoisier — the crucial year: The background and origin of his first experiments on combustion in 1772, 1961
- (en) Schüring, J., Schulz, H. D., Fischer, W. R., Böttcher, J., Duijnisveld, W. H. (éditeurs), Redox: Fundamentals, Processes and Applications [PDF], Springer-Verlag, Heidelberg, 1999, 246 p. (ISBN 978-3-540-66528-1)
- Paul Arnaud, Cours de chimie physique, 3e éd., Dunod (ISBN 2 10 001640 7)
- Maurice Bernard, Cours de chimie minérale, 2e éd., Dunod (ISBN 2 10 002067 6)
- (en) International Union of Pure and Applied Chemistry (IUPAC), Nomenclature of Inorganic Chemistry, Recommendations 1990, Blackwell Science (ISBN 0-632-02494-1)
Voir aussi
Articles connexes
- Auto-oxydation
- Combustion
- Combustible
- Comburant
- Corrosion
- Coupellation
- Électrochimie
- Feu
- Liste de potentiels standard
- Oxydation à haute température
- Oxydation et réduction en chimie organique
- Oxyde
Liens externes
- Table des potentiels standard courants [PDF], sur sbeccompany.fr
- Site internet déterminant les demi-équations électroniques, sur wsphynx.com