فيتامين د (Vitamin D) هو فيتامين من مجموعة السيكوسترويد القابلة للذوبان في الدهون. يعتبر فيتامين(د) في البشر فريد من نوعه لأنه يمكن تناوله على أنه كوليكالسيفيرول (فيتامين د3) أو إركوكالسيفـرول (فيتامين د2) ولأن الجسم يمكن أيضاً أن يصنعها (من الكوليسترول) عند التعرض الكافي لأشعة الشمس (ومن هنا لقب بـ"فيتامين أشعة الشمس").
على الرغم من أن فيتامين (د) يسمى فيتاميناً، إلا أنه ليس بالفيتامين الغذائي الأساسي بالمعنى الدقيق، حيث أنه يمكن تصنيعه بكميات كافية من أشعة الشمس عند جميع الثدييات. فهو يعتبر مركباً كيميائياً عضوياً (أو مجموعة من المركبات ذات الصلة) ويسمى فيتامين من الناحية العلمية فقط عند عدم استطاعة توليفها بكميات كافية من قبل الكائن حي، وبهذه الحالة يجب الحصول عليها من النظام الغذائي. وكما هو الحال مع المركبات الأخرى تسمى بالفيتامينات، فإن فيتامين(د) تم اكتشافه في المحاولة للحصول على مادة غذائية كانت غائبة عن الأمراض كالكساح (أحد أشكال تلين العظام في مرحلة الطفولة)[1]. بالإضافة إلى ذلك كغيره من الفيتامينات، في العالم الحديث يتم إضافة فيتامين (د) إلى المواد الغذائية الأساسية، كالحليب، لتجنب الأمراض الناتجة عن نقصه.
تعكس قياسات مستويات الدم التكوين الذاتي جراء التعرض لأشعة الشمس وكذلك تناول الغذاء، ويعتقد أن هذا التكوين قد يساعد في الحفاظ على تركيزات كافية للمصل. تشير الدلائل إلى أن تكوين فيتامين (د) من التعرض لأشعة الشمس يعمل في حلقة التغذية المرتدة التي تمنع التسمم، لكن بسبب عدم اليقين بشأن خطر الإصابة بالسرطان من أشعة الشمس، لم تصدر أية توصيات من معهد الطب في الولايات المتحدة الأمريكية لمقدار التعرض للشمس اللازم لتلبية الاحتياجات من فيتامين د. وبناء على ذلك فإن المرجع للكميات الغذائية لفيتامين(د) يفترض أنه لا يحدث تكوين والفيتامين الموجود بالشخص يكون من النظام الغذائي، على الرغم من ندرة حدوثه في الواقع العملي.
تاريخه
- عام 1913 اكتشف الباحثان الأمريكيان إلمر ماكولوم وديفيس مارغريت مادة في زيت كبد سمك القد سميت في ما بعد بـ"فيتامين أ". وقد لاحظ الطبيب البريطاني إدوارد ميلانبي أن الكلاب التي تم تغذيتها بزيت كبد القد لم يتطور الكساح لديها وأستخلص من ذلك إلى أن (فيتامين أ) أو عامل مرتبط يساعد في الوقاية من المرض.
- في عام 1921، أجرى إلمر ماكولوم اختبارا لزيت كبد القد ولكن معدل حيث أزال منه (فيتامين أ). وقد عالج الزيت المعدل الكلاب المريضة، وأستنتج ماكولوم أن عامل في زيت كبد سمك القد مختلف عن (فيتامين أ) هو المسؤول عن الشفاء من الكساح، وقد سماه بـ فيتامين (د) لأنه كان الفيتامين الرابع الذي أطلق عليه اسماً.[2][3][4] ولم يكن معروفا أنه يختلف عن الفيتامينات الأخرى حيث يمكن تصنيعه في جسم الإنسان عن طريق التعرض للأشعة الفوق البنفسجية. وقد ثبت ذلك في عام 1923 عندما تم إشعاع المركب 7-ديهيدروكوليستيرول مع الضوء، ونتج عنه شكل من أشكال الفيتامينات التي تذوب في الدهون (تعرف الآن باسم د3). وبين ألفريد فابيان هيس أن "الضوء يساوي فيتامين د".[5]
- في عام 1928 نال أدولف فينداوس من جامعة غوتنغن في ألمانيا على جائزة نوبل في الكيمياء نظراً لأبحاثه في علاقة الستيرولات بالفيتامينات.[6]
- في عام 1929 عمل فريق من المعهد الوطني للبحوث الطبية في هامبستيد، لندن على التركيبة الهيكلية لفيتامين (د)، الذي كان وقتها لا يزال مجهولا، وكذلك تركيبة الستيرويدات. عقد اجتماع بين كل من جون هالدين، جون ديزموند برنال ودوروثي هودجكن لمناقشة التركيب الهيكلي المحتمل لجزيئات ستيرول، وقد بينت مبحث تصوير البلورات بالأشعة السينية أن جزيئات الستيرول كانت مسطحة، ليست كما اقترحه أدولف فينداوس.
- في عام 1932 نشر كل من أوتو روزنهايم وهارولد كينج ورقة تطرح تركيبة الستيرول وحموض المرارة حيث وجدت قبول سريعا.[7] كان تفكك الأفكار بين أعضاء الفريق (بورديلون، روزنهايم، كينج وكينيث كالو ) مثمر للغاية وأدى إلى عزل ووصف الفيتامين د.[8] لم تكن سياسة مجلس البحوث الطبية البريطاني في هذا الوقت لبراءات الاكتشافات، بل كان يجب أن تكون نتائج البحوث الطبية مفتوحة للجميع. وفي الثلاثينات وضح "فينداوس" التركيب الكيميائي لفيتامين د بشكل أوضح.[9]
- في عام 1923، وضح عالم الكيمياء الحيوية الأمريكي هاري ستينبوك في جامعة ويسكونسن-مادسون أن الأشعاع بواسطة الفوق بنفسجية أدى إلى زيادة محتوى فيتامين د للأطعمة والمواد العضوية الأخرى.[10] اكتشف ستينبوك بعد أن عرض أغذية فئران التجارب على هذه الاشعة، انها قد شفيت هذه الفئران من الكساح. وقد عرف أن نقص فيتامين D هو سبب الكساح، سجلت براءة اختراع ستينبوك باستخدام 300 دولار من ماله الخاص. وقد تم استخدام أسلوبه في تشعيع المواد الغذائية. بعد انتهاء براءة اختراعه في عام 1945، كان الكساح قد أثر على الجميع ولكن تم القضاء عليه في الولايات المتحدة.[11]
الآثار الصحية
آثار مكملات فيتامين(د) غير مؤكدة على الصحة.[12] يبين تقرير معهد الطب في الولايات المتحدة الأمريكية ما يلي: "النتائج المتعلقة بالسرطان، أمراض القلب وارتفاع ضغط الدم والسكري ومتلازمة الأيض، الأداء البدني، المناعة واضطرابات المناعة الذاتية، والالتهابات، أداء الفيزيولوجيا العصبية، ومقدمات الارتعاج قد لا تكون مرتبطة بشكل صحيح مع تناول الكالسيوم أو فيتامين د وغالبا ما تكون متعارضة."[13] يدعي بعض الباحثين أن معهد الطب كان حاسما جدا في توصياته وقد ارتكب أخطاء حسابية عند قياس مستوى فيتامين(د) في الدم المرتبط بصحة العظام.[14] وقد حافظ أعضاء فريق معهد الطب على أستخدام "إجراءات قياسية للتوصيات الغذائية" ويستند التقرير بقوة على البيانات. الأبحاث لا تزال مستمرة عن مكملات فيتامين د، بما فيها التجارب السريرية الواسعة النطاق.[14]
الوفيات
توجد علاقة بين انخفاض مستويات فيتامين-د في الدم وزيادة معدل الوفيات[15]، يبدو أن إعطاء المكملات المدعمة بفيتامين-د3 لكبار السن من النساء في الرعاية قلل من خطر الموت[16]. ولم تثبت فعالية كل من فيتامين-د2[16]، الفاكالسيدول، والكالسيتريول. ومع ذلك، فإن زيادة أو نقصان فيتامين-د قد تسبب أداء غير طبيعي وشيخوخة مبكرة[17][18][19]. فكانت العلاقة بين مستوى الكالسيديول في الدم ومعدل الوفيات على شكل حرف U [13]، يعتبر ضرر نقص فيتامين-د عند ذوي البشرة السوداء أكثر من ذوي البشرة البيضاء[13].
صحة العظام
يتسبب نقص فيتامين د بلين العظام (يسمى الكساح عندما يحدث في الأطفال). وأكثر من ذلك، فقد ارتبط السقوط وانخفاض كثافة المعادن في العظام مع انخفاض مستويات فيتامين د في الدم.[20]
الأدلة على الآثار الصحية لمكملات فيتامين(D) على صحة القلب والأوعية الدموية ضعيفة.[21][22][23] قد تقلل الجرعات المتوسطة إلى العالية من مخاطر أمراض القلب والأوعية الدموية.[21][24]
التصلب المتعدد (اللويحي)
- مقالة مفصلة: التصلب اللويحي
يرتبط انخفاض مستوى فيتامين(D) مع التصلب المتعدد أو اللويحي. وقد يكون لمكملات فيتامين(D) تأثير وقائي لهذا المرض ولكن هناك شكوك وأسئلة لم يرد عليها.[25][26][27] الأسباب التي يعتقد أن نقص فيتامين(D) يكون أحد عوامل الخطر لمرض التصلب المتعدد هي:
- يزداد مرض التصلب المتعدد كلما ابتعدنا عن خط الإستواء، التي تقل فيها مدة وكثافة الأشعة فوق البنفسجية المستمدة من أشعة الشمس وبالتالي تقل تركيزات فيتامين(D).
- انتشار مرض التصلب العصبي المتعدد هو أقل مما كان متوقعا في السكان المتواجدون في مناطق خطوط العرض العالية (القريبة من القطبين الشمالي أو الجنوبي) بسبب الاستهلاك العالي للأسماك الدهنية الغنية بفيتامين(D).
- يقل خطر مرض التصلب المتعدد مع الهجرة من خطوط العرض العالية إلى المنخفضة.[25]
بدأت تجربة سريرية في عام 2011 برعاية شاريتيه (برلين)، ألمانيا تهدف لدراسة فعالية، سلامة وسماحية فيتامين(D3) في علاج التصلب المتعدد.[28][29]
السرطان
يرتبط نقص فيتامين (D) مع بعض أنواع السرطانات ومع النتائج السيئة في بعض السرطانات، ولكن يبدو أن تناول مكملات لا يساعد الذين يعانون من سرطان البروستاتا.[30] حاليا تعتبر الأدلة غير كافية لتدعم المكملات في هذه الأنواع من السرطانات.[30] ونتائج التأثير الوقائي أو الضارة لمكملات فيتامين(D) في الأنواع الأخرى من السرطان غير حاسمة.[12][31]
تأخير الشيخوخة
أجرت كلية كنج (لندن) البريطانية دراسة على أكثر من 2,000 امرأة، فظهرت النتيجة أن اللاتي لديهن مستويات أعلى من فيتامين(D) تأخرت لديهن الشيخوخة بسبب التغيرات في حمضهن النووي (DNA). إن المادة الوراثية داخل كل خلية لديها "ساعة" داخلية، يبدأ العد التنازلي فيها كلما استنسخت الخلية نفسها. الطريقة الوحيدة لدراسة تقدم الشيخوخة على المستوى الخلوي هي قصر التيلوميرات في الحمض النووي. وقد وجد فريق من كلية كنج أنه عندما تتأثر أنسجة الجسم من الالتهابات الكثيرة فإن خلايا الدم البيضاء تميل لمعدلات تقلب أسرع وبالتالي أسرع في تقصير التيلوميرات. جرى البحث في ما مجموعه 2160 امرأة تتراوح أعمارهن بين 18 و 79 وأخذ عينة من مستويات فيتامين(D) في دمائهم، وقارنوا أطوال التيلوميرات في خلايا الدم البيضاء. ووجد الباحثون بعد ضبط النتائج لعمر المتطوعين، أن النساء اللاتي لديهن مستويات فيتامين(D) أعلى كان لديهن تيلوميرات أطول في الخلايا، والعكس بالعكس.
قال البروفيسور برنت ريتشاردز، الذي قاد هذه الدراسة: "أن هذه النتائج مثيرة لأنها تثبت للمرة الأولى أن الناس الذين لديهم مستويات أعلى من فيتامين(D) يكون التقدم بالعمر لديهم أكثر بطء من الناس الذين لديهم مستويات منخفضة من فيتامين(D)، وهذا يمكن أن يساعد على تفسير كيفية أن فيتامين(D) له تأثير وقائي على أمراض كثيرة متصلة بالشيخوخة، مثل أمراض القلب والسرطان."[32]
الربو
قال باحثون بريطانيون إن مقدار تعرض مرضى الربو لأشعة الشمس قد يكون له تأثير على المرض. وقال الفريق الطبي بجامعة كينج إن انخفاض مستويات فيتامين (د)، الذي يكونه الجسم عند التعرض للشمس، يرتبط بتفاقم أعراض هذا المرض. وتظهر أحدث الأبحاث التي أجراها الفريق الطبي أن فيتامين (د) يهدئ جزءا بجهاز المناعة يزداد نشاطه لدى مرضى الربو. إلا أن علاج مرضى الربو عن طريق فيتامين (د) لم يخضع للاختبارات بعد. وقد يجد المصابون بمرض الربو صعوبة في التنفس عندما تصاب الممرات الهوائية في الجهاز التنفسي لديهم بالالتهاب، التورم، والضيق. ويتم علاج أغلب المرضى عن طريق أدوية بمنشطات الستيرويد، لكنها ليست فعالة في جميع الحالات.
وتقول كاثرين هاوريلويز الأستاذة الجامعية وعضو فريق البحث : "نحن نعرف أن من لديهم مستويات عالية من فيتامين (د) أكثر قدرة على السيطرة على مرض الربو، وهذه العلاقة لافتة للنظر جدا". ودرس الباحثون تأثير فيتامين (د) على مادة كيميائية في الجسم، وهي مادة إنترلوكين-17 ، التي تمثل جزءا حيويا من جهاز المناعة الذي يساعد في محاربة العدوى. ولكن يمكن لهذا الجزء أن يتسبب في حدوث مشكلات عند ارتفاع مستوياته بدرجة كبيرة في الجسم، كما أن له علاقة كبيرة بمرض الربو. وفي الدراسة المنشورة بدورية "الحساسية والمناعة السريرية" في بريطانيا، وجد الباحثون أن فيتامين (د) له قدرة على خفض مستويات هذه المادة في الجسم عندما أضيف لعينات الدم التي أخذت من 28 مريضا.
ويجري الفريق حاليا اختبارات سريرية لمعرفة ما إذا كان تزويد المرضى بفيتامين (د) قد يخفف من أعراض مرض الربو لديهم، كما يفحص الفريق المرضى الذين لا يستجيبون للعلاج باستخدام عقاقير الستيرويد، الذين يفرزون مادة انترلوكين-17 أكثر بسبع مرات من المرضى الآخرين. وقالت الباحثة هاوري لويز "نعتقد أن العلاج باستخدام فيتامين (د) قد يجعل المرضى الذين لا يستجيبون للعلاج بعقاقير الستيرويد يستجيبون لهذا العلاج، أو يسمح للمرضى الذين يمكنهم السيطرة على المرض أن يستخدموا جرعات أقل من الستيرويد". وأضافت أن ثقافة الاحتجاب عن الشمس واستخدام الدهانات المضادة للشمس ربما زادت من معدلات الربو، ولكن "هذه رسالة حذرة، لأن التعرض كثيرا جدا للشمس أمر ضار أيضا."
وتقول مليكة رحمن من مؤسسة الربو البريطانية الخيرية "بالنسبة لغالبية الأشخاص المصابين بمرض الربو، تعد العقاقير المتاحة حاليا طريقة فعالة للتعامل مع المرض، لكننا نعلم أنها ليست فعالة في جميع الحالات، وهو ما يجعل إجراء أبحاث للتوصل لطرق جديدة للعلاج أمرا مهما". وتضيف "ونعلم أيضا أن الكثير من الأشخاص الذين يعانون من مرض الربو لديهم مخاوف بشأن الأعراض الجانبية للعقاقير، وبالتالي إذا أمكن لفيتامين (د) أن يخفض من جرعات هذه العقاقير، فسيكون لهذا تأثير كبير على طبيعة حياة هؤلاء الأشخاص. كما أننا نتطلع إلى التعرف على نتائج الاختبارات السريرية".[33]
هرمون التستوستيرون
تعتبر المسالك في الجهاز التناسلي الذكري أحد الأنسجة المستهدفة لفيتامين(D)، وتبين إلى وجود علاقة بين مركب (25(OH)D) مع مستويات هرمون التستوستيرون لدى الرجال، فكلما زاد مستوى فيتامين(D) زاد مستوى هرمون التستوستيرون.
أخرى
يبدو أن لفيتامين (D) آثار على وظيفة المناعة.[34] كما أنه من المفترض أن له دور بالإصابة بالأنفلونزا مع نقص مركبات فيتامين (D) خلال فصل الشتاء، وهذا يفسر ارتفاع معدلات حالات العدوى بالأنفلونزا خلال فصل الشتاء.[35] يبدو أن تدني مستويات فيتامين(D) تعتبر أحد العوامل الخطرة لمرض السل،[36] وقديما كانت تستخدم كعلاج،[37] واعتبارا من عام 2011 جرت ابحاث في التجارب السريرية التي تسيطر عليها.[37] قد يلعب فيتامين(D) أيضا دورا في فيروس العوز المناعي البشري.[38] بالرغم من وجود بيانات مبدئية تربط انخفاض مستويات فيتامين(D) بمرض الربو [39] ألا أن هناك أدلة غير حاسمة تدعم التأثير المفيد للمكملات. ولكن لم يتم حاليا التوصية للمكملات لعلاج أو الوقاية من الربو.[40] وكذلك لا توضح البيانات الأولية دور المكملات في تعزيز نمو الشعر البشري.[41]
النقص
يسبب النظام الغذائي الذي يفتقر فيتامين(د) إلى تلين العظام (الكساح عند الأطفال). ويعتبران نادرين في العالم المتقدم.[42][43] عدم التعرض للشمس قد يسبب نقص الكالسيديول (25 هيدروكسي فيتامين د) في الدم.[44] وهذا النقص يسبب ضعف في تمعدن العظام ويؤدي إلى مرض تليين العظام [45] وهما بالتفصيل :
- الرخد (الكساح): هذا المرض نتيجة إعاقة وتشوه في نمو العظام الطويلة، وقد يكون بسبب نقص الكالسيوم أو الفسفور بالإضافة إلى نقص فيتامين(D)؛ يكثر هذا المرض حاليا في البلدان ذات الدخل المنخفض مث أفريقيا،آسيا أو الشرق الأوسط،[46] وعند الذين لديهم اضطرابات وراثية مثل كساح نقص شبيه فيتامين(د).[47] تم وصف الكساح لأول مرة في عام 1640بواسطة فرانسيس جليسون الذي قال انه ظهر لاول مرة قبل حوالي 30 عاما في مقاطعات دورست وسومرست.[48] في عام 1857، استنتج جون سنو ان الكساح سينشر على نطاق واسع في بريطانيا بسبب غش الخبازين بخلط الخبز مع الشب.[49] خلال الفترة 1918-1920 بين إدوارد ميلانبي دور النظام الغذائي في تطور الكساح.[50][51][52] يوجد كساح سوء التغذية في البلدان ذات أشعة الشمس الكثيفة على مدار السنة مثل نيجيريا وبالإمكان حدوثه حتى بدون نقص فيتامين(د).[53][54] على الرغم من الكساح ولين العظام هي نادرة الآن في بريطانيا، إلا أن هناك تفشي في بعض المجتمعات المهاجرة الذين يعانون من لين العظام وشملت النساء اللاتي تعرضن لضوء النهار لكن بالملابس الغربية.[55] البشرة الداكنة وتقليل أوقات التعرض لأشعة الشمس لا ينتج عنه الكساح إذا كان النظام الغذائي يتميز بكميات عالية من اللحوم، والأسماك والبيض وكميات قليلة من الحبوب عالية الاستخراج. وتكمن عوامل الخطر الغذائية للكساح بالامتناع عن الأطعمة الحيوانية.[56][57][58] يبقى نقص فيتامين(D) هو السبب الرئيسي للكساح بين الأطفال في معظم البلدان، ويمكن السبب قلة فيتامين(D) في حليب الأم وكذلك العادات الاجتماعية والظروف المناخية التي تمنع التعرض الكافي للأشعة الفوق بنفسجية. في البلدان المشمسة مثل نيجيريا، جنوب أفريقيا، وبنغلاديش، يحدث هذا المرض بين كبار السن والأطفال، والسبب يعود إلى انخفاض كميات الكلسيوم في غذائهم الذي يتميز بالحبوب الأساسية فقط مع محدودية فرص الحصول على منتجات الألبان.[58] كان الكساح في السابق مشكلة صحية عامة رئيسية بين سكان الولايات المتحدة؛ في دنفر، كولورادو حيث الأشعة فوق البنفسجية فيها تقريبا 20% أقوى مما هي عليه عند مستوى سطح البحر على نفس خط العرض،[59] في أواخر العشرينات كان ما يقرب من ثلثين من أصل 500 طفل مصاب بكساح خفيف.[60][61] في القرن العشرين ساهمت الزيادة في نسبة البروتين الحيواني في الغذائي الأميركي إلى جانب زيادة استهلاك الحليب [62][63] المدعم بكمية من فيتامين(D) مع الانخفاض الشديد في حالات الكساح.[64]
- تلين العظام: هو مرض ترقق في العظام يحدث للبالغين فقط، يتصف بضعف العضلات القريبة وهشاشة العظام. يساهم آثار هذا المرض في آلام مزمنة في العضلات والعظام،[65][66] ولا يوجد أي دليل مقنع بانخفاض مستوى فيتامين(D) في من يعانون من الألم المزمن.[67]
يقول المدير العام للبحوث والتنموية وكبير المستشارين العلميين لوزارة الصحة في المملكة المتحدة وهيئة الخدمات الصحية الوطنية أنه خلال فصل الشتاء ينبغي إعطاء مكملات فيتامين(D) للأطفال الذين تتراوح أعمارهم ما بين ستة أشهر إلى خمس سنوات. ولا ينصح بأخذ هذه المكملات للناس الذين يحصلون على ما يكفي من فيتامين(D) من خلال وجباتهم الغذائية ومن أشعة الشمس.[68]
تظهر بعض البحوث أن الناس ذوي البشرة الداكنة الذين يعيشون في المناخ المعتدل لديهم مستويات متدنية من فيتامين(د).[69][70][70] والمستنتج من ذلك أن الناس ذوي البشرة الداكنة هم أقل كفاءة في تصنيع فيتامين(D) لأن الميلانين في الجلد يعوق توليف فيتامين(D)، ولكن دراسة حديثة تقول أن نقص فيتامين(D) في أوساط الأفارقة قد يكون راجعا إلى أسباب أخرى.[71] الأدلة الحديثة تقول أن هرمون الغدة الدرقية هو السبب في النتائج السلبية للقلب والأوعية الدموية، وأن النساء السود لديهن زيادة في هرمون الغدة الدرقية عند أدنى مستوى للمركب 25(OH)D مقارنة بالنساء البيض.[72] وجدت دراسة واسعة النطاق للمحددات الوراثية لقصور فيتامين(D) في القوقازيين ليس له علاقة بالتصبغ.[73][74]
من ناحية أخرى، فإن حدوث انخفاض موحد للمركب 25(OH)D عند الهنود الذين يعيشون في الهند [75] والصينيين في الصين،[76] لا تدعم الفرضية القائلة بأن انخفاض المستويات المشاهدة عند المصطبغ الأكثر بسبب عدم وجود توليف من الشمس عند خطوط العرض العليا؛ حث صاحب الدراسة المهاجرين ذوي البشرة الداكنة بأخذ مكملات فيتامين(D) مع ذلك، يقول: "لا أرى أي خطر، أو جانب سلبي، هناك فقط فائدة محتملة"[77][78].
ضغط الدم
أكد الباحثون من معهد صحة الطفل في جامعة لندن بإنجلترا أن نقص فيتامين د في الجسم قد يؤدي إلى ارتفاع ضغط الدم (المصدر)
الجرعة الزائدة (السمية)
التناول المستمر عند البالغين الأصحاء لأكثر من 1250 ميكروغرام في اليوم أي ما يعادل (50,000 وحدة دولية) يمكن أن ينتج عنه تسمم واضح بعد عدة شهور؛[79] أولئك الذين لديهم حالات طبية معينة مثل فرط الدريقات[80] هم أكثر حساسية لفيتامين(D) وتطور فرط كالسيوم الدم استجابة لأية زيادة فيتامين(د) في الغذاء، في حين أن فرط كالسيوم الدم عند الأمهات خلال فترة الحمل قد يزيد حساسية الجنين بسبب تأثيرات فيتامين(D) ويؤدي إلى متلازمة التخلف العقلي وتشوهات الوجه.[80][81] يجب على النساء الحوامل أو المرضعات استشارة الطبيب قبل تناول مكملات فيتامين(د). بالنسبة للرضع (حتى 12 شهرا) ضبط الحد الأعلى المسموح (الكمية القصوى التي يمكن تحملها دون ضرر) في 25 ميكروغرام/يوم (1000 وحدة دولية). تسبب ألف ميكروجرام (40,000 وحدة دولية) في اليوم الواحد عند الرضع سمية في غضون شهر واحد. في 30 نوفمبر 2010 زاد معهد الطب الحد الأعلى المسموح به بعد ما كلف من قبل الحكومتين الكندية والأمريكية وذلك كما يلي :
- 2500 وحدة دولية/يوم للأعمار ما بين سنة و 3 سنوات.
- 3000 وحدة دولية/يوم للأعمار ما بين 4 و 8 سنوات.
- 4000 وحدة دولية/يوم للأعمار ما بين 9 وأكبرمن 71 سنة (بما في ذلك النساء الحوامل أو المرضعات).[82]
تسبب الجرعة الزائدة من فيتامين(D) فرط كالسيوم الدم، وأهم أعراضها : فقدان الشهية، غثيان، يمكن أن يحدث قيء كثيرا ما يعقبه بوال، عطاش، الضعف، الأرق، عصبية، حكة، وفي نهاية المطاف فشل كلوي. وقد يتطور إلى بيلة بروتينية، أسطوانة بولية، آزوتيمية، وتكلس نقيلي (وخصوصا في الكلى).[79] يتم التعامل مع سمية فيتامين(D) بإيقاف مكملات الفيتامين وتقييد كمية الكالسيوم. عندها قد يكون الفشل الكلوي لا رجعة فيه. التعرض الطويل لأشعة الشمس لا يسبب عادة تسمم.[80] التعرض للأشعة الفوق بنفسجية لذوي البشرة الفاتحة في غضون 20 دقيقة (3-6 مرات أطول للبشرة المصطبغة) تصل عندهم تركيزات فيتامين(D) للسلائف المنتجة في الجلد إلى التوازن، وأي زيادة من فيتامين(D) يتم إنتاجه يتحلل.
نشرت حالات تسمم تنطوي على فرط كالسيوم الدم التي كانت فيها جرعات فيتامين(د) و25-هيدروكسي فيتامين(د) في اليوم الواحد أعلى من 40,000 وحدة دولية (1000 ميكروغرام).[80]
أشكاله
| فيتامين د | التركيب الكيميائي | الهيكل |
|---|---|---|
| د1 | الجزيئية مركب من إركوكالسيفـرول مع لوميسترول ، 1:1 | |
| د2 | إركوكالسيفـرول (مصنوعة من إرغوستيرول) | 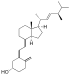
|
| د3 | كوليكالسيفيرول (مصنوعة من 7-ديهيدروكوليستيرول في الجلد). | 
|
| د4 | 22-ثنائي هيدروإرغوكالسيفيرول | 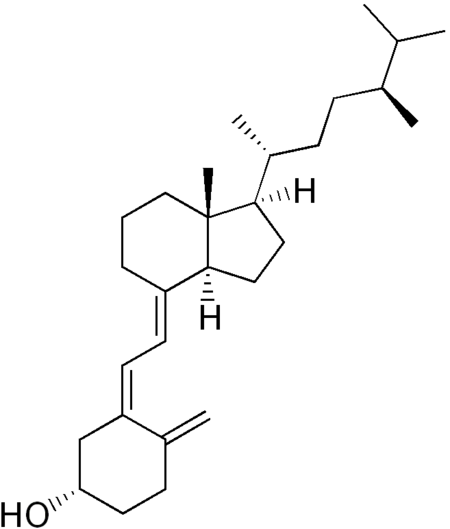
|
| د5 | سيتوكالسيفرول (مصنوعة من 7-ديهيدروسيتوستيرول) | 
|
توجد أشكال متعددة (فيتامير) من فيتامين(D) (انظر الجدول). أهم شكلين هما:
- فيتامين(D2) أو إركوكالسيفـرول
- فيتامين(D3) أو كوليكالسيفيرول
ويشير فيتامين(D) بدون لاحقة سفلية إلى إما (D2) أو (D3) أو إلى كليهما، وتعرف مجتمعة باسم كالسيفرول.[83] وقد تم التعرف على فيتامين(D2) كيميائيا في عام 1932. في عام 1936 تم تأكيد البنية الكيميائية لفيتامين(D3) وثبت أنه ينتج من الإشعاع فوق البنفسجي للمركب (7-ديهيدروكوليستيرول).[84]
الأشكال المختلفة كيميائيا من فيتامين(D) هي سيكوسترويد؛ مثل ستيرويدات أحد روابط الستيرويدات الحلقية المكسورة.[85] الفرق بين التركيبة الهيكلية لفيتامين(D2) وفيتامين(D3) في السلسلة الجانبية لهما. تحتوي السلسلة الجانبية لفيتامين(D2) على رابطة ثنائية بين ذرتي الكربون 22 و 23، ومجموعة الميثيل على الكربون 24.
يتم إنتاج فيتامين(D3) (كوليكالسيفيرول) عن طريق الأشعة فوق البنفسجية من سلفه 7-ديهيدروكوليستيرول. يحدث هذا الجزيء بشكل طبيعي في جلد الحيوانات والحليب. ويمكن تكوين فيتامين(D3) عن طريق تعرض الجلد للأشعة الفوق البنفسجية، أو من خلال تعريض الحليب مباشرة للأشعة فوق البنفسجية (تعتبر إحدى الطرق التجارية).
فيتامين(D2) هو مشتق من إرغوستيرول، وهو غشاء الستيرول لفطر الإرغوت الذي تنتجه بعض الكائنات الحية مثل العوالق النباتية، واللافقاريات، والخمائر، والفطريات الراقية مثل المشروم. يتم إنتاج فيتامين(D2) إرغوكالسيفيرول في كل هذه الكائنات من الإرغوستيرول، وذلك استجابة للأشعة فوق البنفسجية. ومع ذلك، مثل جميع الأشكال لفيتامين(D) فإنه لا يمكن تصنيعها دون الأشعة الفوق البنفسجية. ولا يتم إنتاج فيتامين(D2) من النباتات البرية أو الفقاريات لأنها تفتقر إلى سلائف إرغوستيرول.[86] ومن المتوقع أن يكون المصير البيولوجي لإنتاج 25(OH)D من فيتامين(D2) نفسه بالنسبة لـ25(OH)D3، ويمكن لفيتامين(D2) أن يكون بديلا عن فيتامين(D3) في النظام الغذائي للإنسان بالرغم من بعض الخلافات على صحة ذلك.[87][88]
الإنتاج في الجلد
يتكون فيتامين(D3) في الجلد عندما يتفاعل 7-ديهيدروكوليستيرول مع الأشعة فوق البنفسجية (نوع B) عند الأطوال الموجية ما بين 270 و 300 نانومتر، وتكون ذروة التكوين ما بين 295 و 297 نانومتر.[89] وتكون هذه الأطوال الموجية في ضوء الشمس عندما يكون مؤشر الأشعة فوق البنفسجية أكبر من ثلاثة، وكذلك في الضوء المنبعث من المصابيح الفوق البنفسجية في سرير حمام الشمس (التي تنتج الأشعة الفوق بنفسجية الطويلة (نوع A)، ولكن عادة ما تنتج ما بين 4% إلى 10% من إجمالي انبعاثات الأشعة (نوع B)). يمكن تكوين فيتامين(D3) في الجلد عندما يكون مؤشر الأشعة فوق البنفسجية أكبر من ثلاثة، والذي يحدث في المناطق الاستوائية بشكل يومي، وبشكل يومي في المناطق المعتدلة فقط خلال مواسم الربيع والصيف، وشبه معدومة داخل دوائر القطبين.
يتكون الجلد من طبقتين رئيسيتين:
- الطبقة الداخلية تسمى الأدمة، تتألف إلى بشكل كبير من النسيج الضام.
- الطبقة الخارجية وهي البشرة الرقيقة.
البشرة السميكة في باطن القدم والراحتين تتكون من خمسة طبقات؛ وهي من الخارج إلى الداخل :
ويتم إنتاج فيتامين(D) في الطبقتين الأعمق (القاعدية والشائكة).
يتم إنتاج الكوليكالسيفيرول (D3) بتفاعل كيميائي ضوئي للمركب (7-ديهيدروكوليستيرول) في الجلد؛ ويتم إنتاج -ديهيدروكوليستيرول بكميات كبيرة في الجلد لأغلب الحيوانات الفقارية، تشمل الإنسان. ويتضح أن مركب الكوليكالسيفيرول ناقص بشكل طبيعي عند فئران الخلد العارية ومستويات المركب (25(OH)D) لا يمكن كشفها. إن وجود الفراء أو الريش في بعض الحيوانات يمنع الأشعة فوق البنفسجية من الوصول إلى الجلد ففي الطيور والثدييات ذات الفراء يتم تصنيع فيتامين (D) من الإفرازات الدهنية للجلد على الريش أو الفرو ويتم الحصول على الفيتامين عن طريق الاستمالة ولعق الفراء.
الإنتاج الصناعي
يتم إنتاج فيتامين د3 (كوليكالسيفيرول) صناعيا من خلال تعريض 7-ديهيدروكوليستيرول لضوء الأشعة فوق البنفسجية، ويلي ذلك تعقيمه.[90] إن المركب 7-ديهيدروكوليستيرول (7-dehydrocholesterol)هو عبارة عن مادة طبيعية موجودة في دهن الصوف (اللانولين) في الأغنام والحيوانات الأخرى ذات الصوف. ويتم إنتاج فيتامين د2 (إركوكالسيفـرول) بنفس الطريقة باستخدام إركوستيرول من الخميرة أو الفطر كمادة أولية.[90]
التركيب
| في الجلد، 7-ديهيدروكوليستيرول مشتق من الكولسترول، حيث أنه محلل ضوئيا بواسطة الأشعة فوق البنفسجية في دوران وتفاعل إلكتروحلقي لـ 6-الإلكترون. والنتيجة هي طليعة الفيتامين د3. | 
|
| يتم مزامرة طليعة الفيتامين د3 تلقائيا إلى فيتامين د3 (كوليكالسيفيرول). يستغرق تحول طليعة الفيتامين د3 إلى فيتامين د3 حوالي 12 يوما كي يكتمل وفي درجة حرارة الغرفة. | 
|
| يعالج كوليكالسيفيرول بالهيدروكسيل في الكبد في الموقع 25 (اليمنى العلوي للجزيء) لتشكيل 25-هيدروكسيكوليكالسيفيرول (كالسيديول أو 25(OH)D)،سواء في الجلد أو بأبتلاعها. يتم تحفيز هذا التفاعل من قبل الانزيم الميكروسومي فيتامين د 25-هيدروكسيلاز [91] التي تنتجها خلايا الكبد، حينها يتم تحرير المنتج في البلازما، حيث تنضم إلى الغلوبيولين-الفا، البروتين الرابط لفيتامين د.[92] | 
|
| ينتقل الكالسيديول إلى الأنابيب القريبة للكلى، حيث أنه بعالج بالهيدروكسيل في الموقع 1-α (يمين اسفل الجزيء) لتشكيل الكالسيتريول (الملقب 1,25-ديهيدروكسيكوليكالسيفيرول ويختصر بـ1,25(OH)2D). هذا المنتج ربيطة قوية من مستقبلات فيتامين د تتوسط معظم الإجراءات الفسيولوجية للفيتامين. يتم تحويل كالسيديول إلى كالسيتريول بتحفيز من إنزيم 25-هيدروكسي فيتامين د3 1-ألفا-هيدروكسيلاز، المستوى الذي يزداد بواسطة هرمون الدريقات (وكذلك بواسطة كميات منخفضة من الكالسيوم أو الفوسفات). | 
|
آلية العمل
يتم تحويل فيتامين(د) في الكبد إلى كالسيديول والذي يعرف بالكالسيفيديول، أو 25-هيدروكسيكوليكالسيفيرول (25-hydroxycholecalciferol) أو 25-هيدروكسيفيتامين(د) (25-hydroxyvitamin D)؛ تختصر بـ 25(OH)D؛ وهي مستقلب فيتامين(د) محدد يتم قياسها في الدم لتحديد حالة فيتامين (د) في الشخص[93][94]. يتم تحويل جزء من الكالسيديول عن طريق الكلى بواسطة وحيدات البلاعم في جهاز المناعة إلى كالسيتريول الشكل النشط بيولوجيا من فيتامين(د)[95]. يتوزع الكالسيتريول كهرمون في الدم، وتنظيم تركيز الكالسيوم والفوسفات في جريان الدم ويعزز النمو الصحي وإعادة تشكيل العظام. كما يتم تحويل الكالسيديول إلى الكالسيتريول خارج الكلى لأغراض أخرى مثل التكاثر، التمايز والموت المبرمج للخلايا؛ الكالسيتريول يؤثر أيضا على الوظائف العصبية العضلية والالتهابات[96].
تتوسط آثار الكالسيتريول البيولوجية عن طريق الربط بمستقبلات فيتامين د (VDR)، التي تقع أساسا في نوى الخلايا المستهدفة. يسمح الكالسيتريول لمستقبلات فيتامين د لتكون بمثابة عامل إنساخ ينظم التعبير الجيني للبروتينات الناقلة، التي تشارك في امتصاص الكالسيوم في الأمعاء.[97]
تنتمي مستقبلات فيتامين (د) إلى طائفة المستقبلات النووية لمستقبلات هرمون ستيرويد/الدرقية، يتم إنتاج مستقبلات فيتامين(د) بواسطة الخلايا في معظم الأعضاء مثل الدماغ، القلب، الجلد، الغدد التناسلية، البروستاتا والثدي. يؤدي تنشيط مستقبلات فيتامين(د) في الأمعاء، العظام، الكلى، خلايا الغدة الدرقية إلى الحفاظ على مستويات الكالسيوم والفوسفور في الدم (بمساعدة هرمون الغدة الدرقية والكالسيتونين) وكذلك الحفاظ على مكونات العظام.[64]
يزيد فيتامين د من الضغط على جين الهيدروكسيلاز التيروزين في الخلايا النخامية الكظرية. كما تشارك في التركيب الحيوي لعوامل التغذية العصبية وتجميع سينسيز اكسيد النيتريك، وزيادة مستويات الجلوتاثيون.[98]
المصادر الغذائية
| الغذاء | الكمية | الوحدة الدولية |
|---|---|---|
| سمك السردين، معلب في الزيت أو مجفف | 50 جرام | 250 |
| سمك السلور، مطبوخ | 85 جرام | 425 |
| سمك الإسقمري، مطبوخ | 100 جرام | 345 |
| سمك أبو سيف، مطبوخ | 85 جرام | 566 |
| سمك السلمون، مطبوخ | 100 جرام | 360 |
| سمك التونة، معلب في الماء، بالزيت أو مجفف | 100 جرام | 235 |
| ثعبان البحر، مطبوخ | 100 جرام | 200 |
| زيت كبد سمك القد | (ملعقة طعام واحدة) = 15 مل | 1,360 |
| كبد البقر، مطبوخة | 100 جرام | 15 |
| بيض، (كامل) | 60 جرام | 20 |
الجرعة الموصّى بها
| العمر | وحدة دولية | ميكروغرام |
|---|---|---|
| 0–12 شهر | 400 | 10 |
| 1–13 سنة | 600 | 15 |
| 14–18 سنة | 600 | 15 |
| 19–50 سنة | 600 | 15 |
| 51–70 سنة | 600 | 15 |
| أكبر من 70 سنة | 800 | 20 |
فيتامين د الذي يكون على شكل مكملات (كبسولات) يمكن الحصول عليه كفيتامين د 2 (ergocalciferol) أو كفيتامين د 3 (cholecalciferol). تحتوي الكبسولات متعددة الفيتامين (Multivitamins) في العادة على جرعة فيتامين د الموصّى بها عموما 200-400 آي يو (وحدة دولية)، أو 5-10 ميكروغرام، كلّ يوم. 400 آي يو توجد في حبوب فيتامينات ما قبل وبعد الولادة.
المسنون والمصابين بمتلازمة سوء الامتصاص، والفشل الكبدي، ومتلازمة الالتهاب الكلوي، يأخذون مكملات تحتوي على 50,000 آي يو، أو 1,255 ميكروجرام، أسبوعيا لفترة ثمانية أسابيع.
هذه العلاجات يجب أن ترتّب تحت إشراف الطبيب.
- الشمس هي المصدر الآمن لفيتامين D وهي تعطي الجسم أكثر من حاجته من الأشعة فوق البنفسجية (Ultraviolet) اللازمة لإنتاج فيتامين D، وقال الأطباء ان الفترة الواقعة بين العاشرة صباحا والثالثة بعد الظهر هي أفضل فترة لتعرض الجسم لأشعة الشمس حيث تكون الأشعة متعامدة على الأرض[99].
- وفي البلاد المشمسة لا يتعرض السكان عادة لنقص في فيتامين د، حيث يتكون هذا الفيتامين بواسطة الأشعة الشمسية في الجلد والبشرة ويتوزع على الجسم. هذا ولا يحتاج المرء تعريض نفسه لاشعة الشمس أكثر من اللازم لتوليد هذا الفيتامين بل يكفي التصرف المعتاد في بلاد مثل البلاد العربية.
عند البالغين، تناول أكثر من 1250 مغ يومياً يمكن أن ينتج عن تسمم بعد عدّة أشهر.[100]
المصادر
- Wolf G (2004). "The discovery of vitamin D: the contribution of Adolf Windaus". J. Nutr. 134 (6): 1299–302. PMID 15173387.
- "Age-old children's disease back in force". Thestar.com. 2007-07-25. مؤرشف من الأصل في 17 مايو 200824 أغسطس 2010.
- Elena Conis (2006-07-24). "Fortified foods took out rickets". لوس أنجلوس تايمز. مؤرشف من الأصل في 06 مارس 201624 أغسطس 2010.
- McClean, F.C.; Budy, A.M. (28 January 1964). "Vitamin A, Vitamin D, Cartilage, Bones, and Teeth". In Harris, R.S. (المحرر). Vitamins and Hormones. 21. Academic Press. صفحات 51–52. .
- "Unraveling The Enigma Of Vitamin D" الأكاديمية الوطنية للعلوم - تصفح: نسخة محفوظة 04 فبراير 2013 على موقع واي باك مشين.
- "Adolf Windaus – Biography". Nobelprize.org. 2010-03-25. مؤرشف من الأصل في 24 يوليو 201825 مارس 2010.
- Rosenheim, O.; King, H. (1932). "The Ring-system of sterols and bile acids. Part II". J. Chem. Technol. Biotechnol. 51: 954–7. doi:10.1002/jctb.5000514702.
- "Crystalline vitamin D". Proc R. Soc. Lond. B. 109: 488–506. 1932. JSTOR 81571.
- Hirsch AL. (2011). "Industrial aspects of vitamin D". In Feldman DJ, Pike JW, Adams JS. (eds.) (المحرر). Vitamin D. London; Waltham, MA: Academic Press. صفحة 73. . مؤرشف من الأصل في 8 فبراير 2017.
- Arvids A. Ziedonis; Mowery, David C.; Nelson, Richard R.; Bhaven N. Sampat (2004). Ivory tower and industrial innovation: university-industry technology transfer before and after the Bayh-Dole Act in the United States. Stanford, Calif: Stanford Business Books. صفحات 39–40. . مؤرشف من الأصل في 8 فبراير 2017.
- Marshall, James (2005). Elbridge A. Stuart Founder of the Carnation Company. Kessinger Publishing. صفحة 235. .
- Chung M, Balk, EM, Brendel, M, Ip, S, Lau, J, Lee, J, Lichtenstein, A, Patel, K, Raman, G, Tatsioni, A, Terasawa, T, Trikalinos, TA (2009). "Vitamin D and calcium: a systematic review of health outcomes". Evidence report/technology assessment (183): 1–420. PMID 20629479.
- Ross AC, Taylor CL, Yaktine AL Del Valle HB (2011). Dietary Reference Intakes for Calcium and Vitamin D. Washington, D.C: National Academies Press. صفحة 435. . مؤرشف من الأصل في 1 فبراير 2015.
- Maxmen A (2011). "Nutrition advice: the vitamin D-lemma". Nature. 475 (7354): 23–5. doi:10.1038/475023a. PMID 21734684.
- Zittermann A, Gummert, JF, Börgermann, J (2009). "Vitamin D deficiency and mortality". Current opinion in clinical nutrition and metabolic care. 12 (6): 634–9. doi:10.1097/MCO.0b013e3283310767. PMID 19710612.
- Bjelakovic G, Gluud, LL, Nikolova, D, Whitfield, K, Wetterslev, J, Simonetti, RG, Bjelakovic, M, Gluud, C (2011). "Vitamin D supplementation for prevention of mortality in adults". Cochrane database of systematic reviews (Online) (7): CD007470. doi:10.1002/14651858.CD007470.pub2. PMID 21735411.
- Tuohimaa P (2009). "Vitamin D and aging". The Journal of Steroid Biochemistry and Molecular Biology. 114 (1–2): 78–84. doi:10.1016/j.jsbmb.2008.12.020. PMID 19444937.
- Tuohimaa P, Keisala T, Minasyan A, Cachat J, Kalueff A (2009). "Vitamin D, nervous system and aging". Psychoneuroendocrinology. 34: S278–86. doi:10.1016/j.psyneuen.2009.07.003. PMID 19660871.
- Manya H, Akasaka-Manya K, Endo T (2010). "Klotho protein deficiency and aging". Geriatr Gerontol Int. 10 (Suppl 1): S80–7. doi:10.1111/j.1447-0594.2010.00596.x. PMID 20590845.
- Cranney A, Horsley, T, O'Donnell, S, Weiler, H, Puil, L, Ooi, D, Atkinson, S, Ward, L, Moher, D, Hanley, D, Fang, M, Yazdi, F, Garritty, C, Sampson, M, Barrowman, N, Tsertsvadze, A, Mamaladze, V (2007). "Effectiveness and safety of vitamin D in relation to bone health". Evidence report/technology assessment (158): 1–235. PMID 18088161.
- Pittas AG, Chung, M, Trikalinos, T, Mitri, J, Brendel, M, Patel, K, Lichtenstein, AH, Lau, J, Balk, EM (2010). "Vitamin D and Cardiometabolic Outcomes: A Systematic Review". Annals of internal medicine. 152 (5): 307–14. doi:10.1059/0003-4819-152-5-201003020-00009. PMC . PMID 20194237.
- Pittas AG, Chung M, Trikalinos T, Mitri J, Brendel M, Patel K, Lichtenstein AH, Lau J, Balk EM (2010). "Vitamin D and Cardiometabolic Outcomes: A Systematic Review". Annals of Internal Medicine. 152 (5): 307–14. doi:10.1059/0003-4819-152-5-201003020-00009. PMC . PMID 20194237.
- McGreevy C, Williams D (2011). "New insights about vitamin d and cardiovascular disease: A narrative review". Annals of internal medicine. 155 (12): 820–6. doi:10.1059/0003-4819-155-12-201112200-00004. PMID 22184689.
- Wang L, Manson, JE, Song, Y, Sesso, HD (2010). "Systematic review: Vitamin D and calcium supplementation in prevention of cardiovascular events". Annals of internal medicine. 152 (5): 315–23. doi:10.1059/0003-4819-152-5-201003020-00010. PMID 20194238.
- Ascherio A, Munger, KL, Simon, KC (2010). "Vitamin D and multiple sclerosis". Lancet neurology. 9 (6): 599–612. doi:10.1016/S1474-4422(10)70086-7. PMID 20494325.
- Pierrot-Deseilligny C, Souberbielle, JC (2010). "Is hypovitaminosis D one of the environmental risk factors for multiple sclerosis?". Brain : a journal of neurology. 133 (Pt 7): 1869–88. doi:10.1093/brain/awq147. PMID 20584945.
- Pierrot-Deseilligny C, Souberbielle, JC (2011). "Widespread vitamin D insufficiency: A new challenge for primary prevention, with particular reference to multiple sclerosis". Presse medicale (Paris, France : 1983). 40 (4 Pt 1): 349–56. doi:10.1016/j.lpm.2011.01.003. PMID 21333483.
- موقع التجارب السريرية NCT01440062 Efficacy of Vitamin D Supplementation in Multiple Sclerosis (EVIDIMS)
- Dörr J, Ohlraun S, Skarabis H, Paul F (2012). "Efficacy of vitamin D supplementation in multiple sclerosis (EVIDIMS Trial): study protocol for a randomized controlled trial". Trials. 13 (1): 15. doi:10.1186/1745-6215-13-15. PMC . PMID 22316314. مؤرشف من الأصل في 4 فبراير 2014.
- Buttigliero C, Monagheddu, C, Petroni, P, Saini, A, Dogliotti, L, Ciccone, G, Berruti, A (2011). "Prognostic role of vitamin d status and efficacy of vitamin d supplementation in cancer patients: a systematic review". The oncologist. 16 (9): 1215–27. doi:10.1634/theoncologist.2011-0098. PMID 21835895.
- "Vitamin D and Cancer Prevention - National Cancer Institute". Cancer.gov. 2010-06-16. مؤرشف من الأصل في 13 فبراير 201513 يونيو 2012.
- BBC NEWS | Health | Vitamin D 'may help slow ageing' - تصفح: نسخة محفوظة 09 مارس 2018 على موقع واي باك مشين.
- دراسة: فيتامين "د" قد يساهم في علاج الربو - BBC Arabic - تصفح: نسخة محفوظة 20 أبريل 2014 على موقع واي باك مشين.
- Beard JA, Bearden, A, Striker, R (2011). "Vitamin D and the anti-viral state". Journal of clinical virology : the official publication of the Pan American Society for Clinical Virology. 50 (3): 194–200. doi:10.1016/j.jcv.2010.12.006. PMID 21242105.
- Cannell JJ, Vieth R, Umhau JC, Holick MF, Grant WB, Madronich S, Garland CF, Giovannucci E (2006). "Epidemic influenza and vitamin D". Epidemiology and Infection. 134 (6): 1129–40. doi:10.1017/S0950268806007175. PMC . PMID 16959053.
- Nnoaham KE, Clarke, A (2008). "Low serum vitamin D levels and tuberculosis: a systematic review and meta-analysis". International Journal of Epidemiology. 37 (1): 113–9. doi:10.1093/ije/dym247. PMID 18245055.
- Luong K, Nguyen, LT (2011). "Impact of vitamin D in the treatment of tuberculosis". The American journal of the medical sciences. 341 (6): 493–8. doi:10.1097/MAJ.0b013e3182070f47. PMID 21289501.
- Spector SA, Nguyen, LT (2011). "Vitamin D and HIV: letting the sun shine in". Topics in antiviral medicine. 19 (1): 6–10. PMID 21852710.
- Hart, PH (2012 Jun). "Vitamin D supplementation, moderate sun exposure, and control of immune Diseases". Discovery medicine. 13 (73): 397–404. PMID 22742645.
- Paul G, Brehm, JM, Alcorn, JF, Holguín, F, Aujla, SJ, Celedón, JC (2012). "Vitamin D and asthma". American Journal of Respiratory and Critical Care Medicine. 185 (2): 124–32. doi:10.1164/rccm.201108-1502CI. PMID 22016447.
- Amor KT, Rashid RM, Mirmirani P (2010). "Does D matter? The role of vitamin D in hair disorders and hair follicle cycling". Dermatology online journal. 16 (2). PMID 20178699.
- "Rickets". هيئة الخدمات الصحية الوطنية (المملكة المتحدة). Last reviewed 08/03/2012. مؤرشف من الأصل في 11 أكتوبر 201709 يوليو 2012.
- مدلاين بلس Rickets
- Schoenmakers I, Goldberg GR, Prentice A (2008). "Abundant sunshine and vitamin D deficiency". British Journal of Nutrition. 99 (6): 1171–3. doi:10.1017/S0007114508898662. PMC . PMID 18234141.
- Grant WB, Holick MF (2005). "Benefits and requirements of vitamin D for optimal health: a review". Alternative medicine review. 10 (2): 94–111. PMID 15989379.
- Lerch C, Meissner T, Lerch C (2007). "Interventions for the prevention of nutritional rickets in term born children". Cochrane database of systematic reviews (Online) (4): CD006164. doi:10.1002/14651858.CD006164.pub2. PMID 17943890.
- Zargar AH, Mithal A, Wani AI, Laway BA, Masoodi SR, Bashir MI, Ganie MA (2000). "Pseudovitamin D deficiency rickets—a report from the Indian subcontinent". Postgraduate Medical Journal. 76 (896): 369–72. doi:10.1136/pmj.76.896.369. PMC . PMID 10824056.
- Gibbs D (1994). "Rickets and the crippled child: an historical perspective". Journal of the Royal Society of Medicine. 87 (12): 729–32. PMC . PMID 7503834.
- Dunnigan M (2003). "Commentary: John Snow and alum-induced rickets from adulterated London bread: an overlooked contribution to metabolic bone disease". International Journal of Epidemiology. 32 (3): 340–1. doi:10.1093/ije/dyg160. PMID 12777415.
- Pileggi V, De Luca HF, Steenbock H (1955). "The role of vitamin D and intestinal phytase in the prevention of rickets in rats on cereal diets". Archives of Biochemistry and Biophysics. 58 (1): 194–204. doi:10.1016/0003-9861(55)90106-5. PMID 13259690.
- Ford JA, Colhoun EM, McIntosh WB, Dunnigan MG (1972). "Biochemical Response of Late Rickets and Osteomalacia to a Chupatty-free Diet". British Medical Journal. 3 (5824): 446–7. doi:10.1136/bmj.3.5824.446. PMC . PMID 5069221.
- Rajakumar K (2003). "Vitamin D, cod-liver oil, sunlight, and rickets: a historical perspective". Pediatrics. 112 (2): e132–5. doi:10.1542/peds.112.2.e132. PMID 12897318.
- Oramasionwu GE, Thacher TD, Pam SD, Pettifor JM, Abrams SA (2008). "Adaptation of calcium absorption during treatment of nutritional rickets in Nigerian children". The British journal of nutrition. 100 (2): 387–92. doi:10.1017/S0007114507901233. PMID 18197991.
- Fischer PR, Rahman A, Cimma JP, Kyaw-Myint TO, Kabir AR, Talukder K, Hassan N, Manaster BJ, Staab DB (1999). "Nutritional rickets without vitamin D deficiency in Bangladesh". Journal of tropical pediatrics. 45 (5): 291–3. doi:10.1093/tropej/45.5.291. PMID 10584471.
- Dunnigan MG, Henderson JB (1997). "An epidemiological model of privational rickets and osteomalacia". The Proceedings of the Nutrition Society. 56 (3): 939–56. doi:10.1079/PNS19970100. PMID 9483661.
- Robertson I, Ford JA, McIntosh WB, Dunnigan MG (1981). "The role of cereals in the aetiology of nutritional rickets: the lesson of the Irish National Nutrition Survey 1943–8". The British journal of nutrition. 45 (1): 17–22. doi:10.1079/BJN19810073. PMID 6970590.
- Clements MR (1989). "The problem of rickets in UK Asians". Journal of Human Nutrition and Dietetics. 2 (2). doi:10.1111/j.1365-277X.1989.tb00015.x.
- Pettifor JM (2004). "Nutritional rickets: deficiency of vitamin D, calcium, or both?". المجلة الأمريكية للتغذية العلاجية. 80 (6 Suppl): 1725S–9S. PMID 15585795.
- "US National Institutes Of Health, National cancer Institute". Science.education.nih.gov. مؤرشف من الأصل في 11 مايو 201324 أغسطس 2010.
- Weick MT (1967). "A history of rickets in the United States". المجلة الأمريكية للتغذية العلاجية. 20 (11): 1234–41. PMID 4862158.
- Garrison, R.H.; Somer, E. (1997). The Nutrition Desk Reference. McGraw-Hill. . مؤرشف من الأصل في 8 فبراير 2017.
- DuPuis., E.M. (2002). Nature's Perfect Food: How Milk Became America's Drink. .
- Teegarden D, Lyle RM, Proulx WR, Johnston CC, Weaver CM (1999). "Previous milk consumption is associated with greater bone density in young women". المجلة الأمريكية للتغذية العلاجية. 69 (5): 1014–7. PMID 10232644.
- Holick MF (2004). "Sunlight and vitamin D for bone health and prevention of autoimmune diseases, cancers, and cardiovascular disease". المجلة الأمريكية للتغذية العلاجية. 80 (6 Suppl): 1678S–88S. PMID 15585788. مؤرشف من الأصل في 20 أغسطس 2012.
- Holick MF (2003). "Vitamin D: A millenium perspective". Journal of cellular biochemistry. 88 (2): 296–307. doi:10.1002/jcb.10338. PMID 12520530.
- Stewart B. Leavitt. "Vitamin D – A Neglected 'Analgesic' for Chronic Musculoskeletal Pain" ( كتاب إلكتروني PDF ). Pain-Topics.org. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 9 ديسمبر 201325 مارس 2009.
- Straube S, Andrew Moore R, Derry S, McQuay HJ (2009). "Vitamin D and chronic pain". Pain. 141 (1–2): 10–3. doi:10.1016/j.pain.2008.11.010. PMID 19084336.
- "All under-fives should take vitamin D pills to avoid rickets, says Government's health chief". Daily Mail. 27 January 2011. مؤرشف من الأصل في 24 سبتمبر 2015. ""]..
- Azmina Govindji RD (1 July 2010). "When it's sunny, top up your vitamin D". TheIsmaili.org. مؤرشف من الأصل في 18 يوليو 201401 يوليو 2010.
- Ford L, Graham V, Wall A, Berg J (2006). "Vitamin D concentrations in an UK inner-city multicultural outpatient population". Annals of Clinical Biochemistry. 43 (6): 468–73. doi:10.1258/000456306778904614. PMID 17132277.
- Signorello LB, Williams SM, Zheng W, Smith JR, Long J, Cai Q, Hargreaves MK, Hollis BW, Blot WJ (2010). "Blood vitamin D levels in relation to genetic estimation of African ancestry". Cancer Epidemiology, Biomarkers & Prevention. 19 (9): 2325–31. doi:10.1158/1055-9965.EPI-10-0482. PMC . PMID 20647395.
- Aloia JF, Chen DG, Chen H (2010). "The 25(OH)D/PTH Threshold in Black Women". The Journal of Clinical Endocrinology and Metabolism. 95 (11): 5069–73. doi:10.1210/jc.2010-0610. PMC . PMID 20685862.
- Wang TJ, Zhang F, Richards JB, Kestenbaum B, Van Meurs JB, Berry D, Kiel DP, Streeten EA, Ohlsson C (2010). "Common genetic determinants of vitamin D insufficiency: a genome-wide association study". Lancet. 376 (9736): 180–8. doi:10.1016/S0140-6736(10)60588-0. PMC . PMID 20541252.
- Bouillon R (2010). "Genetic and environmental determinants of vitamin D status". Lancet. 376 (9736): 148–9. doi:10.1016/S0140-6736(10)60635-6. PMID 20541253.
- Harinarayan CV, Joshi SR (2009). "Vitamin D status in India—its implications and remedial measures". The Journal of the Association of Physicians of India. 57: 40–8. PMID 19753759.
- Lips P (2010). "Worldwide status of vitamin D nutrition". The Journal of Steroid Biochemistry and Molecular Biology. 121 (1–2): 297–300. doi:10.1016/j.jsbmb.2010.02.021. PMID 20197091.
- CBC "Dark-skinned immigrants urged to take vitamin D". February 16, 2010. CBC News. نسخة محفوظة 20 مارس 2020 على موقع واي باك مشين.
- Stephen Strauss."The vitamin D debate". February 13, 2008.CBC News. نسخة محفوظة 20 مارس 2020 على موقع واي باك مشين.
- Vitamin D في الطبعة المهنية لدليل ميرك للتشخيص والعلاج
- Vieth R (1999). "Vitamin D supplementation, 25-hydroxyvitamin D concentrations, and safety" ( كتاب إلكتروني PDF ). المجلة الأمريكية للتغذية العلاجية. 69 (5): 842–56. PMID 10232622. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 3 يوليو 2012.
- Tolerable Upper Intake Limits for Vitamins And Minerals ( كتاب إلكتروني PDF ). الهيئة الأوروبية لسلامة الأغذية. ديسمبر 2006. . مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 6 مايو 2019.
- Ross AC, Manson JE, Abrams SA, Aloia JF, Brannon PM, Clinton SK, Durazo-Arvizu RA, Gallagher JC, Gallo RL, Jones G, Kovacs CS, Mayne ST, Rosen CJ, Shapses SA (2011). "The 2011 Report on Dietary Reference Intakes for Calcium and Vitamin D from the Institute of Medicine: What Clinicians Need to Know". Journal of Clinical Endocrinology & Metabolism. 96 (1): 53–8. doi:10.1210/jc.2010-2704. PMC . PMID 21118827.
- Dorland's Illustrated Medical Dictionary, under Vitamin (Table of Vitamins)
- History of Vitamin D University of California, Riverside, Vitamin D Workshop. نسخة محفوظة 28 نوفمبر 2011 على موقع واي باك مشين.
- About Vitamin D Including Sections: History, Nutrition, Chemistry, Biochemistry, and Diseases. University of California Riverside نسخة محفوظة 15 نوفمبر 2011 على موقع واي باك مشين.
- "Vitamin D". عيادة مايو - تصفح: نسخة محفوظة 02 يناير 2014 على موقع واي باك مشين.
- Houghton LA, Vieth R (2006). "The case against ergocalciferol (vitamin D2) as a vitamin supplement" ( كتاب إلكتروني PDF ). المجلة الأمريكية للتغذية العلاجية. 84 (4): 694–7. PMID 17023693. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 3 يوليو 2012.
- Holick, M. F.; Biancuzzo, R. M.; Chen, T. C.; Klein, E. K.; Young, A.; Bibuld, D.; Reitz, R.; Salameh, W.; Ameri, A.; Tannenbaum, A. D. (2007). "Vitamin D2 is as Effective as Vitamin D3 in Maintaining Circulating Concentrations of 25-Hydroxyvitamin D". Journal of Clinical Endocrinology & Metabolism. 93 (3): 677–681. doi:10.1210/jc.2007-2308. PMC . PMID 18089691.
- Hume EM, Lucas NS, Smith HH (1927). "On the Absorption of vitamin D from the Skin". Biochemical Journal. 21 (2): 362–367. PMC . PMID 16743844.
- Holick MF, Brehm, JM, Alcorn, JF, Holguín, F, Aujla, SJ, Celedón, JC (2005). "The Vitamin D Epidemic and its Health Consequences" ( كتاب إلكتروني PDF ). Journal of Nutrition. 135 (11): 2739S–48S. PMID 16251641. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 18 نوفمبر 2017.
- Cheng JB, Levine MA, Bell NH, Mangelsdorf DJ, Russell DW (2004). "Genetic evidence that the human CYP2R1 enzyme is a key vitamin D 25-hydroxylase". Proc Natl Acad Sci U S A. 101 (20): 7711–7715. Bibcode:2004PNAS..101.7711C. doi:10.1073/pnas.0402490101. PMC . PMID 15128933.
- Laing, C.J.; Cooke, N.E. (2004). "Section I: Ch. 8: Vitamin D Binding Protein". In Feldman, D.; Glorieux, F.H.; Pike, J.W. (المحرر). Vitamin D. 1 (الطبعة 2). Academic Press. صفحات 117–134. . مؤرشف من الأصل في 8 فبراير 2017.
- 25-hydroxy vitamin D test: MedlinePlus Medical Encyclopedia - تصفح: نسخة محفوظة 05 يوليو 2016 على موقع واي باك مشين.
- Hollis BW (1996). "Assessment of vitamin D nutritional and hormonal status: what to measure and how to do it". Cacif Tissue Int. 58 (1): 4–5. doi:10.1007/BF02509538. PMID 8825231.
- Holick MF, Schnoes HK, Deluca HF, Suda T, Cousins RJ (1971). "Isolation and identification of 1,25-dihydroxycholecalciferol. A metabolite of vitamin D active in intestine". Biochemistry. 10 (14): 2799–804. doi:10.1021/bi00790a023. PMID 4326883.
- "Dietary Supplement Fact Sheet: Vitamin D". Office of Dietary Supplements (ODS). معاهد الصحة الوطنية الأمريكية (NIH). مؤرشف من الأصل في 13 فبراير 201211 أبريل 2010.
- Bouillon R, Van Cromphaut S, Carmeliet G (2003). "Intestinal calcium absorption: Molecular vitamin D mediated mechanisms". Journal of Cellular Biochemistry. 88 (2): 332–9. doi:10.1002/jcb.10360. PMID 12520535.
- Puchacz E, Stumpf WE, Stachowiak EK, Stachowiak MK (1996). "Vitamin D increases expression of the tyrosine hydroxylase gene in adrenal medullary cells". Molecular Brain Research. 36 (1): 193–6. doi:10.1016/0169-328X(95)00314-I. PMID 9011759.
- "علامات و أعراض نقص فيتامين د و أسبابه وطرق العلاج". www.nmisr.com. مؤرشف من الأصل في 25 أغسطس 201825 أغسطس 2018.
- Vitamin D - Nutritional Disorders - Merck Manuals Professional Edition - تصفح: نسخة محفوظة 13 أكتوبر 2014 على موقع واي باك مشين.


