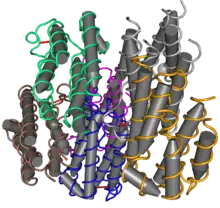
Les interférons (IFN) sont des protéines (glycoprotéines de la famille des cytokines). Ils sont naturellement produits par les cellules du système immunitaire, mais également par d'autres types cellulaires (cellules dendritiques, mononucléées, épithéliales, etc.) en fonction des sous types.
Chez la plupart des vertébrés, ils sont produits en réponse à la présence d'une double hélice d'ARN étranger dans l'organisme (plus généralement par la présence de structures moléculaires associées à des pathogènes[1]). Ils ont pour effet de défendre l'organisme des agents pathogènes tels les virus, bactéries, parasites et cellules tumorales. Ils le font en induisant la production de protéines de la fonction immunitaire (notamment antivirales et anti-bactériennes, ou à effet sur la réponse immune, et à visée anti-prolifératives).
Leur nom d'interféron donné en 1957 par Isaacs et Lindenman[2] vient du fait qu'ils interfèrent avec la réplication virale dans les cellules de l'hôte, en activant des cellules NK et les macrophages et en améliorant la résistance des cellules de l'hôte aux infections virales. Ils sont donc un des indicateurs possibles d'une infection virale.
Ils sont utilisés dans le traitement de maladies virales (hépatites, virus des papillomes, VIH, etc.), éventuellement en cancérologie (un groupe d'étude européen et américain de l'ostéosarcome EURAMOS fait une étude randomisée relative aux stratégies thérapeutiques pour ce type de sarcome). Ils sont plus rarement utilisés en traitement préventif (interférons à forte dose avec immunothérapie dans le cas de la rage avec morsure au visage).
Types (chez l'humain)
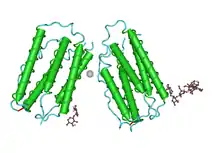
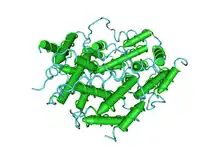
Trois types d'interféron humain coexistent : deux proviennent de cellules infectées par un virus, les molécules d'interférons sont libérées en petites quantités et diffusent vers les cellules voisines pour y empêcher la multiplication virale ; un troisième type d'interféron est produit par les lymphocytes :
- Interféron de type I : ce sont tous les types d'interférons qui se lient à un récepteur de surface cellulaire complexe connu sous le nom de l'IFN-α récepteur (IFNAR) qui rassemblent les configurations en chaines IFNAR1 (en) et IFNAR2 (en). Les interférons de type I sont chez l'homme IFN-α, IFN-β et IFN-ω [3] ;
- Interféron de type II : lié à IFNGR (en) (pour l'anglais : Interferon-gamma receptor). Chez l'homme c'est l'IFN-γ ;
- Interféron de type III : il agit sur un récepteur complexe composé de IL10R2 (aussi nommé CRF2-4) et IFNLR1 (récepteur 28 de l'interleukine, sous-unité alpha, IL28RA étant le gène humain en cause[4]) (aussi nommé CRF2-12).
Toutes les classes d'interférons sont très importantes dans la lutte contre les infections par des virus à ARN, bien que leur activité soit aussi responsable de certains symptômes tels que douleurs musculaires et fièvre (dans la lutte contre la maladie, comme lors de traitements à l’interféron).
Principes
La production d'interférons est essentiellement une réponse des cellules à des attaques microbiennes (bactériennes ou virales) et à leurs produits (glycoprotéines virales, ARN viral, toxine virale ou bactérienne, flagelle, sites CpG, etc.), aussi bien que les mitogènes et autres cytokines (interleukine 1, interleukine 2, Interleukine 12) et facteurs de nécrose tumorale ou facteurs de prolifération (Colony-Stimulating Factor) par exemple). Des interférons sont synthétisés en réponse à l'apparition d'antigènes variés dans le corps.
Fonctions naturelles
Les interférons sont :
- antiviraux ;
- antioncogéniques ;
- activateurs des macrophages et des cellules tueuses naturelles (lymphocytes NK) ;
- ce sont des glycoprotéines de classes I et II participant du complexe majeur d'histocompatibilité, et donc à la présentation des peptides étrangers (microbiens et viraux) aux Lymphocytes T ;
- antifongiques (via l'activation de la production de DRO par les neutrophiles[5]).
Induction de production d'interférons par les virus
Ils sont sécrétés lorsque des quantités anormales de doubles hélices d'ARN sont détectées par le système immunitaire à l'intérieur de la cellule.
L'ARN double-brin étranger dans une cellule agit comme déclencheur de la production de l'interféron par cette cellule, et par les cellules voisines. L’« alarme » est donnée par un récepteur de type TLRs (le TLR3) de la famille des PRRs. Le système immunitaire inné entre alors en jeu, avec l'activation du facteur de transcription IRF3 pour arriver à la phase « Beta NF kappa ». Le gène codant cette cytokine est activé dans toute cellule infectée, mais il s’active aussi chez les cellules voisines pour y synthétiser de l'interféron. La cellule originelle meurt, tuée par le virus à ARN ; par cytolyse virale. Elle libère des milliers de virus qui vont infecter les cellules voisines. Toutefois, ces cellules auront déjà commencé à produire ou recevoir des interférons, qui en quelque sorte « ont prévenu les cellules périphériques qu'il y avait un loup dans la bergerie ». Ces cellules ont en réaction déjà commencé à produire de grandes quantités d'une protéine dite « protéine-kinase R (en) » (ou PKR).
Si un virus infecte une cellule « pré-mise en garde » par l'interféron, la PKR est activé indirectement par l'ARN viral (en fait, par les 2'-5 'oligoadénylates produites par les 2'-5'-oligoadénylates synthétases, qui sont produites en raison de l'activation TLR3). Commence alors le transfert de groupements phosphate (phosphorylation) à une protéine dite eIF-2 (eIF-2 signifie « Eukaryotic Initiation Factor 2 » chez les eucaryotes). Après la phosphorylation, eIF2 a une capacité réduite de traduction de l'ARN et donc de production de protéines codées par l'ARN, ce qui freine ou empêche la réplication virale et inhibe la fonction des ribosomes dans la cellule, tuant les virus (et la cellule hôte si la réponse est activée assez longtemps). Tous les ARN au sein de la cellule sont également dégradés, ce qui freine l'infection, même si certains des eIF2 n'ont pas été phosphorylés.
En outre, dans le cadre de la réponse aux signaux inflammatoires, l'interféron rétroagit sur le complexe majeur d'histocompatibilité de classe I (CMH I), ce qui conduit :
- à accroître la présentation de peptides viraux aux cellules tueuses CD8 T ;
- à un changement dans le complexe enzymatique multiprotéique dit « protéasome » (alors connu sous le nom d’immunoprotéasome), par échange de quelques sous-unités bêta par b1i, b2i, b5i, qui conduit à une augmentation de la production de peptides compatibles avec le CMH I.
L'interféron agit sur la protéine p53 (une protéine qui interagit avec les virus en train d'infecter une cellule, et impliquée dans certains cancers). L’interféron agit sur cette dernière comme un inducteur provoquant une augmentation de la production du gène p53. Cela favorise l'apoptose cellulaire, ce qui limite la capacité du virus à se dupliquer.
Une augmentation des niveaux de transcription est également observée dans les cellules voisines non-infectés, mais seules les cellules infectées déclenchent une apoptose. Cette augmentation de la transcription pourrait servir à préparer les cellules en danger et à une réaction plus rapide en cas d'infection. Lorsque la protéine p53 est induite par la présence virale, elle se comporte différemment qu'elle ne le fait habituellement. Certains gènes de la p53 sont exprimées sous l’effet de la charge virale, mais d'autres, en particulier ceux qui répondent aux dommages de l'ADN, ne le sont pas. L'un des gènes qui n'est pas activé (le p21) peut favoriser la survie des cellules. Maintenir ce gène inactif contribuerait à promouvoir l'effet apoptotique. L'interféron renforce les effets apoptotiques de p53, mais il n'est cependant pas strictement nécessaire. Les cellules normales présentent une plus forte réponse apoptotique de cellules sans p53[6],[7]. L'interféron a un intérêt thérapeutique démontré contre certains cancers, probablement en raison de ses effets sur la p53, ce qui le rend utile pour compléter ou remplacer une chimiothérapie médicamenteuse activant la p53, mais il peut aussi produire des effets secondaires indésirables[6] dont certains peuvent être sérieux, sévères et durables.
Cinétique dans l'organisme
Les interférons passent rarement la barrière placentaire, mais peuvent traverser la barrière hémato-encéphalique.
Leur métabolisation et l'excrétion des métabolites d'interférons se déroulent principalement dans le foie et les reins.
Usages pharmaceutiques
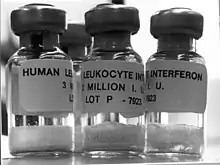
Ils sont utilisés :
- comme médicaments anti-infectieux et anti-oncogènes notamment (en combinaison avec la chimiothérapie et la radiothérapie) contre de nombreux cancers ;
- dans le traitement de la sclérose en plaques (interféron bêta-1a) ;
- dans le traitement de l'hépatite C chronique (interféron alpha-2b) ; plus de 50 % des hépatite C traités par interféron répondent au traitement avec élimination durable du virus (selon analyses de sang et études histologiques hépatiques sur biopsie). Donner immédiatement de l'interféron après une infection peut également prévenir l'infection chronique par hépatite C, mais cela peut rarement être fait car les personnes infectées par le VHC ne présentent pas de symptômes avant plusieurs mois, voire avant plusieurs années ;
- en prévention de maladies respiratoires virales telles que rhumes et grippe, en administration intranasale de très faibles doses d'interféron. Ce traitement est largement utilisé en Europe de l'Est et Russie, mais sans que les mécanismes de leur action aient été bien compris (on estime habituellement qu’il faut des doses plus élevées de plusieurs ordres de grandeur pour avoir un effet sur ces virus). C'est pourquoi la plupart des scientifiques occidentaux sont sceptiques quant à l’efficacité de ce traitement[8].
Un traitement à l'interféron pourrait peut-être protéger des cancers futurs.
Types d'interférons thérapeutiques
Plusieurs types d'interféron sont maintenant approuvés pour utilisation chez l'homme.
Aux États-Unis, la Food and Drug Administration (FDA) a approuvé en 2001 et 2002 plusieurs formules de « pegylated interferon-alpha » dans lequel du polyéthylène glycol a été ajouté à l'interféron pour le faire durer plus longtemps dans l'organisme. Cette forme « pégylatée » est injectée une fois par semaine au lieu de trois pour les traitements classiques à l’interféron. Utilisé en combinaison avec des antiviraux (ex. : ribavirine), l'interféron pégylé donne des taux de guérison durable de 75 % ou plus chez les personnes touchées par une hépatite C de génotype 2 ou 3 (facile à traiter), mais reste inférieur à 50 % chez les personnes atteintes par le génotype 1 (le plus commun aux États-Unis et en Europe occidentale).
L'interféron-bêta-1a et l’interféron bêta-1b sont utilisés pour traiter ou contrôler la sclérose en plaques. Par un mécanisme encore inconnu, l'interféron-bêta inhibe la production de cytokines Th1 et l'activation des monocytes.
Voie d'administration
En thérapie systémique, IFN-α et IFN-γ sont le plus souvent administrés en injection intramusculaire.
L'injection d'interférons dans le muscle, dans la veine ou sous la peau est généralement bien tolérée.
Une production d'interféron alpha peut également être induite par de petites molécules d’imidazoquinoléine, par l'activation du récepteur TLR7. L’Aldara (imiquimod) en crème utilise ce mécanisme pour inciter l’organisme à produire l'IFN alpha et l'IL12. Ce médicament est approuvé par la FDA pour le traitement de certaines kératoses (kératose actinique), de carcinomes basocellulaires superficiels et de verrues génitales externes.
Effets indésirables
Les effets indésirables les plus fréquents correspondent à des symptômes pseudo-grippaux :
- hausse de la température corporelle ;
- douleurs musculaires, fatigue, céphalées ;
- convulsions, vertiges ;
- amincissement des cheveux ;
- dépression ;
- insomnie, troubles de l'humeur, diarrhées ;
- et parfois des érythèmes, une douleur et une induration au lieu d’injection.
L’interféron étant immunosuppresseur, il peut (en particulier en cas de neutropénie) donner lieu à des infections opportunistes[9]. Tous ces effets indésirables sont généralement réversibles et disparaissent quelques jours après la fin de la thérapie.
De nombreux cas signalés montrent une persistance de certains effets secondaires jusqu'à 20 années plus tard.
L'interféron peut induire des dysfonctionnements de la conduction du muscle cardiaque provoquant une arythmie de type auriculaire.
Sur le marché
Sont par exemple disponibles :
- Rebif, forme liquide d'interféron beta 1a ;
- Avonex, forme lyophilisée d'interféron beta 1a ;
- Biocad, biosimilaire de l'interferon beta 1a prouve par le ministère de la santé Russe ;
- Cinnovex, forme générique/biosimilaire d'interféron beta 1a (Avonex) ;
- Betaferon, forme lyophilisée d'interféron beta 1b ;
- Extavia, forme lyophilisée d'interferon beta 1b ;
- Roferon A, regular Interferon-alpha2a ;
- Intron-A, regular Interferon-alpha2b ;
- Imukin, Interferon gamma ;
- PEGASYS, « pegylated Interferon alpha 2a » ;
- PegIntron, « pegylated Interferon alpha 2b » ;
- Reiferon Etard, « pegylated Interferon alpha 2a » ;
- Multiferon, Sous-type d'interféron alpha humain.
Notes et références
- ↑ George D Kalliolias et Lionel B Ivashkiv, « Overview of the biology of type I interferons », Arthritis Research & Therapy, vol. 12, no Suppl 1, , S1 (ISSN 1478-6354, PMID 20392288, PMCID 2991774, DOI 10.1186/ar2881, lire en ligne, consulté le )
- ↑ Isaacs et Lindenmann observent que des cellules de poulet infectées par le virus de la grippe produisent une cytokine permettant à d’autres cellules de devenir résistantes à ce virus. Cf Isaacs A., Lindenmann J. (1957) Virus interference. I. The interferon. Proc. R. Soc. London Ser. B 147:258–267.
- ↑ Liu YJ, IPC: professional type 1 interferon-producing cells and plasmacytoid dendritic cell precursors, Journal : Annu Rev Immunol, 2005, Volume 23, pages 275 à 306, ; doi:10.1146/annurev.immunol.23.021704.115633
- ↑ Entrez Gene: IL28RA interleukin 28 receptor, alpha (interferon, lambda receptor)
- ↑ (en) Vanessa Espinosa, Orchi Dutta, Constance McElrath et Peicheng Du, « Type III interferon is a critical regulator of innate antifungal immunity », Science Immunology, vol. 2, no 16, , eaan5357 (ISSN 2470-9468, PMID 28986419, PMCID PMC5880030, DOI 10.1126/sciimmunol.aan5357, lire en ligne, consulté le )
- 1 2 (en) Takaoka A, Hayakawa S, Yanai H. et al. « Integration of interferon-alpha/beta signalling to p53 responses in tumour suppression and antiviral defence » Nature 2003; vol. no 424 question = 6948, pages 516 à 523. DOI 10.1038/nature01850 [http:/ / www.nature.com/nature/journal/v424/n6948/pdf/nature01850.pdf url])
- ↑ (en) O Moiseeva, Mallette FA, Moores A, Ferbeyre G. « DNA damage signaling and p53-dependent senescence after prolonged beta-interferon stimulation » Mol Biol Cell. 2006; volume 17, Chap 4, pages 1583-92. DOI 10.1091/mbc.E05-09-0858
- ↑ Source
- ↑ (en) Bhatti Z, Berenson CS, « Adult systemic cat scratch disease associated with therapy for hepatitis C » BMC Infect Dis. 2007;7:8. {{Doi :10.1186/1471-2334-7-8}}