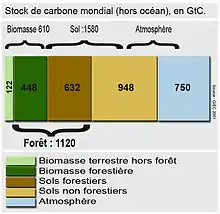
Un puits de carbone ou puits CO2 est un réservoir de carbone (naturel ou artificiel) absorbant du carbone depuis le cycle du carbone. Ce carbone est séquestré dans le réservoir avec un temps de résidence très long par rapport à celui dans l'atmosphère.
Les puits de carbone principaux sont les océans[1] par dissolution et le vivant par assimilation via la flore (forêt, tourbière, prairies, phytoplancton), la faune, et les sols (humus). Les bactéries photosynthétiques, les organismes végétaux et la chaine alimentaire ainsi que la nécromasse qui en dépendent contribuent aux puits de carbone.
En stabilisant la quantité de CO2 atmosphérique, les puits de carbone influent sur le climat planétaire, les écosystèmes et la présence des espèces. Les équilibres récents sont désormais menacés par la production massive de carbone anthropique et sa diffusion dans l'atmosphère. Les puits de carbones absorbent et séquestrent une partie seulement de ce nouvel apport. Ces puits sont eux-mêmes dégradés : la végétation potentielle diminuée par les activités humaines a réduit sa capacité de stockage de carbone par assimilation de 900 à 450 pétagrammes/an[2].
En France, la loi Grenelle II prévoit[3] qu'un rapport du Gouvernement au Parlement portera sur « l'évaluation des puits de carbone retenu par les massifs forestiers » et leur « possible valorisation financière pour les territoires » (art. 83).
Sur le temps long, les processus biologiques d'assimilation et dépôts ont permis l'accumulation d'importants stocks de carbone fossile sous forme de charbon, pétrole, gaz naturels, hydrates de méthane et roches calcaires. Ces stocks datent principalement du Carbonifère.
Puits naturels
Tourbières, toundra
Ces écosystèmes comptaient parmi les meilleurs puits de carbone, mais de nombreuses tourbières ont été exploitées, drainées (ce qui entraine une minéralisation avec perte de carbone), brûlées (en Indonésie par exemple pour planter des palmiers à huile), ou simplement, sous l'effet du réchauffement peuvent voir leur sol rapidement évoluer (et des études expérimentales de sols légèrement réchauffés montrent que les pertes de carbone des sols induites par le réchauffement sont les plus importantes en zone périarctique là où les stocks de carbone sont les plus importants ; si l'eau ne manque pas le réchauffement augmente la photosynthèse, mais sans compenser les émissions de CO2 ou de méthane dues à une activité accrue des microbes du sol, activité d'autant plus importante que le sol est riche en carbone[4]).
Une estimation faite en 2016 pour un réchauffement de 2 °C en 2100, avec l'hypothèse la plus prudente en termes de perte de carbone, a conclu à une perte nette minimale de 55 pétagrammes de carbone (1 Pg = 1015 g) entre 2015 et 2050, soit l'équivalent de cinq ans d'émissions anthropiques actuelles[4]. La majeure partie des pertes se fera dans l'hémisphère nord[4].
Forêts
L'écosystème forestier (et en particulier le système arbre/sol) est, après le plancton océanique et avec les tourbières et les prairies, le principal puits de carbone naturel planétaire, essentiel au cycle du carbone. Il accumule d'énormes quantités de carbone dans le bois, les racines, le sol et l'écosystème via la photosynthèse. L'ONU/FAO estime que « l'expansion des plantations d'arbres pourrait compenser « 15 % des émissions de carbone des combustibles fossiles » dans la première moitié du XXIe siècle sous réserve qu'elles ne le relarguent pas prématurément[6], et qu'on n'ait pas surestimé les surfaces enforestées et leur capacité de stockage[6] et qu'il ne s'agisse pas que de plantation d'essences à croissance rapide[6].
En effet, les plantes absorbent le CO2 de l'atmosphère, stockant une partie du carbone prélevée et rejetant de l'oxygène dans l'atmosphère. Chez les arbres, les essences pionnières, à croissance rapide (ex : Peuplier, saule ou bouleau en zone tempérée, Bois-canon (creux, à la manière du bambou) en zone tropicale), n'absorbent généralement que peu de carbone et le relarguent vite et facilement. Au contraire, les bois durs et denses en contiennent beaucoup plus, et pour le plus longtemps, mais ils croissent généralement bien plus lentement (siècles à millénaires pour les « très gros bois »). À maturité, l'absorption est moindre, mais le carbone représente 20 % de leur poids (en moyenne, et jusqu'à 50 % et plus pour des bois denses tropicaux).
Quand l'arbre meurt, il est décomposé par des communautés saproxylophages (bactéries, champignons et invertébrés) qui recyclent son carbone sous forme de biomasse, nécromasse (cadavres, excrétas et excréments de ces organismes) et sous forme de gaz (CO2, méthane, libérés dans l'atmosphère ou l'eau). La forêt et d'autres écosystèmes continueront à stocker ou recycler ce carbone via une régénération naturelle. Toutes les forêts tempérées (hors incendies et exploitation) accumulent le carbone. Une grande partie des forêts tropicales (hors forêts tourbeuses) sont réputées à l'équilibre (source = puits), et les forêts boréales jouent un rôle plus complexe (plus sensibles aux défoliations et au feu).
Il arrive localement que les arbres morts, roseaux et plantes des marais se décomposent lentement et imparfaitement, en conditions anaérobies, sous la surface du marais, produisant des tourbes. Le mécanisme est suffisamment lent pour que, dans la plupart des cas, le marais grandisse assez vite et permette de fixer plus de carbone atmosphérique que ce qui est libéré par la décomposition. Un quart du carbone absorbé par les forêts l'est par les plantes et le sol[7].
Pour l'ONU, la FAO, pour ses statistiques et inventaires forestiers, distingue[8] cinq différents stocks de carbone :
- la biomasse aérienne : « Carbone présent dans toute la biomasse vivante au-dessus du sol, y compris les tiges, les souches, les branches, l’écorce, les graines et le feuillage »[8] ;
- la biomasse souterraine : « Carbone présent dans toute la biomasse de racines vivantes. Les radicelles de moins de deux mm de diamètre sont exclues car il est souvent difficile de les distinguer empiriquement de la matière organique du sol ou de la litière »[8] ;
- le carbone du bois mort : de la nécromasse ligneuse – hors de la litière – « soit sur pied, soit gisant au sol, soit dans le sol. Le bois mort comprend le bois gisant à la surface, les racines mortes et les souches dont le diamètre est supérieur ou égal à dix cm ou tout autre diamètre utilisé par le pays »[8] ;
- le carbone de la litière : « Carbone présent dans toute la biomasse non vivante dont le diamètre est inférieur au diamètre minimal pour le bois mort (p. ex. dix cm), gisant à différents stades de décomposition au-dessus du sol minéral ou organique »[8] ;
- le carbone dans le sol : « Carbone organique présent dans les sols minéraux et organiques (y compris les tourbières) jusqu’à une profondeur spécifique indiquée par le pays et appliquée de façon cohérente à travers toutes les séries chronologiques »[8].
Remarque : En 2015, des chercheurs de l'université de Brême ont (dans Atmospheric Chemistry and Physics début janvier), à partir de données satellitaires, estimé que les forêts européennes extrairaient plus de deux fois plus de dioxyde de carbone qu'on ne le pensait jusqu'ici[9], mais une tendance au recul continu ou à la minéralisation des tourbières forestières ou paraforestières et au développement rapide de valorisation du bois (voire du petit-bois et des feuilles mortes) en biomasse-énergie laisse penser que cette absorption de carbone pourrait souvent être suivie d'un relargage rapide dans l'atmosphère.
Mais dans un contexte climatique incertain, certaines forêts plus vulnérables peuvent devenir des « sources » de CO2 (le contraire d'un puits de carbone), notamment en cas d'incendie, ou provisoirement après les grands chablis couchés par de fortes tempêtes ou après les grandes coupes rases. En 2016 une étude a conclu que la toundra et la taïga sont les écosystèmes qui risquent proportionnellement (notamment parce que leur sol était très riches en carbone), de perdre le plus de carbone du sol d'ici 2100, au risque de basculer d'une situation globale de puits de carbone, vers une situation d'émetteur, qui pourrait alors encore exacerber le réchauffement climatique[4].
Certaines techniques de génie écologique (BRF, conservation de gros bois mort, réintroduction du castor, restauration des zones humides et tourbières, etc.) peuvent contribuer à augmenter la résilience écologique de certaines forêts (Europe, Canada, Amérique du Nord, etc.). Les travaux récents (2017) issus des données du satellite OCO-2 montrent notamment que dans les années 2010, près d'un quart du CO2 anthropique est absorbé par l'océan (en l'acidifiant) et un autre quart est absorbé par les sols et écosystèmes terrestres. Toutefois, les lieux et processus de puits terrestres de carbone restent mal cernés en particulier concernant les parts respectives des forêts tempérées, tropicales et équatoriales, eurasiennes notamment (certains auteurs comme Baccini & al. (2017) estiment à partir des données MODIS qu'une partie importante de ces régions est actuellement source nette et importante de CO2 en raison de la déforestation, des incendies[10], et que cela pourrait empirer avec un risque croissant de sécheresses, dégradation des sols et incendies de forêt). Il y a au moins consensus sur le fait que ces puits varient quantitativement beaucoup selon les années[11]. Il n'y a pas encore de consensus sur la quantité de carbone réellement stocké et/ou libéré à court, moyen ou long terme, mais le satellite OCO-2 devrait d'ici 2020 apporter des données permettant de mieux comprendre ces phénomènes. OCO-2 va notamment permettre de préciser le rôle et la part et l'efficacité des différents puits planétaires et donc d'améliorer la prospective climatique et les possibilités de correction et d'adaptation.
Forêt française, stock et puits de carbone
.jpg.webp)
Dans le monde, la forêt métropolitaine française compte peu en termes de stock de carbone. À l'échelle du pays, elle joue un rôle important, mais variant régionalement[6]. Sa taille augmente, mais après une longue phase de régression.
Plusieurs estimations ont été faites : en 1990 l'IFN estimait à deux milliards de tonnes environ[12]. Ce chiffre a été porté en 2004[13] à 2,5 milliards de tonnes de carbone (soit l’équivalent de 9,2 milliards de tonnes de CO2 absorbé). De 2000 à 2004, environ 24,4 millions de tonnes (Mt)/an de carbone auraient ainsi été provisoirement séquestrées par les arbres et les sols forestiers (89 Mt/an de CO2). L'estimation a ensuite baissé au niveau de 62 Mt/an de CO2 (soit 17 Mt/an de carbone) entre 2005 et 2011 dont en raison de la tempête de 2009 et de la sécheresse de 2003[14]. Au vu de la surface boisée de France métropolitaine, 1,68 t de carbone/ha/an auraient été séquestrées de 2000 à 2004 (14,5 Mha[15]) et de 1,04 t/ha/an sur 2005-2011 (16,5 Mha[16]).
Cette quantité de carbone serait stockée pour moitié dans les sols (litière plus humus) et plus provisoirement peut-être pour moitié dans les arbres (feuilles, branches, racines y compris)[13]. Seule une petite partie de ce carbone peut être considérée comme durablement stockée.
Le prix de la tonne de CO2 stockée a chuté de 32 € en avril 2006, puis 0,20 € en 2007), ce serait 0,6 milliard d’euros, 2,8 milliards d’euros et 0,02 milliard d’euros économisés[13]. Cette variation des prix dictée par le marché ne permet pas d'évaluer la valeur financière de la fonction puits de carbone des forêts, mais cette valeur devrait a priori augmenter avec le temps.
La filière bois, selon la durée de vie du bois extrait et manufacturé, contribue ou non à la lutte contre le réchauffement climatique. Elle a en 2004 utilisé 98 Mt de carbone (équivalant 359 Mt de CO2) mais dont une partie (papier, carton, cagettes, etc.) ne contribue pas à stocker du carbone[13].
La forêt française, qui s'étend sur 168 000 km2, soit un tiers du territoire métropolitain, piège de moins en moins de carbone. Depuis le milieu des années 2000, ses capacités de stockage s'érodent sous l'effet du réchauffement climatique. Elles sont passées de 45 Mt de CO2 au milieu des années 2000 à environ 35 Mt en 2015 et seulement 14 Mt en 2020 selon le Citepa. Or la Stratégie nationale bas carbone (SNBC) prévoit de plus que doubler entre 2015 et 2050 la taille du puits de carbone de la France, à 80 Mt, afin de compenser les émissions résiduelles. La SNBC compte sur des solutions telles que la plantation de haies (quintuplement des surfaces plantées et « agroforestées »), l'arrêt du retournement des prairies, la baisse de l'artificialisation des terres, la relance des plantations et la prolongation dans le temps du stockage du carbone en valorisant la matière bois dans des filières comme celles des produits bois à longue durée de vie, plutôt que dans le chauffage[17].
Océans
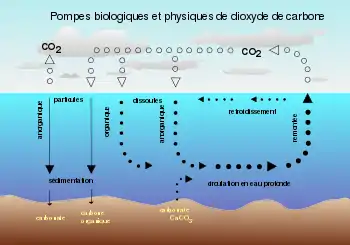


Les océans sont les principaux puits naturels de carbone, assimilé via le plancton, les coraux et les poissons, puis transformé en roche sédimentaire ou biogénique. On estime qu'ils concentrent 50 fois plus de carbone que l'atmosphère, 90 % par la pompe physique (en), 10 % par la pompe biologique. Mais ces chiffres de stock doivent être nuancés par les flux annuels. Une estimation sur la période 2000–2006 donne les chiffres suivants : les émissions anthropiques de dioxyde de carbone sont absorbées à 45 % dans l'atmosphère, 30 % par la terre et 24 % par les océans[19].
50 % environ des coraux des eaux chaudes semblent malades ou morts ces dernières décennies, et lorsque le niveau de CO2 s'accroît au-delà d'un seuil critique dans l'atmosphère, en augmentant également l'acidité des eaux marines, créant potentiellement de désastreux océans acides qui pourraient tuer le plancton qui piégeait le mieux le carbone, et rendant l'océan plus acide encore. De plus des zones mortes s'étendent dans les océans, qui deviennent émettrices de carbone ou de méthane. Les mers contiennent une quantité variable de CO2 dissoute, fonction de la biomasse et de la nécromasse, de la disponibilité en nutriments, de la température et de la pression.
Le phytoplancton marin, à l'instar des arbres, utilise la photosynthèse pour extraire le carbone du CO2. Il est le point de départ de la chaîne alimentaire océanique. Le plancton et d'autres organismes marins utilisent le CO2 dissous dans l'eau ou prélevé dans leur nourriture pour constituer leurs squelettes et coquilles à base de calcaire minéral, CaCO3. Ce mécanisme élimine le CO2 contenu dans l'eau et favorise la dissolution de celui contenu dans l'air. Les squelettes et coquilles calcaires ainsi que le « carbone organique » (nécromasse, excrétas et excréments) de ces organismes tombent finalement en une « pluie » continue (dite « neige marine ») dans les fonds marins où ils sédimentent pour lentement former des roches sédimentaires. Le carbone des cellules du plancton doit être immergé entre 2 000 et 4 000 mètres de profondeur pour être emprisonné pour plusieurs milliers à millions ou milliards d'années sous forme de roche, les sédiments superficiels étant pour partie brassés, remis en suspension et réutilisés comme nutriments par la biosphère.
Résultats contradictoires sur l'état et capacités des puits de carbone océaniques
- Une étude qui cherchait à affiner la mesure de la dissolution récente du CO2 dans l'océan (utilisant les chlorofluorocarbones comme marqueurs), publiée en 2003 laissait penser que la capacité des océans à absorber le CO2 avait été sous-estimée[20], cependant ceci est aussi le signe d'une accélération de l'acidification des océans qui peut mettre en péril le puits de carbone océanique et se traduire par un relargage de CO2.
- Inversement, des travaux récents concluent à une émission importante de CO2 et de méthane par les estuaires, et à une saturation du puits océanique pour l'hémisphère sud, ou plutôt à une dégradation de la capacité de ces mers à pomper du carbone en raison des changements climatiques qui affectent les vents et l'agitation de l'eau. Selon Nicolas Metzl et son équipe, les mesures faites de 1998 à 2007 par le service d'observation de l'océan indien (OISO) et les données accumulées depuis 1991 montrent que le taux de CO2 a augmenté plus vite dans les eaux de surface de cet océan que dans l'air (sachant que la diffusion du CO2 dépend de la température et de la différence de concentration dans l'air et l'eau). Cependant, les vents ont augmenté dans l'hémisphère sud, induisant un brassage des eaux de surface qui leur font perdre du CO2, et qui induisent un mélange avec les eaux profondes plus riches en CO2. Les puits de carbone de l'océan indien pourraient donc être environ 10 fois moins efficace qu'on ne l'avait antérieurement estimé.
Un autre programme, européen, CARBOOCEAN a également conclu à une situation mauvaise au nord : la capacité de puits de CO2 aurait été divisée par deux aux latitudes élevées de l'hémisphère nord, depuis 1996.
Les hydrates de méthane piégés dans l'océan sont également un facteur à prendre en compte en cas de début de réchauffement marqué, qu'ils pourraient accélérer.
Ces quatre éléments, sous réserve de confirmation pourraient significativement modifier les modélisations quand elles les intègreront[21]. - Une étude[22]. du début 2009 a montré qu'on avait fortement sous-estimé l'importance des poissons qui, par leur capacité à constamment produire dans leur intestin des carbonates peu solubles, contribuent aussi à séquestrer du carbone des eaux marines. Par exemple, le flet européen synthétise et rejette chaque heure et en moyenne 18 micromoles de carbone par kg de poisson (sous forme de calcite)[22]. Les poissons contribueraient ainsi à 3 %[23] à 15 %[24] du puits de carbone océanique (voire 45 % si l'on prenait les hypothèses les plus hautes)[22]. De plus, un climat chaud associé à la surpêche tendent à réduire le nombre de grands poissons ; or, une petite taille du poisson et un eau plus chaude favorisent la formation de carbonates de calcium ou de magnésium (qui sont éliminés avec la nécromasse, les fèces ou des boulettes de mucus)[22].
Hélas, ces carbonates plus riche en magnésium sont aussi plus solubles à grande profondeur. Ils peuvent alors relarguer une partie de leur carbone, mais en tamponnant le milieu, au point que cela pourrait expliquer jusqu'à un quart de l'augmentation de l'alcalinité titrable des eaux marines dans les 1 000 mètres sous la surface (cette anomalie de dureté de l'eau était jusqu'ici controversée car non expliquée par les océanographes)[22].
Hélas encore, c'est aussi dans les zones les plus favorables à ce piégeage du carbone (plateaux continentaux où se concentre environ 80 % de la biomasse en poisson) que la surpêche est la plus intense et que les zones mortes ont fait disparaître le plus de poissons.
Rôle encore mal compris de la grande faune marine
Selon l'université Flinders[25] (Australie), les cachalots jouent par exemple un rôle important dans le recyclage du fer, via ses excréments qui en contiennent de grandes quantités ; le fer - quand il est biodisponible - est un stimulant connu de la productivité phytoplanctonique, qui est à la base de la pompe à carbone océanique[25]. Les 12 000 cachalots d'Antarctique contribuent ainsi à permettre l'absorption d'environ 400 000 t de carbone (environ deux fois ce que les cachalots émettent en respirant). Leurs excréments dispersent annuellement environ 50 t/an (de fer) dans les océans, ce serait au moins dix fois plus, s'ils n'avaient pas été pourchassés depuis deux siècles[25]. Sans la chasse à la baleine, on estime qu'il y aurait aujourd'hui environ 120 000 (90 % plus qu'en réalité) cachalots rien que dans l'océan Austral[25].
Restaurer ou améliorer la séquestration naturelle
Séquestration par l'arbre et la forêt
Certaines forêts stockent beaucoup de carbone dans leur biomasse et nécromasse, et via leur sol (ex : certaines tourbières boisées d'Indonésie atteignent 40 m d'épaisseur). D'autres forêts ne stockent que peu de carbone et le puits n'existe que si elles grandissent ou si leur sol s'enrichit durablement en carbone. Des incendies répétés peuvent leur faire perdre en quelques heures une grande partie du carbone stocké durant des décennies ou siècles.
La séquestration forestière est néanmoins faible au regard des rejets de CO2 liés à la combustion de carbone fossile (charbon, pétrole et gaz naturel). Il y a un consensus sur l'importance de protéger les forêts relictuelles, notamment contre les incendies de forêt, mais même les scénarios les plus optimistes concluent que planter massivement de nouvelles forêts ne suffirait pas à contrebalancer l'augmentation des émissions de gaz à effet de serre ni endiguer le réchauffement climatique. Ainsi, réduire les émissions américaines de carbone de 7 %, comme stipulé dans le protocole de Kyoto, nécessiterait la plantation d'une forêt de la taille du Texas tous les 30 ans, selon William H. Schlesinger, doyen de l'« École Nicolas sur l'environnement et les sciences de la terre » à l'université Duke de Durham, N.C. Pour compenser leurs émissions, la plupart des régions développées devraient planter une surface bien plus grande que l'ensemble de leur territoire. Il faudrait au total boiser une surface plus grande que celle qui est disponible sur les terres émergées (champs, villes et routes inclus).
De plus, on a montré en 2005 que si la croissance du taux de CO2 de l'air a dopé la croissance à court terme de certains arbres (notamment d'une gamme d'espèces européennes d'arbres), cette croissance accélérée s'accompagne aussi d'une croissance des champignons et bactéries symbiotes des arbres et d'autres des microorganismes, ce qui se traduit in fine par une augmentation significative de la « respiration microbienne du sol et une diminution marquée de la séquestration du carbone dérivé des racines dans le sol. Si de tels processus sont à l'oeuvre dans les écosystèmes forestiers, la taille du puits de carbone terrestre annuel peut être considérablement réduite, en entraînant une rétroaction positive sur le taux d'augmentation de la concentration de dioxyde de carbone atmosphérique »[26].
Pour les forêts d'altitude d'Afrique orientale, une étude de 2019 montre que le potentiel de stockage a au contraire été sous-estimé[2] et il n'est pas négligeable, surtout si l'on vise des bois durs et denses et l'enrichissement des sols en matière organique, en zone tempérée notamment[27].
On a récemment (2017) montré que certains sols forestiers sont aussi des « puits de méthane » significatifs grâce aux bactéries méthanotrophes qu'ils abritent, et que la consommation de méthane augmente avec l’âge des peuplements et avec la porosité des sols[28].
Le type de forêt est important : les forêts tempérées poussent le plus vite, mais les forêts tourbeuses nordiques forment aussi de bons puits de carbone (tourbières). Les forêts tropicales ont d'abord été jugées neutres à l'égard du carbone, mais une étude de 2008[29] (mesures faites sur deux millions d'arbres dans le monde) a montré qu'elles étaient globalement aussi des puits de carbone, fonction qui pourrait cependant bientôt être limitée par le stress hydrique et les incendies, tout comme en zone de taïga.
Le type de gestion importe également : une très jeune forêt plantée sur coupe rase peut avoir un bilan-carbone négatif les dix ou douze premières années, perdant plus de carbone (décomposition, lessivage) qu'elle n'en stocke. La coupe rase favorise l'érosion des sols et la perte du carbone qu'ils contenaient (significative en zone tempérée et froide).
Le « réseau forestier de puits de CO2 » à long terme est exposé aux incendies, aux tempêtes, aux maladies. La canopée modifie la réflexion de la lumière solaire, ou albédo. Les forêts de haute à moyenne latitude ont un albédo plus faible en périodes de neige que les forêts enneigées de latitude basse, contribuant au réchauffement local, contrebalancé par une augmentation de l'évapotranspiration. Divers programmes proposent à des entreprises d'acheter des parcelles de forêt pour les protéger (ex action « Cool Earth »), en échange de « crédits-carbone » compensant des émissions industrielles ou de particuliers. Cette approche est discutée. Ainsi en octobre 2007, Davi Kopenawa (chamane amérindien (yanomami) ayant obtenu le prix Global 500 du PNUE en 1991) a remis à Gordon Brown (Premier ministre britannique) un rapport montrant que la protection de la forêt par la reconnaissance des droits fonciers de leurs populations autochtones permettrait de protéger rapidement 15 000 fois la surface concernée par le programme « Cool Earth » (162 millions d'ha de forêt tropicale ont déjà ainsi été protégées, par reconnaissance des droits des populations qui y vivent, à la suite notamment du mouvement lancé par Chico Mendes dans les années 1970)[30].
Selon l'étude de Beverly Law (2008) menée sur 519 plots forestiers âgés de l'hémisphère nord, ces arbres anciens ont bien un bilan de capture de CO2 positif.
L'arbre urbain et la forêt urbaine jouent un rôle très mineur par rapport aux émissions urbaines, mais leur capacité de stockage semble avoir été sous-estimée ; Une étude faite à Leicester[18] de ses puits de carbone (publiée en 2011) a montré que la flore urbaine y stockait en tout 231 521 tonnes de carbone, soit 3,16 kg m−2 en moyenne. Les jardins privés en stockent plus que le milieu rural agricole (environ 0,76 kg, soit un peu plus qu’une prairie anglaise (0,14 kg m−2).
Mais ce sont surtout les grands arbres urbains qui formaient le principal puits de carbone (stockant plus de 97 % de la quantité totale de carbone de la biomasse végétale totale urbaine), avec en moyenne 28,86 kg m−2 pour les espaces verts publics boisés. Or, les grands arbres sont rares à Leicester où les espaces verts sont surtout engazonnés et pauvres en arbres[18]. Si 10 % de ces gazons étaient plantés d’arbres, le stockage de carbone de la ville augmenterait de 12 % selon cette étude qui a aussi montré que les estimations existantes au Royaume-Uni avaient sous-estimé d’un ordre de grandeur l’importance de ce stock urbain de carbone[18].
Le rôle des forêts tend à être intégré dans les accords internationaux sur le climat, notamment dans le cadre de l'Accord de Paris sur le climat pour aider les pays a atteindre leurs cibles d'atténuation du changement climatique[31]. Si les CND étaient vraiment mis en œuvre, la forêt pourrait pourvoir un quart des réductions d'émissions prévues par les pays[32]. Ceci impliquerait cependant une plus grande transparence dans les engagements des pays et une amélioration de la confiance dans les chiffres, dont en réconciliant les estimations des rapports nationaux avec les études scientifiques (≈ 3 GtCO2/an)[32].
Séquestration océanique
L'océan est le principal puits de carbone planétaire, la dissolution du carbone atmosphérique dans l'océan conduit à l'Acidification des océans.
L'ajout de microparticules de fer (hématite) ou de sulfate de fer dans l'eau a été proposé pour doper la séquestration du carbone par l'océan par le plancton . Le fer naturel est un oligoélément, facteur limitant pour la croissance du phytoplancton. Il provient des remontées d'eau profonde le long de côtes (« upwellings »), des rivières et retombées d'aérosols et poussières. Certains estiment que les sources naturelles de fer diminuent depuis quelques décennies, limitant la productivité organique et la biomasse océaniques (NASA, 2003) et donc le pompage biologique du CO2 atmosphérique par la photosynthèse.
En 2002 , un test dans l'océan Pacifique près de l'Antarctique a suggéré qu'entre 10 000 et 100 000 atomes de carbone sont absorbés lorsqu'un atome de fer est ajouté dans l'océan. Des travaux allemands (2005) ont laissé penser que tout type de biomasse carbonique des océans, soit enfoui en profondeur, soit recyclé dans la zone euphotique, représente un stockage à long terme du carbone. L'apport de nutriments ferreux dans des zones sélectionnées de l'océan, à juste mesure, pourrait alors doper la productivité océanique et limiter les effets désastreux des émissions humaines de CO2 dans l'atmosphère.
Le Pr Wolfgang Arlt de l'université Friedrich-Alexander d'Erlangen-Nuremberg (Allemagne) propose d'injecter du CO2 dissous à grande profondeur, en veillant à le répartir à l'échelle planétaire et en le tamponnant éventuellement avec des substances alcalines. Il estime que ce CO2 n'aurait qu'un faible impact en termes d'acidification s'il était injecté dans des eaux froides et denses plongeant dans l'océan profond, et que le CO2 ainsi injecté près de l'Europe serait redistribué jusqu'en Australie en un siècle, selon lui sans affecter la vie marine ni la vie des fonds marins.
D'autres doutent de la fiabilité de la méthode, notamment à long terme . Ils argumentent que les effets globaux d'adjonction de fer sur le phytoplancton et sur les écosystèmes océaniques sont mal connus, et nécessitent des études plus poussées.
- Le phytoplancton produit des nuages via la libération de sulfure de diméthyle (DMS) qui est converti en aérosols sulfatés dans l'atmosphère et formant un noyau de condensation nuageuse (ou CCN en anglais), l'eau vapeur étant un gaz à effet de serre et les nuages contribuant à modifier l'insolation et donc la photosynthèse ;
- Le risque d'eutrophisation doit être localement pris en compte (les zones marines mortes sont plus nombreuses et s'étendent) ;
- les effets de l'adjonction de fer dans un contexte d'acidification doivent être mieux compris ;
- Enfin, ce sont les mers du Sud qui se sont montrées pauvres en fer, alors qu'il ne manque pas dans l'hémisphère Nord, là où les émissions de CO2 sont les plus importantes et où la bioproductivité est la plus élevée ;
- Une campagne (KEOPS[33]) a montré[34] autour des îles Kerguelen, zone de floraison estivale annuelle de phytoplancton, que le phénomène était corrélé à la présence de fer venant des eaux profondes, mais que le puits de carbone était au moins deux fois plus important avec le fer naturel que dans le cas d'une fertilisation artificielle, et qu'il fallait bien moins de fer dans le cas de cette « fertilisation » naturelle qui s'est montrée plus de 10 fois plus efficace que les expérimentations d'ensemencement de la mer en fer.
Ceci jette le doute sur les propositions d'intervention par l'homme (géo-ingénierie), tout en confirmant l'importance des apports naturels de fer qui pourraient aussi être modifiés par des modifications des courants profonds, ce qui pourrait expliquer certaines fluctuations paléoclimatiques. - La restauration des forêts de varech au moyen de la Permaculture marine . Un article publié en 2016 dans Nature Geosciences a compilé les données d'études antérieures afin de fournir une estimation de la quantité de carbone atmosphérique éliminée par les macroalgues. Leur estimation approximative suggère qu'environ 200 millions de tonnes de dioxyde de carbone sont séquestrées par les macroalgues chaque année[35].
Le GIEC reste très prudent sur les capacités de l'océan à absorber plus de carbone, mais juge que l'étude des impacts et du comportement du CO2 dans l'océan profond doit être mieux étudiée.
L'OMI et la convention de Londres ont estimé fin 2008 que les activités de fertilisation de l'océan autres que pour des expérimentations scientifiques devaient être interdites[36].
Le cycle du méthane dans les écosystèmes et dans les eaux est par ailleurs encore également mal connu.
La recherche se poursuit, dont sous l'égide de conventions (OSPAR, ou de résolutions du réseau de collectivités KIMO[37].
Sols
On estime que les sols stockaient à la fin du XXe siècle environ 2 000 gigatonnes de carbone sous forme de matière organique (et d'hydrates de méthane en zone très froide), essentiellement en zone périarctique (toundra, taïga, pergélisols) et dans les forêts tempérées. C'est presque trois fois le carbone atmosphérique, et quatre fois le carbone de la biomasse végétale. Mais cette fonction se dégrade rapidement et presque partout, dans les sols agricoles labourés surtout. La respiration du sol (s'il n'est pas tassé ou trop déshydraté) augmente avec la température ; son réchauffement peut être source de relargage de carbone allant jusqu'au bilan négatif (plus d'émission que de stockage) dans les sols déjà très riches en carbone[38].
Restaurer de grandes quantités d'humus et de tourbes (deux matières riches en matière organique stabilisée) permettraient d'améliorer la qualité de ces sols et la quantité de carbone séquestré. Le semis direct, la vraie jachère et la restauration de sols vivants par des techniques de type BRF (Bois raméal fragmenté) peuvent y contribuer.
Le sous-sol stocke deux fois plus que le sol très superficiel.
- Les prairies accumulent d'énormes quantités de matières organiques, essentiellement sous forme de racines et micro-organismes, de manière relativement stable sur de longues durées. Mais dans le monde, depuis 1850, une grande partie de ces prairies ont été converties en champs ou urbanisées, perdant ainsi par oxydation et minéralisation de grandes quantités de carbone.
- Une agriculture sans labour augmente le carbone stocké dans le sol, y compris en zone tempérée (ex : à Boigneville dans le Bassin parisien on a doublé le stockage annuel de carbone sous une rotation maïs-blé dans le sol les 20 premières années (passant d'environ 0,10 t de C/ha et par an à 0,20), après quoi un effet de saturation semble intervenir[39].
- Une conversion de champs en pâturage extensif bien gérée emprisonne encore plus de carbone.
- Les mesures de lutte contre l'érosion, le maintien d'une couverture végétale hivernale et une rotation des cultures augmentent aussi le taux de carbone des sols.
L’augmentation du CO2 de l’air pourrait ne pas être compensée par une plus grande séquestration dans les sols, contrairement aux objectifs annoncés par l'initiative 4p1000. Une étude[40] a montré que l’exposition longue à un doublement du taux de CO2 atmosphérique accélère fortement la dégradation de la matière organique des sols forestiers d’un boisement de chênes (⇒ déstockage de carbone du sol). Les arbres ont stocké plus de carbone (212 g/m2 en aérien et 646 g/m2 dans les racines), mais 442 g/m2 de carbone ont été perdus dans le sol, essentiellement dans les 10 cm superficiels, en raison semble-t-il des impacts du CO2 sur le sol (acidification et stimulation de l'activité enzymatique des micro-organismes du sol qui augmente la décomposition de la matière organique, et plus encore s’il y a des apports carbonés (litière)). Cette étude doit être confirmée par des études sur sols riches, car il s’agissait ici de sols pauvres où le carbone était à 75 % constitué de chaînes carbonées fragiles.
Séquestration artificielle

Pour le vocabulaire officiel de l'environnement en France (tel que défini par la commission d'enrichissement de la langue française en 2019), l’expression « absorption anthropique de carbone » est définie comme : « Absorption de dioxyde de carbone dans des puits de carbone naturels conservés ou aménagés par l'homme, ou dans des installations de captage et de stockage du CO2 ». Cette commission ajoute que l'expression « absorption anthropique de carbone » est parfois généralisé à certains gaz à effet de serre autres que le dioxyde de carbone, tel le méthane. (Équivalent étranger : anthropogenic removal)[41].
Pour séquestrer du carbone artificiellement (i.e. sans utiliser le processus naturel de cycle de carbone), il doit préalablement être capturé. Ensuite, il est stocké par différents moyens.
Les usines de purification du gaz naturel doivent éliminer le dioxyde de carbone, pour éviter que la glace carbonique obstrue les camions-citernes ou empêcher les concentrations de CO2 d'excéder les 3 % maximum permis sur le réseau de distribution de gaz naturel.
Au-delà, une des techniques prometteuses de capture du carbone est la capture du CO2 émis par les centrales électriques (dans le cas du charbon, ceci est connu en tant que « charbon propre »). Ainsi, une centrale électrique au charbon d'une puissance de 1 000 MW produisant typiquement de l'ordre de 6 TWh électriques par an, elle rejette environ 6 millions de tonnes de CO2 chaque année. La méthode la plus simple et la plus courante pour capturer le CO2 qu'elle émet consiste à faire passer les gaz d'échappement issus de la combustion dans un liquide dans lequel le CO2 va se dissoudre, puis ce liquide est transporté dans un dispositif permettant de récupérer le CO2 dissous. Cette méthode, applicable à la combustion de n'importe quel combustible fossile, renchérit fortement le coût de production de l'électricité (typiquement, pour le charbon et dans les pays développés, de près d'un facteur 2), et consomme 10 à 20 % de l'énergie obtenue en brûlant le combustible fossile. La technologie de gazéification du charbon, utilisée dans de nouvelles installations, permet de réduire ce surcoût, sans toutefois l'annuler (l'électricité coûte alors 10 à 12 % plus cher que celle produite par une combustion classique sans capture).
Le transport du dioxyde de carbone doit répondre à des normes de sécurité sévères, car il entraine la mort par asphyxie à des concentrations supérieures à 10 %, comme l'a montré le tragique dégazage du lac Nyos (plus dense que le dioxygène, il s'accumule au niveau du sol et en chasse ce dernier). La conception de navires de transport de CO2 (sur le même principe que les méthaniers ou de futurs transporteurs d'hydrogène[42]), est à l'étude.
Capture du carbone
Actuellement, l'absorption du CO2 se fait à grande échelle au moyen de dissolvants aminés, surtout avec l'éthanolamine (2-aminoéthanol, selon la nomenclature UICPA). D'autres techniques sont à l'étude, comme l'absorption par variation rapide de température/pression, la séparation des gaz et la cryogénie.
Dans les centrales électriques à charbon, les principales alternatives aux absorbeurs de CO2 à base d'amine sont la gazéification du charbon et la combustion oxygène-fioul. La gazéification produit un gaz primaire constitué d'hydrogène et de monoxyde de carbone, qui est brûlé pour donner du dioxyde de carbone. La combustion oxygène-fioul brûle le charbon avec de l'oxygène à la place de l'air, produisant ainsi uniquement du CO2 et de la vapeur d'eau, facilement séparables. Cependant, cette combustion produit une température extrême et les matériaux supportant cette température restent à créer.
Une autre option à long terme est la capture du carbone de l'air en utilisant des hydroxydes. L'air sera littéralement dépouillé de tout son CO2. Cette idée est une alternative aux combustibles non fossiles pour le secteur des transports (voiture, camion, transports en commun, etc.).
Un test mené à l'usine d'électricité de 420 mégawatts de la société Elsam, à Esbjerg (Danemark) a été inauguré le 15 mars 2006[43] dans le cadre du projet européen Castor piloté par l'Institut français du pétrole (IFP) qui rassemble une trentaine de partenaires industriels et scientifiques. Ce procédé postcombustion doit permettre de diviser de moitié le coût de capture du CO2, le ramenant entre 20 et 30 euros la tonne.
Son coût sur quatre ans (2004-2008) est de 16 millions d'euros, dont 8,5 millions sont financés par l'Union européenne. Castor vise à valider des technologies destinées aux grosses unités industrielles – usine électrique, aciérie, cimenterie, etc. –, dont l'activité engendre 10 % des émissions européennes de CO2, afin que cette technique soit en rapport avec le prix européen des permis d'émission de CO2 (alors à 27 € la tonne).
Capture post-combustion
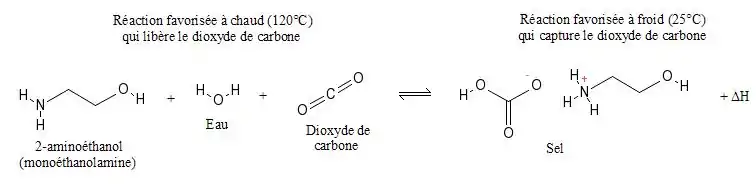
Les rejets de centrales thermiques sont constitués de moins de 20 % de dioxyde de carbone. Ainsi, avant de l'enfouir sous la terre, il faut le capturer : c'est la capture post-combustion. En étant en contact avec des gaz acides (comme le CO2), une solution aqueuse de 2-aminoéthanol forme un sel à température ambiante. La solution est alors transportée dans un milieu fermé où elle est chauffée à environ 120 °C, ce qui, selon le principe de Le Châtelier, libère le CO2 (pur) et régénère, en solution aqueuse, le 2-aminoéthanol.
Océans
L'injection directe du carbone dans l'océan est un autre type de séquestration envisageable. Dans cette méthode, le CO2 est enfoui dans les eaux profondes, afin de former un « lac » de CO2 liquide piégé par la pression exercée en profondeur. Des expériences menées entre 350 et 3 600 mètres indiquent que le CO2 liquide réagit à la pression en se solidifiant en hydrate de dioxyde de carbone (en)[44], qui se dissout graduellement dans les eaux environnantes. L'emprisonnement n'est donc que temporaire.
Cette technique a des conséquences environnementales dangereuses. Le CO2 réagit avec l'eau pour former de l'acide carbonique H2CO3. L'équilibre biologique des fonds marins, mal connu, sera probablement affecté. Les effets sur les formes de vie benthique des zones pélagiques sont inconnus. D'un point de vue politique, il n'est pas certain que le stockage du carbone dans ou sous les océans soit compatible avec la Convention de Londres sur la prévention de la pollution marine .
Une autre méthode de séquestration océanique à long terme est le rassemblement de résidus de récoltes (comme les fanes de blés ou l'excès de paille) dans de grands ballots de biomasse, puis leur dépôt dans les zones « d'éventails alluviaux » (alluvial fan) des bassins océaniques profonds. Immerger ces résidus dans les éventails alluviaux aura pour effet de les enterrer rapidement dans la vase du plancher océanique, emprisonnant la biomasse pour un temps très important. Les éventails alluviaux existent dans tous les océans et mers du monde où les rivières des deltas se jettent dans le plateau continental, comme pour l'éventail alluvial du Mississippi dans le golfe du Mexique et l'éventail du Nil dans la mer Méditerranée.
Utilisation spécifique d'algues
La ville de Libourne envisage d'équiper un de ses parkings de « lampadaires absorbeurs de CO2 ». Ils se trouveraient munis d'un réservoir contenant des algues. Celles-ci, placées à proximité d'une source de lumière, absorberaient le dioxyde de carbone et émettraient du dioxygène[45].
La sélection d'organismes adaptés permet d'envisager d'importants rendements. On estime qu'un dispositif de ce type d'un volume de 1,5 m3 pourrait absorber jusqu'à une tonne de CO2 par an.
Sols
l'Institut national de la recherche agronomique (INRA) a proposé en France l'initiative 4p1000 ou « 4 pour 1000, les sols pour la sécurité alimentaire et le climat »[46] qui a atténué le changement climatique en séquestrant du carbone atmosphérique dans les sols, tout en améliorant leur fertilité ainsi que la résilience des agroécosystèmes face au réchauffement climatique. Ce nouveau défi mondial est proposé à 570 millions de fermes et plus de 3 milliards de personnes en zone rurale[47] ; il vise à restaurer ou améliorer le taux de carbone de tous les sols agricoles et forestiers, par des pratiques appropriées, de manière à équilibrer les émissions anthropiques de CO2[48],[47].
Le principe général est que « augmenter chaque année le stock de carbone des sols de 4 pour 1000 dans les 40 premiers centimètres du sol permettrait, en théorie, de stopper l’augmentation actuelle de la quantité de CO2 dans l’atmosphère, à condition de stopper la déforestation » environ 860 milliards de tonnes de carbone pourraient être ainsi stockés, la cible 4 ‰, tant qu'elle est atteinte, correspondant à un stockage de 3,4 milliards de tonnes de carbone dans le sol chaque année. Selon l'INRA, ce carbone se stockerait dans les sols pour vingt à trente ans après la mise en place des bonnes pratiques, si celles-ci sont maintenues[47].
Une étude « Potentiel de l’agriculture et de la forêt françaises en vue de l’objectif d’un stockage de carbone dans les sols à hauteur de 4 pour mille » a été commandée par l’Agence de l'environnement et de la maîtrise de l'énergie (ADEME) et le ministère de l’Agriculture et de l’Alimentation, et confiée à l'INRA. Elle visait à évaluer le total de carbone que la France pourrait ainsi stocker, et à lister et qualifier les « meilleures pratiques » (en termes de performance, mais aussi de coûts) ; son rendu sera fait à Paris le 13 juin 2019[49].
Sous-sol
Le projet Castor prévoit l'étude de quatre sites de stockage géologique du CO2 : le réservoir pétrolier de Casablanca qui se situe au large des côtes nord-est de l'Espagne, le gisement de gaz naturel d'Atzbach-Schwanenstadt (Autriche), le champ de gaz de Snøhvit (Norvège) et le gisement de gaz naturel K12B exploité par Gaz de France au large de la Hollande, desquels il est nécessaire de s'assurer de l'étanchéité. D'autres projets d'esprit similaire sont en cours de par le monde.
Selon le BRGM[50], les 20 milliards de tonnes de dioxyde de carbone émis chaque année devront être stockées dans les aquifères salins. Ces derniers sont des nappes d'eau trop salées pour être exploitées. Leur capacité d'accueil est estimée de 400 à 10 000 milliards de tonnes, à comparer aux 40 milliards des gisements de charbons inaccessibles, aux 950 milliards des gisements d'hydrocarbures et aux 20 milliards des émissions annuelles actuelles. Le gaz doit être injecté à une profondeur d'au moins 800 mètres sous 800 bars de pression, à une température de 40 °C, sous une forme « supercritique » en équilibre avec son environnement. Il formera progressivement de l'eau gazeuse.
Stockage géologique
La « séquestration géologique » (plus rarement dite « géoséquestration ») consiste à injecter du dioxyde de carbone directement dans des formations géologiques souterraines. Les champs pétrolifères et aquifères salins qui ne sont plus exploités sont des sites de stockage idéaux. Les cavernes et anciennes mines parfois utilisées pour stocker le gaz naturel, ne sont et seront pas utilisées à cause d'un manque de sécurité dans le stockage.
Depuis plus de 30 ans du CO2 est injecté dans des champs de pétrole en déclin pour augmenter le rendement du puits. Cette option présente l'intérêt d'un coût de stockage compensé par la vente du pétrole additionnel qui a été généré. L'opérateur bénéficie aussi d'infrastructures existantes et des données géophysiques et géologiques obtenues pour et par l'exploration du pétrole. Tous les champs de pétrole disposent d'une barrière géologique empêchant la remontée de fluides gazeux (tel le CO2 dans le futur), mais ils ont comme inconvénient que leur distribution géographique et leurs capacités sont limitées. De plus la pratique devenue presque systématique de la fracturation a déstructuré la roche mère. Enfin, des fuites via les forages d'injection apparaissent plus fréquentes que prévu : une méta-analyse récente de 25 études ayant porté sur les problèmes d'intégrité physique des tubages de puits de production, d'injection ; actifs, inactifs et/ou abandonnés, tant onshore qu'offshore pour des réservoirs conventionnels ou non conventionnels a conclu que les pertes d'intégrité de tubages et de colmatages de puits sont assez courants (avec des variations de risque selon le type de forage et l'âge des puits)[51]. Les forages pétroliers anciens fuient couramment (ex : 70 % des puits terrestres du champ pétrolier de Santa Fe étudiés en 2005 présentent des pertes d'intégrité (avec des observations parfois de bulles de gaz remontant en surface le long des tubes)[52]. Ces puits sont anciens, mais pour 8030 autres puits récemment forés dans les schistes de Marcellus et inspectés en Pennsylvanie de 2005 à 2013, 6,3 % présentaient au moins une fuite. 3533 autres puits inspectés en Pennsylvanie de 2008 à 2011 présentaient eux 85 défaillances (de ciment ou de cuvelages d'acier), et 4 de ces puits ont connu une éruption et 2 des fuites importantes de gaz[51]. En cas de violent tremblement de terre, on ignore comment le tubage et les bouchons de béton de tels puits se comporteront.
Puits de carbone et protocole de Kyoto
Le protocole de Kyoto affirmant que la végétation absorbe du CO2, les pays ayant des forêts étendues peuvent en déduire une certaine partie de leurs émissions (article 3, alinéa 3 du protocole de Kyoto); leur facilitant l'accès au niveau d'émission qui leur a été fixé.
On estime qu'en 2030, les combustibles fossiles représenteront encore plus des trois quarts de l'énergie utilisée. Ceux qui sauront piéger le CO2 à sa source (22 % des émissions viennent de l'industrie, 39 % de la production électrique) auront un levier puissant sur le futur marché mondial des quotas d'émissions[43].
Notes et références
- ↑ (en) Christopher L. Sabine, Richard A. Feely, Nicolas Gruber et Robert M. Key, « The Oceanic Sink for Anthropogenic CO2 », Science, (lire en ligne, consulté le )
- 1 2 (en) Karl-Heinz Erb, Thomas Kastner, Christoph Plutzar et Anna Liza S. Bais, « Unexpectedly large impact of forest management and grazing on global vegetation biomass », Nature, vol. 553, no 7686, , p. 73–76 (ISSN 0028-0836 et 1476-4687, PMID 29258288, PMCID PMC5756473, DOI 10.1038/nature25138, lire en ligne, consulté le ).
- ↑ Article 83 de la Loi Grenelle II, p. 115/308 de la version [PDF]
- 1 2 3 4 Davidson E.A (2016) Biogeochemistry : Projections of the soil-carbon deficit. Nature, 540(7631), 47 |résumé.
- ↑ Giec, Changements climatiques 2001 : Rapport de synthèse. Résumé à l’intention des décideurs, 2001, 37 p.
- 1 2 3 4 Voir carte mondiale, in Joël Boulier, Géographie et environnement ; Les forêts au secours de la planète : quel potentiel de stockage du carbone ? ; L'Espace géographique 2010/4 (t. 39), 98 p., Belin ; (ISBN 9782701156217) (Résumé)
- ↑ (en) The case of the missing sink
- 1 2 3 4 5 6 Évaluation des ressources forestières mondiales 2010 ; Rapport principal, évaluation la plus complète jamais faite des forêts mondiales jamais effectuée, pour 233 pays et zones et pour la période 1990 à 2010 et pour plus de 90 variables clés relatives à l’étendue, l’état, les utilisations et les valeurs des forêts.. Version francophone, FAO, 2010
- ↑ (en)Is Europe an underestimated sink for carbone dioxide ?, site de l'Agence spatiale européenne, 5 janvier 2015.
- ↑ (en) A. Baccini et al., « Tropical forests are a net carbon source based on aboveground measurements of gain and loss », Science, vol. 358, no 6360, (DOI 10.1126/science.aam5962, lire en ligne).
- ↑ (en) A. Eldering et al., « The Orbiting Carbon Observatory-2 early science investigations of regional carbon dioxide fluxes », Science, vol. 358, no 6360, (lire en ligne).
- ↑ IFN, La forêt française : un puits de carbone ? son rôle dans la limitation des changements climatiques, l'IF, 7 mars 2005
- 1 2 3 4 L’environnement en France - édition 2010, page 83, Coll. Références Commissariat général au développement durable, juin 2010 par le service de l'observation et des statistiques
- ↑ L'environnement en France - édition 2014, page 92, Observations et statistiques du Ministère de l'environnement
- ↑ « IF no 7 - La forêt française, un puits de carbone? », sur inventaire-forestier.ign.fr, (consulté le )
- ↑ « Le mémento Édition 2014 », sur inventaire-forestier.ign.fr, (consulté le )
- ↑ Réchauffement climatique : le bois français, un puits de carbone hautement stratégique, Les Échos, 20 août 2022.
- 1 2 3 4 Zoe G. Davies, Jill L. Edmondson, Andreas Heinemeyer, Jonathan R. Leake et Kevin J. Gaston, Mapping an urban ecosystem service: quantifying above-ground carbon storage at a city-wide scale, Journal of Applied Ecology, vol. 48, Issue 5, p. 1125–1134, octobre 2011 ; en ligne le 11 juillet 2011 ; DOI 10.1111/j.1365-2664.2011.02021.x (Résumé)
- ↑ (en) Josep G. Canadell et al., « Contributions to accelerating atmospheric CO2 growth from economic activity, carbon intensity, and efficiency of natural sinks », Proceedings of the National Academy of Sciences, vol. 104, no 47, , p. 18866–18870 (DOI 10.1073/pnas.0702737104).
- ↑ (en) McNeil et al., Anthropogenic CO2 Uptake by the Ocean Based on the Global Chlorofluorocarbon, Science, 10 janvier 2003, 235, DOI 10.1126/science.1077429 (résumé
- ↑ Deep-sea Research, Par II, Colloque SOCOVV, Unesco/IOCCP, 8 février 2009
- 1 2 3 4 5 R. W. Wilson ; F. J. Millero ; J. R. Taylor ; P. J. Walsh ; V. Christensen ; S. Jennings ; M. Grosell ; « Contribution of Fish to the Marine Inorganic Carbon Cycle » ; Science, 16 janvier 2009, vol. 323, no 5912, p. 359, 362, DOI 10.1126/science.1157972 ; 2009
- ↑ ...si on estime qu'il y a 812 millions de tonnes de poissons dans les mers (fourchette basse)
- ↑ ...si l'on estime qu'il y a 2,05 milliards de tonnes (fourchette haute crédible)
- 1 2 3 4 Trish J. Lavery, Ben Roudnew, Peter Gill, Justin Seymour1, Laurent Seuront, Genevieve Johnson, James G. Mitchell et Victor Smetacek (2010) ; Iron defecation by sperm whales stimulates carbon export in the Southern Ocean ; Journal de recherche biologique de la Royal Society : Proceedings of the Royal Society, Biological Sciences ; en ligne (ISSN 1471-2954) ([résumé])
- ↑ James Heatedward & al. (2005) Rising Atmospheric CO2 Reduces Sequestration of Root-Derived Soil Carbon, Science, 9 Sep 2005, Vol 309, Issue 5741, p. 1711-1713 DOI: 10.1126/science.1110700
- ↑ (en-GB) Damian Carrington, « Tree planting 'has mind-blowing potential' to tackle climate crisis », The Guardian, (ISSN 0261-3077, lire en ligne, consulté le ).
- ↑ Thomas Lerch (université Paris-Est Créteil Val-de-Marne) & Jacques Ranger (INRA Centre Grand Est Nancy) (2017) « Les sols forestiers, puits de méthane : un service écosystémique méconnu » par Daniel Epron, Caroline Plain (université de Lorraine, INRA) ; dans la Revue forestière française - avril 2017 ; no 4-2016.
- ↑ Chave J, Condit R, Muller-Landau HC, Thomas SC, Ashton PS, et al. (2008), Assessing Evidence for a Pervasive Alteration in Tropical Tree Communities, PLoS Biol. 6(3) : e45
- ↑ Source : Courrier international du 24 novembre 2007, et Survival International
- ↑ Adoption of the Paris Agreement Report No. FCCC/CP/2015/L.9/Rev.1 (UNFCCC, 2015); http://unfccc.int/resource/docs/2015/cop21/eng/l09r01.pdf
- 1 2 Giacomo Grassi & al. (2017), The key role of forests in meeting climate targets requires science for credible mitigation ; Nature Climate Change 7, 220–226 ; doi:10.1038/nclimate3227, mis en ligne le 27 février 2017 (résumé)
- ↑ Kerguelen Ocean and Plateau compared Study, associant seize laboratoires de recherche dans le monde (français, australien, belge et néerlandais)
- ↑ Stéphane Blain et al., Effect of natural iron fertilization on carbon sequestration in the Southern Ocean, Nature, 26 avril 2007.
- ↑ Sylvia Hurlimann, "How Kelp Naturally Combats Global Climate Change"
- ↑ « Communiqué »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?) de la Convention de Londres et de l'OMI intitulé Ocean fertilization operations should be allowed only for research, say Parties to international treaties
- ↑ KIMO, Résolution 2/99 ; The Ocean Dumping of CO2 programme
- ↑ Lloyd, J., & Taylor, J. A. (1994). On the temperature dependence of soil respiration. Functional ecology, 315-323 |résumé
- ↑ A. Metay, B. Mary, D. Arrouays, J. Labreuche, M. Martin, B. Nicolardot, J.-C. Germon, Effets des techniques culturales sans labour sur le stockage de carbone dans le sol en contexte climatique tempéré ; Canadian Journal of Soil Science, 2009, 89:(5) 623-634, 10.4141/CJSS07108 (Résumé)
- ↑ Expérience faite par le Smithsonian Environmental Research Center, dans le Merritt Island Wildlife Refuge, (Cape Canaveral, Floride) sur des chênes de Turquie (Quercus laevis) poussant sur sols pauvres et exposés six ans à un doublement du taux de CO2. Source : Karen M. Carney, Bruce A. Hungate, Bert G. Drake et J. Patrick Megonigal, Altered soil microbial community at elevated CO2 leads to loss of soil carbon, Proc. Natl. Acad. Scie. USA, publié le 13 mars 2007, 10.1073/pnas.0610045104, texte intégral)
- ↑ Commission d'enrichissement de la langue française (2019) « Vocabulaire de l'environnement : climat-carbone » NOR : CTNR1926055K ; liste du 24-9-2019 - J.O. du 24-9-2019 ; Ref MENJ - MESRI – MC.
- ↑ Mertens, J., Hillegeer, C., Lepaumier, H., Makhloufi, C., Baraton, L., & Moretti, I. (2018). L'hydrogène au long cours.
- 1 2 Le Monde du 19 mars 2006
- ↑ Gerald D. Holder, « Clathrate Hydrates of Natural Gases, 2nd ed., Revised and Expanded. Chemical Industries Series/73 By E. Dendy Sloan, Jr. Marcel Dekker, Inc.: New York. 1998. 754 pages. $195.00. (ISBN 0-8247-9937-2). », Journal of the American Chemical Society, vol. 120, no 43, , p. 11212–11212 (ISSN 0002-7863 et 1520-5126, DOI 10.1021/ja9856194, lire en ligne, consulté le )
- ↑ Archives du Monde, lampadaires à algues-absorbeurs de CO2 de Libourne, proposés par la société Tyca
- ↑ « Welcome to the "4 per 1000" Initiative », sur www.4p1000.org (consulté le )
- 1 2 3 « Des sols pour la sécurité alimentaire et le climat », sur INRA, (version du 6 avril 2016 sur Internet Archive).
- ↑ Une conférence internationale est prévue sur ce thème du 17 AU 21 juin 2019 à Poitiers (86), organisée par l'INRA et l'Université de Poitiers ; voir aussi le résumé en 4 pages (INRA)
- ↑ Colloque de restitution d'Étude, INRA, consulté le 29 mai 2019
- ↑ Cité par Libération, 3 juin 2006, p. 37
- 1 2 Davies, R. J., Almond, S., Ward, R. S., Jackson, R. B., Adams, C., Worrall, F., … & Whitehead, M. A. (2014). Oil and gas wells and their integrity : Implications for shale and unconventional resource exploitation. Marine and Petroleum Geology, 56, 239-254.
- ↑ G. Chillingar, B. Endres (2005) Environmental hazards posed by the Los Angeles Basin urban oilfields: an historical perspective of lessons learned | Environ. Geol., 47, p. 302-317|résumé
Voir aussi
Bibliographie
- Arrouays D. et al. Estimation de stocks de carbone organique des sols à différentes échelles d’espace et de temps, reçu : mai 2003, accepté : novembre 2003, Étude et Gestion des Sols, vol. 10, 4, 2003, p. 347-355
- Apps M.-J. (2003). Les forêts, le cycle mondial du carbone et le changement climatique. Actes du XIIe Congrès forestier mondial, Québec, Canada, 2003. (consulté le 8 octobre 2007).
- Dupouey Jean-Luc, Pignard Gérôme (2001). Quelques problèmes posés par l’évaluation des flux de carbone forestier au niveau national. Revue Forestière Française, n° spécial les 40 ans de l’IFN, 3-4-2001
- Dupouey Jean-Luc, Pignard Gérôme, Hamza Nabila (2006). INRA, La séquestration de carbone en forêt ; consulté le 5 octobre 2007.
- EurObserv’ER (2006), Le baromètre biomasse solide, Systèmes solaires no 176, décembre 2006, lire en ligne, consulté le 25 octobre 2007.
- IFN (Inventaire Forestier National) (2005). L’IF no 7, La forêt française : un puits de carbone ? Son rôle dans la limitation des changements climatiques [PDF] en ligne. L’IF, mars 2005.
- Ministère de l'Écologie, du Développement et de l’Aménagement Durables (2006). Qu’est-ce qu’un projet domestique CO2 ? ; décembre 2006.
- Pignard Gérôme (2000). Évolution récente des forêts françaises : surface, volume sur pied, productivité. Revue Forestière Française, Tome LII, n° spécial 2000, p. 27-36.
- Pignard Gérôme, Hamza Nabila, Dupouey Jean-Luc (2004). Estimation des stocks et des flux de carbone dans la biomasse des forêts françaises à partir des données de l’Inventaire forestier national, In Loustau Denis (coord.). Rapport final du projet CARBOFOR : Séquestration de Carbone dans les grands écosystèmes forestiers en France. Quantification, spatialisation, vulnérabilité et impacts de différents scénarios climatiques et sylvicoles, juin 2004.
Filmographie
- Nicolas Koutsikas et Stephan Poulle, Carbon Public Enemy No 1, Georama TV/BlueWing/2d3d Anamations/ERT, sur carbon-the-film.com
Articles connexes
- Cycle du carbone
- Carbone fossile
- Réchauffement climatique
- Gaz à effet de serre
- Terra preta (sols amazoniens produits par l'homme, à très haute teneur en carbone)
- Tourbière, Bois mort, Humus, Matière organique
- Sol, Semis direct
- Field-Map - technologie pour le suivi des stocks de carbone
- Neutralité carbone
- 4p1000
Liens externes
- Notice dans un dictionnaire ou une encyclopédie généraliste :
- Note de Manicore sur la capacité des puits de carbone à absorber ou non le surplus de CO2
- Pour voir l'évolution des puits de carbone de 1850 à nos jours, animation Flash
- CARBOOCEAN IP, projet visant à évaluer précisément les sources et puits de carbone océaniques (anglais)
- Site officiel du 4p1000