| Méthane | |
   Structure de la molécule de méthane. |
|
| Identification | |
|---|---|
| Nom UICPA | méthane |
| Synonymes |
hydrure de méthyle[1] |
| No CAS | |
| No ECHA | 100.000.739 |
| No CE | 200-812-7 |
| PubChem | 297 |
| SMILES | |
| InChI | |
| Apparence | gaz comprimé ou liquéfié, incolore et inodore[2] |
| Propriétés chimiques | |
| Formule | CH4 [Isomères] |
| Masse molaire[3] | 16,042 5 ± 0,001 1 g/mol C 74,87 %, H 25,13 %, |
| Propriétés physiques | |
| T° fusion | −182,47 °C[4] |
| T° ébullition | −161,52 °C[4] |
| Solubilité | 22 mg l−1 (eau, 25 °C)[5] |
| Paramètre de solubilité δ | 11,0 MPa1/2 (25 °C)[6] |
| Masse volumique | 422,62 kg·m-3 (−161 °C, liquide) 0,670 9 kg·m-3 (15 °C, 1 bar, gaz)[4] |
| T° d'auto-inflammation | 537 °C[2] |
| Point d’éclair | Gaz Inflammable[2] |
| Limites d’explosivité dans l’air | 4,4–17 %vol[4] |
| Pression de vapeur saturante | 2 atm (−152,3 °C); 5 atm (−138,3 °C); |
| Point critique | 4 600 kPa[8], −82,6 °C[9] |
| Vitesse du son | 1 337 m·s-1 (liquide, −161,5 °C) 450 m·s-1 (gaz, 27 °C, 1 atm)[10] |
| Thermochimie | |
| ΔfH0gaz | −74,87 kJ·mol-1[11] |
| Cp | |
| PCS | 890,8 kJ·mol-1[13] (25 °C, gaz) |
| PCI | 803,3 kJ·mol-1[14] |
| Propriétés électroniques | |
| 1re énergie d'ionisation | 12,61 ± 0,01 eV (gaz)[15] |
| Précautions | |
| SGH[16] | |
  Danger |
|
| SIMDUT[17] | |
  A, B1, |
|
| Transport | |
| Écotoxicologie | |
| LogP | 1,09[2] |
| Unités du SI et CNTP, sauf indication contraire. | |
Le méthane est un composé chimique de formule chimique CH4, découvert et isolé par Alessandro Volta entre 1776 et 1778. C'est l'hydrocarbure le plus simple et le premier terme de la famille des alcanes. Comme fluide frigorigène, il porte la dénomination « R50 » dans la nomenclature des réfrigérants, régie par la norme 34-1992 d'ANSI/ASHRAE.
Assez abondant dans le milieu naturel, le méthane est un combustible à fort potentiel. Gazeux dans les conditions normales de température et de pression, il peut être transporté sous cette forme, généralement par gazoduc, ou à l'état liquéfié par des méthaniers et plus rarement des camions.
D'énormes quantités de méthane sont enfouies dans le sous-sol sous forme de gaz naturel. L'essentiel du méthane des terrains sédimentaires est produit de façon anaérobie par les archées dites méthanogènes. De grandes quantités, difficiles à évaluer, sont également produites par réaction de l'eau de mer sur les péridotites des dorsales océaniques et présentes sur le plancher océanique sous forme d'hydrates de méthane (stables à basse température et haute pression). Les volcans de boue, les énergies fossiles, les décharges publiques (gaz de décharge), la digestion du bétail (notamment des ruminants), les rizières, les estuaires pollués (méthane des zones humides, gaz de marais) et les feux de forêts dégagent aussi beaucoup de méthane.
Le méthane est naturellement présent dans l'atmosphère terrestre, mais les apports anthropiques ont plus que doublé sa concentration depuis la révolution industrielle. Elle atteignait 1 748 ppb en 1998. Après une période de stabilisation de 1999 à 2006 à environ 1 774 ppb, la croissance de sa concentration a repris en 2007 à un rythme de 5 à 15 ppb par an, atteignant 1 879 ppb en 2020. Des analyses isotopiques suggèrent que cet accroissement récent du méthane atmosphérique serait principalement d'origine non fossile.
Le méthane persiste moins de dix ans dans l'atmosphère où il est détruit par des radicaux hydroxyle OH•, mais c'est un gaz à effet de serre bien plus puissant que le dioxyde de carbone CO2, avec un potentiel de réchauffement global 28 fois plus élevé, responsable, au niveau actuel de sa concentration, de quelques pour cent de l'effet de serre total à l'œuvre dans notre atmosphère. Ainsi, à titre comparatif, sur un horizon de 100 ans, relâcher une certaine quantité de méthane dans l'atmosphère a un effet sur le réchauffement climatique environ neuf fois plus important que de brûler cette même quantité de méthane en CO2.
Histoire
En 1776, Alessandro Volta découvre le méthane en étudiant le gaz des marais de l'îlet Partegora, qui s'échappait de zones humides proches de sa maison[18]. Il en prélève des capsules issues du sédiment du lac Majeur[19] et en isole la fraction inflammable[20] dont il comprend qu'il est issu de la décomposition des plantes[21].
En 1910, Söhngen écrit que le méthane se forme de façon si considérable aux Pays-Bas « qu'en différents lieux on s'en sert pour l'éclairage et le chauffage de fermes et de maisons »[21].
C'est à cause du grisou (essentiellement constitué de méthane), responsable jusqu'à nos jours de nombreuses catastrophes minières, que sont mises au point les lampes de sûreté dans les mines de charbon, notamment la lampe de Davy (1817).
L'impact du méthane sur le climat est inconnu, puis suspecté jusqu'en 1976 où l'on démontre que le méthane est effectivement un puissant gaz à effet de serre[22].
Les observations issues de l'exploration spatiale ont montré l'omniprésence du méthane dans l'Univers.
Méthane, paléo-environnement et paléoclimats
Sur la Terre, en tant que gaz à effet de serre, le méthane a toujours joué un rôle majeur dans le cycle du carbone, la chimie atmosphérique et le climat mondial. Du méthane d'origine abiotique, comme du CO2, était très présent dans l'atmosphère de la Terre primitive avant que la vie n'y apparaisse et n'y introduise l'oxygène (qui a permis l'apparition de la couche d'ozone). Après l'apparition de la vie bactérienne, l'essentiel du méthane terrestre a eu une origine biologique (fossile ou directe).
Des émissions géologiques naturelles de méthane fossile existent encore, aujourd'hui principalement liées au volcanisme (environ 52 Tg, soit 52 Mt par an de méthane émis, représentant 10 % environ des émissions annuelles)[23].
Le calcul des émissions géologiques passées, et plus encore l'évaluation des sources de méthane selon les époques, ont été associés à de grandes incertitudes, mais elles se précisent. En 2017, Petrenko et al. ont quantifié dans des carottages de glace polaire le méthane contenant du radiocarbone (14CH4), montrant que le méthane d'origine géologique n'a pas dépassé durant la dernière période de réchauffement (fin de la dernière glaciation) 15,4 Tg/an, soit 15,4 Mt (95 % de confiance), en moyenne lors du réchauffement brutal qui s'est manifesté entre le Dryas récent et le préboréal (il y a environ 11 600 ans). Ces émissions « géologiques » n'étant a priori pas moindres que celles d'aujourd’hui[24],[25], les auteurs ont conclu sur cette base que les émissions actuelles de méthane géologique (environ 52 Tg/an, soit 52 Mt)[26],[27] sont surestimées, et donc que les estimations actuelles d'émissions anthropiques de méthane[27] ont, elles, été sous-estimées[23].
Cette étude a aussi confirmé les données antérieures[28],[29],[30] montrant que l’augmentation rapide d’environ 50 % de la fraction molaire de méthane atmosphérique lors de l’événement préboréal-Dryas était en très grande partie due à des sources telles que les zones humides et secondairement (moins de 19 %) aux anciens réservoirs de carbone que sont les clathrates marins[31], pergélisol[32] et le méthane emprisonné sous la glace[33].
Formation, stockages naturels
Surface et sous-sol
Le méthane est l'hydrocarbure naturel le plus présent dans l'air. C'est le principal constituant du biogaz issu de la fermentation de matières organiques animales ou végétales en l'absence de dioxygène. Une quantité importante de méthane est aussi produite en milieu aérobie[34].
Méthane issu d'environnements anoxiques
C'est le produit final de la décomposition anoxique de la matière organique par des archées méthanogènes ne vivant qu'en milieu anaérobie (sans oxygène)[35].
Il est naturellement produit par voie enzymatique, lors du métabolisme énergétique anaérobie des archées[36], dans les zones humides peu oxygénées comme les marais, tourbières et certains estuaires et lagunes, ainsi que dans certains sols cultivés (plutôt tropicaux, sans grandes différences entre système labouré, en semis direct ou en travail superficiel)[37] et/ou longuement inondés (mais dans ces milieux peuvent également se trouver des organismes méthanotrophes qui en consomment une partie ou la totalité)[38]. Les sols en semis direct absorbent cependant en moyenne 0,4 kg C-CH4 par hectare et par an de plus qu'en cas de labours[37].
Le CH4 se forme aussi dans le rumen et le tube digestif de nombreux animaux (de certains invertébrés jusqu'aux mammifères, herbivores principalement). Il est présent en faible quantité dans les gaz intestinaux humains[39].
C'est le seul hydrocarbure classique pouvant être obtenu rapidement et facilement via un processus biologique naturel. Loin derrière le gaz naturel (méthane fossile), le méthane renouvelable (biogaz) est néanmoins en plein développement (Suède, Allemagne, Danemark, Viêt Nam, Cambodge, Chine, Inde, etc.) (voir section #Utilisation).
Méthane non-bactérien et d'origine aérobique
Depuis les années 2000, les biologistes découvrent ou confirment que des végétaux[40],[41], des champignons[42], des algues[43] et les cyanobactéries (terrestres et aquatiques)[44] peuvent aussi produire du méthane, de même qu'en présence d'oxygène[45], via des voies de production et des exigences biologiques longtemps incomprises, mais en quantité importante[46] : les estimations varient entre 10 et 60 millions de tonnes de méthane émises par an, pour les seules feuilles des plantes, pour un total compris entre 60 et 240 millions de tonnes par an, soit 10 à 30 % des émissions annuelles globales. Ce gaz non bactérien provient aux deux tiers des régions tropicales. Ces émissions par la végétation, ajoutées à celles des marécages et peut-être à celles des fonds marins, seraient un des moteurs du changement climatique historique.
En 2022, trois chercheurs russes (Bruskov, Masalimov et Chernikov) montrent que Bacillus subtilis et Escherichia coli produisent du méthane quand elles sont en présence de fer libre et d'espèces réactives de l'oxygène (ROS), issues du métabolisme et renforcés par le stress oxydatif)[47]. Les ROS produisent des radicaux méthyle, eux-mêmes issus de composés organiques contenant des groupes méthyle liés au soufre ou à l'azote. Ces radicaux méthyle sont alors l'intermédiaire nécessaire à l'apparition du méthane dans les cellules (phénomène aussi maintenant connu chez beaucoup d'autres organismes des domaines Bacteria, Archaea et Eukarya et dans plusieurs lignées cellulaires animales (y compris humaines), chez lesquels le stress oxydatif semble toujours augmenter cette production de méthane. Les auteurs supposent même que « toutes les cellules vivantes possèdent probablement un mécanisme commun de formation de CH4 exploitant les interactions entre les ROS, les donneurs de fer et de méthyle » (ce qui ouvre des pistes nouvelles pour l'étude du cycle biochimiques du méthane, du fer[48] et peut être l'amélioration de la production de biogaz).
Ce phénomène étant plus important en zone tropicale chaude et l'augmentation de la température de l'eau augmentant la production des ROS[49], on peut craindre que ce méthane puisse aussi contribuer aux boucles de rétroaction positive contribuant à accélérer le réchauffement climatique.
Fonds marins
Le méthane produit par la réaction de serpentinisation entre les péridotites et l'eau de mer dans les dorsales océaniques peut rester piégé sous forme d'hydrates de méthane (clathrates) ou s'échapper dans l'atmosphère.
Des quantités importantes de méthane sont stockées sous forme d'hydrates de méthane au fond des océans (où leur exploitation est envisagée) et dans les pergélisols. Ces deux réservoirs pourraient jouer un rôle important dans les cycles climatiques et, selon des observations d'une équipe d'océanographes en 2014, ils commencent à perdre une quantité croissante de méthane dans l'atmosphère[50],[51].
Le débullage de méthane à partir des sédiments marins, sur les lignes de fractures du plancher océanique, est considéré comme un indice de risque sismique élevé, voire comme un possible précurseur des tremblements de terre (sous réserve de confirmation à la suite des expériences en cours, en mer de Marmara, sur la faille nord-anatolienne au large de la Turquie)[52].
Un documentaire intitulé Méthane, rêve ou cauchemar sur Arte (2014 fait état de la découverte que le méthane issu des planchers océaniques, à une profondeur minimale de 400 m, est presque totalement absorbé par des bactéries avant d'atteindre une remontée de 200 m)[53]. L'accident de la plateforme de Deepwater Horizon, survenu dans le golfe du Mexique, a libéré une très grande quantité de méthane sur le plancher océanique dont aucune trace ne subsistait après six mois, un temps considéré comme très court au regard de la quantité de méthane s'étant échappé du puits d'extraction endommagé. Le fait que le méthane ait été absorbé par des micro-organismes n'implique pas pour autant que l'incident n'ait pas de conséquence pour l'environnement, en particulier à cause de l'acidification de l'océan qui en résulte.
Propriétés physico-chimiques
Dans les conditions normales de température et de pression, le méthane est un gaz incolore et inodore. Environ deux fois plus léger que l'air, il est explosif en milieu confiné (grisou). En milieu non confiné il se dilue dans l'air et s'échappe vers la haute atmosphère, où il a moins tendance à former des nuages explosifs que les gaz plus lourds que l'air (propane, butane) ; par contre c'est un puissant gaz à effet de serre.
Solubilité du méthane dans l'eau
Elle dépend beaucoup de la température et de la pression (il diminue avec l'une et augmente avec l'autre). Ainsi le grisou minier peut être en partie solubilisé et transporté par de l'eau (qui contient alors aussi du radon ainsi que du dioxyde de carbone et du dioxyde de soufre qui l'acidifient). Selon l'Ineris une eau à 10 °C initialement saturée en gaz de mine sous une pression de 10 bars (équivalente à 100 m de charge hydraulique), va perdre lors de sa détente environ 0,5 m3 de méthane et 12 m3 de CO2 par m3 d'eau[54].
Dégazage spontané
Les hydrates de méthane immergés fondent en libérant des chapelets de bulles, mais sans variation brusque[45]. De même, les micropoches de méthane produites par les bactéries du sédiment se libèrent en formant des bulles qui remontent dans la colonne d'eau, notamment dans la tourbe (où le phénomène est difficile à suivre[55]) et les vases estuariennes[56], et plus ou moins vite selon la teneur en matière organique[57] et la porosité/viscosité du substrat[58],[59]. Ce bullage représente dans les zones humides une fraction importante et probablement sous-estimée des émissions de méthane et de gaz à effet de serre[60]. Des chambres à flux automatisées fonctionnant en continu ont été combinées à un spectroscope pour mieux quantifier ces bulles et leur teneur en CH4[61].
À titre d'exemple, dans un milieu pauvre de zone tempérée, en 2009, le bullage variait d’une heure à l’autre, avec un pic nocturne de libération (de 20 h 00 à 06 h 00, heure locale) bien que les flux stables (c’est-à-dire ceux avec une augmentation linéaire de la concentration de CH4 dans l’espace de tête de la chambre) ne présentaient pas de variabilité quotidienne. Les taux de bullage moyens saisonniers ont culminé à 843,5 ± 384,2 « événements » par mètre carré et par jour en été, avec en moyenne 0,19 mg de CH4 rejetée par « événement ».
Il est aussi démontré que la flore des marais (y compris salée) influe sur la quantité de méthane saisonnièrement libérée dans l'air ou l'eau (avec par exemple Carex rostrata[62]. Les dates et l'importance des inondations ou des sécheresses jouent aussi[63].
Inflammation et combustion
Le méthane est un combustible qui compose jusqu'à 90 % le gaz naturel. Son point d'auto-inflammation dans l'air est de 540 °C[64]. La réaction de combustion du méthane s'écrit :
La combustion du méthane à 25 °C libère une énergie de 39,77 MJ/m3 (55,53 MJ/kg)[alpha 1], soit 11,05 kWh/m3 (15,42 kWh/kg)[alpha 2].
Le gaz naturel (constitué à plus de 90 % de méthane) est transporté par navires (méthaniers) à une température de −162 °C et à une pression voisine de la pression atmosphérique. Les réservoirs sont construits sur le principe de la bouteille isotherme et leur capacité peut aller jusqu'à 200 000 m3 de gaz liquide par réservoir. Un méthanier comportant plusieurs réservoirs, sa cargaison peut actuellement atteindre 154 000 m3 de gaz naturel liquéfié (GNL). Les futurs méthaniers pourront transporter jusqu'à 260 000 m3 de GNL. Le volume du méthane à l'état gazeux est égal à 600 fois son volume à l'état liquide, à pression atmosphérique.
Présent à tous les stades de l'industrie pétrolière, mais mal valorisé, il est fréquemment brûlé en torchère, ce qui contribue à l'effet de serre (les pétroliers restreignent donc ce procédé).
Dans l'Univers
Dans les nuages interstellaires
Du méthane a été retrouvé à l'état de traces dans plusieurs nuages interstellaires.
Sur Titan
Le méthane est présent partout sur Titan, et même à l'état liquide sous forme de lacs, de rivières, et de mers, particulièrement près du pôle nord de l'astre. Sa présence en a été établie dès 1944. Au point que la chaleur dégagée par la sonde Huygens, lors de l'impact du a provoqué un notable dégagement de méthane gazeux.
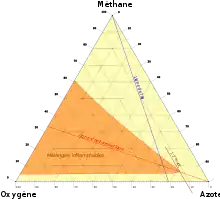
L'atmosphère de Titan, satellite de Saturne, est principalement constituée d'azote avec une proportion de méthane allant de 1,4 % dans la stratosphère jusqu'à 4,9 % au niveau du sol. Il ne pleuvait pas lorsque la sonde Huygens s'est posée sur Titan, mais l'ESA n'exclut pas que des averses de méthane y soient fréquentes. Simplement, l'aridité du sol absorberait rapidement ces précipitations, à la manière des déserts terrestres.
Sur Mars
L'un des résultats les plus étonnants de la sonde spatiale Mars Reconnaissance Orbiter, en orbite autour de Mars depuis le , provient de l'étude détaillée en 2008 de la région de Nili Fossae, identifiée début 2009 comme source d'importants dégagements de méthane[65]. Ce gaz a été détecté dès 2003 dans l'atmosphère de Mars, aussi bien par des sondes telles que Mars Express que depuis la Terre ; ces émissions de CH4 se concentreraient notamment en trois zones particulières de la région de Syrtis Major Planum[66]. Or le méthane est instable dans l'atmosphère martienne, des études récentes suggérant même qu'il soit six cents fois moins stable qu'estimé initialement (on évaluait sa durée de vie moyenne à 300 ans) car le taux de méthane n'a pas le temps de s'uniformiser dans l'atmosphère et demeure concentré autour de ses zones d'émission, ce qui correspondrait à une durée de vie de quelques centaines de jours ; la source de méthane correspondante serait par ailleurs 600 fois plus puissante qu'estimé initialement, émettant ce gaz une soixantaine de jours par année martienne, à la fin de l'été de l'hémisphère nord[67].

Les analyses géologiques menées en 2008 par la sonde Mars Reconnaissance Orbiter dans la région de Nili Fossae ont révélé la présence d'argiles ferromagnésiennes (smectites), d'olivine (silicate ferromagnésien (Mg,Fe)2SiO4, détectée dès 2003[69]) et de magnésite (carbonate de magnésium MgCO3)[70], ainsi que de serpentine[71]. La présence simultanée de ces minéraux permet d'expliquer assez simplement la formation de méthane, car, sur Terre, du méthane CH4 se forme en présence de carbonates — tels que le MgCO3 détecté dans la région en 2008 — et d'eau liquide lors du métamorphisme hydrothermal d'oxyde de fer(III) Fe2O3 ou d'olivine (Mg,Fe)2SiO4 en serpentine (Mg,Fe)3Si2O5(OH)4, particulièrement lorsque le taux de magnésium dans l'olivine n'est pas trop élevé et lorsque la pression partielle de dioxyde de carbone CO2 est insuffisante pour conduire à la formation de talc Mg3Si4O10(OH)2 mais aboutit au contraire à la formation de serpentine et de magnétite Fe3O4, comme dans la réaction :
- 12/x Mg2-xFexSiO4 + 2+(8(2-x)/x) H2O + CO2 → 4(2-x)/x Mg3Si2O5(OH)4 + (8x-4)x SiO2 + 4 Fe3O4 + CH4.
La probabilité de ce type de réactions dans la région de Nili Fossae est renforcée par la nature volcanique de Syrtis Major Planum et par l'étroite corrélation, observée dès 2004, entre le taux d'humidité d'une région et la concentration de méthane dans l'atmosphère[72].
Le méthane détecté par Curiosity lors d'une trentaine d'analyses de l’atmosphère n'est présent qu'à l'état de traces (0,4 ppb, à comparer aux 1 800 ppb de la Terre), mais sa fluctuation saisonnière (passage de 0,3 à 0,7 ppb) intrigue, car elle est trois fois plus importantes que ce que prévoient les théories disponibles[73]. Elle pourrait éventuellement être l'indice d’une présence de vie microbienne (actuelle ou fossile) et/ou résulter d'une ou plusieurs source(s) abiotique(s) : réaction d'eaux chaudes avec des olivines (évoquées plus haut), attaque par des UV solaires de météoroïdes et poussières stellaires riches en carbone minéral (car deux pics saisonniers se sont produits environ 15 jours après une pluie de météores martiens), désorption à partir d’une roche dont les pores ou feuillets s’ouvrent en été quand il fait plus chaud ; ou peut être ne s’agit il que d’une augmentation relative (ce serait le CO2 qui gelant en hiver aux pôles diminuerait dans l'atmosphère en donnant l’impression qu’il y a plus de méthane à ce moment, mais le phénomène devrait alors être plus marqué en plein hiver martien, à moins que des courants aériens n’apporte en fin d’été ce méthane jusqu’à l’emplacement de Curiosity)… Le débat est en cours[73].
Sur les planètes géantes

On trouve également du méthane sous forme de nuages et de brume sur Uranus et Neptune, de gaz non condensé dans les atmosphères de Jupiter et de Saturne ; ainsi que peut-être sur les exoplanètes Epsilon Eridani c et Fomalhaut b.
Utilisation
Les gisements fossiles de gaz naturel comportent entre 50 et 60 % de méthane, le gaz naturel brut est épuré avant d'être injecté sur le réseau de distribution.
La proportion de méthane présent dans le gaz naturel que nous utilisons est supérieure à 90 % dans la plupart des gaz.
Le méthane « biologique » ou biogénique, ou biogaz, qui est produit par la fermentation anaérobie de matière organique comporte 50 à 80 % de méthane, (60-65 % généralement)
Le biogaz produit dans les décharges pourrait être (bien davantage) récupéré et valorisé sous forme d'électricité, de chaleur ou comme carburant automobile. Pour l'instant, seules quelques expériences isolées (dans des fermes, des déchetteries…) ont vu le jour, spécialement dans les régions les plus froides (nord de l'Allemagne, de la France, Scandinavie, etc.). Ainsi, une installation à plus grande échelle a été créée par l'Institut des sciences et des technologies de Kigali (en) dans les prisons rwandaises, confrontées à une surpopulation : les déjections des détenus sont converties en méthane, qui est valorisé en éclairage et chaleur, utilisée dans la moitié des brûleurs des cuisines[74].
Le méthane est valorisable comme combustible mais d'autres usages en seraient possibles. Par exemple, des chercheurs ont réussi à transformer à température presque ambiante (40 °C) du méthane en un ester (propanoate d'éthyle) potentiellement valorisable. Pour ce faire, un carbène (composé très réactif) a été introduit dans une liaison du méthane via un catalyseur organométallique[75].
Biocarburant de troisième génération
Pour produire un méthane de décharge assez pur et pour faire un bon biocarburant de troisième génération, un « digesteur anaérobie » inspiré de la digestion anaérobie à l'œuvre dans la panse des bovins est expérimenté au Canada. Des microorganismes méthanogènes vivant en symbiose avec les vaches savent produire plus de méthane que de CO2, mais ils ont des besoins précis, en température et humidité notamment. La difficulté est de conserver les conditions de vies optimales de ces organismes dans un milieu constitué de déchets, ce qui est expérimenté au moyen d'électrodes régulant la température du milieu. Ce sont ensuite des fibres creuses constituées d'une membrane perméable qui devraient séparer le CO2 du méthane, lequel pourra ensuite être brûlé comme source d'énergie, utilisé par la carbochimie ou compressé et stocké[76].
Il est aussi possible de produire du méthane à partir du CO2 aérien par électrométhanogénèse, c'est-à-dire à l'aide d'un courant électrique grâce à une biocathode ou de façon abiotique[77].
Stockage énergétique
Dans la perspective d'une transition vers des énergies renouvelables, des chercheurs de l'entreprise autrichienne Solar Fuel Technology (Salzbourg), en coopération avec l'Institut Fraunhofer de recherche sur l'énergie éolienne de Leipzig (IWES), le Centre de recherche sur l'énergie solaire et l'hydrogène de Stuttgart (ZSW) et l'université de Linz ont mis au point une solution de stockage de l'énergie sous forme de méthane[78],[79]. L'énergie électrique excédentaire d'origine éolienne ou photovoltaïque est utilisée pour décomposer de l'eau en dihydrogène et dioxygène (électrolyse de l'eau), puis le dihydrogène est combiné avec du dioxyde de carbone par une réaction de méthanation (réaction de Sabatier).
L'un des principaux intérêts de ce procédé est d'utiliser les infrastructures (réservoirs et conduites de gaz) existantes, dont la capacité de stockage serait suffisante pour couvrir les besoins de méthane de l'Allemagne pendant plusieurs mois, par exemple pendant[80] une période où le solaire et l'éolien ne peuvent couvrir les besoins énergétiques.
Contribution au réchauffement climatique
Un gaz à effet de serre
Le méthane est un gaz à effet de serre qui contribue au réchauffement climatique, pris en compte en tant que tel par la directive 2003/87/CE. Il absorbe une partie du rayonnement infrarouge émis par la Terre, et l'empêche ainsi de s'échapper vers l'espace.
De plus, il contribue aussi indirectement à l'effet de serre, en diminuant la capacité de l'atmosphère à oxyder d'autres gaz à effet de serre (comme les fréons). Son utilisation comme combustible émet du dioxyde de carbone CO2 à hauteur de 380 Mt/an (les émissions industrielles avoisinent 6 000 Mt/an).
L'influence du méthane sur le climat est moins importante que celle du CO2, mais est tout de même préoccupante[81]. L'un des principaux enseignements du cinquième rapport d'évaluation du Groupe d'experts intergouvernemental sur l'évolution du climat (GIEC) en 2014 est que l'influence du méthane a longtemps été sous-estimée, son potentiel de réchauffement global (PRG) à cent ans passant de 21 dans le cadre du protocole de Kyoto, à 28 et même 34 en prenant en compte les rétroactions climatiques[82].
Le méthane persiste moins de dix ans dans l'atmosphère, où il est détruit par des radicaux hydroxyle OH•, mais c'est un gaz à effet de serre bien plus puissant que le CO2, responsable, au niveau actuel de sa concentration, de quelques pour cent de l'effet de serre total à l'œuvre dans notre atmosphère[83]. Ainsi, à titre comparatif, sur un horizon de 100 ans, relâcher une certaine quantité de méthane dans l'atmosphère a un effet sur le réchauffement climatique environ neuf fois plus important que brûler cette même quantité de méthane en CO2[84].
Le méthane est le deuxième gaz responsable du dérèglement climatique[85] (forçage radiatif de 0,97 W/m2 en 2011) derrière le CO2 (1,68 W/m2), mais loin devant les fréons (0,18 W/m2) et le protoxyde d'azote[86] (0,17 W/m2). Une molécule de méthane absorbe en moyenne 28 fois plus de rayonnement qu'une molécule de dioxyde de carbone sur une période de 100 ans, son PRG est donc de 28 ; à échéance de 20 ans, son PRG est même de 72[87].
Une étude publiée en décembre 2016 par plus de 80 scientifiques issus de laboratoires du monde entier[alpha 3] met en garde contre la sous-estimation usuelle de la contribution du méthane au réchauffement climatique : le méthane contribue pour 20 % au réchauffement en cours (contre 70 % pour le CO2), parce que, malgré sa concentration beaucoup plus faible, son potentiel de réchauffement global (PRG) est 28 fois plus élevé. Ceci implique que pour tenir l'objectif de rester sous la barre des 2 °C on ne peut se contenter de limiter les émissions de dioxyde de carbone, mais qu'il faut aussi réduire celles de méthane[88].
En 2019, l'Agence américaine d’observation océanique et atmosphérique (NOAA) annonce que les concentrations atmosphériques de méthane ont atteint un record en 2018[89].
En juillet 2020, une étude réalisée par une centaine de chercheurs réunis dans le Global Carbon Project révèle une hausse continue des émissions de méthane depuis 2007 (+9 % par an), avec une forte accélération depuis 2014. Ces émissions atteignaient 596 Mt en 2017, dont 60 % dues aux activités humaines : agriculture et déchets 227 Mt (38 %), production et utilisation de combustibles fossiles 108 Mt (18 %), biomasse et biocarburant 28 Mt (5 %). Elles proviennent pour 193 Mt (32 %) d'Asie, dont 56 Mt (9 %) de Chine, pour 117 Mt (20 %) d'Afrique et du Moyen-Orient, 105 Mt d'Amérique du sud, pour 93 Mt (16 %) d'Amérique du nord, pour 44 Mt de Russie et Asie centrale et 30 Mt d'Europe. Les chercheurs estiment que l'agriculture et les déchets ont contribué à hauteur de 60 % à la hausse des émissions mondiales, l'exploitation du pétrole et du gaz à plus de 20 %, et celle du charbon à plus de 10 %. Ils prônent une quantification plus régulière des émissions de méthane, à l’image de ce qui est fait pour le CO2 : le méthane ayant une durée de vie plus courte que le dioxyde de carbone dans l’atmosphère, une baisse des émissions peut être rapidement bénéfique pour le climat[90].
Méthane et ozone
Le méthane interagit avec l'ozone, différemment dans les hautes et les basses couches de l'atmosphère.
Selon les modélisations tridimensionnelles disponibles en chimie de la troposphère, diminuer les émissions anthropiques de CH4 pourrait être « un puissant levier pour réduire à la fois le réchauffement climatique et la pollution de l'air par l'ozone de fond troposphérique »[91].
Variation historique (depuis l'Empire romain)
Les émissions de méthane provenant des marais, des bovins, des feux de végétation, ou des combustibles fossiles ont toutes une signature isotopique spécifique[92]. Les bactéries méthanogènes des zones humides absorbent plus d'isotopes plus légers du carbone (12C) alors que le méthane fossile est plutôt enrichi en carbone plus lourd (13C). Le méthane issu des incendies de brousse ou de forêt est situé entre les deux[93].
On sait aussi aujourd’hui finement analyser le méthane piégé dans les glaces, ce qui a par exemple permis en 2012 de confirmer l'hypothèse posée il y a quelques années par le climatologue William Ruddiman, qui estimait que l'impact de l'humanité sur le climat date d'avant le récent « Anthropocène » et de bien avant la révolution industrielle. Selon l'étude isotopique du méthane des glaces antarctiques parue dans la revue Nature en octobre 2012[94], les variations passées du taux de méthane et sa composition démontrent que des feux de végétation probablement anthropiques enrichissent depuis le XVIe siècle au moins le taux atmosphérique de méthane. L'analyse fine de deux carottes de glace du forage glaciaire NEEM1 (Groenland)[95] couvrant environ 2 000 ans a été faite avec une précision jamais atteinte en termes de dosage, analyse et résolution temporelle. Elle montre ou confirme qu'entre un siècle av. J.-C. et le XIXe siècle, le monde avait déjà connu trois périodes d'augmentation des taux de méthane (à l'échelle de quelques siècles) et une tendance longue à la décroissance de la signature isotopique 13C du méthane[94]. Selon ces données, les modèles d'équilibre isotopique de l'atmosphère[96] et les données paléoclimatiques de cette période (température, précipitations) ainsi qu'au vu des données de la démographie humaine, les feux de végétation liés à la déforestation, au chauffage, à la cuisson et la métallurgie avaient diminué au moment du déclin de l'Empire romain et de celui de la dynastie Han (Chine), pour réaugmenter durant les grandes déforestations et l'expansion médiévale[94]. L'Homme semble être responsable de 20 à 30 % des émissions totales de méthane par les feux de végétation entre un siècle av. J.-C. et le XVIe siècle[94].
Variations récentes de teneur de l'air
Le taux de méthane dans l'atmosphère terrestre atteignait 1 644 ppb en 1984[97]. Il a augmenté graduellement jusqu'à atteindre 1 748 ppb (Partie par milliard) en 1998[98]. Après une période de stabilisation de 1999 à 2006 à environ 1 774 ppb, la croissance de sa concentration a repris en 2007 à un rythme de 5 à 15 ppb par an, atteignant 1 879 ppb en 2020[97]. Des analyses isotopiques suggèrent que cet accroissement récent du méthane atmosphérique serait principalement d'origine non-fossile[99].
Le taux est en 2018 entre 1 850 et 1 900 ppb, soit 0,000 19 % ou 1,9 ppm. Il s'est maintenu[100],[101] entre 1 780 et 1 810 ppb de 2000 à 2010 avec une grande variation suivant la latitude[102]. Dans le passé, le taux de méthane dans l'atmosphère a varié souvent parallèlement à la température. Ce taux a augmenté d'environ 150 % depuis 1750 et atteint aujourd'hui un taux inégalé[103] dans l'histoire, principalement en raison des activités humaines. Une augmentation des teneurs a été constatée en 2008-2009[104]. Les modélisations informatiques du taux du CH4 dans l'air ont permis de remonter à la source des émissions pour les vingt dernières années de mesures atmosphériques. Selon ces travaux, la réduction des émissions et/ou une utilisation plus efficace du gaz naturel dans l'hémisphère Nord (amélioration de l'étanchéité des tuyaux de gaz, récupération du grisou ou du gaz de décharge pour produire de l'électricité, etc.) ont permis une baisse des émissions dans les années 1990, mais une nette augmentation des émissions provenant de combustibles fossiles dans le nord de l'Asie a ensuite de nouveau été constatée (2006…). Le recul des zones humides, par drainage entre autres, et, dans une moindre mesure, les feux de brousse, expliquent aussi les variations mesurées du CH4 atmosphérique sur vingt ans[105].
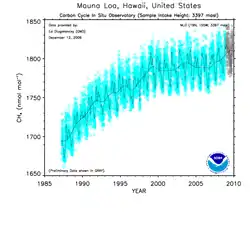
 |
 | |
Taux de méthane à la limite supérieure de la troposphère. |
Saisonnalité relevée par la NOAA. |
Le méthane serait responsable d'environ 20 % du réchauffement moyen enregistré depuis le début de la révolution industrielle.
On estime que sans sa présence, la température moyenne de surface de la Terre serait plus basse de 1,3 °C. Le calcul du potentiel de réchauffement global (PRG) du méthane est périodiquement réévalué par le GIEC au vu des connaissances nouvelles.
Ce PRG tend à augmenter[106], il y a doublement du forçage radiatif additionnel qui lui est attribué entre 2007 et 2013, ce qui le rapproche du CO2 (il est passé de 0,48 à 0,97 W/m2 tous effets confondus et le forçage radiatif du CO2 est 1,68 W), les scientifiques montrant qu'il contribue plus que ce que l'on pensait au réchauffement, avec une source nouvelle et en augmentation forte aux États-Unis qui sont les fuites de méthane des forages et installations de gaz de schiste ou gaz de couche ou encore les émissions du pergélisol[107]. D’après le cinquième rapport du GIEC, paru en 2013, le PRG relatif du méthane est estimé à 28.
L'augmentation régulière de la concentration du méthane dans l'atmosphère pourrait aussi être en partie liée à une diminution de la teneur de l'atmosphère en radical hydroxyle (le destructeur naturel du méthane dans l'air)[108].
Origine des émissions
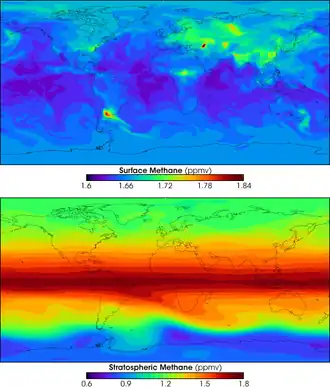
Globalement, les émissions de méthane vers l’atmosphère sont estimées entre 500 et 900 Mt/an, dont environ 60 % sont d’origine anthropique[111],[109].
Les principales sources sont, par ordre décroissant d'importance quantitative, estimées comme suit[109] :
- la fermentation anaérobie sous l'eau (32 % des émissions) : elle a surtout lieu dans les zones humides (naturelles ou artificielles avec en particulier les rizières et les barrages hydroélectriques qui ont inondé des forêts ou accumulé une importante charge organique. Il peut aussi s'agir d'estuaires devenus dystrophes ou de n'importe quelle zone d'accumulation de pollution organique, décharge par exemple).
- Les marais, les mangroves tropicales et les rizières sont sujets à l’action d'archées méthanogènes en milieu anaérobie.
- La température agit sur les émissions, qui atteignent leur valeur maximale entre 37 °C et 48 °C, d’où une amplification des émissions en cas de réchauffement. En présence d'une quantité suffisante d'oxygène, l'activité des archées elles-mêmes contribue à échauffer le matériau, mais avec émission de CO2. L'analyse des gaz piégés il y a 10 000 ans dans les glaces polaires et l'étude du rapport isotopique carbone 13/carbone 12 du carbone de ces molécules de méthane (δ13CH4) ont montré un doublement des taux de CH4 lors de la dernière transition glaciaire-interglaciaire. Ce doublement est dû, à près de 50 %, aux régions marécageuses tropicales, renforcées par les émissions des tourbières boréales favorisées par la transition climatique[112] ;
- les énergies fossiles (21 % des émissions) : le gaz naturel est composé à 90 % de méthane. Les fuites dans l'atmosphère lors de son extraction, de son transport, de son traitement et de sa distribution pourraient représenter jusqu'à 2 % de la production de gaz naturel, les trois quarts de ces fuites ayant lieu chez le client, après le compteur. Le graphe ci-contre montre l'importance des pertes lors de la production, notamment dans certains grands champs gaziers de mer Caspienne et de Sibérie.
- Plusieurs études scientifiques ont montré que les émissions de méthane dues à l'exploitation de gaz de schiste sont beaucoup plus élevées que celles des gisements de gaz conventionnels[113],[114],[115] au point que l'empreinte en équivalent CO2 d’un puits de gaz de schiste en 20 ans serait de 20 à 50 % plus élevée que si on avait utilisé du charbon pour produire la même quantité d'énergie[116],[117]. Plus récemment, en 2018, la NASA a révélé une forte accélération de la croissance de la concentration de méthane dans l’atmosphère, au cours des dix dernières années ; les auteurs de l’étude concluent qu’elle serait en grande partie liée à l'activité du secteur des énergies fossiles[118]. En février 2022, un article paru dans la revue Science révèle que les observations satellitaires du TROPOspheric Monitoring Instrument (TROPOMI) en 2019-2020 ont détecté plusieurs centaines de rejets de méthane de grande ampleur par les installations pétrolières et gazières, totalisant environ huit millions de tonnes de méthane par an, soit 8 à 12 % des émissions de ces industries. Ces rejets se produisent lors d'opérations de maintenance ou de défaillances des équipements ; leur atténuation est réalisable à bas coût[119].
- De même, le gaz piégé dans les filons de charbon lors de sa formation (le grisou) est relâché lors de l'extraction du minerai. En 2018, les majors du pétrole, via l'OGCI (Oil and Gas Climate Initiative) notamment constitué de Total, Saudi Aramco, BP, récemment rejoints par les américains Chevron et ExxonMobil se sont pour la première fois donné un objectifs (à horizon 2025) : « réduire d'un cinquième l'intensité méthane moyenne collective », soit passer de 0,32 % du méthane vendu perdu dans les fuites en 2017 à 0,25 % en 2015 (par rapport au volume total vendu), ce qui correspond - selon l'OGCI - à diminuer l'injection collective de méthane dans l'atmosphère de 350 000 t/an[120] ;
- les ruminants (eructations flatulences, fumiers et lisiers) : dans les années 1990, on montre que les élevages bovins, via leur digestion et leur fumier, contribuent significativement aux émissions mondiales de méthane[121] (environ 16 % vers 2010). En France, en 2008 l'élevage était la source (fumier d'étable compris) de 80 % du méthane émis (contre 69 % en 1990, avec un accroissement relatif de 4,6 % en 18 ans). L'élevage lui-même serait responsable de 92 % des émissions nationales de méthane (dont 70 % sont dues à la fermentation entérique et 30 % aux émanations des lisiers[122]).
- Une seule vache peut émettre 100 à 500 litres de méthane par jour (5 % venant des flatulences et 95 % d'éructations liées à la rumination), quantité qui varie beaucoup selon l'alimentation de l'animal, avec par exemple une moyenne de 100 kg par vache laitière (VL) et par an (variant de 63 à 102 kg) selon Dollé et al. (2006)[123], ou de 117,7 kg en moyenne (de 90 à 163 kg) selon Vermorel et al. (2008)[124], quand la production de lait passe de 3 500 à 11 000 kg/an[125]. « Les concentrés riches en amidon (orge, blé, maïs) ont un effet dépressif sur la méthanogénèse plus important que les concentrés riches en parois digestibles (pulpe de betterave). Martin et al. (2006) citent une étude qui montre que chez la vache laitière, le remplacement des pulpes de betteraves (70 % de la ration) par de l’orge a entraîné une diminution de 34 % des pertes d’énergie sous forme de méthane. » Des plantes plus riches en tanin (dont légumineuses telles que le sainfoin, le lotier et le sulla) diminuent la dégradation des protéines alimentaires mais aussi la méthanogenèse ruminale. Supprimer le soja (féculent) et le remplacer par des graines de lin extrudées (8,4 % sur matière sèche) améliore la qualité nutritionnelle du lait (+34 % d’acides gras insaturés, +120 % d’omégas-3) tout en diminuant l'émission de méthane du troupeau (-10 à -20 % de méthane par jour et efficience azotée améliorée de 16 %) sans diminuer la production laitière, mais avec des taux butyreux et protéique moindre (de -8 % et -3 % respectivement) dans le lait[126].
- Les excréments (fumier d'étable) qui continuent leur décomposition avec une méthanisation plus ou moins anaérobie selon le contexte sont aussi source de méthane.
- Parmi les solutions étudiées[127] : améliorer l'alimentation animale, éviter le stockage des déchets qui ne produisent du méthane qu'à l'abri de l'air, ou mieux récupérer ce méthane et le valoriser énergétiquement. Les féculents comme le soja augmentent la quantité de méthane émise par les bovins quand ils remplacent l'herbe dans l'alimentation industrielle. L’apport dans le rumen de bactéries acétogènes ou capables d'oxyder le méthane), ou l'apport de lipides alimentaires riches en acides gras polyinsaturés dans la ration des ruminants est une piste prometteuse. Des essais menés sur vaches laitières au centre INRA de Clermont ont montré qu'un apport de 6 % de lipides issus de la graine de lin a diminué la production de méthane des animaux de 27 à 37 %[128]. Des chercheurs néo-zélandais ont réussi par des méthodes de sélection à réduire de 10 % les rots et les pets de moutons. Leurs travaux ont montré que ces rejets sont liés en partie à des traits héréditaires[129],[130]. Réintroduire des fibres végétales dans l'alimentation porcine diminue la volatilisation de l'ammoniac et la production de méthane des effluents, sans perte de productivité[131].
- les déchets humains (11 % des émissions) : les décharges fermentent et émettent de grandes quantités de méthane (gaz de décharge) ; ce biogaz peut être utilisé comme source d’énergie[132]. Les égouts peuvent aussi en émettre ;
- la biomasse (10 % des émissions) ; le méthane émis provient surtout de l'oxydation incomplète des végétaux, lors de certains processus de décomposition organique naturelle (comme les feuilles mortes des sous-bois accumulées sous l'eau, fermentation de vases riches en matière organique) ; certaines espèces (termites) peuvent produire des quantités significatives de méthane ; l'utilisation de la biomasse comme source d'énergie est aussi source de quelques fuites de CH4 dans l'air ;
- les sédiments et les océans (4 % des émissions, mais qui pourrait fortement augmenter) : les hydrates contenant du méthane (clathrates) pourraient émettre du gaz en cas de perturbation de la température océanique et/ou du dégel de certains sols riches de la toundra sibérienne et canadienne. Ces émissions sont actuellement limitées mais le réchauffement global pourrait entraîner une augmentation de l'émission de CH4 par les clathrates (dont en périphérie des calottes polaires[133]). Cette source pourrait donc constituer une véritable « bombe à retardement climatique » en cas de réchauffement des fonds océaniques et des calottes glaciaires ;
- les pergélisols : ils contiennent du méthane, libéré quand le climat se réchauffe[134]. Dans les années 2000, une étude internationale[135] (2003-2008) dans les eaux du plateau arctique de Sibérie orientale (plus de deux millions de kilomètres carrés) a montré que les pergélisols immergés perdent du méthane, plus et plus vite que prévu par les modèles : durant cinq ans, plus de 50 % des eaux de surface et plus de 80 % des eaux profondes étudiées présentaient un taux de méthane environ huit fois supérieur à la normale[136]. Le taux actuel moyen de CH4 en Arctique est au tout début du XXIe siècle d'environ 1,85 ppm, soit la plus élevée depuis 400 000 ans, alerte Natalia Chakhova[136]. Un taux encore plus élevé au-dessus du plateau arctique sibérien oriental fait que par N. Chakhova évoque de signes d'instabilité dans le permafrost immergé : « S'il continue à se déstabiliser, les émissions de méthane […] seront beaucoup plus importantes »[136].
- les inlandsis : en 2018, ils ne sont toujours pas comptabilisés dans les « budgets » mondiaux du méthane[137],[138], mais il est démontré depuis peu que des écosystèmes microbiens assez actifs existent sous la calotte polaire arctique, alimentés par d'anciens sols organiques, chaque été, quand l'eau liquide est présente[139] ; cette matière organique provient des anciennes zones humides, toundra et tourbières qui prospéraient là lors des interglaciaires précédents). Le cycle du méthane y est actif[140] mais reste encore à évaluer. Des indices (paléo-climatiques notamment[141]) laissent cependant penser que ce CH4 pourrait amplifier le réchauffement climatique[139],[142],[143],[144]. Ce méthane pouvant influencer les cycles biogéochimiques planétaires, des scientifiques appellent à accélérer l'étude de la biogéochimie des écosystèmes microbiens sous-glaciaire ; ces études ont commencé sous le glacier Russel en limite ouest du Groenland, où du méthane est abondamment produit par des bactéries, mais en partie consommé par d'autres bactéries (méthanotrophes). Lors des deux étés 2012 et 2013, en conditions aérobies (qui n'existent que localement), plus de 98 % du méthane de l'eau sous-glaciaire échantillonnée était consommé par des microbes méthanotrophes (en environ 30 jours d'incubation à +/- 4 °C). À chaque saison chaude se forment sous l'indlandsis des réseaux de ruisseaux, de torrents, tunnels, lacs, etc. d'où émergent des « bouffées » d'eaux sursaturées en méthane (CH4(aq)) qui perdent ensuite une grande partie de ce CH4 dans l'air[145] (l'« évasion atmosphérique » est dans cette région le principal puits de méthane une fois que le ruissellement atteint la bordure de la calotte de glace). Pour la zone étudiée, la première estimation de ce flux saisonnier était de 6,3 tonnes (moyenne ; allant de 2,4 à 11 tonnes) de CH4 dissous (CH4aq) transporté latéralement depuis le dessous de la calotte glaciaire.
- L'hydrologie sous-glaciaire doit être mieux connue ; elle l'est moins sous une grande partie de l'arctique que sous les glaciers alpins[146] ou dans certains contextes paléoclimatologiques européens[147], or elle apparait en arctique être un facteur crucial dans le « contrôle » des flux de méthane[148],[149].
Détection par satellite
Un réseau de mesures et d'analyse se met en place au niveau mondial, à l'initiative de différents groupes comme Climate TRACE et Carbon Mapper, parfois à l'aide d'intelligence artificielle, exploitant des images satellites accessibles aux scientifiques. Ce réseau devrait permettre d'identifier les émissions afin de les réduire[150].
La mission d'observation de la Terre EMIT de la NASA, lancée dans l'espace en juillet 2022, a identifié une cinquantaine de sites « super-émetteurs » dégageant d'importantes quantités de méthane. Au Turkménistan, l'instrument a identifié douze panaches issus d'une infrastructure gazière et pétrolière à l'est de la ville portuaire de Hazar ; certains de ces panaches s'étendent sur plus de 32 kilomètres. Dans l'État américain du Nouveau-Mexique, un autre panache long d'environ 3,3 kilomètres a été détecté au niveau de l'un des plus grands champs pétrolifères du monde. En Iran, au sud de Téhéran, un panache d'au moins 4,8 kilomètres a été observé, issu d'un complexe de traitement des déchets. D'autres émetteurs ont été identifiés en Asie centrale, au Moyen-Orient et dans le sud-ouest des États-Unis[151].
Prospective
Les variations futures de ces émissions sont incertaines, mais on prévoit une augmentation de consommation des sources fossiles, marines et agricoles, des déchets, du fait de la démographie mondiale, de l’industrialisation de certains pays et de la demande croissante en énergie, ainsi que du réchauffement climatique.
Le taux atmosphérique mondial de méthane s'était stabilisé puis est reparti à la hausse (+3 % environ de 2007 à 2015)[152]) outre l’augmentation des sources déjà connues[153], cette hausse pourrait aussi être due à une baisse du taux atmosphérique d'hydroxyle, une molécule qui « joue le rôle de détergent atmosphérique », notamment vis-à-vis du méthane qu'elle dégrade[152]. Des inondations tropicales accrues et un effet du réchauffement sont peut-être aussi en cause. Comme la fonte de la glace de mer arctique, ceci est un nouveau signal d'une perturbation écologique et climatique du système Terre[152].
Remarque : certaines archées méthanotrophes (qui consomment le méthane) sont à l'origine de puits naturels de méthane (par exemple dans les forêts anciennes[154]).), mais leur rôle écosystémique et leurs usages potentiels sont encore mal évalués.
Puits de méthane
Ils sont encore mal cernés, mais la contribution du méthane à certains réseaux trophiques, et certains mécanismes de dégradation du méthane dans l'eau ou l'air pourraient avoir été sous-estimés.
On sait aujourd’hui que :
- les différents mécanismes d’élimination du méthane atmosphérique retirent environ 515 Mt/an ;
- le principal puits à CH4 est le radical hydroxyle OH• contenu dans l’atmosphère, qui contribue à 90 % de la disparition de CH4. Le radical OH•, agent oxydant des principaux polluants de l’atmosphère (CH4, CO, NOx, composés organiques), provient de la dissociation photochimique de O3 et de H2O. La teneur en radical hydroxyle est donc influencée par la concentration atmosphérique en CH4 mais aussi par celle de ses produits, dont CO. De même, divers mécanismes affectent la teneur en OH• :
- l’augmentation de concentration urbaine en NOx engendre plus de formation d’O3 et donc plus de dissociation en OH•,
- la chute de la concentration d’O3 stratosphérique induit plus de rayonnement UV atteignant la troposphère et donc plus de dissociation d’O3 troposphérique,
- l’augmentation de la vapeur d’eau résultant de l’augmentation de la température moyenne produit plus de nuages bloquant les flux de protons, effet réduisant la formation d’OH•, et plus de vapeur d’eau, réactif de formation d’OH•.
- On a constaté que depuis 1750, le niveau d’OH• a diminué d’environ 20 % du fait de l’augmentation en CO et CH4, et est aujourd’hui stable. D’ici 2050, ce niveau devrait encore diminuer de 25 %, ce qui aura un impact important sur les teneurs en éléments traces gazeux. Les 10 % restants sont dus à l’oxydation du méthane en terrain sec par des archées méthanotrophes qui l’utilisent comme source de carbone, ainsi que par son transfert vers la stratosphère ;
- dans le sol, dans certaines nappes, dans les sédiments marins ou dans les zones humides vivent des archées qui consomment du méthane. Elles sont localement à l'origine d'un réseau trophique (pélagique) et d'un « puits biologique » de méthane importants, en mer mais aussi dans certains lacs, notamment en hiver où ces archées deviennent une source alimentaire plus importante pour le zooplancton, ce qui a été démontré par des analyses isotopiques[155], par exemple en alimentant certaines larves de chironomes (phénomène observé à la suite de la découverte inattendue de larves de chironomidae dont l'organisme était anormalement appauvri en 13C (toujours dans des lacs eutrophes et pauvres en oxygène)[156] ;
- le méthane est souvent associé à des HAP toxiques. Certaines des archées méthanotrophes sont mobiles et on a montré qu'elles pouvaient améliorer le transport des HAP dans le sous-sol. Cette qualité peut être utilisée pour épurer une nappe polluée par les HAP[157], mais peut aussi expliquer la pollution de nappes ou certaines distribution ou dispersion de HAP[158].
L'évolution de la concentration de l'air en méthane semble marquer le pas[159] (2007) ; cela pourrait s'expliquer par une destruction accélérée de molécules d'ozone O3, catalysée par des radicaux NO• en plus grande quantité[160],[161].
Réduire les émissions de méthane
La réduction des émissions de méthane, comparée à celle du dioxyde de carbone, peut se révéler plus économique et plus efficace dans l'atténuation du changement climatique, étant donné son fort potentiel de réchauffement global et son temps de séjour dans l'atmosphère relativement court, de neuf ans[162].
Divers moyens permettent de réduire les émissions de méthane pour diminuer son action sur l'effet de serre :
- capter le méthane, ou biogaz, émis au niveau des décharges d'ordures ou stations d'épuration et le brûler (la combustion forme du CO2 qui a un effet de serre moins important), ou le purifier par distillation puis l'injecter dans le réseau de distribution du gaz naturel[163], ce qui permettrait de remplacer en partie le gaz importé au lieu de brûler en torchère le gaz de décharge comme c'est souvent le cas actuellement ;
- capter et utiliser le méthane, ou biogaz, produit au niveau des systèmes de stockage des effluents d'élevages ; récupérer le méthane émis lors de l'exploitation minière et après celle-ci ;
- modifier l'alimentation des bovins pour réduire la production de méthane lors de la digestion : les chercheurs de l'Inra Clermont-Ferrand ont montré qu'en remplaçant une partie de leur alimentation par des lipides issus de la graine de lin, voire de colza, les bovins émettraient jusqu'à 40 % de méthane en moins. Néanmoins, Michel Doreau, le chercheur à l'origine de ces travaux, demeure prudent, soulignant l'obstacle du coût, et estime qu'il est possible d'arriver à une baisse globale de seulement 10 % des émissions[163]. 650 éleveurs de l'association Bleu Blanc Cœur se sont ainsi lancés dans cette démarche, et le projet européen Eco-méthane associe huit pays ; les producteurs suisses devraient s'engager massivement dans la démarche dès 2017 ; planter 250 000 hectares de lin, contre 50 000 aujourd'hui, suffirait pour l'élevage français. L'industrie étudie aussi des additifs alimentaires de synthèse agissant sur la flore microbienne des animaux[163]. Selon Paul Hawken, la consommation par les ruminants d'algues Asparagopsis taxiformis, contenant du bromoforme, serait une autre piste pour la réduction de ce type de production de méthane[164] ;
- développer une riziculture moins productrice de méthane, diminuer les taux de fertilisants, lutter contre la turbidité des eaux et la production de sédiments méthanogènes, et donc en amont contre l'érosion, la régression et dégradation des sols. Des études menées en Asie ont montré que le simple fait de drainer les rizières deux fois par an permettrait de réduire leurs émissions de 80 %[163] ;
- au niveau personnel :
- réduire sa consommation de viande rouge et de produits laitiers[165]
- réduire sa consommation de riz[165] (voir le lien entre riziculture et effet de serre),
- composter ses déchets en veillant à ce que le compost soit suffisamment aéré et drainé.
Stratégie européenne de réduction des émissions de méthane
La Commission européenne présente le 14 octobre 2020 sa stratégie de réduction des émissions de méthane : création d'un observatoire international afin d'améliorer la mesure et le partage d'informations, renforcement de la surveillance via la galaxie satellitaire Copernicus, directive prévue en 2021 pour imposer aux industriels des énergies fossiles de mieux détecter et réparer les fuites de méthane et interdire les pratiques de torchage et de dégazage systématiques, extension du champ d'application de la directive relative aux émissions industrielles aux secteurs émetteurs de méthane non encore couverts, demande aux États membres d'un effort de traitement des mines de charbon abandonnés, pression sur les pays partenaires commerciaux pour réduire l'impact méthane de l'énergie importée, incitations à réduire les émissions dans l'agriculture par l'innovation en matière d'alimentation animale et de gestion d'élevage, renforcement de la collecte des déchets et résidus agricoles non recyclables qui peuvent servir à produire du biogaz et des biomatériaux, amélioration de la gestion du gaz de décharge[166].
Le 15 décembre 2021, la Commission européenne présente son projet détaillé pour la réduction des émissions de méthane du secteur de la production d'énergie, qu'elle espère réduire de 80 % en 2030 par rapport à 2020 : les industriels du gaz, du charbon et du pétrole devront effectuer des mesures régulières à la source de leurs fuites de méthane, avec vérification par des experts indépendants. Les industriels auront ensuite, selon la nature des problèmes identifiés, de 5 à 15 jours pour y remédier. Afin de lutter contre les « émissions importées » de méthane, elle imposera aux importateurs d'énergie fossile la transparence sur le niveau d'émissions de méthane de leurs fournisseurs et les efforts de ces derniers pour les réduire, puis, à compter de 2025, elle durcira les règles sur les importations d'énergie fossile issue de producteurs aux efforts jugés insuffisants[167].
COP26
Le 2 novembre 2021, lors de la COP26, à l'appel des États-Unis et de l'Union européenne, plus de 80 pays s'engagent à réduire d'ici à 2030 d'au moins 30 % les émissions de méthane. Selon l'ONU, tenir ce nouvel objectif pourrait éviter 0,3 °C de réchauffement d'ici aux années 2040. L'administration américaine a dévoilé auparavant une série de nouvelles réglementations destinées à faire la chasse au méthane dans l'industrie pétrolière et gazière aux États-Unis, susceptibles de réduire de 41 millions de tonnes ses émissions de 2023 à 2035, selon l'Agence américaine de protection de l'environnement. Cependant, certains des plus grands émetteurs de méthane issu des mines de charbon n'ont pas signé l'accord, en particulier la Chine, la Russie et l'Inde, qui représentent un tiers des émissions[168].
Synthèse du méthane
Synthèse photocatalytique
Des chercheurs du laboratoire d’électrochimie moléculaire de l'Université Paris-Diderot ont montré que la conversion photochimique de CO2 en méthane à température ambiante et par un catalyseur sélectif, abondant, non-polluant, non-toxique et peu coûteux, associé à la lumière solaire était possible, ce qui ouvre de nouvelles perspectives qui, à long terme, peuvent espérer aboutir à des applications industrielles[169]. Elle pourrait alors — en principe — réduire les effets de la consommation de combustibles fossiles et aider à diminuer les émissions de CO2[170],[171].
Jusqu’ici, les principales voies explorées pour l’élimination physicochimique du CO2 industriel étaient principalement électrochimiques. Pour être « soutenables », elles nécessitent une production renouvelable et propre d’électricité[172] mais des approches photochimiques activées par la lumière du soleil sont également envisageables[173],[174]. Parmi les photocatalyseurs et les électrocatalyseurs moléculaires inventoriés, seuls quelques-uns semblent à la fois stables et sélectifs pour la réduction du CO2. Mais la plupart de ces catalyseurs produisent surtout du monoxyde de carbone (CO, toxique) ou de l’acide formique (HCOOH)[169]. Les catalyseurs pouvant dans certaines conditions générer avec un rendement faible à modéré des hydrocarbures semblent encore plus rares[175],[176],[177],[178],[179],[180],[181],[182].
Un complexe électrocatalytique moléculaire s’était déjà montré comme le plus efficace et le plus sélectif pour convertir le CO2 en CO ; il s’agit de la tétraphénylporphyrine de fer fonctionnalisée par des groupes triméthylammonium[183],[184],[185]. On a montré en 2017 que sous irradiation ultraviolette il peut aussi catalyser la réduction de CO2 en méthane à température et pression ambiantes. Utilisé dans une solution d'acétonitrile contenant un photosensibilisateur et un donneur d'électrons sacrificiel, ce catalyseur fonctionne avec régularité durant quelques jours, en produisant principalement du CO (par photoréduction du CO2) mais Heng Rao et ses collègues ont constaté qu’une exposition du CO2 à ce produit conduite en deux stades permet d'abord de réduire le CO2 en CO puis de synthétiser du méthane (avec une sélectivité atteignant jusqu'à 82 % et un « rendement quantique » (efficacité légère) de 0,18 %).
On est encore très loin d’un prototype industriel, mais les auteurs estiment que cette expérience pourrait être un prélude à d’autres découvertes de catalyseurs moléculaires qui rendraient possible une production lente mais douce d'un combustible gazeux à partir de CO2 et des ultraviolets de la lumière solaire[169].
Biosynthèse
Le méthane est considéré comme une source d'énergie intéressante et durable s'il n'est pas d'origine fossile mais renouvelable et soutenable dans sa fabrication. Comme l'humanité émet trop de dioxyde de carbone CO2 dans l'air, un système de conversion directe de CO2 en CH4 est activement recherchée pour à la fois protéger le climat et stocker une énergie renouvelable. Des solutions sans catalyseur rare, cher ou toxique sont recherchées.
Les chercheurs peuvent pour cela s'inspirer du vivant (biomimétique) car du méthane pur est depuis des milliards d'années efficacement et abondamment produit par quelques espèces microbiennes dites « méthanogènes », dans l'eau ou dans l'appareil digestif d'autres organismes.
Une clé semble être la méthyl-coenzyme M réductase, l'enzyme de la biogenèse du méthane (qui permet aussi l'utilisation du méthane comme source d'énergie (par oxydation anaérobie)[186]). Cette enzyme a un facteur auxiliaire dit « coenzyme F430 », un tétrapyrrole modifié contenant du nickel qui favorise la catalyse à travers un intermédiaire méthyle radical/Ni(II)-thiolate intermédiaire. On ignore encore comment la coenzyme F430 est synthétisée (à partir d'une composé commun, le uroporphyrinogène III), mais on sait que sa synthèse implique une chélation, une amidation, une réduction d'anneau macrocyclique, une lactamisation et la formation d'anneau carbocyclique[186].
Les protéines catalysant la biosynthèse de la coenzyme F430 (à partir de sirohydrochlorine, appelée CfbA-CfbE) ont été récemment identifiées, permettant d'envisager des systèmes recombinants basés sur ces groupes métalloprothétiques[186]. Cette meilleure compréhension de la biosynthèse d'un coenzyme de la production de méthane par les microbes complète les voies biosynthétiques connues pour une famille des composés importants incluant la chlorophylle, l'hème et la vitamine B12[187],[186]. Dans la nature, la plupart du méthane est produit dans un milieu aqueux, ce qui peut inspirer des solutions techniques immergées[188], mais la plupart des sources massives de CO2 anthropique sont gazeuses.
Une première méthode de conversion de CO2 en CH4 (pilotée/catalysée par la lumière et utilisant une hème, c'est-à-dire une porphyrine contenant du fer) a été proposé en 2018 par deux chercheurs allemands (Steinlechner et Junge) du Leibniz Institut für Katalyse (de) de l'Université de Rostock[189] et d'autres chercheurs travaillent sur des complexes métalliques ou organométalliques utiles[190] et sur les moyens de doper ce type de réaction chimique[191],[192].
Méthane et biodiversité
Le méthane a probablement depuis longtemps des effets sur la biodiversité et inversement, notamment via le climat qu'il peut modifier[193] ou via les communautés microbiennes formant le microbiote intestinal des animaux.
Une hypothèse est que certains groupes d'invertébrés (métazoaires dont le métabolisme et le cycle de reproduction peuvent alors augmenter) ont par le passé bénéficié de phases de réchauffement marins ; l'explosion cambrienne (« Big Bang de l'évolution ») pourrait avoir été liée à des alternances assez rapprochées de phases intenses de puits (clathrates) et d'émissions de méthane bionique, liées à des déplacements tectoniques de plaques (migration vers les pôles puis l'équateur). Ces migrations (True Polar Wander (en) ou TPW) auraient eu des conséquences tectoniques, biogéochimiques et donc climato-écologiques, notamment via des changements de la circulation thermohaline océanique, conséquences intimement reliées entre elles ; l'aspect stochastique de ces évènements aurait au Cambrien dopé la radiation évolutive des métazoaires. Selon Kirschvink et Raub en 2003, une « mèche au méthane » aurait pu mettre l'étincelle de cette explosion cambrienne[194]. Remarque : au cambrien le soleil était un peu plus petit et moins chaud qu'aujourd'hui. Lors du dernier grand réchauffement (maximum thermique du passage Paléocène-Éocène), il y a 56 millions d'années, les ancêtres des mammifères sont apparus, mais de nombreux autres groupes se sont éteints.
Si le méthane est aujourd'hui essentiellement associé à des milieux anoxiques pauvres en espèce, on y trouve aussi quelques espèces méthanotrophes qui en dépendent. On a par exemple récemment identifié :
- un nématode sans bouche ni intestin (Astomonema southwardorum (nl)) qui, en mer du Nord, dominait la microfaune du sédiment d'une zone riche en méthane[195] ;
- le « vers de glace de méthane » (Hesiocaeca methanicola) ;
- des communautés microbiennes qui peuvent former des biofilms dans des installations de laboratoires ou industrielles utilisant ou filtrant le méthane[196].
Mesure
Sa mesure en laboratoire est bien maitrisée, mais on cherche à développer des moyens de mesures plus légers, rapides, faciles à utiliser et moins coûteux, pour mesurer les faibles doses de méthane discrètement émises dans les eaux douces, salées, estuariennes, l'air, les sols & sédiments ou lors de certains phénomènes (évents marins, fonte de pergélisols, geysers, fuites de gaz, dont de gaz de schiste, etc.)[197].
Notes et références
Notes
- ↑ Le pouvoir calorifique à 25 °C vaut PCI = 890,8 × 103 J/mol et le volume molaire V = 22,4 × 10−3 m3/mol donc PCI/V = 39,77 × 106 J/m3. La masse molaire vaut M = 16,042 5 × 10−3 kg/mol donc PCI/M = 55,53 × 106 J/kg.
- ↑ 1 kWh = 3,6 × 106 J.
- ↑ Dont, en France, le CEA, le CNRS et l'université de Versailles Saint-Quentin-en-Yvelines (UVSQ).
Références
- ↑ Édouard Grimaux, Chimie Organique Élémentaire, 376 p. (ISBN 978-5-87612-781-5, lire en ligne), p. 21.
- 1 2 3 4 METHANE, Fiches internationales de sécurité chimique
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- 1 2 3 4 Entrée « Methane » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 26 mai 2009 (JavaScript nécessaire)
- 1 2 « METHANE », sur Hazardous Substances Data Bank (en)
- ↑ (en) James E. Mark, Physical Properties of Polymer Handbook, Springer, , 2e éd., 1076 p. (ISBN 978-0-387-69002-5 et 0-387-69002-6, lire en ligne), p. 294
- 1 2 (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, États-Unis, McGraw-Hill, , 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50
- ↑ (en) Iwona Owczarek et Krystyna Blazej, « Recommended Critical Pressures. Part I. Aliphatic Hydrocarbons », Journal of Physical and Chemical Reference Data, vol. 35, no 4, , p. 1461 (DOI 10.1063/1.2201061)
- ↑ (en) Iwona Owczarek et Krystyna Blazej, « Recommended Critical Temperatures. Part I. Aliphatic Hydrocarbons », J. Phys. Chem. Ref. Data, vol. 32, no 4, , p. 1411 (DOI 10.1063/1.1556431)
- ↑ (en) William M. Haynes, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, , 91e éd., 2610 p. (ISBN 9781439820773, présentation en ligne), p. 14-40
- ↑ (en) Irvin Glassman et Richard A. Yetter, Combustion, Elsevier, , 4e éd., 773 p. (ISBN 978-0-12-088573-2), p. 6
- ↑ (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams : Organic Compounds C8 to C28, vol. 1, 2 et 3, Huston, Texas, Gulf Pub. Co., , 396 p. (ISBN 0-88415-857-8, 978-0-88415-858-5 et 978-0-88415-859-2)
- ↑ (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press, , 83e éd., 2664 p. (ISBN 0849304830, présentation en ligne), p. 5-89
- ↑ Magalie Roy-Auberger, Pierre Marion, Nicolas Boudet, Gazéification du charbon, éd. Techniques de l'Ingénieur, référence J5200, 10 décembre 2009, p. 4
- ↑ (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, , 89e éd., 2736 p. (ISBN 9781420066791, présentation en ligne), p. 10-205
- ↑ Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- ↑ « Méthane » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ Biographie | http://www.cartage.org.lb/en/themes/biographies/MainBiographies/V/Volta/1.html
- ↑ (it) Alessandro Volta, Lettere del Signor Don Alessandro Volta… Sull' Aria Inflammabile Nativa delle Paludi, Milan, éd. Guiseppe Marelli, 1777.
- ↑ (en) « Methane », BookRags (consulté le ).
- 1 2 Söhngen N.L, Sur le rôle du methane dans la vie organique, Recueil des Travaux Chimiques des Pays-Bas et de la Belgique, 29(7), 1910, 238-274.
- ↑ (en) Wang, W.-C., Y.L. Yung, A.A. Lacis, T. Mo et J.E. Hansen, « Greenhouse effects due to man-made perturbation of trace gases », Science, no 194, 1976, DOI 10.1126/science.194.4266.685 p. 685-690.
- 1 2 Petrenko, V. V., Smith, A. M., Schaefer, H., Riedel, K., Brook, E., Baggenstos, D.... & Fain, X. (2017) Minimal geological methane emissions during the Younger Dryas–Preboreal abrupt warming event. Nature, 548(7668), 443.
- ↑ Etiope, G., Milkov, A. V. & Derbyshire, E. Did geologic emissions of methane play any role in Quaternary climate change? Global Planet. Change 61, 79–88 (2008)
- ↑ Luyendyk, B., Kennett, J. & Clark, J. F. (2005) Hypothesis for increased atmospheric methane input from hydrocarbon seeps on exposed continental shelves during glacial low sea level. Mar. Pet. Geol. 22, 591–596
- ↑ Etiope, G., Lassey, K. R., Klusman, R. W. & Boschi, E. (2008) Reappraisal of the fossil methane budget and related emission from geologic sources. Geophys. Res. Lett. 35, L09307
- 1 2 Schwietzke S et al. (2016) Upward revision of global fossil fuel methane emissions based on isotope database. Nature 538, p. 88–91.
- ↑ (en) Petrenko, V. V. et al. 14CH4 measurements in Greenland ice: investigating last glacial termination CH4 sources. Science 324, 506–508 (2009)
- ↑ Schaefer, H. et al. Ice record of δ13C for atmospheric CH4 across the Younger Dryas–Preboreal transition. Science 313, 1109–1112 (2006)
- ↑ Sowers, T. Late quaternary atmospheric CH4 isotope record suggests marine clathrates are stable. Science 311, 838–840 (2006)
- ↑ Kennett, J. P., Cannariato, K. G., Hendy, I. L. & Behl, R. J. (2003) Methane Hydrates in Quaternary Climate Change: The Clathrate Gun Hypothesis (AGU)
- ↑ Walter, K. M., Edwards, M. E., Grosse, G., Zimov, S. A. & Chapin, F. S. (2007) III. Thermokarst lakes as a source of atmospheric CH4 during the last deglaciation. Science 318, 633–636
- ↑ Weitemeyer K.A & Buffett B.A (2006) Accumulation and release of methane from clathrates below the Laurentide and Cordilleran ice sheets. Global Planet. Change 53, 176–187 (résumé)
- ↑ (en) Q. Wang et al., « Aerobic bacterial methane synthesis », Proc. Natl Acad. Sci. USA 118, e2019229118 (2021)
- ↑ Biogaz issus de déchets alimentaires pour cogénération / CHP, Clarke Energy.
- ↑ (en) Rudolf K. Thauer, « Methyl (Alkyl)-Coenzyme M Reductases: Nickel F-430-Containing Enzymes Involved in Anaerobic Methane Formation and in Anaerobic Oxidation of Methane or of Short Chain Alkanes », Biochemistry, vol. 58, no 52, , p. 5198–5220 (ISSN 0006-2960 et 1520-4995, DOI 10.1021/acs.biochem.9b00164, lire en ligne, consulté le )
- 1 2 B. Nicolardot et J.C. Germon, « Émissions de méthane (CH4) et d’oxydes d’azote (N2O et NOx) par les sols cultivés : Aspects généraux et effet du non-travail du sol » [PDF], Étude et Gestion des Sols, volume 15, numéro 3, 2008, p. 171-182.
- ↑ P.A. Roger, J. Le Mer et C. Joulian, « L'émission et la consommation de méthane par les sols : mécanismes, bilan, contrôle. », Comptes Rendus de l'Académie d'Agriculture, volume 85, numéro 6, p. 193-210 (résumé).
- ↑ (en) F. Suarez, J. Furne, J. Springfield et M Levitt, « Insights into human colonic physiology obtained from the study of flatus composition », American Journal of Physiology, vol. 272 (5 Pt 1), , G1028–33.
- ↑ (en) Frank Keppler, John T. G. Hamilton, Marc Braß et Thomas Röckmann, « Methane emissions from terrestrial plants under aerobic conditions », Nature, vol. 439, no 7073, , p. 187–191 (ISSN 0028-0836 et 1476-4687, DOI 10.1038/nature04420).
- ↑ (en) Andy R. McLeod, Stephen C. Fry, Gary J. Loake et David J. Messenger, « Ultraviolet radiation drives methane emissions from terrestrial plant pectins », New Phytologist, vol. 180, no 1, , p. 124–132 (ISSN 0028-646X et 1469-8137, DOI 10.1111/j.1469-8137.2008.02571.x).
- ↑ (en) Katharina Lenhart, Michael Bunge, Stefan Ratering et Thomas R. Neu, « Evidence for methane production by saprotrophic fungi », Nature Communications, vol. 3, no 1, (ISSN 2041-1723, DOI 10.1038/ncomms2049).
- ↑ (en) Thomas Klintzsch, Gerald Langer, Gernot Nehrke et Anna Wieland, « Methane production by three widespread marine phytoplankton species: release rates, precursor compounds, and potential relevance for the environment », Biogeosciences, vol. 16, no 20, , p. 4129–4144 (ISSN 1726-4189, DOI 10.5194/bg-16-4129-2019).
- ↑ (en) Paul Bodelier, « Faculty Opinions recommendation of Aquatic and terrestrial cyanobacteria produce methane. », Science Advances, (DOI 10.3410/f.737215871.793570092).
- 1 2 Frank Keppler, Thomas Röckmann, « Méthane, plantes et climat », Pour la science, (lire en ligne, consulté le ).
- ↑ (en) Jan F. Hartmann, Marco Günthel, Thomas Klintzsch et Georgiy Kirillin, « High Spatiotemporal Dynamics of Methane Production and Emission in Oxic Surface Water », Environmental Science & Technology, vol. 54, no 3, , p. 1451–1463 (ISSN 0013-936X et 1520-5851, DOI 10.1021/acs.est.9b03182).
- ↑ (en) Leonard Ernst, Benedikt Steinfeld, Uladzimir Barayeu et Thomas Klintzsch, « Methane formation driven by reactive oxygen species across all living organisms », Nature, (ISSN 0028-0836 et 1476-4687, DOI 10.1038/s41586-022-04511-9, lire en ligne, consulté le ).
- ↑ (en) Volkmar Braun et Klaus Hantke, « Recent insights into iron import by bacteria », Current Opinion in Chemical Biology, vol. 15, no 2, , p. 328–334 (ISSN 1367-5931, DOI 10.1016/j.cbpa.2011.01.005)
- ↑ (en) V. I. Bruskov, Zh. K. Masalimov et A. V. Chernikov, « Heat-Induced Generation of Reactive Oxygen Species in Water », Doklady Biochemistry and Biophysics, vol. 384, nos 1/6, , p. 181–184 (DOI 10.1023/A:1016036617585, lire en ligne, consulté le ).
- ↑ Laurent Sacco, « Des suintements de méthane préoccupants dans le Pacifique », sur Futura-Sciences, (consulté le )
- ↑ (en) Susan L. Hautala et al., « Dissociation of Cascadia margin gas hydrates in response to contemporary ocean warming », sur Wiley-On line library, (consulté le )
- ↑ Présentation du programme MARMESONET, IFREMER.
- ↑ Pascal Cuissot, Luc Riolon et Rachel Seddoh, Méthane, rêve ou cauchemar, Arte, 5 décembre 2014.
- ↑ INERIS, Rapport d'étude : L'élaboration des plans de prévention des risques miniers, Guide méthodologique, volet technique relatif à l'évaluation de l'aléa. Les risques de mouvements de terrain, d'inondations et d'émissions de gaz de mine, rapport DRS 06 51198/R01, 4 mai 2006, p. 81/140, « Transport de gaz sous forme dissoute dans l'eau ».
- ↑ (en) Jorge A. Ramirez, Andy J. Baird, Tom J. Coulthard and J. Michael Waddington (2015), Ebullition of methane from peatlands: Does peat act as a signal shredder ?, Geophysical Research Letters, 42, 9, (3371-3379).
- ↑ (en) Xi Chen, Karina V. R. Schäfer and Lee Slater (2017), Methane emission through ebullition from an estuarine mudflat: 2. Field observations and modeling of occurrence probability, Water Resources Research, 53, 8, (6439-6453)
- ↑ (en) Zhaosheng Fan, Anthony David McGuire, Merritt R. Turetsky, Jennifer W. Harden, James Michael Waddington and Evan S. Kane (2012), The response of soil organic carbon of a rich fen peatland in interior Alaska to projected climate change, Global Change Biology, 19, 2, (604-620).
- ↑ (en) Jorge A. Ramirez, Andy J. Baird, Tom J. Coulthard and J. Michael Waddington (2015), Testing a simple model of gas bubble dynamics in porous media, Water Resources Research, 51, 2, (1036-1049).
- ↑ (en) Jorge A. Ramirez, Andy J. Baird and Tom J. Coulthard (2016), The effect of pore structure on ebullition from peat, Journal of Geophysical Research: Biogeosciences, 121, 6, (1646-1656).
- ↑ (en) Jorge A. Ramirez, Andy J. Baird and Tom J. Coulthard (2017), The effect of sampling effort on estimates of methane ebullition from peat, Water Resources Research, 53, 5, (4158-4168).
- ↑ (en) Nguyen Thanh Duc, Samuel Silverstein, Lars Lundmark, Henrik Reyier, Patrick Crill & David Bastviken, Automated Flux Chamber for Investigating Gas Flux at Water–Air Interfaces, Environmental Science & Technology, 10.1021/es303848x, 47, 2, (968-975), (2012).
- ↑ (en) Genevieve L. Noyce, Ruth K. Varner, Jill L. Bubier and Steve Frolking, Effect of Carex rostrata on seasonal and interannual variability in peatland methane emissions, Journal of Geophysical Research: Biogeosciences, 119, 1, (24-34), (2014).
- ↑ (en) Sparkle L. Malone, Gregory Starr, Christina L. Staudhammer and Michael G. Ryan (2013), Effects of simulated drought on the carbon balance of Everglades short‐hydroperiod marsh, Global Change Biology, 19, 8, (2511-2523).
- ↑ Température d'auto-inflammation du méthane dans l'air.
- ↑ (en) NASA Explores the Red Planet, 15 janvier 2009, Martian Methane Reveals the Red Planet is not a Dead Planet.
- ↑ (en) Michael J. Mumma, Geronimo L. Villanueva, Robert E. Novak, Tilak Hewagama, Boncho P. Bonev, Michael A. DiSanti, Avi M. Mandell et Michael D. Smith, « Strong Release of Methane on Mars in Northern Summer 2003 », Science, vol. 323, no 5917, , p. 1041-1045 (DOI 10.1126/science.1165243, lire en ligne [PDF]).
- ↑ (en) Franck Lefèvre et François Forget, « Observed variations of methane on Mars unexplained by known atmospheric chemistry and physics », Nature, vol. 40, , p. 720-723 (DOI 10.1038/nature08228, résumé)
- ↑ (en) NASA Explores the Red Planet, 15 janvier 2009, Mars Methane Press Conference - Media Page.
- ↑ (en) Todd M. Hoefen, Roger N. Clark, Joshua L. Bandfield, Michael D. Smith, John C. Pearl et Philip R. Christensen, « Discovery of Olivine in the Nili Fossae Region of Mars », Science, vol. 203, no 5645, , p. 627-630 (DOI 10.1126/science.1089647, résumé).
- ↑ (en) NASA Mars Reconnaissance Orbiter, 18 décembre 2008, Mineral Spectra from Nili Fossae, révélant la présence d'argiles riches en fer et en magnésium, d'olivine et de carbonate de magnésium
- ↑ (en) 40th Lunar and Planetary Science Conference – 2009, B.L. Ehlmann, J.F. Mustard et S.L. Murchie, Detection of serpentine on Mars by MRO-CRISM and possible relationship with olivine and magnesium carbonate in Nili Fossae.
- ↑ (en) ESA News – 20 septembre 2004 Water and methane maps overlap on Mars: a new clue?
- 1 2 Hand E (2018) « On Mars, atmospheric methane—a sign of life on Earth—changes mysteriously with the seasons », Science News, 3 janvier
- ↑ Maxence Layet, « Les latrines des prisons rwandaises alimentent les bâtiments en énergie », sur Novethic, (version du 31 janvier 2011 sur Internet Archive).
- ↑ Brève d’Actualité Pour la science, no 405, juillet 2011, p. 7.
- ↑ Brève, entretien avec Edith Labelle, de l'Institut de technologie des procédés chimiques et de l'environnement, Conseil national de recherches Canada, (consulté le )
- ↑ (en) Cheng, Xing, Call et Logan, « Direct Biological Conversion of Electrical Current into Methane by Electromethanogenesis », Environmental Science & Technology, vol. 43, no 10, , p. 3953–3958 (ISSN 0013-936X, PMID 19544913, DOI 10.1021/es803531g, Bibcode 2009EnST...43.3953C, résumé).
- ↑ Communiqué sur le site de veille technologique de l'ADIT
- ↑ (de) Communiqué sur le site de l'entreprise Fraunhofer
- ↑ (en) Specht et al., Storing bioenergy and renewable electricity in the natural gas grid, p. 70.
- ↑ Benjamin Dessus, Bernard Laponche et Hervé Le Treut, « Réchauffement climatique : importance du méthane », Les cahiers de Global Chance, Global Chance, no 24, , p. 3 (lire en ligne [PDF]).
- ↑ (en) GIEC, chap. 8 « Anthropogenic and Natural Radiative Forcing », dans Climate Change 2013: The Physical Science Basis. Contribution of Working Group I to the Fifth Assessment Report of the Intergovernmental Panel on Climate Change, (lire en ligne [PDF]), p. 714, voir Cinquième rapport d'évaluation du GIEC.
- ↑ (en) J.T. Kiehl et Kevin E. Trenberth, « Earth’s Annual Global Mean Energy Budget », Bulletin of the American Meteorological Society, vol. 78, no 2, , p. 197-208 (DOI 10.1175/2008BAMS2634.1, lire en ligne [PDF]).
- ↑ Le méthane : d’où vient-il et quel est son impact sur le climat ? (rapport), Académie des technologies, (lire en ligne [PDF]), Chapitres 1 et 6, p. 11-24, 107-120 et 170.
- ↑ GIEC, « Changements climatiques 2013, Les éléments scientifiques : Résumé à l’intention des décideurs » [PDF], sur ipcc.ch, (consulté le ), p. 12.
- ↑ Benjamin Dessus et Bernard Laponche, « Forçage radiatif et PRG du méthane dans le rapport AR5 du GIEC », Les cahiers de Global chance, Global Chance, no 35, (lire en ligne [PDF], consulté le ).
- ↑ Benjamin Dessus, Bernard Laponche et Hervé Le Treut, « Réchauffement climatique : importance du méthane » [PDF], sur AIEA, , p. 4/14.
- ↑ Anne Feitz, « Les émissions de méthane, un danger pour le climat », Les Échos, (lire en ligne).
- ↑ « La mystérieuse et inquiétante flambée des émissions de méthane », Le Monde, (lire en ligne, consulté le ).
- ↑ Muryel Jacque, Climat : les émissions mondiales de méthane atteignent des niveaux records, Les Échos, 15 juillet 2020.
- ↑ Fiore, A.M., D.J. Jacob, B.D. Field, D.G. Streets, S.D. Fernandes et C. Jang (2002), Linking ozone pollution and climate change: The case for controlling methane, Geophys. Res. Lett., 29(19), 1919, DOI 10.1029/2002GL015601 (Résumé).
- ↑ Université Grenoble-Alpes, Recherche, Du méthane émis par les activités humaines depuis l'Empire romain,
- ↑ (en) Jeff Tollefson (2019) Tropical Africa could be a key to solving methane mystery ; Project analyses wetlands’ contribution to a spike in atmospheric concentrations of the potent greenhouse gas, Nature News, 06 février.
- 1 2 3 4 (en) C.J. Sapart, G. Monteil, M. Prokopiou, R.S.W. Van de Wal, J.O. Kaplan, P. Sperlich, K.M. Krumhardt, C. Van der Veen, S. Houweling, M.C. Krol, T. Blunier, T. Sowers, P. Martinerie, E. Witrant, D. Dahl-Jensen et T. Röckmann, « Natural and anthropogenic variations in methane sources during the past two millennia », Nature, vol. 490, (DOI 10.1038/nature11461)
- ↑ Présentation officielle du forage glaciaire NEEM, Groenland (2 537 mètres de forage atteints en juillet 2010)
- ↑ LGGE-GIPSA-lab, Grenoble-INP modèle numérique LGGE-GIPSA
- 1 2 (en-US) NOAA US Department of Commerce, « Global Monitoring Laboratory - Carbon Cycle Greenhouse Gases », sur gml.noaa.gov (consulté le )
- ↑ (en) United Nations Environment Programme (UNEP) GRID-Arendal – 2003, Climate Change 2001: Working Group I: The Scientific Basis. Voir 4.2 Trace Gases: Current Observations, Trends, and Budgets – 4.2.1 Non-CO2 Kyoto Gases – 4.2.1.1 Methane (CH4).
- ↑ (en) E. G. Nisbet et al., Rising atmospheric methane: 2007–2014 growth and isotopic shift, American Geophysical Union, 26 septembre 2016.
- ↑ Concentration du méthane mesurée à Mauna Loa (Hawaï), NOAA.
- ↑ Atmospheric CH4 Concentrations from the CSIRO GASLAB Flask Sampling Network, in CDIAC Online Trends , CSIRO : graphique montrant une stabilisation du CH4 atmosphérique, à l'époque non expliquée, de 2000 à 2003.
- ↑ Évolution du taux de méthane atmosphérique
- ↑ http://www.ipcc.ch/pdf/assessment-report/ar4/wg1/ar4-wg1-spm-fr.pdf
- ↑ Bulletin ADIT pour l'Australie numéro 61 (2009 01 15) - Ambassade de France en Australie / ADIT, reprenant une information du CSIRO
- ↑ Explaining the methane mystery, communiqué, CSIRO, 2006, 06/188.
- ↑ Carbone 4 (2014) Le PRG du méthane s’enflamme : la contribution à l’effet de serre du CH4 se fait de plus en plus sentir…, 2014-01-22
- ↑ (2013) Des résultats inquiétants sur le méthane, dans le dernier rapport du GIEC, 2013-11-07
- ↑ Paul Voosen(2016) Why is atmospheric methane surging? (Hint: It's not fracking), Science, .
- 1 2 3 M. Saunois et al., « The Global Methane Budget 2000-2012 », Earth System Science Data, no 8, , p. 697–751 (DOI 10.5194/essd-8-697-2016, présentation en ligne, lire en ligne [PDF]).
- ↑ (en) M. Saunois, R.B. Jackson, P. Bousquet, B. Poulter et J.G. Canadell, The growing role of methane in anthropogenic climate change, 2016, Environmental Research Letters, vol. 11, 120207, DOI 10.1088/1748-9326/11/12/120207.
- ↑ « Gaz à effet de serre : d’où proviennent les émissions de méthane ? », sur connaissancedesenergies.org, (consulté le ).
- ↑ Nature, avril 2008.
- ↑ Gaz de schiste : des fuites de méthane plus importantes que prévu, Le Monde (consulté le 15 janvier 2014).
- ↑ (en) Jeff Tollefson, Air sampling reveals high emissions from gas field, Nature, 7 février 2012.
- ↑ (en) Robert W. Howarth, « Ideas and perspectives: is shale gas a major driver of recent increase in global atmospheric methane? », Biogeosciences, vol. 16, no 15, , p. 3033–3046 (ISSN 1726-4170, DOI https://doi.org/10.5194/bg-16-3033-2019, lire en ligne, consulté le )
- ↑ Valéry Laramée de Tannenberg, Le bilan carbone des gaz de schiste plus élevé que prévu, Journal de l'environnement, 13 avril 2011.
- ↑ Valéry Laramée de Tannenberg, Gaz de schiste: la fuite fatale, journaldelenvironnement.net, 17 février 2012
- ↑ Impact des gaz de schiste sur le climat : une étude de la NASA relance la controverse, Carbone4, 23 janvier 2018.
- ↑ (en) Global assessment of oil and gas methane ultra-emitters, Science, 3 février 2022.
- ↑ AFP, Les majors du pétrole s'engagent à réduire leurs émissions de méthane , connaissancedesenergies.org, 24 septembre 2018
- ↑ Daniel Sauvant, « La production de méthane dans la biosphère : le rôle des animaux d’élevage », Courrier de la Cellule Environnement de l'INRA, INRA, n° 18, 1992 (lire en ligne), 65-70
- ↑ « Élevage, gaz à effet de serre et stockage de carbone », sur INRA, (consulté le ).
- ↑ Dollé J.B. et Robin P., « Émissions de gaz à effet de serre en bâtiment d’élevage bovin », Fourrages, no 186, , p. 205-214 (présentation en ligne, lire en ligne [PDF]).
- ↑ Vermorel M., Jouany J.P., Eugène M., Sauvant D., Noblet J., Dourmad J.Y., « Évaluation quantitative des émissions de méthane entérique par les animaux d'élevage en 2007 en France », INRA Production Animale, 21, 2008, p. 403-418.
- ↑ CIVAM de Bretagne, Synthèse bibliographique 2010 – Plan d’action Agriculture Durable des CIVAM de Bretagne [PDF], 2010, 6 p.
- ↑ Focant M et al., Réduire les émissions de méthane et les rejets d’azote et améliorer la qualité nutritionnelle du lait par l’alimentation des vaches, Fourrages, n°232, 2017, p. 297-304.
- ↑ Martin C., Morgavi D., Doreau M., Jouany J.P., (2006) Comment réduire la production de méthane chez les ruminants ?, Fourrages, 187, p. 283-300
- ↑ Journal of Animal Science, 2007
- ↑ « En Nouvelle-Zélande, on élève des moutons qui pètent et rotent moins », sur huffingtonpost
- ↑ (en) « New Zealand scientists are breeding sheep to fart and burp less », sur abc.net.au
- ↑ G. Jarret, J. Martinez et J.Y. Dourmand, « Effet de l'ajout de sources de fibres dans l'aliment sur la volatilisation de l'ammoniac et la production de méthane des effluents porcins », 42es Journées de la Recherche Porcine, février 2010, Paris, France, p. 269-276 (lire en ligne).
- ↑ AFP. Des bus roulent déjà à Stockholm, et en essai à Oslo et Lille.
- ↑ (en) Weitemeyer K.A & Buffett B.A (2006) Accumulation and release of methane from clathrates below the Laurentide and Cordilleran ice sheets. Global Planet. Change 53, 176–187
- ↑ (en-GB) « Scientists shocked by Arctic permafrost thawing 70 years sooner than predicted », The Guardian, (ISSN 0261-3077, lire en ligne, consulté le ).
- ↑ Étude dirigée par Natalia Chakhova et Igor Semiletov, Université de l'Alaska de Fairbanks
- 1 2 3 TF1, rubrique Science/Environnement, mars 2010 (consulté le 29 avril 2010).
- ↑ Kirschke, S. et al. (2013) Three decades of global methane sources and sinks. Nat. Geosci. 6, 813–823 |url+https://pdfs.semanticscholar.org/5c95/55488862df46651f3e97a9cbbcb0bc0cdabf.pdf
- ↑ (en) H. Schaefer et al., A 21st century shift from fossil-fuel to biogenic methane emissions indicated by 13CH4. Science, 352, 2016, p.80–84 (liren en ligne).
- 1 2 (en) Wadham J.L, Tranter M, Tulaczyk S & Sharp M, Subglacial methanogenesis: a potential climatic amplifier?, Global Biogeochem. Cy., 22, 2008, GB2021| URL=https://agupubs.onlinelibrary.wiley.com/doi/full/10.1029/2007GB002951
- ↑ (en) E.L. Broemsen (2014, Evidence of methane cycling beneath the western margin of the Greenland Ice Sheet
- ↑ (en) Petrenko V.V et al. (2017) Minimal geological methane emissions during the Younger Dryas–Preboreal abrupt warming event, Nature, 548, 443–446 |URL=https://www.nature.com/articles/nature23316
- ↑ (en) Wadham J.L et al. (2012) Potential methane reservoirs beneath Antarctica. Nature 488, 633–637.
- ↑ (en) « Frontiers 2018/19: Emerging Issues of Environmental Concern », sur UN Environment (consulté le )
- ↑ « Methane Emissions in Arctic Cold Season Higher Than Expected », sur NASA/JPL (consulté le )
- ↑ (en) Maurice L, Rawlins B.G, Farr G, Bell R & Gooddy D.C (2017), The influence of flow and bed slope on gas transfer in steep streams and their implications for evasion of CO2, J. Geophys. Res. Biogeosci. 122, 2862–2875.
- ↑ (en) Hubbard, B., & Nienow, P., « Alpine subglacial hydrology », Quaternary Science Reviews, 16(9), 939-955.
- ↑ Piotrowski J.A. (1997) Subglacial hydrology in north-western Germany during the last glaciation: groundwater flow, tunnel valleys and hydrological cycles, Quaternary Science Reviews, 16(2), 169-185.
- ↑ (en) Dieser, M. et al. (2014). Molecular and biogeochemical evidence for methane cycling beneath the western margin of the Greenland Ice Sheet, ISME J., 8, 2305–2316
- ↑ (en) E.H. Stanley et al., « The ecology of methane in streams and rivers: patterns, controls, and global significance », Ecol. Monogr., 86, 2016, p. 146–171.
- ↑ Vincent Nouyrigat, « Espionnage climatique. La traque aux émissions clandestine est lancée », Epsiloon, , p. 21.
- ↑ 26 octobre Climat : une mission de la Nasa aide à détecter les « super-émetteurs » de méthane depuis l'espace, Les Échos, 2022.
- 1 2 3 (en) Paul Voosen, « Scientists flag new causes for surge in methane levels », Science, 23 décembre 2016, vol. 354, n° 6319, p. 1513 (DOI: 10.1126/science.354.6319.1513).
- ↑ « La tendance à la hausse se poursuit: les concentrations de gaz à effet de serre dans l’atmosphère ont atteint de nouveaux sommets en 2018 », sur Organisation météorologique mondiale, (consulté le )
- ↑ Forestopic (2017) Piège à CO2, la forêt renferme aussi un puits de méthane dans ses sols !, publié 12 avril 2017.
- ↑ Bastviken, D., Ejlertsson, J., Sundh, I. et Tranvik, L. (2003), Methane as a source of carbon and energy for lake pelagic food webs, Ecology, 84(4), 969-981 (résumé).
- ↑ Roger I. Jones, Clare E. Carter, Andrew Kelly, Susan Ward, David J. Kelly, Jonathan Grey (2008), Widespread contribution of methane-cycle bacteria to the diets of lake profundal chironomid larvae, Ecology, vol. 89, no 3, mars 2008, p. 857-864, DOI https://dx.doi.org/10.1890/06-2010.1 (résumé)
- ↑ (en) Jenkins, Michael B. ; Lion, Leonard W., Mobile bacteria and transport of polynuclear aromatic hydrocarbons in porous media, Applied and Environmental Microbiology, octobre 1993, 59 (10):3306-3313 (ISSN 0099-2240) (résumé et lien)
- ↑ Jenkins MB, Chen JH, Kadner DJ, Lion LW., Methanotrophic Bacteria and Facilitated Transport of Pollutants in Aquifer Material, Applied and Environmental Microbiology, octobre 1994, 60(10)3491-3498
- ↑ Évolution de la concentration de méthane dans l'atmosphère
- ↑ Réactivité du méthane et de l'ozone en haute atmosphère
- ↑ Inversion des sources et puits de gaz dans l'atmosphère, Laboratoire des sciences du climat et de l'environnement.
- ↑ (en) Charles Giordano, Top-down and bottom-up landfill methane emissions estimates : a comparative study of the European Union and the United States (thèse de maîtrise universitaire en sciences), Université d'Europe centrale, , vii + 109 (lire en ligne [PDF]), « Introduction », p. 1.
- 1 2 3 4 Frank Niedercorn, « Des pistes contre les émissions de méthane », Les Échos, (lire en ligne).
- ↑ Paul Hawken (trad. Amanda Prat-Giral), Drawdown : Comment inverser le cours du réchauffement planétaire, Actes Sud, , 580 p. (ISBN 978-2-330-09613-7)
- 1 2 Christian de Perthuis, « Attention méthane ! », sur connaissancedesenergies.org,
- ↑ Derek Perrotte, L'Europe veut réduire les émissions de méthane, Les Échos, 14 octobre 2020.
- ↑ Environnement : l'Europe déclare la guerre au méthane, Les Échos, 15 décembre 2021.
- ↑ COP26 : États-Unis et UE embarquent 80 pays pour s'attaquer aux rejets de méthane, Les Échos, 2 novembre 2021.
- 1 2 3 Heng Rao, Luciana C. Schmidt, Julien Bonin et Marc Robert, « Visible-light-driven methane formation from CO2 with a molecular iron catalyst », Nature, vol. 548, , p. 74–77 (DOI 10.1038/nature23016, résumé).
- ↑ (en) Jhong, H.-R. M., Ma, S. & Kenis, P. J. A. (2013), Electrochemical conversion of CO2 to useful chemicals: current status, remaining challenges, and future opportunities ; Curr. Opin. Chem. Eng. 2, 191–199
- ↑ (en) Aresta, M., Dibenedetto, A. & Angelini, A. (2014) Catalysis for the valorization of exhaust carbon: from CO2 to chemicals, materials, and fuels. Technological use of CO2. Chem. Rev. 114, 1709–1742
- ↑ Parajuli, R. et al. (2015), Integration of anodic and cathodic catalysts of Earth-abundant materials for efficient, scalable CO2 reduction. Top. Catal. 58, 57–66
- ↑ Sahara, G. & Ishitani, O. (2015) Efficient photocatalysts for CO2 reduction. Inorg. Chem. 54, 5096–5104
- ↑ Takeda, H., Cometto, C., Ishitani, O. & Robert, M. (2017), Electrons, photons, protons and Earth-abundant metal complexes for molecular catalysis of CO2 reduction. ACS Catal. 7, 70–88
- ↑ Shen, J. et al. (2015) Electrocatalytic reduction of carbon dioxide to carbon monoxide and methane at an immobilized cobalt protoporphyrin. Nat. Commun. 6, 8177
- ↑ Weng, Z. et al. (2016), Electrochemical CO2 reduction to hydrocarbons on a heterogeneous molecular Cu catalyst in aqueous solution. J. Am. Chem. Soc. 138, 8076–8079
- ↑ Manthiram, K., Beberwyck, B. J. & Alivisatos, A. P. Enhanced electrochemical methanation of carbon dioxide with a dispersible nanoscale copper catalyst. J. Am. Chem. Soc. 136, 13319–13325 (2014)
- ↑ Wu, T. et al. (2014), A carbon-based photocatalyst efficiently converts CO2 to CH4 and C2H2 under visible light. Green Chem. 16, 2142–2146
- ↑ AlOtaibi, B., Fan, S., Wang, D., Ye, J. & Mi, Z. (2015), Wafer-level artificial photosynthesis for CO2 reduction into CH4 and CO using GaN nanowires. ACS Catal. 5, 5342–5348
- ↑ Liu, X., Inagaki, S. & Gong, J. (2016), Heterogeneous molecular systems for photocatalytic CO2 reduction with water oxidation. Angew. Chem. Int. Ed. 55, 14924–14950
- ↑ Wang, Y. et al. (2016), Facile one-step synthesis of hybrid graphitic carbon nitride and carbon composites as high-performance catalysts for CO2 photocatalytic conversion. ACS Appl. Mater. Interf. 8, 17212–17219
- ↑ Zhu, S. et al. (2016) Photocatalytic reduction of CO2 with H2O to CH4 over ultrathin SnNb2O6 2D nanosheets under visible light irradiation. Green Chem. 18, 1355–1363
- ↑ Azcarate, I., Costentin, C., Robert, M. & Savéant, J.-M. (2016), A study of through-space charge interaction substituent effects in molecular catalysis leading to the design of the most efficient catalyst of CO2-to-CO electrochemical conversion. J. Am. Chem. Soc. 138, 16639–16644
- ↑ Bonin, J., Maurin, A. & Robert, M. Molecular catalysis of the electrochemical and photochemical reduction of CO2 with Fe and Co metal based complexes. Recent advances. Coord. Chem. Rev. 334, 184–198 (2017)
- ↑ Costentin, C., Robert, M., Savéant, J.-M. & Tatin, A. (2015), Efficient and selective molecular catalyst for the CO2-to-CO electrochemical conversion in water. Proc. Natl Acad. Sci. USA 112, 6882–6886
- 1 2 3 4 Simon J. Moore, Sven T. Sowa, Christopher Schuchardt, Evelyne Deery, Andrew D. Lawrence et al. (2017), Elucidation of the biosynthesis of the methane catalyst coenzyme F430, Nature, mis en ligne le 22 février 2017, DOI 10.1038/nature21427 (résumé)
- ↑ Tadhg P. Begley (2017), Biochemistry: Origin of a key player in methane biosynthesis ; mis en ligne le 22 février 2017 ; DOI 10.1038/nature21507, Nature ; (résumé)
- ↑ Xie, S. L., Liu, J., Dong, L. Z., Li, S. L., Lan, Y. Q., & Su, Z. M. (2019). Hetero-metallic active sites coupled with strongly reductive polyoxometalate for selective photocatalytic CO 2-to-CH 4 conversion in water. Chemical Science, 10(1), 185-190.
- ↑ Steinlechner, C., & Junge, H. (2018) Renewable Methane Generation from Carbon Dioxide and Sunlight. Angewandte Chemie International Edition, 57(1), 44-45.
- ↑ Fukuzumi, S., Lee, Y. M., Ahn, H. S., & Nam, W. (2018) Mechanisms of catalytic reduction of CO 2 with heme and nonheme metal complexes. Chemical science, 9(28), 6017-6034.
- ↑ Di, J., Zhu, C., Ji, M., Duan, M., Long, R., Yan, C.... & Li, H. (2018). Defect‐Rich Bi12O17Cl2 Nanotubes Self‐Accelerating Charge Separation for Boosting Photocatalytic CO2 Reduction. Angewandte Chemie, 130(45), 15063-15067.
- ↑ Lodh, J., Mallick, A., & Roy, S. (2018). Light-driven carbon dioxide reduction coupled with conversion of acetylenic group to ketone by a functional Janus catalyst based on keplerate {Mo 132}. Journal of Materials Chemistry A, 6(42), 20844-20851. (résumé).
- ↑ Guillaume Dera, Le rôle des changements paléoclimatiques sur l'évolution de la biodiversité au Pliensbachien et au Toarcien (thèse de doctorat en géologie), Dijon, (SUDOC 150641303, présentation en ligne).
- ↑ (en) J.L. Kirschvink et T.D. Raub, « A methane fuse for the Cambrian explosion: carbon cycles and true polar wander », Comptes Rendus Geoscience, 335(1), 2003 (lire en ligne), p. 65-78.
- ↑ (en) Austen, M.C., Warwick, R.M. et Ryan, K.P. (1993), « Astomonema southwardorum sp. nov., a gutless nematode dominant in a methane seep area in the North Sea », Journal of the Marine Biological Association of the United Kingdom, 73(03), p. 627-634.
- ↑ P. Viens, Étude de la biodiversite de la communaute microbienne d'un biofiltre traitant le methane en fonction de différentes concentrations d'ammonium, 111 p. [PDF], in Masters Abstracts International, vol. 49, n°4, 2010.
- ↑ (en) Hannah M. Roberts et Alan M. Shiller, « Determination of dissolved methane in natural waters using headspace analysis with cavity ring-down spectroscopy », Analytica Chimica Acta, vol. 856, , p. 68–73 (DOI 10.1016/j.aca.2014.10.058, lire en ligne, consulté le )
Voir aussi
Bibliographie
- Benjamin Dessus, « Effet de serre : on oublie le méthane », in Alternative Économique, 2010/4, no 290, 128 p.
- (en) Wunch, D., Jones, D. B. A., Toon, G. C., Deutscher, N. M., Hase, F., Notholt, J., Sussmann, R., Warneke, T., Kuenen, J., Denier van der Gon, H., Fisher, J. A. et Maasakkers, J. D., « Emissions of methane in Europe inferred by total column measurements », Atmos. Chem. Phys., 19, 2019, 3963-3980, doi:10.5194/acp-19-3963-2019, 2019.
Articles connexes
- Émissions de méthane des zones humides
- Reformage du méthane
- Gaz à effet de serre
- Changement climatique
- Pyrolyse
- Gazogène
- Environnement
- Hydrate de méthane
- Relargage du méthane de l'Arctique
- Méthanisation
- Métabolisme méthanogène (espèce produisant du méthane)
- Méthanotrophe (espèce se nourrissant de méthane)
Liens externes
- Ressources relatives à la santé :
- Notices dans des dictionnaires ou encyclopédies généralistes :
- « Méthane, ho la vache ! », La Méthode scientifique, France Culture, 23 février 2022.

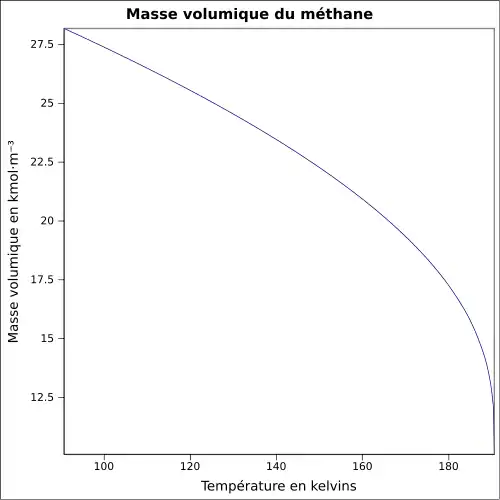

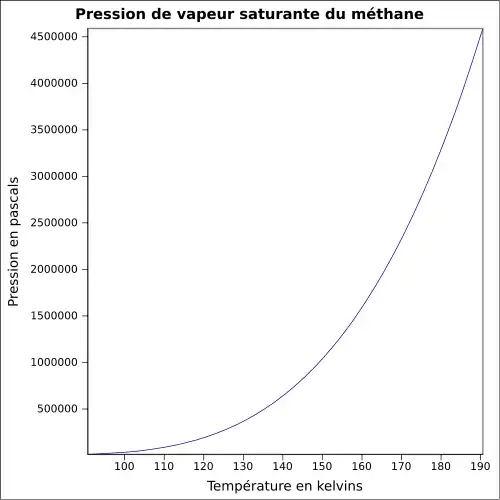





.jpg.webp)