مرض آلزهايمر (اختصارًا آلزهايمر) هو مرضٌ تحلليٌ عصبيٌ مزمنٌ، عادةً ما يبدأ بطيئًا ويُصبح أسوءًا تدريجيًا مع مرور الوقت.[1][4] يُعتبر سببًا لحوالي 60-70% من حالاتِ الخَرَف.[1][4] يبدأ عادةً بحدوث صعوبةٍ في تذكر الأحداث الأخيرة،[1] ومع تقدم المرض، تظهرُ أعراضٌ تتضمن مشاكلًا في اللغة، وتَوَهانًا (يشملُ الضَياع بسهولة)، وتقلباتٍ في المزاج، وضعفًا في الدافِع، عدم القُدرة على العناية بالنفس، ومشاكلًا سلوكية.[1][4] مع ازدياد سوء حالة الشخص، فإنهُ غالبًا ما ينسحبُ من بيئة الأسرة والمجتمع.[1] وتدريجيًا، يفقدُ الشخص وظائفه الجسمية، مما يؤدي في النهاية إلى الوفاة.[10] تختلفُ سرعة تقدم المرض من حالةٍ لأخرى، ولكن على الرغم من هذا، إلا أنَّ متوسط العُمر المتوقع بعد التشخيص يتراوح بين 3-9 سنوات.[6][11]
| مرض آلزهايمر | |
|---|---|
| Alzheimer's disease | |
مقارنةٌ بين دماغٍ سليم في مرحلة الشيخوخة (اليسار) ودماغٍ لشخصٍ مصابٍ بآلزهايمر (اليمين). تظهرُ الفروقات بين الدماغين على الصُورة.
| |
| النطق | altshʌɪməz |
| معلومات عامة | |
| الاختصاص | طب الجهاز العصبي |
| الأسباب | |
| الأسباب | غير مفهومةٍ بوضوح[1] |
| عوامل الخطر | الوراثة، وإصابات الرأس، والاكتئاب، وارتفاع ضغط الدم[1][2] |
| المظهر السريري | |
| البداية المعتادة | فوق سِن 65 عامًا[3] |
| الأعراض | صعوبةٌ في تذكر الأحداث القريبة، ومشاكلٌ في اللغة، وتَوَهانٌ، وتقلبات مزاجية[1][4] |
| المدة | طويل الأمد[4] |
| الإدارة | |
| التشخيص | يعتمدُ على الأعراض والاختبارات المعرفية، وذلك بعد استبعاد الأسباب المُحتملة الأخرى[5] |
| أدوية | |
| المآل | متوسط العمر المتوقع 3-9 سنوات[6] |
| حالات مشابهة | الشيخوخة الطبيعية[1] |
| الوبائيات | |
| انتشار المرض | 29.8 مليون (2015)[4][8] |
| الوفيات | 1.9 مليون (2015)[9] |
| التاريخ | |
| سُمي باسم | ألويس ألزهايمر |
سببُ حدوث مرض آلزهايمر غير مفهومٍ جيدًا.[1] يُعتقدُ أنَّ حوالي 70% من خطر الحدوث مرتبطٌ بوراثة المرض من والدي الشخص مع كثيرٍ من الجينات المُتأثرة.[2] تتضمن عوامل الخطر وجود تاريخٍ لإصابات الرأس والاكتئاب وارتفاع ضغط الدم.[1] ترتبطُ آلية المرض باللويحات والتشابكات اللييفية العصبية في الدماغ.[2] يعتمدُ توقع التشخيص على تاريخ المرض والاختبارات المعرفية (الإدراكية) مع تصويرٍ طبي وتحاليل الدم؛ وذلك بهدف استبعاد الأسباب المحتملة الأخرى.[5] غالبًا ما يُخلط بين الأعراض الأولية لمرض آلزهايمر مع الشيخوخة الطبيعية.[1] يجب إجراء فحصٍ لنسيج الدماغ لتأكيد التشخيص النهائي.[2] قد تُساعد التدريبات البدنية والعقلية وتجنب السُمنة على تقليل خطر الإصابة بمرض آلزهايمر، ولكن الأدلة التي تدعم هذه التوصيات ضعيفة.[2][12] لا تُوجد أدوية أو مُكملات تُقلل من خطر حدوث آلزهايمر.[13]
لا تُوجد علاجات تُوقف أو تعكس تقدم مرض آلزهايمر، ولكن بعض العلاجات قد تُحسن الأعراض مؤقتًا.[4] يزدادُ مع الوقت اعتمادُ مرضى آلزهايمر على الآخرين في مساعدتهم، وغالبًا ما يضعون عبئًا على مُقدمي الرعاية،[14] وقد يكون العبء اجتماعيًا أو نفسيًا أو جسديًا أو حتى اقتصاديًا.[14] قد تكون برامج التمرين مفيدةً فيما يتعلق بأنشطة الحياة اليومية وقد تُساعد في تحسين النتائج.[15] عادة ما تُعالج المشاكل السلوكية أو الذهان الناجم عن الخرف باستعمال مضادات الذهان، ولكن عادةً لا يُنصح باستعمالها، حيث لا تُوجد فائدةٌ كبيرة من استعمالها مع زيادة خطر الوفاة المبكرة.[16][17]
كان هناك حوالي 29.8 مليون شخصٍ مُصابين بآلزهايمر في جميع أنحاء العالم عام 2015.[4][8] عادةً ما يبدأ المرض في الأشخاص الذين تزيد أعمارهم عن 65 عامًا، وذلك على الرغم من أن 4-5% من الحالات مبكرة الحدوث.[3] يُصيب آلزهايمر حوالي 6% من الأشخاص الذين تزيد أعمارهم عن 65 عامًا.[1] أدى الخرف إلى وفاة حوالي 1.9 مليون شخص في عام 2015.[9] وُصف مرض آلزهايمر لأول مرة بواسطة عالم الأمراض والطبيب النفسي الألماني ألويس آلزهايمر في عام 1906، وتمت تسميته فيما بعد.[18] يعد مرض آلزهايمر واحدًا من أكثر الأمراض كلفةً ماليةً في الدول المتقدمة.[19][20]
العلامات والأعراض
- آثار الشيخوخة على الذاكرة وليس مرض آلزهايمر
- نسيان الأشياء أحيانًا
- وضع الأشياء في غير مكانها أحيانًا
- فقدانٌ طفيف في الذاكرة قصيرة الأمد
- عدم تذكر التفاصيل الدقيقة
- المرحلة المُبكرة لمرض آلزهايمر
- عدم تذكر نوبات النسيان
- نسيان أسماء أفراد العائلة أو الأصدقاء
- يُمكن للأصدقاء أو الأقارب فقط ملاحظةُ التغييرات
- ارتباكٌ بسيط في بعض المواقف غير المألوفة
- المرحلة المتوسطة لمرض آلزهايمر
- صعوبةٌ أكبر في تذكر المعلومات التي تعلمها مؤخرًا
- تعمُق الارتباك في العديد من المواقف
- مشاكلٌ في النوم
- مشكلةٌ في تحديد الموقع
- المرحلة المتأخرة لمرض آلزهايمر
- ضعفُ القدرة على التفكير
- مشاكلٌ في التحدث
- تكرار نفس المُحادثات
- يكون أكثر إساءةً أو قلقًا أو زَوَرانًا(1)
ينقسم مسارُ المرض إلى أربع مراحل، مع نمطٍ تدريجي للضعف المعرفي والوظيفي.
مرحلة ما قبل الخرف
تُنسب الأعراضُ الأولية للمرض بشكلٍ خاطئٍ غالبًا إلى الشيخوخة أو الضغط النفسي.[22] قد تُساعد الفحوصات النفسية العصبية المُفصلة في الكشف عن صعوباتٍ إدراكيةٍ طفيفةٍ قد تصل إلى ثماني سنواتٍ قبل ظهور الأعراض السريرية المعيارية لتشخيص مرض آلزهايمر.[23] قد تؤثر الأعراض الأولية على أنشطة الحياة اليومية الأكثر تعقيدًا.[24] يُعتبر فقدان الذاكرة قصيرة الأمد أبرز عجزٍ يحدثه آلزهايمر، حيثُ يظهرُ كصعوبةٍ في تذكر المعلومات والحقائق التي تعلمها الفرد مؤخرًا، مع عدم القدرة على اكتساب معلوماتٍ جديدة.[23][25]
قد تظهرُ أعراضٌ أوليةٌ أُخرى لمرض آلزهايمر، وتتمثل بمشكلاتٍ دقيقةٍ في الوظائف التنفيذية للانتباه والتخطيط والمرونة والتفكير التجريدي أو بضعفٍ في الذاكرة الدلالية (ذاكرة المعاني والعلاقات بين المفاهيم).[23] يُمكن ملاحظة حدوث لامبالاةٍ لدى الفرد في هذه المرحلة من مسار المرض، وتُعتبر اللامبالاة أكثر الأعراض العصبية النفسية استمرارًا طوال مسار مرض آلزهايمر.[26] يشيعُ أيضًا حدوث أعراضٍ اكتئابية، بالإضافة لتهيجٍ وانخفاض الوعي بصعوبات الذاكرة الدقيقة.[27]
تُسمى هذه المرحلة أيضًا بالخلل الإدراكي البسيط (MCI)،[25] وهي المرحلة التي تسبقُ ظهور الأعراض السريرية، وغالبًا ما تكون مرحلةً انتقالية من الشيخوخة الطبيعية إلى الخرف. قد تظهرُ أعراضٌ متنوعةٌ مع الخلل الإدراكي البسيط، وعندما يُصبح فقدان الذاكرة عرضًا سائدًا، فإنَّ المرحلة تُسمى بالخلل الإدراكي البسيط النسياني (Amnestic MCI)، وغالبًا ما يُنظر إليها على أنها مرحلةٌ بادرية (أولية) لمرض آلزهايمر.[28]
المرحلة المبكرة
يؤدي الضعفُ المُتزايد في التعلم والذاكرة لدى الأشخاص المُصابين بآلزهايمر في الوصول إلى تشخيصٍ نهائيٍ لحالتهم. في نسبةٍ صغيرةٍ من المرضى، تكون الصعوبات في التعلم والوظائف الإدراكية والإدراك الحسي (العمه) أو الصعوبات في تنفيذ الحركات (العمه الحركي) أكثر وضوحًا من مشاكل الذاكرة.[29] لا يؤثر آلزهايمر بالتساوي على جميع قدرات الذاكرة، حيث تتأثر الذكريات القديمة لحياة الشخص (الذاكرة العرضية) والمعلومات التي تعلمها الشخص (الذاكرة الدلالية) والذاكرة الضمنية (ذاكرة الجسم حول كيفية القيام بالأشياء، مثل استخدام الشوكة للأكل أو كيفية الشرب من الكوب) بدرجةٍ أقل من الذكريات والحقائق والمعلومات الحديثة.[30][31]
تتميز المشاكل اللغوية أساسيًا بتقلصٍ في المفردات وانخفاضٍ في طلاقة الكلمات، مما يؤدي لفقرٍ عامٍ في اللغة المكتوبة والمنطوقة.[29][32] يكون الشخص المُصاب بمرض آلزهايمر في هذه المرحلة قادرًا على إيصال الأفكار الأساسية بشكلٍ كافٍ.[29][32][33] قد تظهر صعوباتٍ في التنسيق والتخطيط (قصورٍ في الأداء) أثناء أداء المهام الحركية الدقيقة مثل الكتابة والرسم وارتداء الملابس، ولكنها عادةً تكون غير واضحةٍ.[29] مع تقدم مرض آلزهايمر، قد يستمرُ الأشخاص الذين يعانون من المرض في أداء العديد من المهام بشكلٍ مُستقل، ولكن قد يحتاجون إلى مساعدةٍ أو إشرافٍ في كثيرٍ من الأنشطة التي تحتاجُ إلى إدراكٍ معرفي.[29]
المرحلة المتوسطة
يؤدي التدهور التدريجي المُستمر في المرض إلى عرقلة استقلالية الأفراد، حيثُ يُصبح الأفراد غيرُ قادرين على أداء أنشطة الحياة اليومية الشائعة.[29] كما تُصبح صعوبات النطق أكثر وضوحًا في هذه المرحلة؛ وذلك بسبب عدم القدرة على تذكر المفردات، مما يؤدي إلى استبدال خاطئٍ متكررٍ للكلمات (خطل التسمية). تُفقدُ أيضًا مهارات القراءة والكتابة تدريجيًا،[29][33] وتُصبح التسلسلات الحركية المُعقدة أقل تنسيقًا مع مرور الوقت وتقدم المرض، مما يزيدُ من خطر السقوط.[29] خلال هذه المرحلة، تزداد مشاكل الذاكرة سوءًا، وقد يفشل الشخص في التعرف على الأقارب.[29] أما الذاكرة طويلة الأمد والتي كانت سليمةً سابقًا، فإنها تُصبح ضعيفةً في هذه المرحلة.[29]
تسُودُ التغيرات السلوكية والنفسية العصبية في هذه المرحلة، ومن المظاهر الشائعة التجول والتهيج والتقلقل، مما يؤدي إلى بكاء الشخص، وإظهار عدوانيةٍ غيرُ متعمدةٍ أو مقاومة تقديم الرعاية.[29] قد تحدث أيضًا متلازمة الغروب (اختلاط عقلي عند المغرب).[34] قد يظهر في حوالي 30% من الأفراد المُصابين بمرض آلزهايمر أخطاءٌ وهمية في التعرف وأعراضٌ وهامية أُخرى.[29] يفقدُ المرضى أيضًا بصيرتهم حول آثار وقيود مرضهم فيما يُعرف بعمه المرض.[29] كما قد يحدثُ تبولٌ لاإرادي.[29] تُسبب هذه الأعراض ضغطًا نفسيًا على الأقارب ومُقدمي الرعاية، ويُمكن تقليل الضغط عبر نقل المريض من العناية المنزلية إلى مرافقِ رعايةٍ طويلة الأمد.[29][35]
المرحلة المتقدمة
يعتمدُ المريض تمامًا على مقدمي الرعاية في المراحل النهائية للمرض.[29] حيثُ ينخفضُ النطق إلى عباراتٍ بسيطةٍ أو كلماتٍ مفردةٍ فقط، مما يؤدي في النهاية إلى فقدانٍ كاملٍ للنطق.[29][33] ولكن على الرغم من فقدان القدرات اللغوية اللفظية، إلا أنهُ عادةً يُمكن للمرضى فهمُ الإشارات العاطفية والتفاعل معها.[29] وأيضًا على الرغم من استمرار عدوانية الشخص، إلا أنَّ اللامبالاة والإرهاق الشديد يُعتبران من الأعراض الشائعة.[29] في هذه المرحلة، يُصبح الأشخاص المصابون بآلزهايمر غير قادرين على أداء أبسط المهامٍ بشكلٍ مُستقل، حيثُ تتدهور الكتلة العضلية وقدرتهم على التنقل إلى حدٍ يجعلهم مُلازمي الفراش وغيرُ قادرين على إطعام أنفسهم.[29] عادة ما يكون سببُ الوفاة عاملاً خارجيًا (مثل الإصابة بقرحة الفراش أو التهابٍ رئوي) وليس مرض آلزهايمر نفسه.[29]
الأسباب
لا يزال سببُ معظم حالات آلزهايمر مجهولًا غالبًا، باستثناء 1-5% من الحالات وحُددت فيها الاختلافات الجينية.[36][37] تُوجد العديد من الفرضيات المُتنافسة في محاولة تفسير سبب المرض.
جينيًا
تتراوح نسبة الانتقال الوراثي الجيني لمرض آلزهايمر (ومشاكل الذاكرة المُتعلقة به) ما بين 49-79%، وقد وُضعت اعتمادًا على مراجعاتٍ لدراساتٍ أُجريت على عدة توائم وعائلات.[38] حوالي 0.1% من الحالات تكون أشكالًا عائلية تتبع نمط الوراثة الجسمية (ليست مرتبطة بالجنس) السائدة، والتي تظهر قبل سن 65 عامًا.[39] يُسمى هذا الشكل من المرض باسم مرض آلزهايمر العائلي مُبكر البدء. تُعزى معظم حالات آلزهايمر العائلي الجسمي السائد إلى طفراتٍ في واحدٍ من ثلاث جيناتٍ: التي تُشفر البروتين المنتج للمادة النشوانية (APP)، والبريسنلينات 1 و2.[40] تؤدي معظم هذه الطفرات إلى زيادة إنتاج بروتينٍ صغيرٍ يُسمى Aβ42 (ببتيد بيتا النشواني المُكون من 42 حمضًا أمينيًا)، والذي يُعتبر المكون الرئيسي لِلويحات الشيخوخية.[41] تؤدي بعض الطفرات فقط إلى تغيير النسبة بين Aβ42 والأشكال الأُخرى (خصوصًا Aβ40) دون زيادة مستويات Aβ42.[42] يُوجد جينين آخرين يرتبطان بمرض آلزهايمر الجسمي السائد، وهما ABCA7 وSORL1.[43]
لا تُظهر مُعظم حالات آلزهايمر نمط الوراثة الجسمي السائد، وتُسمى مرض آلزهايمر الفرادي (مرض آلزهايمر الذي يظهر كحالاتٍ فرديةٍ مُتفرقة)، حيثُ قد تلعبُ الاختلافات البيئية والجينية دورًا كعوامل خطر. أَشهر عامل خطر وراثي مَعروف هو وراثة أليل APOEε4 (أليل ε4 لصميم البروتين الشحمي E (APOE)).[44][45] يُوجد بين 40-80% من مرضى آلزهايمر يحملون أليل APOEε4 واحدًا على الأقل.[45] يؤدي هذا الأليل إلى زيادة خطر المرض ثلاث مرات في الحالات مُتغايرة الزيجوت و15 مرة في الحالات مُتماثلة الزيجوت.[39] تؤدي الآثار البيئية والمُعدِلات الجينية إلى نفوذيةٍ غير كاملةٍ، ويحدثُ هذا في العديد من الأمراض البشرية. مثلًا، لا يُظهر بعض السكان النيجيريين أي علاقةٍ بين مقدار APOEε4 والإصابة أو عمر الإصابة بمرض آلزهايمر الموجود عند مجموعاتٍ بشريةٍ أُخرى.[46][47] أجُريت محاولاتٌ مُبكرةٌ لفحص حوالي 400 جينٍ مُتوقعٌ ارتباطها مع مرض آلزهايمر الفرادي متأخر البدء (LOAD)، ولكن كانت نتائج هذه المُحاولات مُنخفضة.[39][40] أظهرت دراسةٌ حديثة للترابط الجينومي الكامل وجود 14 منطقةٍ في الجينات يبدو أنها تُؤثر على خطر حدوث آلزهايمر.[48] هذه الجينات تتضمن: CASS4، وCELF1، وFERMT2، وHLA-DRB5، وINPP5D، وMEF2C، وNME8، وPTK2B، وSORL1، وZCWPW1، وSlC24A4، وCLU، وPICALM، وCR1، وBIN1، وMS4A، وABCA7، وEPHA1، وCD2AP.[48]
ترتبط أليلات الجين TREM2 بزيادة خطر الإصابة بمرض آلزهايمر بحوالي 3 إلى 5 مرات.[49][50] تذكرُ آلية العمل المقترحة أنَّ متغيراتٍ في جين TREM2 تجعل خلايا الدم البيضاء في الدماغ غير قادرةٍ على التحكم في كميات ببتيد بيتا النشواني (Aβ) الموجودة. ترتبط العديد من تعددات أشكال النوكليوتيدات المفردة مع مرض آلزهايمر، حيثُ عملت دراسةٌ في عام 2018 على إضافة 30 تعددًا عبر تمييز مرض آلزهايمر إلى 6 تصنيفاتٍ، تتضمن وظائف الذاكرة واللغة والوظائف البصرية المكانية والوظائف التنفيذية.[51]
الفرضية الكولينية
تُعتبر الفرضية الكولينية أقدم الفرضيات، وتعتمدُ عليها مُعظم العلاجات الدوائية المُتاحة حاليًا.[52] تقترحُ هذه الرضية أنَّ مرض آلزهايمر ناجمٌ عن انخفاضِ اصطناع الناقل العصبي أسيتيل كولين. لم تستطع الفرضية الكولينية أن تُحافظ على دعمٍ كبير، حيثُ أنَّ العديد من الأدوية التي تهدف إلى علاج نقص الأسيتيل كولين لم تكن فعالةً كفايةً.[53]
الفرضية النشوانية
طُرحت الفرضية النَشَوَانِيّة في عام 1991، حيثُ افترضت أنَّ ترسبات ببتيد بيتا النشواني (Aβ) خارج الخلية هي السبب الأساسي لمرض آلزهايمر.[54][55] دُعمت هذه الفرضية عبر موقع جين البروتين المنتج للمادة النشوانية (APP) على الكروموسوم 21، مع حقيقةِ أنَّ الأشخاص المُصابين بتثلث الكروموسوم 21 (متلازمة داون) لديهم نسخةٌ جينية إضافية تُظهر عمومًا الأعراض المُبكرة لمرض آلزهايمر على الأقل عند سن 40 عامًا.[56][57] يُعتبر APOE4 (نظيرٌ خاص من صميم البروتين الشحمي) واحدًا من عوامل الخطر الجينية لمرض آلزهايمر، حيثُ تُعزز صميمات البروتين الشحمي من تكسير ببتيد بيتا النشواني، ولكن بعض النظائر غيرُ فعالةٍ كثيرًا في هذه المهمة (مثل APOE4)، مما يؤدي لتراكمٍ ببتيد بيتا النشواني الزائد في الدماغ.[58] وُجدت أدلةٌ إضافية أيضًا من تجارب الفئران المُعدلة وراثيًا، حيثُ أظهرت شكلًا مُتطفرًا من جين البروتين المنتج للمادة النشوانية البشري، والذي أدى لظهور لويحاتٍ نشوانية لييفية ومرضٍ دماغيٍ يُشبه آلزهايمر مع عجزٍ في التعلم المكاني.[59]
وُجدَ لقاحٌ تجريبي لإزالة اللويحات النشوانية في التجارب البشرية المُبكرة، ولكنه لا يُظهر أي تأثيرٍ كبيرٍ على الخرف.[60] اعتقد الباحثون أنَّ قليلات قسيمات بيتا النشوانية غير اللويحية هي الشكل الأساسي من ببتيد بيتا النشواني المُسبب للمرض. يُشار إلى هذه القُسيمات السامة باسم الربيطات القابلة للانتشار المُشتقة من النشواني (ADDLs)، حيثُ ترتبط بمستقبلٍ سطحي على العصبونات، وتغيرُ من بنية التشابك العصبي، وبالتالي تُعطل التواصل العصبي.[61] قد يكونُ بروتين البريون واحدًا من مُستقبلات قليلات قسيمات بيتا النشوانية، وهو نفس البروتين المُرتبط بمرض جنون البقر والحالات البشرية المُتعلقة به ومنها مرض كروتزفيلد جاكوب، لذلك يُحتمل وجود ترابطٍ في الآلية الكامنة وراء هذه الاضطرابات الانحلالية العصبية مع مرض آلزهايمر.[62]
حُدثت هذه النظرية في عام 2009، حيثُ اقتُرحَ وجود علاقةٍ قريبةٍ لبروتين بيتا النشواني، وليس شرطًا أن يكون ببتيد بيتا النشواني نفسه، وقد يكون السبب الرئيسي للمرض. تُوضح النظرية أنَّ الآلية المرتبطة بالنشواني والتي تقصِّر الروابط العصبية في الدماغ في مرحلة التطور السريع للحياة المبكرة قد تحدثُ عبر بعض العمليات المرتبطة بالشيخوخة في الحياة اللاحقة مُسببةً الذبول العصبي لمرض آلزهايمر.[63] تكون النهاية الأمينية للبروتين المنتج للمادة النشوانية (N-APP) قريبةً من ببتيد بيتا النشواني، حيثُ تُشَق من البروتين المنتج للمادة النشوانية عبر واحدٍ من نفس الإنزيمات. تُحفز هذه النهاية الأمينية مسارًا ذاتيُ التدمير عبر الارتباط بمستقبلٍ عصبيٍ يُسمى مُستقبل الموت 6 (DR6، ويعرف أيضًا باسم TNFRSF21).[63] يتواجد مُستقبل الموت 6 بكثرةٍ في مناطق الدماغ البشري المُتأثرة بمرض آلزهايمر، وبالتالي يُحتمل أنَّ مسار النهاية الأمينية/مستقبل الموت 6 (N-APP/DR6) قد يكون مسيطرًا عليه في الدماغ الشيخوخي لإحداث الضرر. يُظهر هذا النموذج أنَّ ببتيد بيتا النشواني يلعبُ دورًا مكملًا عبر تخفيض وظيفة التشابك العصبي.
فرضية تاو
تقترحُ فرضية تاو أنَّ تشوهاتِ بروتين تاو تؤدي لبدء حدوث تسلسل مرض آلزهايمر.[55] يقترح هذا النموذج أنَّ بروتين تاو المُفسفر بإفراطٍ يبدأ بالارتباط مع بروتينات تاو الأُخرى، حيثُ تُشكل في النهاية تشابكاتٍ لييفية عصبية داخل أجسام الخلايا العصبية.[64] عندما يحدث هذا، فإنَّ الأنيبيبات الدقيقة تَتفكك، وتدمر بنية الهيكل الخلوي للخلية والذي يؤدي لانهيار نظام نقل الخلايا العصبية.[65] قد يؤدي هذا بدايةً إلى حدوثِ خللٍ وظيفيٍ في التواصل الكيميائي الحيوي بين الخلايا العصبية، ولاحقًا إلى موت الخلايا.[66]
فرضيات أخرى
تقترحُ الفرضية الالتهابية أنَّ مرض آلزهايمر يحدثُ بسبب التهابٍ متزايدٍ ذاتي الديمومة في الدماغ، ويبلغُ ذروتهُ بحدوث انحلالٍ عصبي.[67] اقتُرح وجود دورٍ محتملٍ للعدوى المزمنة في دواعم السن[67] والنبيتات الجرثومية المعوية.[68]
اقتُرحت أيضًا فرضيةٌ وعائيةٌ عصبية تنصُ على أن ضعف وظيفة الحاجز الدموي الدماغي قد تلعب دورًا في مرض آلزهايمر.[69] كما رُبط بين العدوى بالبكتيريا الملتوية والخرف.[70][71]
يحدثُ اضطرابٌ في مرض آلزهايمر في استتباب المعادن الحيوية مثل النحاس والحديد والزنك الأيوني، ولكن على الرغم من هذا إلا أنهُ لا يزال غامضًا ما إذا كان هذا الاضطراب ينتجُ عن التغيرات البروتينية أو يُسببها. تؤثر هذه الأيونات وتتأثر ببروتين تاو والبروتين المنتج للمادة النشوانية وصميم البروتين الشحمي E،[72] كما قد يؤدي عدم انتظامها إلى إجهاد تأكسدي قد يسهم في مرضية آلزهايمر.[73][74][75][76][77] وُضعت الانتقادات على جودة بعض هذه الدراسات،[78][79] وما زالت العلاقة المطروحة مثيرةً للجدل.[80] لا يدعم غالبية الباحثين العلاقة السببية مع الألومنيوم.[79]
يُعتبر التدخين واحدًا من عوامل الخطر الرئيسية في مرض آلزهايمر.[81] كما أنَّ الواسمات الجهازية للمناعة الفطرية هي من عوامل الخطر لمرض آلزهايمر متأخر البدء.[82]
تُوجد أدلةٌ مبدئية على أن التعرض لملوثات الهواء قد يكون عاملًا مُساهمًا في حدوث مرض آلزهايمر.[83]
طرحت فرضيةٌ أُخرى أنَّ خللًا يحدث في الخلايا الدبقية قليلة التغصن والميالين المُرتبط بها أثناء الشيخوخة مما يُسهم في تلف المحور العصبي، والذي يؤدي فيما بعد إلى إنتاج بروتين نشواني وحدوث فرط فسفرةٍ في بروتين تاو كأثرٍ جانبي.[84][85]
فرضية العودة للخلف (Retrogenesis) هي فرضية طبية حول تطور وتقدم مرض آلزهايمر، وكان قد اقترحها باري ريسبيرغ في ثمانينات القرن العشرين.[86] تنص الفرضية على أنهُ عندما يمر الجنين بعملية النماء العصبي والتي تبدأ بتكون الأنبوب العصبي وتنتهي بتكون الميالين، فإنَّ أدمغة المصابين بآلزهايمر تمرُ بعملية تدهورٍ عصبيٍ عكسي تبدأ بإزالة الميالين مع موت المحاور العصبية (المادة البيضاء) وتنتهي بموت المادة الرمادية.[87] وأيضًا حسب الفرضية، فإن الأطفال يمرون بحالاتٍ من النمو المعرفي، فإن الأشخاص المُصابين بمرض آلزهايمر يُعانون من عمليةٍ عكسيةٍ للنقص المعرفي التدريجي.[86] طور ريسبيرغ أداةً لتقييم تقديم الرعاية وتعرف باسم "FAST" (Functional Assessment Staging Tool أو أداة تصنيف مراحل التقييم الوظيفي) والتي يذكر بأنها تُتيح لأولئك الذين يهتمون بمرضى آلزهايمر تحديد مراحل تطور المرض، وبالتالي تقدمُ المشورة بشأن نوع الرعاية المطلوبة في كل مرحلة.[86][88]
ارتباط الداء البطني غير واضحٍ، حيث وجدت دراسة عام 2019 عدم وجود زيادة في الخرف عمومًا لدى المصابين بالداء البطني، في حين وجدت مراجعة عام 2018 وجود ارتباطٍ بين الداء البطني مع عدة أنواعٍ من الخرف بما فيها آلزهايمر.[89][90]
الفيزيولوجيا المرضية
- مقالة مفصلة: الكيمياء الحيوية لمرض آلزهايمر

المرضيات العصبية
يتميزُ مرض آلزهايمر بحدوث فقدانٍ في العصبونات والمشابك العصبية في القشرة المخية ومناطق مُعينة تحت القشرة. يؤدي هذا الفقد إلى ضمورٍ جسيم في المناطق المتأثرة، وتتضمن تنكسًا في الفص الصدغي والفص الجداري وأجزاءً من الفص الجبهي والتلفيف الحزامي.[91] يحدثُ التنكس أيضًا في أنوية جذع الدماغ مثل الموضع الأزرق.[92] وثقت دراساتٍ تستخدم التصوير بالرنين المغناطيسي والتصوير المقطعي بالإصدار البوزيتروني انخفاضاتٍ في حجم مناطق معينة من الدماغ لدى المُصابين بمرض آلزهايمر، حيثُ تتطور من ضعفٍ إدراكيٍ طفيف إلى مرض آلزهايمر، وبالمقارنة مع صورٍ مماثلةٍ لبالغين أصحاء.[93][94]
تظهرٌ كلٌ من اللويحات النشوانية والتشابكات اللييفية العصبية بشكلٍ واضحٍ في الفحص المجهري لأدمغة المُصابين بمرض آلزهايمر.[95] تكون اللويحات كثيفةً، ومعظمها رواسب غيرُ قابلةٍ للانحلال من ببتيد بيتا النشواني والمواد الخلوية خارج وحول العصبونات. التشابكات اللييفية العصبية هي تجمعاتٌ من أنيبيباتٍ مرتبطةٍ ببروتين تاو، تكون قد تعرضت لفرط فسفرةٍ وتتراكم داخل الخلايا نفسها. على الرغم من أنَّ العديد من الأفراد الأكبر سنًا تحدثُ لديهم بعض اللويحات والتشابكات نتيجةً للشيخوخة، إلا أنَّ أدمغة المصابين بمرض آلزهايمر لديهم عددٌ أكبرٌ من هذه اللويحات والتشابكات في مناطق معينةٍ من الدماغ مثل الفص الصدغي.[96] يشيعُ وجود أجسام ليوي في أدمغة المصابين بمرض آلزهايمر.[97]
الكيمياء الحيوية
وُجد أنَّ مرض آلزهايمر يتضمنُ سوء تطوي البروتين (اعتلال بروتيني)، والذي يحدثُ بسبب تراكم لويحاتٍ شاذة التطوي من بروتين بيتا النشواني وبروتين تاو في الدماغ.[98] تتكون اللويحاتُ من ببتيداتٍ صغيرة، يبلغُ طولها ما بين 39-43 حمض أميني، وتُسمى ببتيد بيتا النشواني (Aβ)، وهو جزءٌ من بروتينٍ أكبر يُسمى البروتين المنتج للمادة النشوانية والذي يُعتبر بروتين عبر غشائي ينفذُ في غشاء العصبون. يُعتبر البروتين المنتج للمادة النشوانية مهمًا لبقاء ونمو العصبون ولإصلاحه بعد التضرر.[99][100] تعمل غاما سيكريتاز وبيتا سيكريتاز معًا في مرض آلزهايمر، وذلك في عملية حالةٍ للبروتين، مما يُؤدي إلى تفكك البروتين المنتج للمادة النشوانية إلى أجزاءٍ أصغير.[101] تؤدي إحدى هذه الأجزاء إلى ظهور لييفات بيتا النشواني، والتي تُشكل كتلًا تترسب خارج العصبونات في تكويناتٍ كثيفةٍ تُسمى لويحات الشيخوخة.[95][102]
يُعتبر مرض آلزهايمر اعتلالًا في بروتين تاو حيثُ يُحصل فيه تجمعٌ غير طبيعيٍ لبروتين تاو. يمتلكُ كُل عصبونٍ هيكلًا خلويًا، وهو هيكلٌ داخليٌ داعم يتكون جزئيًا من هياكل تُسمى الأنيبيبات الدقيقة. تعمل هذه الأنيبيبات مساراتٍ تُوجه المواد الغذائية والجزيئات من جسم الخلية إلى نهاية المحور العصبي والظهر. يعملُ بروتين تاو على جعل الأنيبيات الدقيقة مُستقرةً عند الفسفرة، لذلك تُسمى بروتين مرتبط بالأنيبيب الدقيق. يخضعُ بروتين تاو في مرض آلزهايمر إلى تغيراتٍ كيميائية، ليُصبح مُفرط الفسفرة، ثم يبدأ بالارتباط مع خيطان أُخرى، مما ينشئ تشابكاتٍ لييفية عصبية ويُفكك نظام النقل في العصبون.[103] قد يؤدي بروتين تاو المرضي إلى موت العصبون عبر خلل التنظيم ال عناصر المنقولة.[104]
آلية حدوث المرض
لا يُعرف بالضبط كيف تؤدي اضطراباتُ تكوين وتجميع ببتيد بيتا النشواني إلى حدوث مرض آلزهايمر.[105][106] تعتبرُ الفرضية النشوانية أنَّ تراكم ببتيد بيتا النشواني هو الحدثُ المركزي في إحداث الانحلال العصبوني. يؤدي تراكم اللييفات النشوانية المُجمعة، والتي يُعتقد أنها الشكل السام للبروتين المسؤول عن تعطيل توازن أيونات الكالسيوم في الخلية، إلى موت الخلية المبرمج (الاستماتة).[107] يُعرض أيضًا أنَّ ببتيد بيتا النشواني (Aβ) يتراكمُ بشكلٍ انتقائي في الميتوكوندريا في خلايا الدماغ المُصاب بمرض آلزهايمر، كما أنه يُثبط بعض وظائف الإنزيم ويثبط استخدام العصبونات للجلوكوز.[108]
التشخيص
المعايير
التقنيات
الوقاية
الأدوية
أسلوب الحياة
التغذية
إدراة المرض
لا يوجد علاج شافٍ لمرض آلزهايمر والعلاجات المتوفرة تتيح انخفاضا صغيرا نسبيا في الأعراض وتبقى تلطيفية في طبيعتها. يمكن تقسيم العلاجات الحالية إلى صيدلانية، نفسية اجتماعية، ورعائية.
الأدوية


تُستخدم حاليا خمسة أدوية لعالجة مشكال الآلزهايمر الإدراكية: أربعة هي مثبطات إستيراز الأسيتيل كولين (تاكرين، ريفاستيجمين، غالانتامين ودونيبيزيل) والخامس هو ميمانتين وهو مناهضة مستقبل نمدا، والفائدة من استخدامهم صغيرة.[7][109][110] لا يوجد دواء يظهر جليا بأنه يؤجل أو يعيق تقدم المرض.
انخفاض نشاط العصبونات كولونية الفعل سمة معروفة جيدا لمرض الآلزهايمر.[111] تُستعمل مثبطات إستيراز الأسيتيل كولين لتخفيض معدل هدم الأسيتيل كولين، وذلك لزيادة تركيزه في الدماغ ومواجهة فقدان الأستيل كولين المسبب بواسطة موت العصبونات كولينية الفعل.[112] يوجد دليل على فعالية هذه الأدوية في المرحلة الخفيفة والمتوسطة من مرض الألزهايمر ،[109][110][113] وبعض الأدلة على استخدامها في المرحلة المتقدمة.[109] استخدام هذه العقارات في الاعتلال الإدراكي الخفيف لم يُبدِ أي تأثير في تأخير بدء مرض الأزهايمر.[114] الآثار الجانبية الأكثر شيوعا هي الغثيان والتقيؤ وكلاهما مرتبط بفائض في النشاط كوليني الفعل. تحدث هذه الآثار الجانبية لدى حوالي 10–20% من المتناولين للأدوية وهي خفيفة إلى متوسطة الشدة ويمكن إدراتها بالتعديل البطيء للجرعات الطبية.[115] تشمل الأعراض الجانبية الثانوية الأقل شيوعا التشنجات العضلية، انخفاض معدل دقات القلب (بطء القلب)، انخفاض الشهية والوزن، وزيادة إنتاج العصارة الهضمية.[113]
حمض الجلوتاميك هو ناقل عصبي استثاري في الجهاز العصبي، يمكن أن يؤدي وجود كميات كبيرة منه في الدماغ إلى موت العصبونات عبر عملية تسمى سمية استثارية وهي الاستثارة الزائدة لمستقبلات حمض الجلوتاميك. لا تحدث السمية الاستثارية في مرض الآلزهايمر فقط، بل تحدث كذلك في أمراض عصبية أخرى مثل مرض باركنسون والتصلب المتعدد.[116] ميمانتين هو مناهضة مستقبل نمدا غير تنافسي استخدم أول مرة كعامل مضاد للإنفلونزا، ويعمل على النظام جلوتاميكي الفعل عبر تثبيط مستقبلات نمدا ومنع استثارتها الزائدة بواسطة حمض الجلوتاميك.[116][117] اتضح أن لميمانتين فائدة صغيرة في علاج مرض الآلزهايمر المتوسط والحاد.[118] والأثار الجانبية المبلغ عنها عند استعماله متوسطة الشدة وغير متواترة وتشمل الهلوسة، الارتباك، الدوخة، الصداع والإعياء.[119] ظهر بأن استخدام ميمانتين مع دونيبيزيل له تأثير إحصائي معتبر لكنه هامشي سريريا.[120]
مضادات الذهان غير النمطية مفيدة بقدر متواضع في تخفيض العدوان والذهان لدى الأفراد المصابين بالآلزهايمر، لكن إيجابيتها تفسدها أعراض جانبية خطيرة مثل: السكتة الدماغية، صعوبات في الحركة و إنخفاض إدراكي.[121] حين استُخدمت على المدى الطويل، ظهر بأن لها صلة بارتقاع الوفيات.[122] إيقاف استخدام مضادات الذهان لدى كبار السن المصابين بالخرف يبدو آمنا.[123]
هوبيرزين أ رغم أنه يبدو واعدا، إلا أنه يتطلب مزيدا من الأدلية قبل أن يوصى باستعماله.[124]
التدخل النفسي الاجتماعي
تُستخدم التدخلات النفسية الاجتماعية كعلاج مساعدٍ للعلاج بالأدوية ويمكن أن تُصنف داخل الأساليب الموجهة للسلوك والعاطفة والإدراك والتنبيه. الأبحاث حول فعاليتها غير متوفرة ونادرة ما تكون متخصصة بالآلزهايمر وعادة ما تركز على الخرف.[125]
تحاول تدخلات تعديل السلوك تحديد وتخفيض سوابق ونواتج السلوكات المشكِلَة. هذا الأسلوب لم يُظهر نجاحا في تغيير السلوك العام،[126] لكن يمكنه المساعدة في تخفيض بعض السلوكات المشكلة مثل التبول اللاإرادي.[127] هنالك انعدام لبيانات عالية الجودة حول تأثير هذه الأساليب في مشاكل سلوكية أخرى مثل الهيام والضياع.[128][129] العلاج بالموسيقى فعال في تخفيض الأعراض السلوكية والنفسية.[130]
تشمل التدخلات الموجهة للعاطفة: العلاج بالتذكر، العلاج بالتقدير ، العلاج النفسي الداعم، علاج التكامل الحسي ويسمى كذلك سنوزلن، وعلاج الحضور المحفز. لم تجد مراجعة لكوكرين أية أدلة على أن هذه التقنيات مؤثرة.[131] لم يحصل العلاج النفسي الداعم سوى على القليل من الدراسة العلمية الرسمية، لكن بعض الأطباء السريريين يجدونه مفيدا في مساعدة الأفراد متوسطي الاعتلال على التأقلم مع مرضهم.[125] في العلاج بالتذكر يتم التحدث حول تجارب الماضي بشكل فردي أو جماعي، مرات عديدة بمساعدة الصور، أغراض في المنزل، الموسيقى والتسجيلات الصوتية، أو أغراض مشابهة أخرى من الماضي. وجدت مراجعةٌ لتأثير العلاج بالتذكر في سنة 2018 أن التأثيرات غير متسقة، صغيرة الحجم وذات اعتبار سريري مشكوك فيه، وأنها تختلف حسب التحضير والمحيط.[132] علاج التواجد المحفز (SPT) مبني على نظريات التعلق ويتم فيه تشغيل تسجيلاتٍ لأصواتِ أقربِ أقرباءِ المريض بالآلزهايمر. يوجد دليل جزئي يشير إلى أن علاج التواجد المحفز يمكن أن يخفض السلوكات التي يصعب التعامل معها.[133] أخيرا، العلاج بالتقدير مبني على قبول واقعِ والحقيقة الشخصية لتجربة شخص آخر، بينما علاج التكامل الحسي مبني على تمارين موجهة لتنبيه الحواس. لا يوجد دليل يدعم فائدة وفاعلية هذه الأساليب العلاجية.[134][135]
غاية العلاجات الموجهة للإدراك -التي تشمل التوجيه نحو الواقع وإعادة تدريب الإدراك- هي تخفيض القصور الإدراكي. يتم في التوجيه نحو الواقع عرض معلومات حول الزمان والمكان لتسهيل فهم المريض لما يحيط به ومكانه فيه. من جهة أخرى، يحاول أسلوب إعادة تدريب الإدراك تحسين القدرات العليلة عبر تدريب القدرات العقلية. أظهر كلا الاسلوبين بعض الفعالية في تحسين القدرات الإدراكية،[136] رغم أن هذه التاثيرات في بعض الدراسات كانت مؤقتة وسلبية مثل الإحباط الذي أبلغ عنه.[125]
تشمل العلاجات الموجهة للتنبية: العلاج بالفن والموسيقى والحيوانات وأي نوع آخر من النشاطات الترفيهية. لعلاجات التنبيه أدلة متواضعة تدعم أنها تحسن السلوك والمزاج، وبصفة أقل الوظيفة. مع ذلك ورغم أهمية هذه التأثيرات فإن الداعم الرئيسي لاستخدام علاجات التنبيه هو تغيير روتين الشخص.[125]
الرعاية
- مقالة مفصلة: رعاية المصابين بالخرف
بما أن مرض الآلزهايمر لا علاج له ونظرا لأنه يجعل المصابين به غير قادرين على قضاء حوائجهم الخاصة، فإن الرعاية هي العلاج المتوفر ويجب تقديمها بعناية على مدار المرض.
أثناء المرحلتين المبكرة والمتوسطة، يمكن لتغيراتٍ في نمط المعيشة والمحيط المعيشي زيادة سلامة المريض والتخفيف من عبء مقدم الرعاية.[137][138] من الأمثلة على هذه التغييرات: الالتزام بالروتينات المبسطة، تركيب أقفال الأمان، عنونة الأدوات المنزلية لمساعدة الفرد المصاب بالمرض أو استخدام أدواتِ حياة يومية معدَّلة.[125][139][140] إذا أصبح تناول الطعام مشكلا، يجب أن يُحضّر الطعام على شكل قطع صغيرة أو حتى مهروسا.[141] حين تظهر صعوبات في الابتلاع، فإن استخدام أنابيب التغذية قد يكون ضروريا. في تلك الحالات، الفعالية الطبية والأخلاقيات اعتبار مهم للاستمرار في الإطعام لدى مقدمي الرعاية وأفراد العائلة.[142][143] استخدام التقييد البدني نادرا ما تكون الحاجة إليه في أي مرحلة من مراحل المرض، مع ذلك توجد حالات يكون فيها التقييد ضروريا لتجنب إيذاء المريض لنفسه أو لمقدمي الرعاية.[125]
مع تقدم المرض، يمكن أن تظهر مشاكل طبية مختلفة مثل مرض الفم والأسنان، سوء التغذية، مشاكل في النظافة، أو إصابات بعدوى تنفسية أو جلدية أو عينية. الرعاية والإدارة الحذرة يمكن أن تحول دون الإصابة بهذه الأمراض، لكن عند الإصابة فإن المعالجة الطبية الاحترافية مطلوبة.[144][145] اثناء المراحل النهائية من المرض، يُركَّز العلاج على تخفيف الآلام وعدم الراحة حتى الوفاة، في العادة بمساعدة مستشفى الحالات النهائية.[146]
مآل المرض

المراحل المبكرة من مرض آلزهايمر صعبة التشخيص، ولا يحدث تشخيص مؤكد حتى يعيق الاعتلال الإدراكي النشاطات اليومية الحياتية، وذلك رغم أن الفرد قد يستمر في العيش مستقلا دون الحاجة لمساعدة. تتطور الأعراض من مشاكل إدراك خفيفة مثل فقدان الذاكرة خلال مراحل متزايدة من الاضطرابات الإدراكية وغير الإدراكية وهو ما يقضي على إمكانية العيش مستقلا، خاصة في المراحل الأخيرة من المرض.[29]
متوسط العمر المتوقع للأفراد المصابين بالآلزهايمر منخفض،[147] ويتراوح عقب التشخيص بين ثلاثة إلى عشرة أعوام.[147]
يعيش أقل من 3% من الأفراد أكثر من 14 سنة.[148] ميزات المرض المرتبطة بانخفاضٍ في البقاء على قيد الحياة هي: زيادة في حدة الاعتلال الإدراكي، انخفاض في مستوى الفعالية والنشاط، واضطرابات في الفحص العصبي. لأمراض متزامنة الأخرى مثل: مشاكل القلب، السكري أو تاريخ في معاقرة الكحول دور كذلك في تخفيض البقاء على قيد الحياة.[149][150][151] كلما كانت بداية المرض في سن مبكر كان إجمالي عدد سنين البقاء على قيد الحياة أكبر، لكن متوسط عمر الحياة منخفض بشكل خاص عندما يُقارن الأفراد الأصغر سنا المرضى مع نظرائهم الأصحاء.[152] معدل سنين البقاء على قيد الحياة لدى الرجال أقل منه لدى النساء.[148][153]
ذات الرئة والتجفاف هما أكثر الأسباب المباشرة تواترا للوفاة التي يُحدثها الآلزهايمر، بينما يعتبر السرطان سببا أقل تواتر في إحداث الوفاة لدى المرضى بالآلزهايمر منه لدى عامة الناس.[153]
وبائيات
| السـن | عدد المصابين لكل ألف شخص كل سنة |
|---|---|
| 65–69 | 3 |
| 70–74 | 6 |
| 75–79 | 9 |
| 80–84 | 23 |
| 85–89 | 40 |
| 90– | 69 |
يُستخدم معياران رئيسيان في دراسات علم الأوبئة هما: معدل الحدوث و مدى الانتشار. معدل الحدوث هو رقم الحالات الجديدة لكل وحدة من الأفراد الذين يكونون عرضة للإصابة، عبر زمن محدد (عادة عدد الحالات الجديدة لكل ألف شخص كل عام)، في حين أن معدل الانتشار هو العدد الإجمالي لحالات المرض في الجمهرة (السكان) في أي وقت.
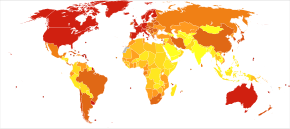
بالنسبة لمعدل الحدوث، توفر دراسات التعرض الطولية (الدراسات التي تتتبع جمهرة خالية من المرض لعدة سنين) معدلات بين 10 إلى 15 إصابة لكل ألفا شخص كل سنة لجميع أنواع الخرف منها 5 إلى 8 إصابات بالآلزهايمر،[154][155] وهذا يعني أن نصف حالات الخرف كل عام تكون بسبب الآلزهايمر. التقدم في السن هو عامل الخطر الرئيسي للمرض ومعدلات الحدوث ليست متساوية بين جميع الأعمار: بعد عمر الـ65 يتضاعف معدل الإصابة بالمرض تقريبا كل خمس سنوات، متزايدا من 3 إلى 69 حالة لكل ألف شخص كل سنة.[154][155] توجد كذلك اختلافات جنسية في معدل الحدوث، فللنساء احتمال أكبر للإصابة بالآلزهايمر خاصة بين النساء التي تفوق أعمارهن 85 سنة.[155][156] في الولايات المتحدة، خطر الوفاة بمرض الآلزهايمر أعلى بـ26% بين السكان البيض من أصل غير إسباني منه لدى السكان السود من أصل غير إسباني، بينما احتمال الوفاة لدى السكان من أصل إسباني أقل بـ30% منه لدى السكان البيض من أصل غير إسباني.[157]
يعتمد انتشار الآلزهايمر في الجمهرات على عوامل مختلفة منها معدل الحدوث والنجاة. مع كون معدل الحدوث يتزايد مع العمر، فإنه مهم بشكل خاص إدراج متوسط عمر الجمهرة التي تتم دراستها. في الولايات المتحدة، قُدِّر انتشار مرض الآلزهايمر بنسبة 1.6% سنة 2000 إجماليا وبين الفئة العمرية 65–74، مع زيادة هذه النسبة إلى 19% في الفئة العمرية 75–84 وإلى 42% لدى الفئة التي يزيد عمرها عن 84 سنة.[158] معدلات الانتشار في المناطق الأقل تطورا أقل من ذلك.[159] قدرت منظمة الصحة العالمية أنه في سنة 2005 0.379% من السكان العالم مصابون بالخرف، وأن الانتشار سيزيد إلى 0.441% سنة 2015 ثم إلى 0.556% سنة 2030.[160] ووصلت دراسات أخرى إلى نفس الاستنتاجات.[159] قدّرت دراسة أخرى أنه في سنة 2006 0.40% من سكان العالم ( تتراوح النسبة بين 0.17–0.89% والعدد المطلق 26.6 مليون، ويتراوح العدد بين 11.4–59.4 مليون) أصيبوا بالآلزهايمر، وأن معدل الانتشار سيتضاعف ثلاث مرات وأن العدد المطلق سيتضاعف أربع مرات بحلول 2050.[161]
التاريخ

ربط فلاسفة وأطباء الإغريق والرومان القدماء كبر السن بتزايد الخرف.[18] ولم يُعرَّف مرض الآلزهاير حتى عام 1902، أين قام الطبيب النفسي الألماني ألويس ألزهايمر بتحديد أول حالة أصبحت تعرف بمرض آلزهايمر -سميت باسمه- لدى امرأة تبلغ من العمر 55 سنة تسمى أوغست ديتر، وقام بتتبع حالتها حتى توفيت عام 1906، وذلك حين أبلغ عنها علنا لأول مرة.[162] خلال الأعوام الخمسة التالية أُبلغ عن إحدى عشر حالة مماثلة في الأدب الطبي، بعضها استخدم مصطلح مرض الآلزهايمر.[18] وُصف المرض أول مرة بأنه مرض مميز ومستقل بواسطة إميل كريبيلن بعد إخفاء بعض السمات السريرية (الوهام والهلوسة) والمرضية (تغيرات في تصلب الشرايين) الموجودة في التقرير الأصلي الخاص بأوغست ديتر.[163] حيث شمله بالذكر -تحت إسم خرف الكهولة- كنوع فرعي من خرف الشيخوخة في الإصدار الثامن من كتابه المدرسي الخاص بالطب النفسي، المنشور في 5 يوليو 1910.[164]
في معظم القرن العشرين، كان التشخيص بمرض الآلزهايمر محصورا في الأفراد الذين أعمارهم بين 45 و65 سنة الذين ظهرت لديهم أعراض الخرف. تغيرت المصطلحات بعد 1977 حين خلص مؤتمر حول الآلزهايمر إلى أن التجليات السريرية والمرضية لخرف الشيخوخة والكهولة متماثلة تقريبا، مع ذلك أضاف الكتاب كذلك أن هذا لا يستبعد إمكانية وجود أسباب مختلفة لهما.[165] أدى هذا في النهاية إلى تشخيص مرض الآلزهايمر بشكل مستقل عن العمر.[166] استُخدم مصطلح خرف الشيخوخة من نوع آلزهايمر (SDAT) لمدة من الزمن لوصف حالة الأفراد الذين تفوق أعمارهم الـ65، واستخدم مصطلح مرض الآلزهايمر الكلاسيكي في وصف حالات الأفرد الأقل سنا. في النهاية، تم تبني مصطلح مرض الآلزهايمر بشكل غير رسمي في التسمية الطبية لوصف الأفراد من جميع الأعمار الذين لديهم نمط أعراض مشترك مميز، مسار المرض، والمرض العصبي.[167]
المجتمع والثقافة
- مقالة مفصلة: منظمات مرض آلزهايمر
التكاليف الاجتماعية
يمكن أن يكون الخرف وتحديدا مرض الآلزهايمر من بين أكثر الأمراض المكلفة للمجتمع في أوروبا والولايات المتحدة،[19][20] بينما تكاليفها في دول أخرى مثل الأرجنتين [168] وكوريا الجنوبية [169] مرتفعة كذلك وتتزايد في الارتفاع أكثر. من المحتمل أن تزيد هذه التكاليف مع تشيخ المجتمع وسيصبح ذلك مشكلا اجتماعيا مهما. تشمل التكاليف المرتبطة بالآلزهايمر: التكاليف الطبية مثل تكاليف دار التمريض والرعاية، التكالف الطبية المباشرة مثل تكاليف الرعاية اليومية بالمنزل، والتكاليف غير المباشرة مثل فقدان إنتاجية كل من المريض ومقدم الرعاية.[20] تختلف الأرقام بين الدراسات لكن قُدرت تكاليف الخرف عالميا بحوالي 160 مليار دولار،[170] بينما تقدر تكاليف مرض الآلزهايمر بالولايات المتحدة بحوالي 100 مليار دولار كل عام.[20]
المصدر الأكبر للتكاليف بالنسبة للمجتمع هو الرعاية طويلة الأجل بواسطة محترفي تقديم الرعاية وبشكل خاص إضفاء الطابع المؤسسي، الذي يعادل حوالي ثلثي إجمالي التكاليف بالنسبة للمجتمع.[19] تكلفة العيش في المنزل مرتفعة جدا كذلك،[19] خاصة حين تؤخذ في الحسبان التكاليف غير الرسمية التي تتحملها العائلة مثل وقت الرعاية والمداخيل المفقودة التي كان سيكسبها مقدم الرعاية.[171]
تتزايد التكاليف مع زيادة حدة الخرف وحدوث الاضطرابات السلوكية،[172] وهي مرتبطة بزيادة وقت تقديم الرعاية المطلوب لتقديم الرعاية الجسدية.[171] لذلك، أي علاج يبطئ التدهور الإدراكي أو يؤخر الإدخال إلى مؤسسة تمريض ورعاية أو يخفض ساعات الرعاية ستكون له فوائد اقتصادية. أظهرت التقييمات الاقتصادية للعلاجات الحالية نتائجا إيجابية.[20]
أعباء تقديم الرعاية
- مقالة مفصلة: رعاية المصابين بالخرف
دور مقدم الرعاية الرئيسي غالبا ما تقوم به الزوجة أو أحد الأقرباء المقربين.[173] مرض الآلزهايمر معروف بأنه يضع أعباء كبيرة على مقدمي الرعاية تشمل نواحي اجتماعية ونفسية وجسدية واقتصادية.[14][174][175] الرعاية بالمنزل عادة ما يكون الخيار المفضل لدى العائلات التي أصيب أفراد منها بالآلزهايمر.[176] هذا الخيار يؤخر أو يزيل الحاجة إلى مستويات أكثر احترافية وتكلفة من الرعاية.[176][177] مع ذلك، ثلثا المقيمين بدور الرعاية مصابون بالخرف.[125]
مقدمو الرعاية للأفراد المصابين بالخرف عرضة لمعدلات عالية من الاضطرابات النفسية والجسدية.[178] من العوامل المرتبطة مع المشاكل النفسية الاجتماعية المرتفعة التي تصيب مقدمي الرعاية الأساسيين: وجود فرد مصاب بالمنزل، كون الراعي هو الزوجة، السلوكيات المتطلبة للرعاية الخاصة بالفرد المصاب مثل الاكتئاب، اضطرابات سلوكية، هلوسات، مشاكل في النوم، اختلالات في المشي والانعزال الاجتماعي.[179][180] بالنسبة للمشاكل الاقتصادية، غالبا ما يتخلى مقدمو الرعاية من أفراد الأسرة عن ساعات من العمل لقضاء ما متوسطه 47 ساعة أسبوعيا مع الفرد المصاب بالآلزهايمر، لأن تكاليف رعايتهم تكون غالية. تُقدر التكاليف المباشرة أو غير المباشرة لرعاية مريض بالآلزهايمر في المتوسط بحوالي 18 ألف إلى 77.5 ألف دولار لكل عام في الولايات المتحدة، وذلك حسب الدراسة.[171][173]
أثبت العلاج الإدراكي السلوكي وتعليم استراتيجيات التأقلم سواء فرديا أو جماعيا فعاليتهما في تحسين الصحة النفسية لمقدمي الرعاية.[14][181]
المشاهير، الإعلام، الأدب والسينيما

أصاب مرض الآلزهايمر الكثير من الناس ولم يستثنِ المشاهير، ومن هؤلاء المشاهير رئيس الولايات المتحدة السابق رونالد ريغان والكاتبة الأيرلندية آيريس مردوك. حقيقة هاتين الإصابتين لم تُغطَّ على نحو واسع إعلاميا وحسب، بل كانت أساسا لمقالات علمية قام فيها الكتاب بدراسة تطور تدهور الوظائف الإدراكية لهاتين الشخصيتين المشهورتين.[182][183] من المشاهير الذين أصيبوا بالمرض كذلك: لاعب كرة القدم فيرينتس بوشكاش،[184] رئيس الوزراء البريطاني السابق هارولد ويلسون، ورئيس الوزراء الإسباني أدولفو سواريث،[185][186] الممثلين: بيتر فالك،[187] ريتا هيوارث،[188] ميخائيل فولكوف وآني جيراردو وشارلتون هيستون،[189] والكاتب تيري براتشيت.[190]
جاء ذكر مرض الآلزهايمر في أفلام مثل: أيريس (2001) بناء على ذكرى زوجة جون بايلي آيريس مردوك،[191] دفتر الملاحظات 2004 بناء على روايةٍ لنيكولاس سباركس سنة 1996 تحمل نفس العنوان،[192] لحظة للذكرى (2004)، ثانماثرا (2005)،[193] ذكريات الغد (2006) بناء على رواية هيروشي أوجيوارا التي تحمل نفس العنوان،[194] بعيدا عنها (2006) بناء على القصة القصيرة لآليس مونرو "جاء الدب فوق الجبل"،[195]، نهوض كوكب القردة (2011)، انفصال نادر وسمين (2011)، المرأة الحديدية (2011)، ما تزال أليس (2014) حول بروفيسور في جامعة كولومبيا أصيبت بمرض الألزهايمر في سن مبكر، بناء على رواية لليزا جينوفا سنة 2007 تحمل نفس الاسم مع جوليان مور في الدور الرئيسي، وفي مسلسل تشريح غراي. الأشرطة الوثائقية حول مرض الآلزهايمر تشمل: مالكوم وباربرا: قصة حب (1999)، ومالكوم وباربرا: وداع الحب (2007) مع بطولة مالكولم بوينتون في كلاهما.[196][197][198]
عربيا جاء ذكر المرض في فيلم بعنوان زهايمر (2010) من بطولة عادل إمام.[199]
الأبحاث
الأدوية
في العقد 2002-2012 تم تقييم 244 مركب في اختبارات المرحلة 1 والمرحلة 2 والمرحلة 3، ولم يحصل سوى واحد منها (ميمانتين) على موافقة إدارة الغذاء والدواء (مازال الآخرون في الأنبوب
البحث حول تأثيرات التأمل في الحفاظ على الوظائف الإدراكية مازال في المرحلة الأولى.[226] تقترح مراجعة سنة 2015 أن التدخلات المبنية على الوعي التام التأملي يمكن أن تمنع أو تؤخر الاعتلال الإدراكي الخفيف ومرض الآلزهايمر.[227]
احتمال الانتقال
حالات نادرة لإمكانية انتقال أمراض النشواني بين الناس هي قيد الدراسة،[228] ومن الأمثلة عليها مرضى هرمون النمو.[229]
العداوى
وُجد فيروس الهربس البسيط (HSV-1) في نفس مناطق وجود اللويحات النشوانية،[230] وهذا يوحي بإمكانية علاج مرض الألزهايمر أو الوقاية منه بواسطة الأدوية المضادة للفيروسات.[230][231] أظهرت دراسات المضادات الفيروسية في المزارع الخلوية نتائجا واعدة.[232]
أُبلِغ عن العدوى الفطرية في الأدمغة المريضة بالألزهايمر كذلك.[233] اقتُرحت هذه الفرضية بواسطة عالم الأحياء الدقيقة ل.كراسكو حين وجد فريقه علاقة ارتباطية إحصائية بين العدوى الفطرية المنتشرة والآلزهايمر.[234] وأظهرت المزيد من الدراسات أن العدوى الفطرية متواجدة في مناطق مختلفة من أدمغة المرضى بالآلزهايمر، وغير متواجدة في مجموعة الأفراد المرجعية.[235][236] الإصابة بالعدوى الفطرية تفسر الأعراض الملاحظة لدى المرضى بالآلزهايمر. التطور البطيء للآلزهايمر يناسب الطبيعة المزمنة لبعض العداوى الفطرية الجهازية والتي يمكن أن تكون عديمة الأعراض وبالتالي لا تتم ملاحظتها ولا علاجها.[235] الفرضية الفطرية متوافقة كذلك مع بعض فرضيات الآلزهايمر الأخرى الموجودة سابقا مثل فرضية النشواني التي يمكن تفسيرها كاستجابة مناعية للإصابة بالعدوى في الجهاز العصبي المركزي.[237][238][239] مثلما وجد ر.موار ور.تانزي في نماذج الفأر والدودة من الآلزهايمر.
التصوير الطبي
من بين العديد من تقنيات التصوير الطبي المتوفرة، يبدو التصوير المقطعي المحوسب بإصدار فوتون واحد (SPECT) الأفضل في تمييز الآلزهايمر من بين أنواع الخرف الأخرى، وتبين أنه يُعطي مستوى عالٍ من الدقة مقارنة بدراسات الاختبار الذهني والتاريخ الطبي.[240] أدت التقدمات التكنولوجية إلى اقتراح معايير تشخيص جديدة.[22][241] تبقى تقنية التصوير المقطعي بالإصدار البوزيتروني بمركب بيتسبرغ B (PiB-PET) استقصائية، لكن تقنيةَ تصويرٍ مقطعيٍ بالإصدار البوزيتروني (PET) مماثلة بدواء مشع يسمى فلوربيتابير -يحتوي على نوكليد مشع أطول أمدا هو الفلور 18- تعتبر وسيلة تشخيصٍ لمرض الآلزهايمر.[242][243]
يُستخدم تصوير النشواني على الأرجح جنبا إلى جنب مع واسمات أخرى بدل أن يكون بديلا.[244] يمكن أن يَكتشف التصوير بالرنين المغناطيسي (MRI) الحجمي تغيرات في حجم مناطق الدماغ. قياس هاته المناطق الضامرة أثناء تطور مرض الآلزهايمر يُبدو واعدا كمؤشر تشخيص، وقد يثبت أنه أقل تكلفة من طرق التصوير الأخرى التي هي قيد الدراسة حاليا.[245] في عام 2011، صوتت هيئة إدارة الغذاء والدواء بالإجماع للتوصية بترخيص استخدام فلوربيتابير.[246] حيث يمكن لعامل التصوير هذا اكتشاف لويحات الألزهايمر بالدماغ.[247] ويُظهر تصوير سلبي بواسطته لويحات ضئيلة متناثرة أو لا يظهرها أصلا وهو ما لا يتوافق مع تشخيص الآلزهايمر.[248]
التشخيص
تركز البحوث حول الآلزهايمر في تشخيص الحالة قبل ظهور الأعراض.[249] طُوِّرت العديد من اختبارات الكشف الكيميائية الحيوية لتمكين التشخيص المبكر للمرض. تقوم بعض هذه الاختبارات بدراسة السائل الدماغي الشوكي للكشف عن بيتا النشواني، مجموع بروتين تاو، وتراكيز بروتين تاو181P المفسفر.[250] لأن سحب السائل الدماغي الشوكي يمكن أن يكون مؤلما، فإن السحب المتكرر له يتم تجنبه. الاختبار الدموي للرنا الميكروي الموجود في الدورة الدموية والواسمات الحيوية للالتهاب هو مؤشر محتمل بديل.[250]
المراجع
بِاللُغة الإنجليزيّة
- Burns A, Iliffe S (فبراير 2009). "Alzheimer's disease". BMJ. 338: b158. doi:10.1136/bmj.b158. PMID 19196745.
- Ballard C, Gauthier S, Corbett A, Brayne C, Aarsland D, Jones E (مارس 2011). "Alzheimer's disease". Lancet. 377 (9770): 1019–31. doi:10.1016/S0140-6736(10)61349-9. PMID 21371747.
- Mendez MF (November 2012). "Early-onset Alzheimer's disease: nonamnestic subtypes and type 2 AD". Archives of Medical Research. 43 (8): 677–85. doi:10.1016/j.arcmed.2012.11.009. PMC . PMID 23178565.
- "Dementia Fact sheet". World Health Organization. 12 December 2017. مؤرشف من الأصل في 07 ديسمبر 2019.
- "Dementia diagnosis and assessment" ( كتاب إلكتروني PDF ). National Institute for Health and Care Excellence (NICE). مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 05 ديسمبر 201430 نوفمبر 2014.
- Querfurth HW, LaFerla FM (يناير 2010). "Alzheimer's disease". The New England Journal of Medicine. 362 (4): 329–44. doi:10.1056/NEJMra0909142. PMID 20107219.
- Commission de la transparence (June 2012). "Drugs for Alzheimer's disease: best avoided. No therapeutic advantage". Prescrire International. 21 (128): 150. PMID 22822592.
- GBD 2015 Disease Injury Incidence Prevalence Collaborators (October 2016). "Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990-2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053): 1545–1602. doi:10.1016/S0140-6736(16)31678-6. PMC . PMID 27733282.
- GBD 2015 Mortality Causes of Death Collaborators (October 2016). "Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980-2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053): 1459–1544. doi:10.1016/S0140-6736(16)31012-1. PMC . PMID 27733281.
- "About Alzheimer's Disease: Symptoms". National Institute on Aging. مؤرشف من الأصل في 15 يناير 201228 ديسمبر 2011.
- Todd S, Barr S, Roberts M, Passmore AP (نوفمبر 2013). "Survival in dementia and predictors of mortality: a review". International Journal of Geriatric Psychiatry. 28 (11): 1109–24. doi:10.1002/gps.3946. PMID 23526458.
- "So, What Can You Do?". National Institute on Aging. 29 يوليو 2016. مؤرشف من الأصل في 03 أبريل 2017.
- Thompson CA, Spilsbury K, Hall J, Birks Y, Barnes C, Adamson J (July 2007). "Systematic review of information and support interventions for caregivers of people with dementia". BMC Geriatrics. 7: 18. doi:10.1186/1471-2318-7-18. PMC . PMID 17662119.
- Forbes D, Forbes SC, Blake CM, Thiessen EJ, Forbes S (April 2015). "Exercise programs for people with dementia". The Cochrane Database of Systematic Reviews (Submitted manuscript). 132 (4): CD006489. doi:10.1002/14651858.CD006489.pub4. PMID 25874613.
- National Institute for Health and Clinical Excellence. "Low-dose antipsychotics in people with dementia". National Institute for Health and Care Excellence (NICE). مؤرشف من الأصل في 05 ديسمبر 201429 نوفمبر 2014.
- "Information for Healthcare Professionals: Conventional Antipsychotics". US Food and Drug Administration. 16 June 2008. مؤرشف من الأصل في 29 نوفمبر 201429 نوفمبر 2014.
- Berchtold NC, Cotman CW (1998). "Evolution in the conceptualization of dementia and Alzheimer's disease: Greco-Roman period to the 1960s". Neurobiology of Aging. 19 (3): 173–89. doi:10.1016/S0197-4580(98)00052-9. PMID 9661992.
- Bonin-Guillaume S, Zekry D, Giacobini E, Gold G, Michel JP (January 2005). "[The economical impact of dementia]". Presse Médicale (باللغة الفرنسية). 34 (1): 35–41. doi:10.1016/s0755-4982(05)83882-5. PMID 15685097.
- Meek PD, McKeithan K, Schumock GT (1998). "Economic considerations in Alzheimer's disease". Pharmacotherapy. 18 (2 Pt 2): 68–73, discussion 79–82. PMID 9543467. مؤرشف من الأصل في 16 أكتوبر 2019.
- "Evaluating Prescription Drugs Used to Treat: Alzheimer's Disease Comparing Effectiveness, Safety, and Price" ( كتاب إلكتروني PDF ). Consumer Reports Drug Effectiveness Review Project. Consumer Reports. May 2012. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 05 سبتمبر 201201 مايو 2013.
- Waldemar G, Dubois B, Emre M, Georges J, McKeith IG, Rossor M, Scheltens P, Tariska P, Winblad B (January 2007). "Recommendations for the diagnosis and management of Alzheimer's disease and other disorders associated with dementia: EFNS guideline". European Journal of Neurology. 14 (1): e1–26. doi:10.1111/j.1468-1331.2006.01605.x. PMID 17222085.
- Bäckman L, Jones S, Berger AK, Laukka EJ, Small BJ (September 2004). "Multiple cognitive deficits during the transition to Alzheimer's disease". Journal of Internal Medicine. 256 (3): 195–204. doi:10.1111/j.1365-2796.2004.01386.x. PMID 15324363.
- Nygård L (2003). "Instrumental activities of daily living: a stepping-stone towards Alzheimer's disease diagnosis in subjects with mild cognitive impairment?". Acta Neurologica Scandinavica. Supplementum. 179 (179): 42–6. doi:10.1034/j.1600-0404.107.s179.8.x. PMID 12603250.
- Arnáiz E, Almkvist O (2003). "Neuropsychological features of mild cognitive impairment and preclinical Alzheimer's disease". Acta Neurologica Scandinavica. Supplementum. 179: 34–41. doi:10.1034/j.1600-0404.107.s179.7.x. PMID 12603249.
- Landes AM, Sperry SD, Strauss ME, Geldmacher DS (December 2001). "Apathy in Alzheimer's disease". Journal of the American Geriatrics Society. 49 (12): 1700–7. doi:10.1046/j.1532-5415.2001.49282.x. PMID 11844006.
- Murray ED, Buttner N, Price BH (2012). "Depression and Psychosis in Neurological Practice". In Bradley WG, Daroff RB, Fenichel GM, Jankovic J (المحررون). Bradley's neurology in clinical practice (الطبعة 6th). Philadelphia, PA: Elsevier/Saunders. .
- Grundman M, Petersen RC, Ferris SH, Thomas RG, Aisen PS, Bennett DA, et al. (January 2004). "Mild cognitive impairment can be distinguished from Alzheimer disease and normal aging for clinical trials". Archives of Neurology. 61 (1): 59–66. doi:10.1001/archneur.61.1.59. PMID 14732621.
- Förstl H, Kurz A (1999). "Clinical features of Alzheimer's disease". European Archives of Psychiatry and Clinical Neuroscience. 249 (6): 288–90. doi:10.1007/s004060050101. PMID 10653284.
- Carlesimo GA, Oscar-Berman M (June 1992). "Memory deficits in Alzheimer's patients: a comprehensive review". Neuropsychology Review. 3 (2): 119–69. doi:10.1007/BF01108841. PMID 1300219.
- Jelicic M, Bonebakker AE, Bonke B (1995). "Implicit memory performance of patients with Alzheimer's disease: a brief review". International Psychogeriatrics. 7 (3): 385–92. doi:10.1017/S1041610295002134. PMID 8821346.
- Taler V, Phillips NA (July 2008). "Language performance in Alzheimer's disease and mild cognitive impairment: a comparative review". Journal of Clinical and Experimental Neuropsychology. 30 (5): 501–56. doi:10.1080/13803390701550128. PMID 18569251.
- Frank EM (September 1994). "Effect of Alzheimer's disease on communication function". Journal of the South Carolina Medical Association. 90 (9): 417–23. PMID 7967534.
- Volicer L, Harper DG, Manning BC, Goldstein R, Satlin A (May 2001). "Sundowning and circadian rhythms in Alzheimer's disease". The American Journal of Psychiatry. 158 (5): 704–11. doi:10.1176/appi.ajp.158.5.704. PMID 11329390.
- Gold DP, Reis MF, Markiewicz D, Andres D (January 1995). "When home caregiving ends: a longitudinal study of outcomes for caregivers of relatives with dementia". Journal of the American Geriatrics Society. 43 (1): 10–6. doi:10.1111/j.1532-5415.1995.tb06235.x. PMID 7806732.
- "What We Know Today About Alzheimer's Disease". Alzheimer's Association. مؤرشف من الأصل في 07 أكتوبر 201101 أكتوبر 2011.
While scientists know Alzheimer's disease involves progressive brain cell failure, the reason cells fail isn't clear.
- Reitz C, Mayeux R (April 2014). "Alzheimer disease: epidemiology, diagnostic criteria, risk factors and biomarkers". Biochemical Pharmacology. 88 (4): 640–51. doi:10.1016/j.bcp.2013.12.024. PMC . PMID 24398425.
- Wilson RS, Barral S, Lee JH, Leurgans SE, Foroud TM, Sweet RA, Graff-Radford N, Bird TD, Mayeux R, Bennett DA (2011). "Heritability of different forms of memory in the Late Onset Alzheimer's Disease Family Study". Journal of Alzheimer's Disease. 23 (2): 249–55. doi:10.3233/JAD-2010-101515. PMC . PMID 20930268.
- Blennow K, de Leon MJ, Zetterberg H (يوليو 2006). "Alzheimer's disease". Lancet. 368 (9533): 387–403. doi:10.1016/S0140-6736(06)69113-7. PMID 16876668.
- Waring SC, Rosenberg RN (مارس 2008). "Genome-wide association studies in Alzheimer disease". Archives of Neurology. 65 (3): 329–34. doi:10.1001/archneur.65.3.329. PMID 18332245.
- Selkoe DJ (يونيو 1999). "Translating cell biology into therapeutic advances in Alzheimer's disease". Nature. 399 (6738 Suppl): A23–31. doi:10.1038/19866. PMID 10392577.
- Borchelt DR, Thinakaran G, Eckman CB, Lee MK, Davenport F, Ratovitsky T, et al. (نوفمبر 1996). "Familial Alzheimer's disease-linked presenilin 1 variants elevate Abeta1-42/1-40 ratio in vitro and in vivo". Neuron. 17 (5): 1005–13. doi:10.1016/S0896-6273(00)80230-5. PMID 8938131.
- Kim, JH (ديسمبر 2018). "Genetics of Alzheimer's Disease". Dementia and Neurocognitive Disorders. 17 (4): 131–36. doi:10.12779/dnd.2018.17.4.131. PMC . PMID 30906402.
- Strittmatter WJ, Saunders AM, Schmechel D, Pericak-Vance M, Enghild J, Salvesen GS, Roses AD (مارس 1993). "Apolipoprotein E: high-avidity binding to beta-amyloid and increased frequency of type 4 allele in late-onset familial Alzheimer disease". Proceedings of the National Academy of Sciences of the United States of America. 90 (5): 1977–81. doi:10.1073/pnas.90.5.1977. PMC . PMID 8446617.
- Mahley RW, Weisgraber KH, Huang Y (أبريل 2006). "Apolipoprotein E4: a causative factor and therapeutic target in neuropathology, including Alzheimer's disease". Proceedings of the National Academy of Sciences of the United States of America. 103 (15): 5644–51. Bibcode:2006PNAS..103.5644M. doi:10.1073/pnas.0600549103. PMC . PMID 16567625.
- Hall K, Murrell J, Ogunniyi A, Deeg M, Baiyewu O, Gao S, Gureje O, Dickens J, Evans R, Smith-Gamble V, Unverzagt FW, Shen J, Hendrie H (يناير 2006). "Cholesterol, APOE genotype, and Alzheimer disease: an epidemiologic study of Nigerian Yoruba". Neurology. 66 (2): 223–27. doi:10.1212/01.wnl.0000194507.39504.17. PMC . PMID 16434658.
- Gureje O, Ogunniyi A, Baiyewu O, Price B, Unverzagt FW, Evans RM, et al. (يناير 2006). "APOE epsilon4 is not associated with Alzheimer's disease in elderly Nigerians". Annals of Neurology. 59 (1): 182–85. doi:10.1002/ana.20694. PMC . PMID 16278853.
- Lambert JC, Ibrahim-Verbaas CA, Harold D, Naj AC, Sims R, Bellenguez C, et al. (ديسمبر 2013). "Meta-analysis of 74,046 individuals identifies 11 new susceptibility loci for Alzheimer's disease". Nature Genetics. 45 (12): 1452–58. doi:10.1038/ng.2802. PMC . PMID 24162737.
- Jonsson T, Stefansson H, Steinberg S, Jonsdottir I, Jonsson PV, Snaedal J, et al. (يناير 2013). "Variant of TREM2 associated with the risk of Alzheimer's disease". The New England Journal of Medicine (Original article). 368 (2): 107–16. doi:10.1056/NEJMoa1211103. PMC . PMID 23150908.
- Guerreiro R, Wojtas A, Bras J, Carrasquillo M, Rogaeva E, Majounie E, et al. (يناير 2013). "TREM2 variants in Alzheimer's disease". The New England Journal of Medicine (Original article). 368 (2): 117–27. doi:10.1056/NEJMoa1211851. PMC . PMID 23150934.
- Mukherjee S, Mez J, Trittschuh EH, Saykin AJ, Gibbons LE, Fardo DW, et al. (ديسمبر 2018). "Genetic data and cognitively defined late-onset Alzheimer's disease subgroups". Molecular Psychiatry. doi:10.1038/s41380-018-0298-8. PMC . PMID 30514930.
- Francis PT, Palmer AM, Snape M, Wilcock GK (فبراير 1999). "The cholinergic hypothesis of Alzheimer's disease: a review of progress". Journal of Neurology, Neurosurgery, and Psychiatry. 66 (2): 137–47. doi:10.1136/jnnp.66.2.137. PMC . PMID 10071091.
- Martorana A, Esposito Z, Koch G (أغسطس 2010). "Beyond the cholinergic hypothesis: do current drugs work in Alzheimer's disease?". CNS Neuroscience & Therapeutics. 16 (4): 235–45. doi:10.1111/j.1755-5949.2010.00175.x. PMC . PMID 20560995.
- Hardy J, Allsop D (أكتوبر 1991). "Amyloid deposition as the central event in the aetiology of Alzheimer's disease". Trends in Pharmacological Sciences. 12 (10): 383–88. doi:10.1016/0165-6147(91)90609-V. PMID 1763432.
- Mudher A, Lovestone S (يناير 2002). "Alzheimer's disease-do tauists and baptists finally shake hands?". Trends in Neurosciences. 25 (1): 22–26. doi:10.1016/S0166-2236(00)02031-2. PMID 11801334.
- Nistor M, Don M, Parekh M, Sarsoza F, Goodus M, Lopez GE, Kawas C, Leverenz J, Doran E, Lott IT, Hill M, Head E (أكتوبر 2007). "Alpha- and beta-secretase activity as a function of age and beta-amyloid in Down syndrome and normal brain". Neurobiology of Aging. 28 (10): 1493–506. doi:10.1016/j.neurobiolaging.2006.06.023. PMC . PMID 16904243.
- Lott IT, Head E (مارس 2005). "Alzheimer disease and Down syndrome: factors in pathogenesis". Neurobiology of Aging. 26 (3): 383–89. doi:10.1016/j.neurobiolaging.2004.08.005. PMID 15639317.
- Polvikoski T, Sulkava R, Haltia M, Kainulainen K, Vuorio A, Verkkoniemi A, Niinistö L, Halonen P, Kontula K (نوفمبر 1995). "Apolipoprotein E, dementia, and cortical deposition of beta-amyloid protein". The New England Journal of Medicine. 333 (19): 1242–47. doi:10.1056/NEJM199511093331902. PMID 7566000.
- الفئران المُعدلة وراثيًا:
- Games D, Adams D, Alessandrini R, Barbour R, Berthelette P, Blackwell C, Carr T, Clemens J, Donaldson T, Gillespie F (فبراير 1995). "Alzheimer-type neuropathology in transgenic mice overexpressing V717F beta-amyloid precursor protein". Nature. 373 (6514): 523–27. doi:10.1038/373523a0. PMID 7845465.
- Masliah E, Sisk A, Mallory M, Mucke L, Schenk D, Games D (سبتمبر 1996). "Comparison of neurodegenerative pathology in transgenic mice overexpressing V717F beta-amyloid precursor protein and Alzheimer's disease". The Journal of Neuroscience. 16 (18): 5795–811. doi:10.1523/JNEUROSCI.16-18-05795.1996. PMID 8795633.
- Hsiao K, Chapman P, Nilsen S, Eckman C, Harigaya Y, Younkin S, Yang F, Cole G (أكتوبر 1996). "Correlative memory deficits, Abeta elevation, and amyloid plaques in transgenic mice". Science. 274 (5284): 99–102. doi:10.1126/science.274.5284.99. PMID 8810256.
- Lalonde R, Dumont M, Staufenbiel M, Sturchler-Pierrat C, Strazielle C (نوفمبر 2002). "Spatial learning, exploration, anxiety, and motor coordination in female APP23 transgenic mice with the Swedish mutation". Brain Research. 956 (1): 36–44. doi:10.1016/S0006-8993(02)03476-5. PMID 12426044.
- Holmes C, Boche D, Wilkinson D, Yadegarfar G, Hopkins V, Bayer A, Jones RW, Bullock R, Love S, Neal JW, Zotova E, Nicoll JA (July 2008). "Long-term effects of Abeta42 immunisation in Alzheimer's disease: follow-up of a randomised, placebo-controlled phase I trial". Lancet. 372 (9634): 216–23. doi:10.1016/S0140-6736(08)61075-2. PMID 18640458.
- Lacor PN, Buniel MC, Furlow PW, Clemente AS, Velasco PT, Wood M, et al. (January 2007). "Abeta oligomer-induced aberrations in synapse composition, shape, and density provide a molecular basis for loss of connectivity in Alzheimer's disease". The Journal of Neuroscience. 27 (4): 796–807. doi:10.1523/JNEUROSCI.3501-06.2007. PMID 17251419.
- Laurén J, Gimbel DA, Nygaard HB, Gilbert JW, Strittmatter SM (February 2009). "Cellular prion protein mediates impairment of synaptic plasticity by amyloid-beta oligomers". Nature. 457 (7233): 1128–32. doi:10.1038/nature07761. PMC . PMID 19242475.
- Nikolaev A, McLaughlin T, O'Leary DD, Tessier-Lavigne M (February 2009). "APP binds DR6 to trigger axon pruning and neuron death via distinct caspases". Nature. 457 (7232): 981–89. Bibcode:2009Natur.457..981N. doi:10.1038/nature07767. PMC . PMID 19225519.
- Goedert M, Spillantini MG, Crowther RA (July 1991). "Tau proteins and neurofibrillary degeneration". Brain Pathology. 1 (4): 279–86. doi:10.1111/j.1750-3639.1991.tb00671.x. PMID 1669718.
- Iqbal K, Alonso A, Chen S, Chohan MO, El-Akkad E, Gong CX, Khatoon S, Li B, Liu F, Rahman A, Tanimukai H, Grundke-Iqbal I (January 2005). "Tau pathology in Alzheimer disease and other tauopathies". Biochimica et Biophysica Acta. 1739 (2–3): 198–210. doi:10.1016/j.bbadis.2004.09.008. PMID 15615638.
- Chun W, Johnson GV (January 2007). "The role of tau phosphorylation and cleavage in neuronal cell death". Frontiers in Bioscience. 12: 733–56. doi:10.2741/2097. PMID 17127334.
- Kamer, Angela R.; Craig, Ronald G.; Dasanayake, Ananda P.; Brys, Miroslaw; Glodzik-Sobanska, Lidia; de Leon, Mony J. (July 2008). "Inflammation and Alzheimer's disease: Possible role of periodontal diseases". Alzheimer's & Dementia (باللغة الإنجليزية). 4 (4): 242–250. doi:10.1016/j.jalz.2007.08.004. PMID 18631974.
- Collins, Stephen M.; Surette, Michael; Bercik, Premysl (November 2012). "The interplay between the intestinal microbiota and the brain". Nature Reviews Microbiology (باللغة الإنجليزية). 10 (11): 735–742. doi:10.1038/nrmicro2876. ISSN 1740-1526.
- Deane R, Zlokovic BV (April 2007). "Role of the blood-brain barrier in the pathogenesis of Alzheimer's disease". Current Alzheimer Research. 4 (2): 191–97. doi:10.2174/156720507780362245. PMID 17430246.
- Miklossy J (August 2011). "Alzheimer's disease - a neurospirochetosis. Analysis of the evidence following Koch's and Hill's criteria". Journal of Neuroinflammation. 8 (1): 90. doi:10.1186/1742-2094-8-90. PMC . PMID 21816039.
- Allen, HB (27 June 2016). "Alzheimer's Disease: Assessing the Role of Spirochetes, Biofilms, the Immune System, and Amyloid-β with Regard to Potential Treatment and Prevention". Journal of Alzheimer's Disease. 53 (4): 1271–76. doi:10.3233/JAD-160388. PMC . PMID 27372648.
- Xu H, Finkelstein DI, Adlard PA (12 June 2014). "Interactions of metals and Apolipoprotein E in Alzheimer's disease". Frontiers in Aging Neuroscience. 6: 121. doi:10.3389/fnagi.2014.00121. PMC . PMID 24971061.
Although we still do not know if the metal ion dyshomeostasis present in AD is a cause or consequence of the disease, there is a growing body of evidence showing a direct correlation between metal ions and key AD-related key proteins.
- Su B, Wang X, Nunomura A, Moreira PI, Lee HG, Perry G, Smith MA, Zhu X (December 2008). "Oxidative stress signaling in Alzheimer's disease". Current Alzheimer Research. 5 (6): 525–32. doi:10.2174/156720508786898451. PMC . PMID 19075578.
- Kastenholz B, Garfin DE, Horst J, Nagel KA (2009). "Plant metal chaperones: a novel perspective in dementia therapy". Amyloid. 16 (2): 81–83. doi:10.1080/13506120902879392. PMID 20536399.
- "Aluminium and Alzheimer's disease". Facts about dementia. Alzheimer's Society. مؤرشف من الأصل في 27 أكتوبر 200514 أكتوبر 2005.
- Bondy SC (January 2016). "Low levels of aluminum can lead to behavioral and morphological changes associated with Alzheimer's disease and age-related neurodegeneration". Neurotoxicology (Submitted manuscript). 52: 222–29. doi:10.1016/j.neuro.2015.12.002. PMID 26687397.
- Kandimalla R, Vallamkondu J, Corgiat EB, Gill KD (March 2016). "Understanding Aspects of Aluminum Exposure in Alzheimer's Disease Development". Brain Pathology. 26 (2): 139–54. doi:10.1111/bpa.12333. PMID 26494454.
- Santibáñez M, Bolumar F, García AM (November 2007). "Occupational risk factors in Alzheimer's disease: a review assessing the quality of published epidemiological studies". Occupational and Environmental Medicine. 64 (11): 723–32. doi:10.1136/oem.2006.028209. PMC . PMID 17525096.
- Lidsky TI (May 2014). "Is the Aluminum Hypothesis dead?". Journal of Occupational and Environmental Medicine. 56 (5 Suppl): S73–79. doi:10.1097/jom.0000000000000063. PMC . PMID 24806729.
- Yegambaram M, Manivannan B, Beach TG, Halden RU (2015). "Role of environmental contaminants in the etiology of Alzheimer's disease: a review". Current Alzheimer Research. 12 (2): 116–46. doi:10.2174/1567205012666150204121719. PMC . PMID 25654508.
- Cataldo JK, Prochaska JJ, Glantz SA (2010). "Cigarette smoking is a risk factor for Alzheimer's Disease: an analysis controlling for tobacco industry affiliation". Journal of Alzheimer's Disease. 19 (2): 465–80. doi:10.3233/JAD-2010-1240. PMC . PMID 20110594.
- Eikelenboom P, van Exel E, Hoozemans JJ, Veerhuis R, Rozemuller AJ, van Gool WA (2010). "Neuroinflammation - an early event in both the history and pathogenesis of Alzheimer's disease". Neuro-Degenerative Diseases. 7 (1–3): 38–41. doi:10.1159/000283480. PMID 20160456.
- Moulton PV, Yang W (2012). "Air pollution, oxidative stress, and Alzheimer's disease". Journal of Environmental and Public Health (Review). 2012: 1–9. doi:10.1155/2012/472751. PMC . PMID 22523504.
- Bartzokis G (August 2011). "Alzheimer's disease as homeostatic responses to age-related myelin breakdown". Neurobiology of Aging. 32 (8): 1341–71. doi:10.1016/j.neurobiolaging.2009.08.007. PMC . PMID 19775776.
- Cai Z, Xiao M (2016). "Oligodendrocytes and Alzheimer's disease". The International Journal of Neuroscience. 126 (2): 97–104. doi:10.3109/00207454.2015.1025778. PMID 26000818.
- Reisberg B, Franssen EH, Hasan SM, Monteiro I, Boksay I, Souren LE, et al. (1999). "Retrogenesis: clinical, physiologic, and pathologic mechanisms in brain aging, Alzheimer's and other dementing processes". European Archives of Psychiatry and Clinical Neuroscience. 249 Suppl 3 (3): 28–36. doi:10.1007/pl00014170. PMID 10654097.
- Alves GS, Oertel Knöchel V, Knöchel C, Carvalho AF, Pantel J, Engelhardt E, Laks J (2015). "Integrating retrogenesis theory to Alzheimer's disease pathology: insight from DTI-TBSS investigation of the white matter microstructural integrity". BioMed Research International. 2015: 291658. doi:10.1155/2015/291658. PMC . PMID 25685779.
- Brenner Carson, Verna (2015). Caregiving for Alzheimer's Disease. New York: Springer New York Academy of Sciences. صفحات 1–9. .
- Zis, Panagiotis; Hadjivassiliou, Marios (26 February 2019). "Treatment of Neurological Manifestations of Gluten Sensitivity and Coeliac Disease". Current Treatment Options in Neurology. 21 (3): 10. doi:10.1007/s11940-019-0552-7. PMID 30806821.
- Makhlouf S, Messelmani M, Zaouali J, Mrissa R (2018). "Cognitive impairment in celiac disease and non-celiac gluten sensitivity: review of literature on the main cognitive impairments, the imaging and the effect of gluten free diet". Acta Neurol Belg (Review). 118 (1): 21–27. doi:10.1007/s13760-017-0870-z. PMID 29247390.
- Wenk GL (2003). "Neuropathologic changes in Alzheimer's disease". The Journal of Clinical Psychiatry. 64 Suppl 9: 7–10. PMID 12934968.
- Braak H, Del Tredici K (December 2012). "Where, when, and in what form does sporadic Alzheimer's disease begin?". Current Opinion in Neurology. 25 (6): 708–14. doi:10.1097/WCO.0b013e32835a3432. PMID 23160422.
- Desikan RS, Cabral HJ, Hess CP, Dillon WP, Glastonbury CM, Weiner MW, Schmansky NJ, Greve DN, Salat DH, Buckner RL, Fischl B (August 2009). "Automated MRI measures identify individuals with mild cognitive impairment and Alzheimer's disease". Brain. 132 (Pt 8): 2048–57. doi:10.1093/brain/awp123. PMC . PMID 19460794.
- Moan R (20 July 2009). "MRI Software Accurately IDs Preclinical Alzheimer's Disease". Diagnostic Imaging. مؤرشف من الأصل في 16 مايو 201607 يناير 2013.
- Tiraboschi P, Hansen LA, Thal LJ, Corey-Bloom J (June 2004). "The importance of neuritic plaques and tangles to the development and evolution of AD". Neurology. 62 (11): 1984–89. doi:10.1212/01.WNL.0000129697.01779.0A. PMID 15184601.
- Bouras C, Hof PR, Giannakopoulos P, Michel JP, Morrison JH (1994). "Regional distribution of neurofibrillary tangles and senile plaques in the cerebral cortex of elderly patients: a quantitative evaluation of a one-year autopsy population from a geriatric hospital" ( كتاب إلكتروني PDF ). Cerebral Cortex. 4 (2): 138–50. doi:10.1093/cercor/4.2.138. PMID 8038565.
- Kotzbauer PT, Trojanowsk JQ, Lee VM (October 2001). "Lewy body pathology in Alzheimer's disease". Journal of Molecular Neuroscience. 17 (2): 225–32. doi:10.1385/JMN:17:2:225. PMID 11816795.
- Hashimoto M, Rockenstein E, Crews L, Masliah E (2003). "Role of protein aggregation in mitochondrial dysfunction and neurodegeneration in Alzheimer's and Parkinson's diseases". Neuromolecular Medicine. 4 (1–2): 21–36. doi:10.1385/NMM:4:1-2:21. PMID 14528050.
- Priller C, Bauer T, Mitteregger G, Krebs B, Kretzschmar HA, Herms J (يوليو 2006). "Synapse formation and function is modulated by the amyloid precursor protein". The Journal of Neuroscience. 26 (27): 7212–21. doi:10.1523/JNEUROSCI.1450-06.2006. PMC . PMID 16822978.
- Turner PR, O'Connor K, Tate WP, Abraham WC (مايو 2003). "Roles of amyloid precursor protein and its fragments in regulating neural activity, plasticity and memory". Progress in Neurobiology. 70 (1): 1–32. doi:10.1016/S0301-0082(03)00089-3. PMID 12927332.
- Hooper NM (أبريل 2005). "Roles of proteolysis and lipid rafts in the processing of the amyloid precursor protein and prion protein". Biochemical Society Transactions. 33 (Pt 2): 335–38. doi:10.1042/BST0330335. PMID 15787600.
- Ohnishi S, Takano K (مارس 2004). "Amyloid fibrils from the viewpoint of protein folding". Cellular and Molecular Life Sciences. 61 (5): 511–24. doi:10.1007/s00018-003-3264-8. PMID 15004691.
- Hernández F, Avila J (September 2007). "Tauopathies". Cellular and Molecular Life Sciences. 64 (17): 2219–33. doi:10.1007/s00018-007-7220-x. PMID 17604998.
- Sun W, Samimi H, Gamez M, Zare H, Frost B (August 2018). "Pathogenic tau-induced piRNA depletion promotes neuronal death through transposable element dysregulation in neurodegenerative tauopathies". Nature Neuroscience. 21 (8): 1038–48. doi:10.1038/s41593-018-0194-1. PMC . PMID 30038280.
- Van Broeck B, Van Broeckhoven C, Kumar-Singh S (2007). "Current insights into molecular mechanisms of Alzheimer disease and their implications for therapeutic approaches". Neuro-Degenerative Diseases. 4 (5): 349–65. doi:10.1159/000105156. PMID 17622778.
- Huang Y, Mucke L (مارس 2012). "Alzheimer mechanisms and therapeutic strategies". Cell. 148 (6): 1204–22. doi:10.1016/j.cell.2012.02.040. PMC . PMID 22424230.
- Yankner BA, Duffy LK, Kirschner DA (أكتوبر 1990). "Neurotrophic and neurotoxic effects of amyloid beta protein: reversal by tachykinin neuropeptides". Science. 250 (4978): 279–82. Bibcode:1990Sci...250..279Y. doi:10.1126/science.2218531. PMID 2218531.
- Chen X, Yan SD (ديسمبر 2006). "Mitochondrial Abeta: a potential cause of metabolic dysfunction in Alzheimer's disease". IUBMB Life. 58 (12): 686–94. doi:10.1080/15216540601047767. PMID 17424907.
- Birks JS, Harvey RJ (June 2018). "Donepezil for dementia due to Alzheimer's disease". The Cochrane Database of Systematic Reviews. 6: CD001190. doi:10.1002/14651858.CD001190.pub3. PMC . PMID 29923184.
- Birks JS, Grimley Evans J (April 2015). Birks JS (المحرر). "Rivastigmine for Alzheimer's disease". The Cochrane Database of Systematic Reviews (4): CD001191. doi:10.1002/14651858.CD001191.pub3. PMID 25858345.
- Geula C, Mesulam MM (1995). "Cholinesterases and the pathology of Alzheimer disease". Alzheimer Disease and Associated Disorders. 9 Suppl 2: 23–28. doi:10.1097/00002093-199501002-00005. PMID 8534419.
- Stahl SM (November 2000). "The new cholinesterase inhibitors for Alzheimer's disease, Part 2: illustrating their mechanisms of action". The Journal of Clinical Psychiatry. 61 (11): 813–14. doi:10.4088/JCP.v61n1101. PMID 11105732.
- Birks J (January 2006). Birks J (المحرر). "Cholinesterase inhibitors for Alzheimer's disease". The Cochrane Database of Systematic Reviews (1): CD005593. doi:10.1002/14651858.CD005593. PMID 16437532.
- Raschetti R, Albanese E, Vanacore N, Maggini M (November 2007). "Cholinesterase inhibitors in mild cognitive impairment: a systematic review of randomised trials". PLOS Medicine. 4 (11): e338. doi:10.1371/journal.pmed.0040338. PMC . PMID 18044984.
- Alldredge BK, Corelli RL, Ernst ME, Guglielmo BJ, Jacobson PA, Kradjan WA, Williams BR (2013). Applied therapeutics : the clinical use of drugs (الطبعة 10th). Baltimore: Wolters Kluwer Health/Lippincott Williams & Wilkins. صفحة 2385. .
- Lipton SA (February 2006). "Paradigm shift in neuroprotection by NMDA receptor blockade: memantine and beyond". Nature Reviews. Drug Discovery. 5 (2): 160–70. doi:10.1038/nrd1958. PMID 16424917.
- "Memantine". US National Library of Medicine (Medline). 4 January 2004. مؤرشف من الأصل في 22 فبراير 201003 فبراير 2010.
- McShane R, Westby MJ, Roberts E, Minakaran N, Schneider L, Farrimond LE, Maayan N, Ware J, Debarros J (May 2019). "Memantine for dementia". The Cochrane Database of Systematic Reviews. 3 (3): CD003154. doi:10.1002/14651858.CD003154.pub6. PMC . PMID 30891742.
- "Namenda prescribing information" ( كتاب إلكتروني PDF ). Forest Pharmaceuticals. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 27 فبراير 200819 فبراير 2008. (primary source)
- Raina P, Santaguida P, Ismaila A, Patterson C, Cowan D, Levine M, Booker L, Oremus M (March 2008). "Effectiveness of cholinesterase inhibitors and memantine for treating dementia: evidence review for a clinical practice guideline". Annals of Internal Medicine. 148 (5): 379–97. doi:10.7326/0003-4819-148-5-200803040-00009. PMID 18316756.
- Ballard C, Waite J (January 2006). Ballard CG (المحرر). "The effectiveness of atypical antipsychotics for the treatment of aggression and psychosis in Alzheimer's disease". The Cochrane Database of Systematic Reviews (1): CD003476. doi:10.1002/14651858.CD003476.pub2. PMID 16437455.
- Ballard C, Hanney ML, Theodoulou M, Douglas S, McShane R, Kossakowski K, Gill R, Juszczak E, Yu LM, Jacoby R (February 2009). "The dementia antipsychotic withdrawal trial (DART-AD): long-term follow-up of a randomised placebo-controlled trial". The Lancet Neurology. 8 (2): 151–57. doi:10.1016/S1474-4422(08)70295-3. PMID 19138567. ضع ملخصا.
- Declercq T, Petrovic M, Azermai M, Vander Stichele R, De Sutter AI, van Driel ML, Christiaens T (March 2013). "Withdrawal versus continuation of chronic antipsychotic drugs for behavioural and psychological symptoms in older people with dementia" ( كتاب إلكتروني PDF ). The Cochrane Database of Systematic Reviews. 3 (3): CD007726. doi:10.1002/14651858.CD007726.pub2. hdl:1854/LU-3109108. PMID 23543555.
- Li J, Wu HM, Zhou RL, Liu GJ, Dong BR (April 2008). Wu HM (المحرر). "Huperzine A for Alzheimer's disease". The Cochrane Database of Systematic Reviews (2): CD005592. doi:10.1002/14651858.CD005592.pub2. PMID 18425924.
- Rabins PV, Blacker D, Rovner BW, Rummans T, Schneider LS, Tariot PN, et al. (Steering Committee on Practice Guidelines) (December 2007). "American Psychiatric Association practice guideline for the treatment of patients with Alzheimer's disease and other dementias. Second edition". The American Journal of Psychiatry. 164 (12 Suppl): 5–56. PMID 18340692.
- Bottino CM, Carvalho IA, Alvarez AM, Avila R, Zukauskas PR, Bustamante SE, et al. (December 2005). "Cognitive rehabilitation combined with drug treatment in Alzheimer's disease patients: a pilot study". Clinical Rehabilitation. 19 (8): 861–69. doi:10.1191/0269215505cr911oa. PMID 16323385.
- Doody RS, Stevens JC, Beck C, Dubinsky RM, Kaye JA, Gwyther L, et al. (May 2001). "Practice parameter: management of dementia (an evidence-based review). Report of the Quality Standards Subcommittee of the American Academy of Neurology". Neurology. 56 (9): 1154–66. doi:10.1212/WNL.56.9.1154. PMID 11342679.
- Hermans DG, Htay UH, McShane R (January 2007). "Non-pharmacological interventions for wandering of people with dementia in the domestic setting". The Cochrane Database of Systematic Reviews (1): CD005994. doi:10.1002/14651858.CD005994.pub2. PMC . PMID 17253573.
- Robinson L, Hutchings D, Dickinson HO, Corner L, Beyer F, Finch T, Hughes J, Vanoli A, Ballard C, Bond J (January 2007). "Effectiveness and acceptability of non-pharmacological interventions to reduce wandering in dementia: a systematic review". International Journal of Geriatric Psychiatry. 22 (1): 9–22. doi:10.1002/gps.1643. PMID 17096455.
- Abraha I, Rimland JM, Trotta FM, Dell'Aquila G, Cruz-Jentoft A, Petrovic M, Gudmundsson A, Soiza R, O'Mahony D, Guaita A, Cherubini A (March 2017). "Systematic review of systematic reviews of non-pharmacological interventions to treat behavioural disturbances in older patients with dementia. The SENATOR-OnTop series". BMJ Open. 7 (3): e012759. doi:10.1136/bmjopen-2016-012759. PMC . PMID 28302633.
- Chung JC, Lai CK, Chung PM, French HP (2002). "Snoezelen for dementia". The Cochrane Database of Systematic Reviews (4): CD003152. doi:10.1002/14651858.CD003152. PMID 12519587.
- Woods B, O'Philbin L, Farrell EM, Spector AE, Orrell M (March 2018). "Reminiscence therapy for dementia". The Cochrane Database of Systematic Reviews. 3: CD001120. doi:10.1002/14651858.CD001120.pub3. PMC . PMID 29493789.
- Zetteler J (November 2008). "Effectiveness of simulated presence therapy for individuals with dementia: a systematic review and meta-analysis". Aging & Mental Health. 12 (6): 779–85. doi:10.1080/13607860802380631. PMID 19023729.
- Neal M, Barton Wright P (2003). Neal M (المحرر). "Validation therapy for dementia". The Cochrane Database of Systematic Reviews (3): CD001394. doi:10.1002/14651858.CD001394. PMID 12917907.
- Chung JC, Lai CK, Chung PM, French HP (2002). Chung JC (المحرر). "Snoezelen for dementia". The Cochrane Database of Systematic Reviews (4): CD003152. doi:10.1002/14651858.CD003152. PMID 12519587. (up to date as of 2009)
- Spector A, Thorgrimsen L, Woods B, Royan L, Davies S, Butterworth M, Orrell M (September 2003). "Efficacy of an evidence-based cognitive stimulation therapy programme for people with dementia: randomised controlled trial". The British Journal of Psychiatry. 183 (3): 248–54. doi:10.1192/bjp.183.3.248. PMID 12948999.
- Gitlin LN, Corcoran M, Winter L, Boyce A, Hauck WW (February 2001). "A randomized, controlled trial of a home environmental intervention: effect on efficacy and upset in caregivers and on daily function of persons with dementia". The Gerontologist. 41 (1): 4–14. doi:10.1093/geront/41.1.4. PMID 11220813.
- Gitlin LN, Hauck WW, Dennis MP, Winter L (March 2005). "Maintenance of effects of the home environmental skill-building program for family caregivers and individuals with Alzheimer's disease and related disorders". The Journals of Gerontology. Series A, Biological Sciences and Medical Sciences. 60 (3): 368–74. doi:10.1093/gerona/60.3.368. PMID 15860476.
- "Treating Behavioral and Psychiatric Symptoms". Alzheimer's Association. 2006. مؤرشف من الأصل في 25 سبتمبر 200625 سبتمبر 2006.
- Dunne TE, Neargarder SA, Cipolloni PB, Cronin-Golomb A (August 2004). "Visual contrast enhances food and liquid intake in advanced Alzheimer's disease". Clinical Nutrition. 23 (4): 533–38. doi:10.1016/j.clnu.2003.09.015. PMID 15297089.
- Dudek SG (2007). Nutrition Essentials for Nursing Practice. Hagerstown, Maryland: Lippincott Williams & Wilkins. صفحة 360. 19 أغسطس 2008.
- Dennehy C (2006). "Analysis of patients' rights: dementia and PEG insertion". British Journal of Nursing. 15 (1): 18–20. doi:10.12968/bjon.2006.15.1.20303. PMID 16415742.
- Chernoff R (April 2006). "Tube feeding patients with dementia". Nutrition in Clinical Practice. 21 (2): 142–46. doi:10.1177/0115426506021002142. PMID 16556924.
- Gambassi G, Landi F, Lapane KL, Sgadari A, Mor V, Bernabei R (July 1999). "Predictors of mortality in patients with Alzheimer's disease living in nursing homes". Journal of Neurology, Neurosurgery, and Psychiatry. 67 (1): 59–65. doi:10.1136/jnnp.67.1.59. PMC . PMID 10369823.
- Medical issues:
- Head B (January 2003). "Palliative care for persons with dementia". Home Healthcare Nurse. 21 (1): 53–60, quiz 61. doi:10.1097/00004045-200301000-00012. PMID 12544465.
- Friedlander AH, Norman DC, Mahler ME, Norman KM, Yagiela JA (September 2006). "Alzheimer's disease: psychopathology, medical management and dental implications". Journal of the American Dental Association. 137 (9): 1240–51. doi:10.14219/jada.archive.2006.0381. PMID 16946428.
- Belmin J (2007). "Practical guidelines for the diagnosis and management of weight loss in Alzheimer's disease: a consensus from appropriateness ratings of a large expert panel". The Journal of Nutrition, Health & Aging. 11 (1): 33–37. PMID 17315078.
- McCurry SM, Gibbons LE, Logsdon RG, Vitiello M, Teri L (October 2003). "Training caregivers to change the sleep hygiene practices of patients with dementia: the NITE-AD project". Journal of the American Geriatrics Society. 51 (10): 1455–60. doi:10.1046/j.1532-5415.2003.51466.x. PMID 14511168.
- Perls TT, Herget M (December 1995). "Higher respiratory infection rates on an Alzheimer's special care unit and successful intervention". Journal of the American Geriatrics Society. 43 (12): 1341–44. doi:10.1111/j.1532-5415.1995.tb06611.x. PMID 7490383.
- Shega JW, Levin A, Hougham GW, Cox-Hayley D, Luchins D, Hanrahan P, Stocking C, Sachs GA (April 2003). "Palliative Excellence in Alzheimer Care Efforts (PEACE): a program description". Journal of Palliative Medicine. 6 (2): 315–20. doi:10.1089/109662103764978641. PMID 12854952.
- Zanetti O, Solerte SB, Cantoni F (2009). "Life expectancy in Alzheimer's disease (AD)". Archives of Gerontology and Geriatrics. 49 Suppl 1: 237–43. doi:10.1016/j.archger.2009.09.035. PMID 19836639.
- Mölsä PK, Marttila RJ, Rinne UK (March 1995). "Long-term survival and predictors of mortality in Alzheimer's disease and multi-infarct dementia". Acta Neurologica Scandinavica. 91 (3): 159–64. doi:10.1111/j.1600-0404.1995.tb00426.x. PMID 7793228.
- Bowen JD, Malter AD, Sheppard L, Kukull WA, McCormick WC, Teri L, Larson EB (August 1996). "Predictors of mortality in patients diagnosed with probable Alzheimer's disease". Neurology. 47 (2): 433–39. doi:10.1212/wnl.47.2.433. PMID 8757016.
- Larson EB, Shadlen MF, Wang L, McCormick WC, Bowen JD, Teri L, Kukull WA (April 2004). "Survival after initial diagnosis of Alzheimer disease". Annals of Internal Medicine. 140 (7): 501–09. doi:10.7326/0003-4819-140-7-200404060-00008. PMID 15068977.
- Jagger C, Clarke M, Stone A (January 1995). "Predictors of survival with Alzheimer's disease: a community-based study". Psychological Medicine. 25 (1): 171–77. doi:10.1017/S0033291700028191. PMID 7792352.
- Dodge HH, Shen C, Pandav R, DeKosky ST, Ganguli M (February 2003). "Functional transitions and active life expectancy associated with Alzheimer disease". Archives of Neurology. 60 (2): 253–59. doi:10.1001/archneur.60.2.253. PMID 12580712.
- Ganguli M, Dodge HH, Shen C, Pandav RS, DeKosky ST (May 2005). "Alzheimer disease and mortality: a 15-year epidemiological study". Archives of Neurology. 62 (5): 779–84. doi:10.1001/archneur.62.5.779. PMID 15883266.
- Bermejo-Pareja F, Benito-León J, Vega S, Medrano MJ, Román GC (January 2008). "Incidence and subtypes of dementia in three elderly populations of central Spain". Journal of the Neurological Sciences. 264 (1–2): 63–72. doi:10.1016/j.jns.2007.07.021. PMID 17727890.
- Di Carlo A, Baldereschi M, Amaducci L, Lepore V, Bracco L, Maggi S, Bonaiuto S, Perissinotto E, Scarlato G, Farchi G, Inzitari D (January 2002). "Incidence of dementia, Alzheimer's disease, and vascular dementia in Italy. The ILSA Study". Journal of the American Geriatrics Society. 50 (1): 41–48. doi:10.1046/j.1532-5415.2002.50006.x. PMID 12028245.
- Andersen K, Launer LJ, Dewey ME, Letenneur L, Ott A, Copeland JR, et al. (December 1999). "Gender differences in the incidence of AD and vascular dementia: The EURODEM Studies. EURODEM Incidence Research Group". Neurology. 53 (9): 1992–97. doi:10.1212/wnl.53.9.1992. PMID 10599770.
- Tejada-Vera B. (2013). Mortality from Alzheimer's Disease in the United States: Data for 2000 and 2010. Hyattsville, MD: U.S. Department of Health and Human Services, Centers for Disease Control and Prevention, National Center for Health Statistics.
- 2000 U.S. estimates:
- Hebert LE, Scherr PA, Bienias JL, Bennett DA, Evans DA (August 2003). "Alzheimer disease in the US population: prevalence estimates using the 2000 census". Archives of Neurology. 60 (8): 1119–22. doi:10.1001/archneur.60.8.1119. PMID 12925369.
- "Profiles of General Demographic Characteristics, 2000 Census of Population and Housing, United States" ( كتاب إلكتروني PDF ). U.S. Census Bureau. 2001. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 19 أغسطس 200827 أغسطس 2008.
- Ferri CP, Prince M, Brayne C, Brodaty H, Fratiglioni L, Ganguli M, Hall K, Hasegawa K, Hendrie H, Huang Y, Jorm A, Mathers C, Menezes PR, Rimmer E, Scazufca M (December 2005). "Global prevalence of dementia: a Delphi consensus study". Lancet. 366 (9503): 2112–17. doi:10.1016/S0140-6736(05)67889-0. PMC . PMID 16360788.
- World Health Organization (2006). Neurological Disorders: Public Health Challenges. Switzerland: World Health Organization. صفحات 204–07. . مؤرشف من الأصل في 10 فبراير 2010.
-
2006 prevalence estimate:
- Brookmeyer R, Johnson E, Ziegler-Graham K, Arrighi HM (July 2007). "Forecasting the global burden of Alzheimer's disease". Alzheimer's & Dementia. 3 (3): 186–91. CiteSeerX . doi:10.1016/j.jalz.2007.04.381. PMID 19595937. مؤرشف من الأصل في 07 ديسمبر 200818 يونيو 2008.
- "Highlights" ( كتاب إلكتروني PDF ). World Population Prospects: The 2006 Revision. Population Division, Department of Economic and Social Affairs, United Nations. 2007. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 19 أغسطس 200827 أغسطس 2008.
- Auguste D.:
- Alzheimer A (1907). "Über eine eigenartige Erkrankung der Hirnrinde". Allgemeine Zeitschrift für Psychiatrie und Psychisch-Gerichtlich Medizin (باللغة الألمانية). 64 (1–2): 146–48.
- Alzheimer A (1987). تُرجم بواسطة H. Greenson. "About a peculiar disease of the cerebral cortex. By Alois Alzheimer, 1907 (Translated by L. Jarvik and H. Greenson)". Alzheimer Disease and Associated Disorders. 1 (1): 3–8. PMID 3331112.
- Ulrike M, Konrad M (2003). Alzheimer: The Life of a Physician and the Career of a Disease. New York: Columbia University Press. صفحة 270. .
- Berrios GE (1990). "Alzheimer's Disease: A Conceptual History". Int. J. Geriatr. Psychiatry. 5 (6): 355–65. doi:10.1002/gps.930050603.
- Kraepelin Emil (2007). Clinical Psychiatry: A Textbook For Students And Physicians (Reprint ). تُرجم بواسطة Diefendorf A. Ross. Kessinger Publishing. صفحة 568. .
- Katzman R, Terry RD, Bick KL, المحررون (1978). Alzheimer's Disease: Senile Dementia and Related Disorders. New York: Raven Press. صفحة 595. .
- Boller F, Forbes MM (June 1998). "History of dementia and dementia in history: an overview". Journal of the Neurological Sciences. 158 (2): 125–33. doi:10.1016/S0022-510X(98)00128-2. PMID 9702682.
- Amaducci LA, Rocca WA, Schoenberg BS (November 1986). "Origin of the distinction between Alzheimer's disease and senile dementia: how history can clarify nosology". Neurology. 36 (11): 1497–9. doi:10.1212/wnl.36.11.1497. PMID 3531918.
- Allegri RF, Butman J, Arizaga RL, Machnicki G, Serrano C, Taragano FE, Sarasola D, Lon L (August 2007). "Economic impact of dementia in developing countries: an evaluation of costs of Alzheimer-type dementia in Argentina". International Psychogeriatrics. 19 (4): 705–18. doi:10.1017/S1041610206003784. PMID 16870037.
- Suh GH, Knapp M, Kang CJ (August 2006). "The economic costs of dementia in Korea, 2002". International Journal of Geriatric Psychiatry. 21 (8): 722–28. doi:10.1002/gps.1552. PMID 16858741.
- Wimo A, Jonsson L, Winblad B (2006). "An estimate of the worldwide prevalence and direct costs of dementia in 2003". Dementia and Geriatric Cognitive Disorders. 21 (3): 175–81. doi:10.1159/000090733. PMID 16401889.
- Moore MJ, Zhu CW, Clipp EC (July 2001). "Informal costs of dementia care: estimates from the National Longitudinal Caregiver Study". The Journals of Gerontology. Series B, Psychological Sciences and Social Sciences. 56 (4): S219–28. doi:10.1093/geronb/56.4.S219. PMID 11445614.
- Jönsson L, Eriksdotter Jönhagen M, Kilander L, Soininen H, Hallikainen M, Waldemar G, et al. (May 2006). "Determinants of costs of care for patients with Alzheimer's disease". International Journal of Geriatric Psychiatry. 21 (5): 449–59. doi:10.1002/gps.1489. PMID 16676288.
- "The MetLife study of Alzheimer's disease: The caregiving experience" ( كتاب إلكتروني PDF ). MetLife Mature Market Institute. August 2006. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 08 يناير 201105 فبراير 2011.
- Schneider J, Murray J, Banerjee S, Mann A (August 1999). "EUROCARE: a cross-national study of co-resident spouse carers for people with Alzheimer's disease: I – Factors associated with carer burden". International Journal of Geriatric Psychiatry. 14 (8): 651–61. doi:10.1002/(SICI)1099-1166(199908)14:8<651::AID-GPS992>3.0.CO;2-B. PMID 10489656.
- Murray J, Schneider J, Banerjee S, Mann A (August 1999). "EUROCARE: a cross-national study of co-resident spouse carers for people with Alzheimer's disease: II – A qualitative analysis of the experience of caregiving". International Journal of Geriatric Psychiatry. 14 (8): 662–67. doi:10.1002/(SICI)1099-1166(199908)14:8<662::AID-GPS993>3.0.CO;2-4. PMID 10489657.
- Zhu CW, Sano M (2006). "Economic considerations in the management of Alzheimer's disease". Clinical Interventions in Aging. 1 (2): 143–54. doi:10.2147/ciia.2006.1.2.143. PMC . PMID 18044111.
- Gaugler JE, Kane RL, Kane RA, Newcomer R (April 2005). "Early community-based service utilization and its effects on institutionalization in dementia caregiving". The Gerontologist. 45 (2): 177–85. doi:10.1093/geront/45.2.177. PMID 15799982.
- Ritchie K, Lovestone S (November 2002). "The dementias". Lancet. 360 (9347): 1759–66. doi:10.1016/S0140-6736(02)11667-9. PMID 12480441.
- Brodaty H, Hadzi-Pavlovic D (September 1990). "Psychosocial effects on carers of living with persons with dementia". The Australian and New Zealand Journal of Psychiatry. 24 (3): 351–61. doi:10.3109/00048679009077702. PMID 2241719.
- Donaldson C, Tarrier N, Burns A (April 1998). "Determinants of carer stress in Alzheimer's disease". International Journal of Geriatric Psychiatry. 13 (4): 248–56. doi:10.1002/(SICI)1099-1166(199804)13:4<248::AID-GPS770>3.0.CO;2-0. PMID 9646153.
- Pusey H, Richards D (May 2001). "A systematic review of the effectiveness of psychosocial interventions for carers of people with dementia". Aging & Mental Health. 5 (2): 107–19. doi:10.1080/13607860120038302. PMID 11511058.
- Garrard P., Maloney L.M., Hodges J.R., Patterson K. (2 2005). "The effects of very early Alzheimer's disease on the characteristics of writing by a renowned author" (journal) (باللغة الإنجليزية). 128 (Pt 2) (الطبعة ). Oxford University Press: 250–260. doi:10.1093/brain/awh341. PMID 15574466.
- Sherman F.T. (9 2004). "Did President Reagan have mild cognitive impairment while in office? Living longer with Alzheimer's Disease" (journal) (باللغة الإنجليزية). 59 (9) (الطبعة Geriatrics): 11, 15. PMID 15461232.
- "Hungary legend Puskas dies at 79". BBC News. 2006-11-17. مؤرشف من الأصل في 25 أغسطس 201125 يناير 2008.
- "Prime Ministers in History: Harold Wilson". London: 10 Downing Street. مؤرشف من الأصل في 25 أغسطس 201118 أغسطس 2008.
- "Mi padre no reconoció al Rey pero notó el cariño". Madrid: El País. 2008. مؤرشف من الأصل في 25 أغسطس 201101 أكتوبر 2008.
- Peter Falk leidet an Alzheimer
- "Chicago Rita Hayworth Gala". Alzheimer’s Association. 2007. مؤرشف من الأصل في 25 أغسطس 201125 يناير 2008.
- "Charlton Heston has Alzheimer's symptoms". CNN. 2002-08-09. مؤرشف من الأصل في 25 أغسطس 201125 يناير 2008.
- Pauli Michelle (2007-12-12). "Pratchett announces he has Alzheimer's". Guardian News and Media18 أغسطس 2008.
- Bayley J (2000). Iris: A Memoir of Iris Murdoch. London: Abacus. . OCLC 41960006.
- Sparks N (1996). The notebook. Thorndike, Maine: Thorndike Press. صفحة 268. .
- "Thanmathra". Webindia123.com. مؤرشف من الأصل في 06 نوفمبر 200724 يناير 2008.
- Ogiwara H (2004). Ashita no Kioku (باللغة اليابانية). Tōkyō: Kōbunsha. . OCLC 57352130.
- Munro A (2001). Hateship, Friendship, Courtship, Loveship, Marriage: Stories. New York: A.A. Knopf. . OCLC 46929223.
- "Malcolm and Barbara: A love story". Dfgdocs. مؤرشف من الأصل في 24 مايو 200824 يناير 2008.
- "Malcolm and Barbara: A love story". BBC Cambridgeshire. مؤرشف من الأصل في 10 نوفمبر 201202 مارس 2008.
- Plunkett J (7 August 2007). "Alzheimer's film-maker to face ITV lawyers". London: Guardian Media. مؤرشف من الأصل في 15 يناير 200824 يناير 2008.
- "أفلام عربية وأجنبية تناولت مرض ألزهايمر". البوابة نيوز15 أبريل 2020.
- Cummings JL, Morstorf T, Zhong K (July 2014). "Alzheimer's disease drug-development pipeline: few candidates, frequent failures". Alzheimer's Research & Therapy. 6 (4): 37. doi:10.1186/alzrt269. PMC . PMID 25024750.
- Gutis, Phillip S. (22 March 2019). "An Alzheimer's Drug Trial Gave Me Hope, and Then It Ended". The New York Times25 مارس 2019.
- Lashuel HA, Hartley DM, Balakhaneh D, Aggarwal A, Teichberg S, Callaway DJ (November 2002). "New class of inhibitors of amyloid-beta fibril formation. Implications for the mechanism of pathogenesis in Alzheimer's disease". The Journal of Biological Chemistry. 277 (45): 42881–90. doi:10.1074/jbc.M206593200. PMID 12167652.
- Dodel R, Neff F, Noelker C, Pul R, Du Y, Bacher M, Oertel W (March 2010). "Intravenous immunoglobulins as a treatment for Alzheimer's disease: rationale and current evidence". Drugs. 70 (5): 513–28. doi:10.2165/11533070-000000000-00000. PMID 20329802. مؤرشف من الأصل في 17 سبتمبر 2011.
- Vaccination:
- Hawkes CA, McLaurin J (November 2007). "Immunotherapy as treatment for Alzheimer's disease". Expert Review of Neurotherapeutics. 7 (11): 1535–48. doi:10.1586/14737175.7.11.1535. PMID 17997702.
- Solomon B (June 2007). "Clinical immunologic approaches for the treatment of Alzheimer's disease". Expert Opinion on Investigational Drugs. 16 (6): 819–28. doi:10.1517/13543784.16.6.819. PMID 17501694.
- Woodhouse A, Dickson TC, Vickers JC (2007). "Vaccination strategies for Alzheimer's disease: A new hope?". Drugs & Aging. 24 (2): 107–19. doi:10.2165/00002512-200724020-00003. PMID 17313199.
- "Study Evaluating ACC-001 in Mild to Moderate Alzheimers Disease Subjects". Clinical Trial. US National Institutes of Health. 11 March 2008. مؤرشف من الأصل في 30 يوليو 201305 يونيو 2008.
- "Study Evaluating Safety, Tolerability, and Immunogenicity of ACC-001 in Subjects with Alzheimer's Disease". US National Institutes of Health. مؤرشف من الأصل في 29 أكتوبر 200805 يونيو 2008.
- "Alzheimer's Disease Vaccine Trial Suspended on Safety Concern". Medpage Today. 18 April 2008. مؤرشف من الأصل في 23 أبريل 200814 يونيو 2008.
- "Bapineuzumab in Patients with Mild to Moderate Alzheimer's Disease/ Apo_e4 Non-carriers" (Clinical Trial). US National Institutes of Health. 29 February 2008. مؤرشف من الأصل في 22 مارس 200823 مارس 2008.
- Sperling RA, Jack CR, Black SE, Frosch MP, Greenberg SM, Hyman BT, Scheltens P, Carrillo MC, Thies W, Bednar MM, Black RS, Brashear HR, Grundman M, Siemers ER, Feldman HH, Schindler RJ (July 2011). "Amyloid-related imaging abnormalities in amyloid-modifying therapeutic trials: recommendations from the Alzheimer's Association Research Roundtable Workgroup". Alzheimer's & Dementia. 7 (4): 367–85. doi:10.1016/j.jalz.2011.05.2351. PMC . PMID 21784348.
- "Safety, Tolerability and Efficacy Study to Evaluate Subjects with Mild Cognitive Impairment" (Clinical Trial). US National Institutes of Health. 11 March 2008. مؤرشف من الأصل في 22 أكتوبر 200823 مارس 2008.
- "Study Evaluating the Safety, Tolerability and Efficacy of PBT2 in Patients with Early Alzheimer's Disease" (Clinical Trial). US National Institutes of Health. 13 January 2008. مؤرشف من الأصل في 31 أغسطس 200823 مارس 2008.
- Etanercept research:
- Tobinick E (September 2009). "Tumour necrosis factor modulation for treatment of Alzheimer's disease: rationale and current evidence". CNS Drugs. 23 (9): 713–25. doi:10.2165/11310810-000000000-00000. PMID 19689163.
- Tobinick E, Gross H, Weinberger A, Cohen H (April 2006). "TNF-alpha modulation for treatment of Alzheimer's disease: a 6-month pilot study". MedGenMed. 8 (2): 25. PMC . PMID 16926764.
- Griffin WS (January 2008). "Perispinal etanercept: potential as an Alzheimer therapeutic". Journal of Neuroinflammation. 5: 3. doi:10.1186/1742-2094-5-3. PMC . PMID 18186919.
- Tobinick E (December 2007). "Perispinal etanercept for treatment of Alzheimer's disease". Current Alzheimer Research. 4 (5): 550–52. doi:10.2174/156720507783018217. PMID 18220520.
- Cheng X, Shen Y, Li R (November 2014). "Targeting TNF: a therapeutic strategy for Alzheimer's disease". Drug Discovery Today. 19 (11): 1822–27. doi:10.1016/j.drudis.2014.06.029. PMID 24998784.
- Wischik CM, Bentham P, Wischik DJ, Seng KM (July 2008). "Tau aggregation inhibitor (TAI) therapy with remberTM arrests disease progression in mild and moderate Alzheimer's disease over 50 weeks". Alzheimer's & Dementia. 4 (4): T167. doi:10.1016/j.jalz.2008.05.43830 يوليو 2008.
- Harrington C, Rickard J, Horsley D (July 2008). "Methylthioninium chloride (MTC) acts as a tau aggregation inhibitor (TAI) in a cellular model and reverses tau pathology in transgenic mouse models of Alzheimer's disease". Alzheimer's & Dementia. 4 (4): T120–21. doi:10.1016/j.jalz.2008.05.259.
- Doody RS, Gavrilova SI, Sano M, Thomas RG, Aisen PS, Bachurin SO, Seely L, Hung D (July 2008). "Effect of dimebon on cognition, activities of daily living, behaviour, and global function in patients with mild-to-moderate Alzheimer's disease: a randomised, double-blind, placebo-controlled study". Lancet. 372 (9634): 207–15. doi:10.1016/S0140-6736(08)61074-0. PMID 18640457.
- Bezprozvanny I (October 2010). "The rise and fall of Dimebon". Drug News & Perspectives (Original article). 23 (8): 518–23. doi:10.1358/dnp.2010.23.8.1500435. PMC . PMID 21031168.
- "Pfizer And Medivation announce results from two phase 3 studies in Dimebon (latrepirdine*) Alzheimer's disease clinical development program (NASDAQ:MDVN)" (Press release). مؤرشف من الأصل في 04 سبتمبر 201216 نوفمبر 2012.
- Wendler A, Wehling M (March 2012). "Translatability scoring in drug development: eight case studies". Journal of Translational Medicine. 10 (1): 39. doi:10.1186/1479-5876-10-39. PMC . PMID 22397594.
- Baddeley TC, McCaffrey J, Storey JM, Cheung JK, Melis V, Horsley D, Harrington CR, Wischik CM (January 2015). "Complex disposition of methylthioninium redox forms determines efficacy in tau aggregation inhibitor therapy for Alzheimer's disease". The Journal of Pharmacology and Experimental Therapeutics. 352 (1): 110–18. doi:10.1124/jpet.114.219352. PMID 25320049.
- Wischik CM, Harrington CR, Storey JM (April 2014). "Tau-aggregation inhibitor therapy for Alzheimer's disease". Biochemical Pharmacology. 88 (4): 529–39. doi:10.1016/j.bcp.2013.12.008. PMID 24361915.
- Feuerstein, Adam (14 February 2017). "Merck Alzheimer's Drug Study Halted Early for Futility". New York City: TheStreet, Inc. مؤرشف من الأصل في 16 فبراير 2017. Merck Alzheimer's Drug Study Halted Early for Futility Independent study monitors concluded that there was "virtually no chance of finding a positive clinical effect."
- "After A Big Failure, Scientists And Patients Hunt For A New Type Of Alzheimer's Drug". NPR.org17 مايو 2019.
- Gallagher, James (2 May 2019). "Dementia is 'greatest health challenge"17 مايو 2019.
- "First drug that can slow Alzheimer's dementia". BBC News. 22 October 2019.
- Morley, John E.; Armbrecht, Harvey James; Farr, Susan A.; Kumar, Vijaya B. (May 2012). "The senescence accelerated mouse (SAMP8) as a model for oxidative stress and Alzheimer's disease". Biochimica et Biophysica Acta (BBA) - Molecular Basis of Disease. 1822 (5): 650–656. doi:10.1016/j.bbadis.2011.11.015. ISSN 0925-4439. PMID 22142563.
- Marciniak R, Sheardova K, Cermáková P, Hudeček D, Sumec R, Hort J (2014). "Effect of meditation on cognitive functions in context of aging and neurodegenerative diseases". Frontiers in Behavioral Neuroscience. 8: 17. doi:10.3389/fnbeh.2014.00017. PMC . PMID 24478663.
- Larouche E, Hudon C, Goulet S (January 2015). "Potential benefits of mindfulness-based interventions in mild cognitive impairment and Alzheimer's disease: an interdisciplinary perspective". Behavioural Brain Research. 276 (276): 199–212. doi:10.1016/j.bbr.2014.05.058. PMID 24893317.
- Jaunmuktane Z, Mead S, Ellis M, Wadsworth JD, Nicoll AJ, Kenny J, et al. (September 2015). "Evidence for human transmission of amyloid-β pathology and cerebral amyloid angiopathy". Nature. 525 (7568): 247–50. Bibcode:2015Natur.525..247J. doi:10.1038/nature15369. PMID 26354483.
- Abbott A (September 2015). "Autopsies reveal signs of Alzheimer's in growth-hormone patients". Nature. 525 (7568): 165–66. Bibcode:2015Natur.525..165A. doi:10.1038/525165a. PMID 26354460.
- Martin C, Solís L, Concha MI, Otth C (June 2011). "[Herpes simplex virus type 1 as risk factor associated to Alzheimer disease]". Revista Médica de Chile (باللغة الإسبانية). 139 (6): 779–86. doi:10.4067/S0034-98872011000600013. PMID 22051760.
- Wozniak MA, Mee AP, Itzhaki RF (January 2009). "Herpes simplex virus type 1 DNA is located within Alzheimer's disease amyloid plaques". The Journal of Pathology (Original study). 217 (1): 131–38. doi:10.1002/path.2449. PMID 18973185.
- Itzhaki RF (2014). "Herpes simplex virus type 1 and Alzheimer's disease: increasing evidence for a major role of the virus". Frontiers in Aging Neuroscience. 6: 202. doi:10.3389/fnagi.2014.00202. PMC . PMID 25157230.
- Itzhaki RF, Lathe R, Balin BJ, Ball MJ, Bearer EL, Braak H, et al. (2016). "Microbes and Alzheimer's Disease". Journal of Alzheimer's Disease. 51 (4): 979–84. doi:10.3233/JAD-160152. PMC . PMID 26967229. مؤرشف من الأصل في 10 نوفمبر 2016.
- Alonso R, Pisa D, Rábano A, Carrasco L (July 2014). "Alzheimer's disease and disseminated mycoses". European Journal of Clinical Microbiology & Infectious Diseases. 33 (7): 1125–32. doi:10.1007/s10096-013-2045-z. PMID 24452965.
- Pisa D, Alonso R, Rábano A, Rodal I, Carrasco L (October 2015). "Different Brain Regions are Infected with Fungi in Alzheimer's Disease". Scientific Reports. 5: 15015. Bibcode:2015NatSR...515015P. doi:10.1038/srep15015. PMC . PMID 26468932.
- "Fungus, the bogeyman". The Economist. 2015-10-22. مؤرشف من الأصل في 08 أغسطس 2017.
- Kumar DK, Choi SH, Washicosky KJ, Eimer WA, Tucker S, Ghofrani J, Lefkowitz A, McColl G, Goldstein LE, Tanzi RE, Moir RD (May 2016). "Amyloid-β peptide protects against microbial infection in mouse and worm models of Alzheimer's disease". Science Translational Medicine. 8 (340): 340ra72. doi:10.1126/scitranslmed.aaf1059. PMC . PMID 27225182.
- Kolata, Gina (2016-05-25). "Could Alzheimer's Stem From Infections? It Makes Sense, Experts Say". The New York Times. مؤرشف من الأصل في 04 فبراير 2017.
- "Alzheimer's culprit may fight other diseases". Science News. 2016-06-16. مؤرشف من الأصل في 26 مايو 2016.
- Dougall NJ, Bruggink S, Ebmeier KP (2004). "Systematic review of the diagnostic accuracy of 99mTc-HMPAO-SPECT in dementia". The American Journal of Geriatric Psychiatry. 12 (6): 554–70. doi:10.1176/appi.ajgp.12.6.554. PMID 15545324.
- Carpenter AP, Pontecorvo MJ, Hefti FF, Skovronsky DM (August 2009). "The use of the exploratory IND in the evaluation and development of 18F-PET radiopharmaceuticals for amyloid imaging in the brain: a review of one company's experience". The Quarterly Journal of Nuclear Medicine and Molecular Imaging. 53 (4): 387–93. PMID 19834448.
- Leung K (8 April 2010). "(E)-4-(2-(6-(2-(2-(2-(18F-fluoroethoxy)ethoxy)ethoxy)pyridin-3-yl)vinyl)-N-methyl benzenamine [[18F]AV-45]". Molecular Imaging and Contrast Agent Database. مؤرشف من الأصل في 07 يونيو 201024 يونيو 2010.
- Rabinovici GD, Jagust WJ (2009). "Amyloid imaging in aging and dementia: testing the amyloid hypothesis in vivo". Behavioural Neurology. 21 (1): 117–28. doi:10.1155/2009/609839. PMC . PMID 19847050. مؤرشف من الأصل في 30 يوليو 2013.
- O'Brien JT (December 2007). "Role of imaging techniques in the diagnosis of dementia". The British Journal of Radiology. 80 Spec No 2 (Spec No 2): S71–77. doi:10.1259/bjr/33117326. PMID 18445747.
- "FDA Panel Recommends Conditional Approval for PET Agent". Imaging Technology News. 2011-01-2117 يونيو 2019.
- Clark CM, Schneider JA, Bedell BJ, Beach TG, Bilker WB, Mintun MA, et al. (January 2011). "Use of florbetapir-PET for imaging beta-amyloid pathology". JAMA. 305 (3): 275–83. doi:10.1001/jama.2010.2008. PMC . PMID 21245183.
- "Amyvid". Community register of medicinal products for human use. European Community. 17 January 201318 أبريل 2018.
- Chong MS, Sahadevan S (September 2005). "Preclinical Alzheimer's disease: diagnosis and prediction of progression". The Lancet. Neurology. 4 (9): 576–79. doi:10.1016/s1474-4422(05)70168-x. PMID 16109364.
- Sharma N, Singh AN (July 2016). "Exploring Biomarkers for Alzheimer's Disease". Journal of Clinical and Diagnostic Research (Review). 10 (7): KE01–06. doi:10.7860/JCDR/2016/18828.8166. PMC . PMID 27630867.
بِاللُغة العربيَّة
مراجع إضافية
- Alzheimer's Disease: Unraveling the Mystery. US Department of Health and Human Services, National Institute on Aging, NIH. 2008. مؤرشف من الأصل في 08 يناير 2012.
- Can Alzheimer's Disease Be Prevented? ( كتاب إلكتروني PDF ). US Department of Health and Human Services, National Institute on Aging, NIH. 2009. مؤرشف من الأصل ( كتاب إلكتروني PDF ) في 02 مايو 2013.
- Caring for a Person with Alzheimer's Disease: Your Easy-to-Use Guide from the National Institute on Aging. US Department of Health and Human Services, National Institute on Aging, NIH. 2009. مؤرشف من الأصل في 08 يناير 2012.
- Russell D, Barston S, White M (19 December 2007). "Alzheimer's Behavior Management: Learn to Manage Common Behavior Problems". helpguide.org. مؤرشف من الأصل في 23 فبراير 200829 فبراير 2008.
- Irvine K, Laws KR, Gale TM, Kondel TK (2012). "Greater cognitive deterioration in women than men with Alzheimer's disease: a meta analysis". Journal of Clinical and Experimental Neuropsychology (Meta-analysis). 34 (9): 989–98. doi:10.1080/13803395.2012.712676. PMID 22913619.